количество статей
7415
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Возможности ингибиторов АПФ в клинической практике
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Кардиология и Ангиология" №2
- Аннотация
- Статья
- Ссылки
Возможности ингибиторов ангиотензин-превращающего фермента (ИАПФ) в кардиологической практике хорошо известны. Но все ли мы о них знаем? На протяжении последнего десятилетия проведены многочисленные исследования, в которых изучалась клиническая эффективность ИАПФ при различных сердечно-сосудистых заболеваниях.
Возможности ингибиторов ангиотензин-превращающего фермента (ИАПФ) в кардиологической практике хорошо известны. Но все ли мы о них знаем? На протяжении последнего десятилетия проведены многочисленные исследования, в которых изучалась клиническая эффективность ИАПФ при различных сердечно-сосудистых заболеваниях.
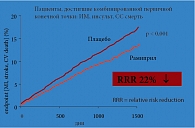
Рис. 1. Исследование HOPE: влияние терапии рамиприлом на частоту первичной конечной точки
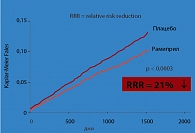
Рис. 2. Исследование HOPE: терапия рамиприлом привела к снижению частоты инфаркта миокарда
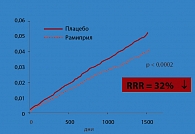
Рис. 3. Исследование HOPE: терапия рамиприлом привела к снижению частоты инсульта

Таблица. Исследование HOPE: влияние терапии рамиприлом на уровень АД
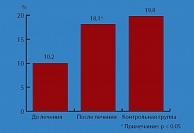
Рис. 4. Динамика ЭЗВД на фоне лечения Хартилом у пациентов с АГ
Результаты этих исследований нашли отражение в отечественных рекомендациях, согласно которым ИАПФ рекомендовано применять у больных артериальной гипертонией, сердечной недостаточностью, острым и перенесенным инфарктом миокарда и диабетической нефропатией [1–3].
ИАПФ являются одним из наиболее изученных классов антигипертензивных препаратов, эффективность которых вслед за диуретиками и β-блокаторами была доказана в крупномасштабных рандомизированных исследованиях с изучением конечных точек. Первым исследованием такого рода было исследование САРРР (Captopril Prevention Project), в котором в течение 6 лет сравнивалась эффективность ИАПФ (каптоприл 50 мг/сут) с β-блокатором атенололом и метопрололом (50–100 мг/сут) или диуретиком гидрохлортиазидом (25 мг/сут) у 10 985 пациентов с АГ. Не было установлено различий в частоте объединенной конечной точки (фатальные и нефатальные инсульты и инфаркты миокарда, а также смертность от других сердечно-сосудистых причин) между группами пациентов, получавших ИАПФ и β-блокаторы и диуретики. В данном исследовании был также продемонстрирован более благоприятный метаболический профиль каптоприла по сравнению с β-блокаторами и диуретиком. Частота возникновения сахарного диабета (СД) к концу исследования в группе каптоприла оказалась на 21% ниже [4].
Вместе с тем, многочисленные исследования свидетельствуют о благоприятных метаболических и сосудистых эффектах. Так, была выявлена способность ИАПФ повышать чувствительность тканей к инсулину при нейтральном или благоприятном влиянии на толерантность к глюкозе у больных АГ в сочетании с СД 2 типа или без него [5, 6]. При этом улучшение чувствительности к инсулину наблюдалось даже после двух лет лечения каптоприлом или его комбинацией с гидрохлортиазидом [7].
В других исследованиях длительное лечение каптоприлом [8], эналаприлом [9] и периндоприлом [10] не оказывало существенного влияния на чувствительность к инсулину и его уровень в крови при глюкозотолерантном тесте при СД 2 типа.
Ряд исследований выявил либо положительное, либо нейтральное влияние ИАПФ на липидный спектр [11, 12].
ИАПФ являются одним из самых эффективных классов препаратов в плане улучшения эндотелиальной функции (ЭФ). Описано, как минимум, два главных возможных механизма влияния ИАПФ на ЭФ. Известно, что ИАПФ увеличивают уровень тканевого брадикинина [13, 14] – мощного стимулятора высвобождения эндотелий-зависимых факторов релаксации: NO, эндотелий-зависимого фактора гиперполяризации и простациклина (PGI2). Другим механизмом действия ИАПФ является блокада образования ангиотензина II (АII), который рассматривается как индуктор оксидантного стресса, снижающего активность NO. АII обладает противоположным действием по отношению к NO, и в настоящее время признается его антагонистом. Ингибирование АПФ может восстанавливать баланс между двумя вазоактивными системами [15–16]. Двойной механизм действия ИАПФ – блокирование образования ангиотензина II и предупреждение разрушения брадикинина, который стимулирует синтез эндотелиального NO, обусловливает антигипертензивное, антипролиферативное и ангиопротективное действие этих лекарственных средств.
Способность ИАПФ улучшать ЭФ и тормозить процессы атерогенеза была впервые продемонстрирована в исследовании TREND (Trial on Reversing Endothelial Dysfunction) [17]. В 6-месячном рандомизированном исследовании у 129 больных с ИБС изучали способность квинаприла восстанавливать нарушенную эндотелиальную функцию коронарных артерий, которую оценивали с помощью пробы с внутрикоронарным введением ацетилхолина при коронарографии. Было выявлено уменьшение на 10–20% выраженности вазоконстрикторных реакций после терапии квинаприлом.
В исследовании BANFF Study была проведена сравнительная оценка коррекции ЭФ при 8-недельной терапии различными классами антигипертензивных препаратов (амлодипином, квинаприлом, эналаприлом, лозартаном) у 80 больных с ИБС. Выборка была представлена в основном мужчинами (80%), средний возраст которых составил 58 ± 0,9 лет. Факторы риска (ФР) распределялись следующим образом: гиперхолестеринемия была у 54% пациентов,
АГ – у 26%, сахарный диабет – у 10%. Инфаркт миокарда (ИМ) в анамнезе зафиксирован у 47% больных, 95% пациентов перенесли коронарную ангиопластику. В процессе лечения АД и липидный спектр крови достоверно не изменились, а эндотелийзависимая вазодилатация (ЭЗВД) плечевой артерии у больных с ФР улучшалась только на фоне лечения квинаприлом, в то время как амлодипин, эналаприл и лозартан не повлияли на ЭФ [18].
Именно улучшением ЭФ объясняют относительно новую область применения ИАПФ – профилактика осложнений и смерти у больных со стабильным течением ИБС и другими клиническими проявлениями атеросклероза. Гипотеза о возможности профилактики осложнений у данной категории пациентов проверялась в ряде крупных многоцентровых исследований: HOPE (Heart Outcomes Prevention Evaluation Study), EUROPEA (EURopean trial ON reduction of cardiac events with Perindopril in stable coronary Artery disease), PEACE (Prevention of events with Angiotensin-converting Enzyme inhibition).
В этом списке особняком стоит исследование HOPE [51], в которой участвовали 9297 мужчин и женщин с подтвержденным атеросклерозом различной локализации (коронарная болезнь сердца, поражение периферических артерий, инсульт) или сахарным диабетом и по крайней мере еще одним фактором риска (артериальная гипертония, курение, микроальбуминурия или дислипидемия). 80% больных имели коронарную болезнь сердца, 55% – стенокардию, 52% – инфаркт миокарда в анамнезе, 43% – атеросклероз периферических артерий, у 25% – нестабильная стенокардия в анамнезе, а у 26% – аортокоронарное шунтирование в анамнезе, у 18% – чрескожная реваскуляризация коронарных артерий, у 11% – инсульт или транзиторная ишемическая атака. Почти половина пациентов страдали АГ и около 40% – СД 2 типа. Больным назначали плацебо или ИАПФ рамиприл (с титрованием доз от 1,25 до 10 мг) и продолжали наблюдение в среднем 5 лет. Первичная конечная точка (сердечно-сосудистая смерть, ИМ или инсульт) была зарегистрирована у 17,8% больных группы плацебо и у 14,0% больных группы рамиприла – снижение риска на 22%, р < 0001 (рис. 1). Терапия рамиприлом привела к снижению частоты важнейших компонентов этой конечной точки – ИМ, МИ (рис. 2, 3).
Кроме того, установлено снижение общей смертности (с 12,2 до 10,4% в течение 5 лет), необходимости реваскуляризации, диабетических осложнений, развитие СД, остановки сердца, прогрессирования стенокардии или сердечной недостаточности. Представляет интерес тот факт, что снижение АД в группе рамиприла было сравнительно небольшим (АД -3/3 мм рт. ст.), поэтому результаты лечения нельзя объяснить только антигипертензивным действием препарата (см. табл.).
Таким образом, в этом исследовании была подтверждена протективная роль рамиприла в профилактике осложнений у пациентов с высоким риском. Причем защитный эффект рамиприла никак не связан со снижением АД.
Дополнительным подтверждением эффективности длительной терапии ИАПФ во вторичной профилактике являются результаты исследования EUROPA [20]. В него были включены 13 655 пациентов группы невысокого риска, без сердечной недостаточности (СН), страдавших стабильной коронарной болезнью сердца. В течение в среднем 4,2 лет им проводили лечение периндоприлом или плацебо. У больных группы периндоприла выявлено снижение частоты сердечно-сосудистых исходов (сердечно-сосудистая смерть, ИМ, внезапная смерть) с 10 до 8% (это означало, что для профилактики одного сердечно-сосудистого исхода необходимо проводить лечение в течение 4,2 лет у 50 больных). Польза ИАПФ была сопоставима во всех подгруппах больных.
Результаты исследования HOPE и EUROPA позволяют говорить об эффективности ИАПФ в плане замедления прогрессирования заболеваний, связанных с атеросклерозом. Вместе с тем, если строго опираться на принципы доказательной медицины, можно говорить о протективном эффекте периндоприла у пациентов со стабильной ишемической болезнью сердца (ИБС) и универсальном протективном эффекте рамиприла у всех пациентов, имеющих клинические проявления атеросклероза (ИБС, инсульты, периферический атеросклероз).
Можно ли протективный эффект рамиприла и периндоприла распространить на весь класс ИАПФ? При отсутствии доказательной базы в отношении других препаратов ответ должен быть отрицательным. Более того, есть исследования, не подтвердившие протективного эффекта других ИАПФ. В плацебо-контролируемом исследовании PEACE с участием 8290 пациентов со стабильной стенокардией без признаков сердечной недостаточности добавление 4 мг трандолаприла на фоне основной терапии не привело к дополнительному снижению осложнений [21]. Аналогично в плацебо-контролируемом исследовании CAMELOT, в котором участвовал 1991 пациент со стабильной ИБС без признаков СН, добавление 20 мг эналаприла к основной терапии не привело к более выраженному снижению осложнений по сравнению с пациентами, получавшими плацебо [22]. Не случайно в Европейских рекомендациях по диагностике и лечению стабильной стенокардии для замедления прогрессирования заболевания и улучшения прогноза у этой категории больных из ИАПФ рекомендованы только рамиприл и периндоприл [2]. Аналогично во втором пересмотре Российских рекомендаций по хронической сердечной недостаточности (ХСН) для профилактики этого заболевания у пациентов с ИБС рекомендуется назначение рамиприла либо периндоприла, как препаратов, имеющих доказательную базу [3].
Вместе с тем на сегодняшний день рамиприл является единственным ИАПФ, имеющим доказательный эффект. В исследовании SECURE, которое проводилось в рамках HOPE, изучалось влияние рамиприла и витамина Е на состояние сонных артерий, оцениваемых с помощью ультразвукового метода. Было показано, что длительная терапия рамиприлом задерживала прогрессирование каротидного атеросклероза у больных с атеросклерозом или СД, не имевших сердечной недостаточности [23].
В другой программе MICRO-HOPE в рамках исследования НОРЕ у 3577 больных СД 2 типа рамиприл снижал риск микрососудистых осложнений СД, таких как хроническая почечная недостаточность на 24% (р = 0,027) и ретинопатия на 22% (р = 0,024) [24]. В двойном слепом рандомизированном исследовании AASK был продемонстрирован выраженный нефропротекторный эффект рамиприла. У 1094 пациентов с гипертензивной нефропатией (СКФ в пределах 20–65 мл/мин) рамиприл в дозе 2,5–10 мг более эффективно, чем амлодипин и метопролол, замедлял снижение СКФ, развитие ХПН и смерть у пациентов [25].
Таким образом, исследования свидетельствуют о мощном вазопротективном эффекте рамиприла, имеющем важное клиническое значение. В клинической практике кроме традиционного применения рамиприла при АГ и сердечной недостаточности необходимо использовать препарат в лечении пациентов практически с любыми проявлениями атеросклероза – коронарного, мозгового и магистральных сосудов, а также больных с нефропатией. В настоящее время на российском фармацевтическом рынке имеется эффективный генерик рамиприла Хартил. Данные недавно завершенного собственного исследования у 35 пациентов с артериальной гипертонией и ожирением продемонстрировали высокую эффективность и безопасность Хартила. По данным суточного мониторирования на фоне 16-недельного лечения с утренним приемом Хартила в дозе 5–10 мг среднесуточная САД снизилась в среднем на 17,7 мм рт. ст., а ДАД в среднем на 9,5 мм рт. ст. У пациентов с вечерним приемом Хартила в дозе 5–10 мг среднесуточная САД снизилась в среднем на 20,0 мм рт. ст., ДАД – на 15,6 мм рт. ст. При этом ни у одного пациента не отмечалось побочных эффектов, приведших к отмене препарата. Кроме того, в исследовании установлена высокая вазопротекторная эффективность Хартила. На фоне лечения Хартилом достоверно увеличилась эндотелийзависимая вазодилатация (ЭЗВД) плечевой артерии (манжеточная проба с помощью ультразвука высокого разрешения): 10,2% до лечения и 18,1% после лечения, р < 0,001 (рис. 4).
При этом величина ЭЗВД плечевой артерии после лечения Хартилом достигла уровня, наблюдаемого у пациентов контрольной группы, т.е. у лиц, не имевших ни одного фактора риска (курение, нарушение липидного обмена, избыточной массы тела) и, следовательно, без нарушения эндотелиальной функции.
Таким образом, представленный выше обзор международных и российских исследований позволяет по-новому взглянуть на возможности ИАПФ. Традиционные ниши применения ИАПФ (АГ, сердечная недостаточность, диабетическая нефропатия) в последние годы расширились благодаря доказательствам мощного вазопротективного эффекта ИАПФ, что открывает новые клинические возможности их применения в плане замедления прогрессирования заболеваний, связанных с атеросклерозом. Особенно это касается двух представителей ИАПФ – рамиприла и периндоприла. По крайне мере, опираясь на данные доказательной медицины, о протективном эффекте в отношении прогрессирования сердечно-сосудистых заболеваний можно говорить только об этих двух препаратах.
ИАПФ являются одним из наиболее изученных классов антигипертензивных препаратов, эффективность которых вслед за диуретиками и β-блокаторами была доказана в крупномасштабных рандомизированных исследованиях с изучением конечных точек. Первым исследованием такого рода было исследование САРРР (Captopril Prevention Project), в котором в течение 6 лет сравнивалась эффективность ИАПФ (каптоприл 50 мг/сут) с β-блокатором атенололом и метопрололом (50–100 мг/сут) или диуретиком гидрохлортиазидом (25 мг/сут) у 10 985 пациентов с АГ. Не было установлено различий в частоте объединенной конечной точки (фатальные и нефатальные инсульты и инфаркты миокарда, а также смертность от других сердечно-сосудистых причин) между группами пациентов, получавших ИАПФ и β-блокаторы и диуретики. В данном исследовании был также продемонстрирован более благоприятный метаболический профиль каптоприла по сравнению с β-блокаторами и диуретиком. Частота возникновения сахарного диабета (СД) к концу исследования в группе каптоприла оказалась на 21% ниже [4].
Вместе с тем, многочисленные исследования свидетельствуют о благоприятных метаболических и сосудистых эффектах. Так, была выявлена способность ИАПФ повышать чувствительность тканей к инсулину при нейтральном или благоприятном влиянии на толерантность к глюкозе у больных АГ в сочетании с СД 2 типа или без него [5, 6]. При этом улучшение чувствительности к инсулину наблюдалось даже после двух лет лечения каптоприлом или его комбинацией с гидрохлортиазидом [7].
В других исследованиях длительное лечение каптоприлом [8], эналаприлом [9] и периндоприлом [10] не оказывало существенного влияния на чувствительность к инсулину и его уровень в крови при глюкозотолерантном тесте при СД 2 типа.
Ряд исследований выявил либо положительное, либо нейтральное влияние ИАПФ на липидный спектр [11, 12].
ИАПФ являются одним из самых эффективных классов препаратов в плане улучшения эндотелиальной функции (ЭФ). Описано, как минимум, два главных возможных механизма влияния ИАПФ на ЭФ. Известно, что ИАПФ увеличивают уровень тканевого брадикинина [13, 14] – мощного стимулятора высвобождения эндотелий-зависимых факторов релаксации: NO, эндотелий-зависимого фактора гиперполяризации и простациклина (PGI2). Другим механизмом действия ИАПФ является блокада образования ангиотензина II (АII), который рассматривается как индуктор оксидантного стресса, снижающего активность NO. АII обладает противоположным действием по отношению к NO, и в настоящее время признается его антагонистом. Ингибирование АПФ может восстанавливать баланс между двумя вазоактивными системами [15–16]. Двойной механизм действия ИАПФ – блокирование образования ангиотензина II и предупреждение разрушения брадикинина, который стимулирует синтез эндотелиального NO, обусловливает антигипертензивное, антипролиферативное и ангиопротективное действие этих лекарственных средств.
Способность ИАПФ улучшать ЭФ и тормозить процессы атерогенеза была впервые продемонстрирована в исследовании TREND (Trial on Reversing Endothelial Dysfunction) [17]. В 6-месячном рандомизированном исследовании у 129 больных с ИБС изучали способность квинаприла восстанавливать нарушенную эндотелиальную функцию коронарных артерий, которую оценивали с помощью пробы с внутрикоронарным введением ацетилхолина при коронарографии. Было выявлено уменьшение на 10–20% выраженности вазоконстрикторных реакций после терапии квинаприлом.
В исследовании BANFF Study была проведена сравнительная оценка коррекции ЭФ при 8-недельной терапии различными классами антигипертензивных препаратов (амлодипином, квинаприлом, эналаприлом, лозартаном) у 80 больных с ИБС. Выборка была представлена в основном мужчинами (80%), средний возраст которых составил 58 ± 0,9 лет. Факторы риска (ФР) распределялись следующим образом: гиперхолестеринемия была у 54% пациентов,
АГ – у 26%, сахарный диабет – у 10%. Инфаркт миокарда (ИМ) в анамнезе зафиксирован у 47% больных, 95% пациентов перенесли коронарную ангиопластику. В процессе лечения АД и липидный спектр крови достоверно не изменились, а эндотелийзависимая вазодилатация (ЭЗВД) плечевой артерии у больных с ФР улучшалась только на фоне лечения квинаприлом, в то время как амлодипин, эналаприл и лозартан не повлияли на ЭФ [18].
Именно улучшением ЭФ объясняют относительно новую область применения ИАПФ – профилактика осложнений и смерти у больных со стабильным течением ИБС и другими клиническими проявлениями атеросклероза. Гипотеза о возможности профилактики осложнений у данной категории пациентов проверялась в ряде крупных многоцентровых исследований: HOPE (Heart Outcomes Prevention Evaluation Study), EUROPEA (EURopean trial ON reduction of cardiac events with Perindopril in stable coronary Artery disease), PEACE (Prevention of events with Angiotensin-converting Enzyme inhibition).
В этом списке особняком стоит исследование HOPE [51], в которой участвовали 9297 мужчин и женщин с подтвержденным атеросклерозом различной локализации (коронарная болезнь сердца, поражение периферических артерий, инсульт) или сахарным диабетом и по крайней мере еще одним фактором риска (артериальная гипертония, курение, микроальбуминурия или дислипидемия). 80% больных имели коронарную болезнь сердца, 55% – стенокардию, 52% – инфаркт миокарда в анамнезе, 43% – атеросклероз периферических артерий, у 25% – нестабильная стенокардия в анамнезе, а у 26% – аортокоронарное шунтирование в анамнезе, у 18% – чрескожная реваскуляризация коронарных артерий, у 11% – инсульт или транзиторная ишемическая атака. Почти половина пациентов страдали АГ и около 40% – СД 2 типа. Больным назначали плацебо или ИАПФ рамиприл (с титрованием доз от 1,25 до 10 мг) и продолжали наблюдение в среднем 5 лет. Первичная конечная точка (сердечно-сосудистая смерть, ИМ или инсульт) была зарегистрирована у 17,8% больных группы плацебо и у 14,0% больных группы рамиприла – снижение риска на 22%, р < 0001 (рис. 1). Терапия рамиприлом привела к снижению частоты важнейших компонентов этой конечной точки – ИМ, МИ (рис. 2, 3).
Кроме того, установлено снижение общей смертности (с 12,2 до 10,4% в течение 5 лет), необходимости реваскуляризации, диабетических осложнений, развитие СД, остановки сердца, прогрессирования стенокардии или сердечной недостаточности. Представляет интерес тот факт, что снижение АД в группе рамиприла было сравнительно небольшим (АД -3/3 мм рт. ст.), поэтому результаты лечения нельзя объяснить только антигипертензивным действием препарата (см. табл.).
Таким образом, в этом исследовании была подтверждена протективная роль рамиприла в профилактике осложнений у пациентов с высоким риском. Причем защитный эффект рамиприла никак не связан со снижением АД.
Дополнительным подтверждением эффективности длительной терапии ИАПФ во вторичной профилактике являются результаты исследования EUROPA [20]. В него были включены 13 655 пациентов группы невысокого риска, без сердечной недостаточности (СН), страдавших стабильной коронарной болезнью сердца. В течение в среднем 4,2 лет им проводили лечение периндоприлом или плацебо. У больных группы периндоприла выявлено снижение частоты сердечно-сосудистых исходов (сердечно-сосудистая смерть, ИМ, внезапная смерть) с 10 до 8% (это означало, что для профилактики одного сердечно-сосудистого исхода необходимо проводить лечение в течение 4,2 лет у 50 больных). Польза ИАПФ была сопоставима во всех подгруппах больных.
Результаты исследования HOPE и EUROPA позволяют говорить об эффективности ИАПФ в плане замедления прогрессирования заболеваний, связанных с атеросклерозом. Вместе с тем, если строго опираться на принципы доказательной медицины, можно говорить о протективном эффекте периндоприла у пациентов со стабильной ишемической болезнью сердца (ИБС) и универсальном протективном эффекте рамиприла у всех пациентов, имеющих клинические проявления атеросклероза (ИБС, инсульты, периферический атеросклероз).
Можно ли протективный эффект рамиприла и периндоприла распространить на весь класс ИАПФ? При отсутствии доказательной базы в отношении других препаратов ответ должен быть отрицательным. Более того, есть исследования, не подтвердившие протективного эффекта других ИАПФ. В плацебо-контролируемом исследовании PEACE с участием 8290 пациентов со стабильной стенокардией без признаков сердечной недостаточности добавление 4 мг трандолаприла на фоне основной терапии не привело к дополнительному снижению осложнений [21]. Аналогично в плацебо-контролируемом исследовании CAMELOT, в котором участвовал 1991 пациент со стабильной ИБС без признаков СН, добавление 20 мг эналаприла к основной терапии не привело к более выраженному снижению осложнений по сравнению с пациентами, получавшими плацебо [22]. Не случайно в Европейских рекомендациях по диагностике и лечению стабильной стенокардии для замедления прогрессирования заболевания и улучшения прогноза у этой категории больных из ИАПФ рекомендованы только рамиприл и периндоприл [2]. Аналогично во втором пересмотре Российских рекомендаций по хронической сердечной недостаточности (ХСН) для профилактики этого заболевания у пациентов с ИБС рекомендуется назначение рамиприла либо периндоприла, как препаратов, имеющих доказательную базу [3].
Вместе с тем на сегодняшний день рамиприл является единственным ИАПФ, имеющим доказательный эффект. В исследовании SECURE, которое проводилось в рамках HOPE, изучалось влияние рамиприла и витамина Е на состояние сонных артерий, оцениваемых с помощью ультразвукового метода. Было показано, что длительная терапия рамиприлом задерживала прогрессирование каротидного атеросклероза у больных с атеросклерозом или СД, не имевших сердечной недостаточности [23].
В другой программе MICRO-HOPE в рамках исследования НОРЕ у 3577 больных СД 2 типа рамиприл снижал риск микрососудистых осложнений СД, таких как хроническая почечная недостаточность на 24% (р = 0,027) и ретинопатия на 22% (р = 0,024) [24]. В двойном слепом рандомизированном исследовании AASK был продемонстрирован выраженный нефропротекторный эффект рамиприла. У 1094 пациентов с гипертензивной нефропатией (СКФ в пределах 20–65 мл/мин) рамиприл в дозе 2,5–10 мг более эффективно, чем амлодипин и метопролол, замедлял снижение СКФ, развитие ХПН и смерть у пациентов [25].
Таким образом, исследования свидетельствуют о мощном вазопротективном эффекте рамиприла, имеющем важное клиническое значение. В клинической практике кроме традиционного применения рамиприла при АГ и сердечной недостаточности необходимо использовать препарат в лечении пациентов практически с любыми проявлениями атеросклероза – коронарного, мозгового и магистральных сосудов, а также больных с нефропатией. В настоящее время на российском фармацевтическом рынке имеется эффективный генерик рамиприла Хартил. Данные недавно завершенного собственного исследования у 35 пациентов с артериальной гипертонией и ожирением продемонстрировали высокую эффективность и безопасность Хартила. По данным суточного мониторирования на фоне 16-недельного лечения с утренним приемом Хартила в дозе 5–10 мг среднесуточная САД снизилась в среднем на 17,7 мм рт. ст., а ДАД в среднем на 9,5 мм рт. ст. У пациентов с вечерним приемом Хартила в дозе 5–10 мг среднесуточная САД снизилась в среднем на 20,0 мм рт. ст., ДАД – на 15,6 мм рт. ст. При этом ни у одного пациента не отмечалось побочных эффектов, приведших к отмене препарата. Кроме того, в исследовании установлена высокая вазопротекторная эффективность Хартила. На фоне лечения Хартилом достоверно увеличилась эндотелийзависимая вазодилатация (ЭЗВД) плечевой артерии (манжеточная проба с помощью ультразвука высокого разрешения): 10,2% до лечения и 18,1% после лечения, р < 0,001 (рис. 4).
При этом величина ЭЗВД плечевой артерии после лечения Хартилом достигла уровня, наблюдаемого у пациентов контрольной группы, т.е. у лиц, не имевших ни одного фактора риска (курение, нарушение липидного обмена, избыточной массы тела) и, следовательно, без нарушения эндотелиальной функции.
Таким образом, представленный выше обзор международных и российских исследований позволяет по-новому взглянуть на возможности ИАПФ. Традиционные ниши применения ИАПФ (АГ, сердечная недостаточность, диабетическая нефропатия) в последние годы расширились благодаря доказательствам мощного вазопротективного эффекта ИАПФ, что открывает новые клинические возможности их применения в плане замедления прогрессирования заболеваний, связанных с атеросклерозом. Особенно это касается двух представителей ИАПФ – рамиприла и периндоприла. По крайне мере, опираясь на данные доказательной медицины, о протективном эффекте в отношении прогрессирования сердечно-сосудистых заболеваний можно говорить только об этих двух препаратах.
1. Второй пересмотр рекомендаций ВНОК по профилактике, диагностике и лечению артериальной гипертензии // Кардиоваскулярная терапия и профилактика. 2004; 3 (3), Ч. 1: 105–120.
2. Российские рекомендации по диагностике и лечению стабильной стенокардии // Кардиоваскулярная терапия и профилактика. Приложение к журналу. 2004.
3. Второй пересмотр российских рекомендаций по диагностике и лечению ХСН // Сердечная недостаточность. 8, №2.
4. CAPPP: Hansson L., Lindholm L.H., Niskanen L. et al. Effect of angiotensin-converting-enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the captopril prevention project (CAPPP) randomized trial // Lancet. 1999; 353: 611–6.
5. Berne C., Pollare T., Lithell H. Effects of antihypertensive treatment on insulin sensitivity with special reference to ACE inhibitors // Diabetes Care. 1991; 14 (suppl 4): 39.
6. Lithell H. Effect of antihypertensive drugs on insulin, glucose, and lipid metabolism // Diabetes Care. 1991; 14: 203–209.
7. Berne C. Metabolic effects of ACE inhibitors // J Int Med. 1991; 229 (suppl 2): 119–125.
8. Seghieri G., Yin W., Boni C. et al. Effect of chronic ACE inhibition on glucose tolerance and insulin sensitivity in hypertensive type 2 diabetic patients // Diabetic Med. 1992; 9: 732–38.
9. Prince M.J., Stuart C.A., Padia M. et al. Metabolic effects of hydrochlorothiazide and enalapril during treatment of the hypertensive diabetic patient. Enalapril for hypertensive diabetics. Arch Intern Med. 1998; 146: 2363–68.
10. Bak J.F., Gerdes L.U., Sorensen N.S. et al: Effects of perindopril on insulin sensitivity and plasma lipid profile in hypertensive non-insulin-dependent diabetic patients. Am J Med. 1992; 92 (suppl 4B): 69–72.
11. Pool P.E., Seagren S.C., Salel A.F. Metabolic consequences of treating hypertension. Am J Hypertens. 1991; 4: 494–502.
12. Norman Ed., Kaplan M. Metabolic aspects of Hypertension. Science Press. 1994, London, UK.
13. Bonner G., Preis S., Schunck U. et al. Hemodynamic effects of bradykinin on systemic and pulmonary circulation in healthy and hypertensive humans. J Cardiovasc Pharmacol. 1990; 15 (suppl 6): 46–56.
14. Busse R., Lamontagne D. Endothelium-derived bradykinin is responsible for the increase in calcium produced by angiotensin-converting enzyme inhibitors in human endothelial cells. Naunyn-Schmiedebergs Arch Pharmacol. 1991; 344: 126–9.
15. Anderson T.J., Overhiser R.W., Haber H., Charbonneau F. A comparative study of four anti–hypertensive agents on endothelial function in patients with coronary disease. J. Am Coll Cardiol. 1998; 31 (2, suppl A): 32–7A. Abstract.
16. Whitebread S., Mele M., Kamber B., de Gasparo M. Preliminary biochemical characterization of two angiotension II receptor subtypes. Biochemic. Biophys. Res. Commun. 1989; 163: 284–91.
17. Mancini G., Henry G., Mancaya C. et al. Angiotensin-converting enzyme inhibition with quinapril improves endothelial vasomotor dysfunction in patients with coronary disease. The TREND (Trial on reversing Endothelial Dysfunction) study. Circulation. 1996; 94: 258–65.
18. Anderson T.J., Elstein E., Haber H., Charbonneau F. Comparative Study of ACE-inhibition, Angiotensin II Antagonism and Calcium Channel Blockade on Flow-mediated Vasodilation in Patients with coronary Disease (BANFF Study). J. Amer. Coll of Cardiology. 2000;V. 35(1): 60–66.
19. НOPE study investigators Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients // N Engl J Med. 2000; 342: 145–53.
20. The EUROPA investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomased, double-blind, placebo-controlled, multicentre trial (the EUROPA study) // Lancet. 2003; 362: 782–788.
21. PEAСE Trial investigators. Angiotensin-converting-enzyme inhibition in stable coronary artery disease // N Engl J Med. 2004; 351: 2058–2068.
22. Nissen S.E., Tuscu E.M., Libby P. et al. Effect of antihypertensive agents on cardiovascular events in patients with coronary artery disease and normal blood pressure. The CAMELOT study: a randomized controlled trial // JAMA. 2004; 292: 2217–26.
23. Lonn E.M., Yusuf S., Dzavic V. et al. Effects of ramipril and vitamin E on atherosclerosis: treated with ramipril and vitamin E (SECURE). Circulation. 2001; 103: 919–25.
24. HOPE Study Investigators. Effects of ramipril on cardiovascular and microvascular outcomes in people with diabetes mellitus: results of the HOPE study and MICRO-HOPE substudy // Lancet. 2000; 355: 253–9.
25. Agodoa L.Y., Appel L., Barkis G.L. et al. Effect of ramipril vs amlodipine on renal outcome in hypertensive nephrosclerosis // JAMA. 2001; 285: 2719–28.
Новости на тему
23.08.2022 01:00:00
05.07.2022 13:12:00
07.04.2022 11:00:00
Отправить статью по электронной почте
Ваш адрес электронной почты:
Возможности ингибиторов ангиотензин-превращающего фермента (ИАПФ) в кардиологической практике хорошо известны. Но все ли мы о них знаем? На протяжении последнего десятилетия проведены многочисленные исследования, в которых изучалась клиническая эффективность ИАПФ при различных сердечно-сосудистых заболеваниях.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
