Возможности применения α-адреноблокаторов в лечении пациенток с императивными нарушениями мочеиспускания
- Аннотация
- Статья
- Ссылки
Актуальность данной проблемы обусловлена широкой распространенностью ГАМП среди населения, как женского, так и мужского пола. По данным последних популяционных исследований, проведенных в европейских странах (Франции, Германии, Италии, Испании, Швеции, Великобритании) и США, симптомы ургентного мочеиспускания отмечает не менее 17% населения старше 40 лет, из них 56% – женщины и 44% – мужчины. Причем с возрастом частота симптомов возрастает до 30% у лиц старше 65 лет и до 40% – после 70 лет (12).
Говоря о причинах ГАМП (синдроме императивных нарушений мочеиспускания), надо отметить, что данное заболевание является многофакторным.
Одной из наиболее частых причин развития данной патологии у женщин являются воспалительные заболевания мочевых путей. По данным разных авторов, от 50 до 70% пациенток, страдающих императивными формами расстройств мочеиспускания, отмечают в анамнезе хронические циститы или уретриты (8).
Второй по значимости и распространенности причиной развития синдрома императивного мочеиспускания является эстрогенная недостаточность. Большинство женщин старше 45 лет указывают на то, что начало заболевания совпадает с наступлением менопаузы. Причем распространенность этого симптомокомплекса зависит от длительности постменопаузы и увеличивается с 15,5% при постменопаузе до 5 лет, до 71,4% при длительности постменопаузы более 20 лет, что связывают с нарастанием эстрогенного дефицита и, как следствие этого, ишемией мочевого пузыря и атрофией уротелия (1, 3, 14).
Причиной развития синдрома императивного мочеиспускания может стать различная неврологическая патология: ишемия головного мозга, инсульт, рассеянный склероз, паркинсонизм, травмы, опухоли, кисты головного и спинного мозга (3, 10). Нередко ГАМП возникает у женщин, перенесших различные гинекологические операции: экстирпация матки, гистерэктомия, а также эндоуретральные операции. Развитие нарушений мочеиспускания и недержания мочи у женщин после радикальных операций на матке связаны с парасимпатической и соматической денервацией мочевого пузыря, уретры и мышц тазового дна, нарушением анатомических взаимоотношений органов малого таза; если при операции удаляются яичники, то дополнительно возникает гипоэстрогения (5, 15).
Среди других причин возникновения данного заболевания некоторые авторы выделяют сахарный диабет и малоподвижный образ жизни (10, 14).
Патогенез ГАМП дискутируется и до настоящего времени до конца не изучен. Старое представление о патогенезе синдрома императивного мочеиспускания базируется на нарушении иннервации мочевого пузыря и уретры. Вышеперечисленные причины (воспаления, ишемия, травмы) могут вызывать повреждение холинэргических нервных волокон, иннервирующих детрузор. В неизмененных холинэргических волокнах развивается повышенная чувствительность к холинэргической нервной стимуляции, что проявляется нестабильными сокращениями детрузора (3, 10).
В настоящее время существуют несколько теорий развития ГАМП. Доминируют: нейрогенная теория и теория миогенной дистрофии детрузора. Согласно нейрогенной теории, мочеиспускание представляет собой сложный рефлекторный акт, контролируемый центрами спинного и головного мозга. Накопление мочи зависит: 1) от спинальных рефлекторных механизмов, активирующих симпатические (через поясничный отдел спинного мозга) и соматические проводящие пути к уретре; 2) от тонической подавляющей системы в головном мозге, которая подавляет передачу парасимпатического возбуждения к детрузору. Мочеиспускание осуществляется посредством угнетения симпатических и соматических путей передачи и активации спинобульбоспинальных парасимпатических рефлекторных путей, проходящих через центр мочеиспускания в «клювовидном мосту» (rostral pons). Результаты экспериментальных, физиологических и анатомических исследований подтверждают предположение о наличии в стволовой части мозга (rostral pons) центра мочеиспускания, который функционирует по типу «вспышек» нейрогенной активности и стимулирует рефлекторную цепь мочеиспускания. Пусковая точка, по-видимому, регулирует «возможности» мочевого пузыря (он начинает функционировать при критическом уровне афферентной активности, поступающей от барорецепторов в стенке мочевого пузыря), а также координирует активность мочевого пузыря и наружного сфинктера уретры. Центр мочеиспускания в стволе находится под влиянием высших регулирующих центров головного мозга. Стимуляция участков переднего и латерального гипоталамуса у животных вызывает сокращения мочевого пузыря и мочеиспускание. Стимуляция задних и медиальных участков гипоталамуса приводит к подавлению активности мочевого пузыря. Исследования у людей с использованием томографии с протонной эмиссией показали, что два участка коры (правый дорсолатеральный префронтальный участок коры и передняя опоясывающая извилина) в момент мочеиспускания активны. Установлено, что активные участки располагаются преимущественно справа − в правой части мозга (3, 5, 9). Таким образом, очевидно, что различные изменения как в периферической, так и в центральной нервной системе могут быть причиной развития гиперактивности детрузора.
Согласно миогенной теории, патогенез ГАМП заключается в том, что в основе дисфункции детрузора лежит недостаточность его энергетического метаболизма, обусловленная многими факторами, в том числе расстройствами кровообращения. Указанное звено патогенеза схематически можно представить следующим образом: повышение активности симпатического отдела вегетативной нервной системы → спазм артериальных сосудов мочевого пузыря → нарушение поступления и утилизации кислорода в гладкомышечных клетках детрузора → энергетическая гипоксия → дистрофические изменения в клетках детрузора → чрезмембранные нарушения транспорта кальция → гиперактивность детрузора → уменьшение резервуарной функции мочевого пузыря → синдром императивного мочеиспускания (2).
В последние годы рассматривается роль уротелия в патогенезе ГАМП (уротелиогенная теория), которая предполагает, что изменения чувствительности и сцепления в сети уротелий – миофибробласт приводит к повышению активности детрузора. Уротелиогенная гипотеза опирается на изменение в уротелии − сети интерстициальных клеток − 1С-LP. Имеющиеся данные свидетельствуют о том, что патология мочевого пузыря приводит к нарушению связей между интерстициальными клетками и миофибробластами, что в свою очередь ведет к формированию функционального синцития с пейсмекерной активностью (автономный водитель ритма), вызывая патологические сокращения детрузора. Несмотря на множество теорий, выделить ведущее звено патогенеза сложно, и вероятнее всего, изменения в центральном и периферическом звеньях сочетаются и усугубляют друг друга.
Гиперактивный мочевой пузырь − это симптомокомплекс, обусловленный избыточной активностью мышцы мочевого пузыря − детрузора, неадекватной реакцией его на наполнение и включающий:
- императивный (ургентный) позыв на мочеиспускание (ощущение неотвратимости мочеиспускания);
- поллакиурию (частые позывы на мочеиспускание – 8 и более раз в сутки);
- ноктурию (частые мочеиспускания в ночное время, более одного эпизода мочеиспускания в ночное время);
- императивное недержание мочи (неудержание мочи при ургентном позыве).
В тяжелых случаях заболевание ведет к снижению работоспособности, развитию неврозов, депрессии, нарушениям сна, сексуальным дисфункциям.
Установление диагноза ГАМП осуществляется на основании тщательно собранного анамнеза, анкетирования, осмотра больной в гинекологическом кресле, определении функциональных проб (кашлевой пробы, пробы Вальсальвы).
Безальтернативным методом для диагностики недержания мочи является комплексное уродинамическое исследование, которое при помощи ряда тестов позволяет определить нарушения функции мочевого пузыря, сфинктерной системы и мочевыводящих путей и осуществить выбор метода лечения данных нарушений (6, 9). Уродинамическими критериями ГАМП являются:
- повышение чувствительности уротелия;
- некоординированные колебания детрузорного давления в фазу наполнения мочевого пузыря (более 10-15 см водн. ст.);
- снижение функционального и максимального цистометрических объемов мочевого пузыря;
- нестабильность уретры.
В настоящее время развитие компьютерных технологий предоставляет новые возможности в ультразвуковом исследовании нижних мочевых путей. Одним из перспективных направлений в УЗИ является трехмерная эхография. При трехмерной реконструкции оценивается объем, толщина стенок в разных отделах мочевого пузыря, состояние слизистой оболочки мочеполового тракта, состояние внутреннего сфинктера уретры, а также, возможно, определить кровоток в области шейки мочевого пузыря и уретры, что позволяет оценить степень ишемии детрузора (5, 10).
Лечение ГАМП, как правило, консервативное, в редких случаях оперативное (денервация мочевого пузыря, пластика мочевого пузыря) (4, 7).
Консервативное лечение подразумевает немедикаментозные и медикаментозные методы, которые применяются в качестве монотерапии и в комбинации друг с другом.
Медикаментозная терапия:
- м-холинолитики;
- a-адреноблокаторы;
- заместительная гормонотерапия;
- ингибиторы обратного захвата серотонина.
Немедикаментозные методы:
- тренировка мышц тазового дна методом биологической обратной связи;
- физиотерапия;
- электростимуляция (индукция сокращений мышц тазового дна);
- нейромодуляция (стимуляция корешка сакрального нерва).
Медикаментозная терапия является основополагающей в лечении императивных нарушений мочеиспускания. От правильности выбора препарата зависит эффективность лечения, которая выражается не только в клиническом улучшении на фоне терапии, но и в длительности последующей ремиссии.
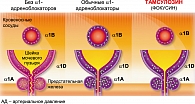
Учитывая ишемический компонент в патогенезе ГАМП, для лечения пациенток с синдромом императивного мочеиспускания в настоящее время достаточно широко применяются a-адреноблокаторы. Препараты этой группы прерывают патогенетическую цепь, связанную с развитием ишемии мочевого пузыря, в самом начале − на уровне адренорецепторов. Блокада a1-адренорецепторов сопровождается стереотипной реакцией детрузора, которая выражается в его расслаблении в фазу наполнения, увеличении резервуарной функции мочевого пузыря (2, 13). Вследствие этого достигаются существенные позитивные изменения функционального состояния нижнего отдела мочевого тракта в ответ на ограничение влияния симпатической нервной системы, что выражается в исчезновении поллакиурии и нормализации суточного профиля мочеиспускания.
Одним из эффективных препаратов группы a-адреноблокаторов, применяемых для лечения ГАМП, является ФокусинÒ (тамсулозин, Zentiva). ФокусинÒ обладает высокой селективностью, избирательно и конкурентно блокируя постсинаптические a1А-адренорецепторы в гладкой мускулатуре шейки мочевого пузыря и проксимальной части уретры, а также a1Д-адренорецепторы в теле мочевого пузыря, в связи с чем развиваются следующие эффекты:
- снижение тонуса гладкой мускулатуры шейки мочевого пузыря и проксимальной части уретры;
- увеличение резервуарной функции мочевого пузыря;
- уменьшение частоты мочеиспусканий в сутки;
- уменьшение ишемии мочевого пузыря;
- уменьшение симптомов обструкции; снижение объема остаточной мочи.
Благодаря последнему фармакологическому эффекту, a-адреноблокаторы являются препаратами выбора для лечения пациенток с явлениями функциональной обструкции, когда на фоне частых, императивных позывов наблюдаются периодически возникающие эпизоды задержки мочи, несвязанные с анатомической патологией.
Высокая селективность препарата ФокусинÒ обеспечивает ему низкую токсичность, он редко вызывает побочные эффекты. Способность Фокусина воздействовать на a1А-адренорецепторы в 20 раз превосходит его способность взаимодействовать с a1В-адренорецепторами, которые расположены в гладких мышцах сосудов, в связи с чем препарат не вызывает какого-либо клинически значимого снижения системного артериального давления (АД) как у лиц с артериальной гипертензией, так и у пациентов с нормальным исходным АД. В результате низкой токсичности Фокусина применение его может быть более длительным: до 6-12 месяцев.
Цель исследования: изучить эффективность и переносимость препарата a-адреноблокатора ФокусинÒ при лечении женщин с императивным и смешанным недержанием мочи.
Материалы и методы. За период с января по апрель 2009 г. в отделении гинекологической эндокринологии ФГУ «НЦАГиП им. академика В.И. Кулакова Росмедтехнологий» препаратом Фокусин пролечены 52 пациентки с недержанием мочи. Все больные были разделены на II группы: I группа − 30 пациенток с ГАМП; II группа − 22 женщины со смешанным недержанием мочи (медикаментозная терапия применялась в качестве I этапа для устранения императивного компонента). Возраст пациенток колебался от 36 до 68 лет (средний возраст – 52 года). ФокусинÒ применялся в дозе 400 мг в сутки в течение 3 месяцев.
Перед началом терапии всем пациенткам проводилось анкетирование, заполнение дневников мочеиспусканий, комплексное уродинамическое исследования (КУДИ). По результатам анкетирования и дневников мочеиспусканий до начала терапии суточный ритм мочеиспусканий у пациенток I группы составил от 9 до 21 раза (в среднем – 15 раз); у пациенток II группы – от 8 до 17 раз (в среднем – 12 раз). По результатам уродинамического исследования у женщин обеих групп определялось снижение функционального и максимального цистометрического объемов, а у 57,4% женщин отмечались признаки нестабильности детрузора, у 30% определялись подпороговые колебания детрузорного давления, у 12,6% – нестабильность уретры. Кроме того, у пациенток II группы отмечались уродинамические признаки стрессового недержания мочи разной степени выраженности.
Результаты. При анализе эффективности медикаментозного лечения с применением препарата ФокусинÒ в течение 3 месяцев мы учитывали оценку, которую давали пациентки, а также результаты обследования (дневников мочеиспусканий, функциональных проб, КУДИ). Всем женщинам после окончания терапии было предложено оценить свое состояние в баллах: 0 − отсутствие эффекта или ухудшение состояния; 1 − минимальные изменения без чувства удовлетворения; 2 − значительное улучшение состояния, при этом остаются редкие эпизоды недержания мочи, возникающие при сильном позыве; 3 − полное исчезновение поллакиурии и непроизвольных потерь мочи. Результат, оцененный больными от 0 до 1, нами рассматривался как отрицательный, от 2 до 3 − как положительный. Анкетирование показало, что 86,6% пациенток I группы оценили результат лечения как положительный (2 или 3 балла).
Во II группе процент положительных результатов был несколько ниже – 77,2%. Суточный ритм мочеиспусканий по дневникам у пациенток I группы после лечения составил от 6 до 10 раз (в среднем – 8 раз); у пациенток II группы – от 7 до 12 раз (в среднем – 9 раз). Высокая эффективность препарата подтверждалась и данными комплексных уродинамических исследований: у всех пациенток отмечалось увеличение функционального и максимального объемов мочевого пузыря; нестабильности детрузора и уретры не было выявлено ни у одной пациентки; у 33,4% женщин из I группы и у 36,4 % из II отмечались подпороговые колебания (от 1 до 8 см водн. ст.) детрузорного давления.
Заключение. Проведенное исследование показало, что a-адреноблокаторы являются эффективными препаратами для лечения пациенток как с императивным, так и со смешанным недержанием мочи (в качестве I этапа лечения).
Блокада a1-адренорецепторов приводит к устранению ишемии мочевого пузыря, к расслаблению детрузора в фазу наполнения, увеличению резервуарной функции мочевого пузыря, что выражается в исчезновении поллакиурии и нормализации суточного профиля мочеиспускания.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.