Выбор антигистаминного препарата с позиции доказательной медицины
- Аннотация
- Статья
- Ссылки
Проблема рационального применения антигистаминных препаратов по объективным причинам является междисциплинарной. Врачи всех специальностей так или иначе сталкиваются с их назначением, но особое место антигистаминные препараты занимают в работе врачей-аллергологов. Современные рекламные проекты и безрецептурный отпуск в аптеках часто приводят к развитию у пациентов страсти к самолечению и нерациональному, а порой безрассудному использованию вышеуказанной группы лекарственных средств. Не удивительно, что в настоящее время растет встречаемость побочных эффектов антигистаминных препаратов; выраженность этих реакций может быть различной и непредсказуемой как по клиническим проявлениям, так и по степени тяжести – вплоть до летальных исходов [1]. Между тем современный клинический подход должен учитывать аспекты безопасности применения АГС при обоснованном выборе лекарств из этой группы с позиции доказательной медицины. При оценке профиля безопасности анализируются данные доклинических научных исследований, результаты международных клинических исследований и опыт клинического применения. Антигистаминные препараты обычно классифицируют как более «старые» – Н1-антигистаминные средства первого поколения, такие как клемастин и хлоропирамин, и «новые» –
Н1-антигистаминные средства второго поколения, такие как дезлоратадин и лоратадин.
АГС первого поколения, большая часть которых применяется в клинике с 1940–50-х гг., имеют такую же химическую основу, что и холинергические антагонисты мускариновых рецепторов, транквилизаторы, нейролептики и гипотензивные средства. Они обладают слабой селективностью к рецепторам и часто вступают во взаимодействие с рецепторами других биологически активных аминов, вызывая антимускариновое, антиальфа-адренергическое и антисеротониновое действия, приводя к серьезным нежелательным эффектам. Например, при назначении в терапевтических дозах АГС первого поколения способны вызывать сухость слизистых оболочек, кокаиноподобное и хинидиноподобное действие, выраженный седативный эффект, усиливающийся при приеме транквилизаторов и алкоголя; нарушение внимания, координации, вялость; повышение или снижение аппетита; нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея, боли в эпигастрии); кардиотропное (удлинение интервала QT) местноанестезирующее действие. Обладающие седативным эффектом АГС не только оказывают влияние на дневную активность, но и нарушают нормальную структуру сна, в результате чего происходит усугубление их нежелательных эффектов. Побочные действия данных лекарственных препаратов описаны в литературе достаточно широко и стали известны практически сразу после появления на рынке 60 лет назад [2].
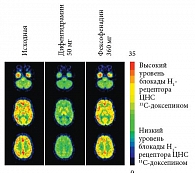
К антигистаминным препаратам первого поколения относятся: диметинден, хлорфенирамин, хлоропирамин, ципрогептадин, клемастин, дифенгидрамин, бромфенирамин, прометазин и др. АГС первого поколения липофильны и поэтому легко проходят гематоэнцефалический барьер. На рисунке 1 [3] представлены данные о степени проникновения различных АГС первого поколения в центральную нервную систему и блокирования центральных H1-гистаминовых рецепторов. Стоит отметить, что максимально допустимый уровень блокады центральных Н1-рецепторов по данным позитронно-эмиссионной томографии, которая является «золотым стандартом» и ориентиром для проведения клинических исследований, составляет 20%. Первое поколение H1-антигистаминных средств блокирует > 80% H1-рецепторов центральной нервной системы (ЦНС), что коррелирует с нарушениями когнитивной/психомоторной функции. Для сравнения, по обобщенным данным, второе поколение АГС блокирует 0–30% H1-рецепторов ЦНС [4].
Значительный прогресс в разработке антигистаминных препаратов наблюдался в 1980-е гг. с выходом на фармацевтический рынок Н1-антигистаминных препаратов второго поколения [5], которые практически не имеют или имеют минимальный седативный эффект, способны лишь в небольшом количестве проникать через гематоэнцефалический барьер. К этим препаратам относятся лоратадин, астемизол и другие. Следует отметить высокую селективность этих препаратов к гистаминовым Н1-рецепторам и отсутствие антихолинергического действия.
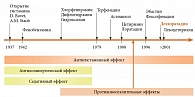
Следующий этап разработки новых подклассов антигистаминных препаратов пришелся на начало 2000-х, когда были представлены препараты (подкласс препаратов второго поколения) – активные метаболиты известных АГС: дезлоратадин, левоцетиризин и другие. Эти средства являются самыми новыми лекарственными соединениями с антигистаминной активностью, которыми располагает современная медицина. На рисунке 2 обобщены главные события, свойства и эволюция антигистаминных препаратов.
В литературных источниках иногда встречаются попытки классифицировать подкласс активных метаболитов лоратадина и цетиризина как третье поколение АГС, тем не менее более правильным представляется относить их ко второму поколению. Препараты обладают сходными фармакологическими свойствами, однако по активности метаболиты превосходят своих предшественников и имеют ряд преимуществ [2].
В основе реализации антигистаминного эффекта лежит единый механизм – взаимодействие с рецепторами гистамина на клетках различных тканей. Гистамин – 5(2-аминоэтил)имидазол – содержится преимущественно в тучных клетках и базофилах. Данному медиатору принадлежит важнейшая роль в патогенезе основных симптомов аллергических заболеваний. Под действием иммунных и неиммунных факторов происходит активация и последующая дегрануляция тучных клеток и базофилов с массивным выбросом медиаторов воспаления, в том числе гистамина. Фармакологическое действие гистамина опосредуется через стимуляцию гистаминовых рецепторов. В настоящее время известно четыре типа рецепторов гистамина. В развитии аллергических реакций в основном участвуют Н1-гистаминовые рецепторы, активация которых приводит к сокращению гладкой мускулатуры бронхов, желудочно-кишечного тракта, повышению проницаемости сосудов, усилению секреции слизи слизистыми железами дыхательных путей и раздражению нервных окончаний. В меньшей степени в реакцию вовлекаются рецепторы классов Н2 и Н4. В результате взаимодействия гистамина с рецепторами в патологический процесс вовлекаются слизистые оболочки дыхательных путей, возникают симптомы аллергического ринита и бронхиальной астмы: зуд в носу, чихание, отек слизистых, гиперсекреция слизи, бронхоспазм. Эффект в отношении слизистой глаз проявляется симптомами аллергического конъюнктивита – зудом глаз, покраснением, отеком и слезотечением. Со стороны кожи типичными клиническими проявлениями действия гистамина являются зуд, гиперемия и формирование волдырей, со стороны желудочно-кишечного тракта – боли в животе, рвота, понос, усиление продукции пепсина и соляной кислоты в желудке, повышенное образование слизи. Реакция на гистамин со стороны сердечно-сосудистой системы проявляется падением артериального давления и нарушением сердечного ритма [6].
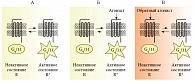
Важно отметить, что Н1-антигистаминные препараты не являются прямыми антагонистами рецепторов гистамина, как считалось ранее, а реализуют свой эффект по схеме обратных (инверсивных) агонистов, которые связываются с рецептором и стабилизируют пассивную конформацию Н1-рецепторов, тем самым препятствуя действию гистамина на Н1-рецепторы. Данная схема представлена на рисунке 3 [7].
Степень смещения равновесия в сторону неактивной конформации будет зависеть от природы обратного агониста. Чем выше сродство Н1-антигистаминных препаратов к Н1-рецептору, тем сильнее выражено их угнетающее действие на зависимое от активации NF-каппа-B (nuclear factor kappa-B – ядерный фактор) образование провоспалительных медиаторов и на связанные с ними клинические проявления. Выраженная способность антигистаминных препаратов второго поколения тормозить спонтанную и стимулированную гистамином активность NF-каппа-B объясняет их ингибирующий эффект в отношении секреции многих медиаторов аллергического воспаления и определяет их лечебное действие.
Что же привело к возросшему интересу к проблемам безопасности антигистаминных препаратов первого поколения на современном этапе? Казалось бы, данные препараты известны уже на протяжении десятилетий, пациенты хорошо их знают и считают, что они «должны быть эффективными и безопасными». Аргументами служат также большой практический опыт их применения, наличие пероральных и инъекционных форм, относительно низкая стоимость. Уверенность в безопасности АГС первого поколения, к сожалению, распространяется не только на самих пациентов, но и на опытных клиницистов, которые по неизвестным причинам игнорируют даже те предостережения, которые указаны в инструкции по медицинскому применению препарата, в том числе о том, что препарат может вызывать сонливость, нарушения внимания и т.д. Этот эффект часто расценивается как позитивный и широко используется в лечении бессонницы.
Ответ на этот вопрос дала в своем выступлении профессор Эстель Саймонс (F. Estelle R. Simons), ведущий специалист в данной области аллергологии, во время мероприятия, посвященного современному состоянию вопроса безопасности применения Н1-антигистаминных препаратов [8]. Докладчик обратила внимание слушателей на то, что Н1-антигистаминные препараты первого поколения появились в распоряжении врачей в середине прошлого века, и на тот момент не существовало правил проведения клинических испытаний и сбора информации о безопасности данных препаратов. Поэтому до сих пор нет никаких научно обоснованных данных о реальном действии Н1- антигистаминных препаратов первого поколения на организм, очень мало фармакокинетических и фармакодинамических исследований, не проводились исследования в особых возрастных группах: среди пожилых людей и детей, дозы препаратов были подобраны эмпирически. Анализ последних данных по безопасности АГС привел к введению запрета на применение у детей до 6 лет любых Н1-антигистаминных препаратов первого поколения на территории Канады и США. Также рассматривается вопрос о запрете безрецептурной продажи этих лекарственных средств во всех возрастных группах.
Ситуация на территории Российской Федерации является не более утешительной, чем в США и Европе. По последним данным, на российском фармацевтическом рынке лидирующие позиции по продажам (73%) сохраняют за собой антигистаминные препараты первого поколения, несмотря на все попытки привлечь внимание клиницистов к аспектам безопасности данных лекарственных средств. Эти цифры говорят сами за себя. Очевидно, что успех невозможен без желания самих пациентов воспринимать новую объективную информацию, проанализированную с позиции доказательной медицины, а не следовать догме: «все то, что было хорошо для наших дедушек, бабушек и наших родителей, должно быть хорошо для меня и моего ребенка».
В рамках своей деятельности по созданию международных рекомендаций сеть GA2LEN (Global Allergy and Asthma European Network – Европейская глобальная сеть по аллергии и бронхиальной астме) организовала специальную комиссию для изучения соотношения «риск/польза» Н1-антигистаминных препаратов первого поколения с седативным эффектом при лечении аллергических заболеваний и заболеваний, сопровождающихся зудом. Специальная комиссия провела анализ материалов по данному вопросу для оценки частоты побочных эффектов Н1-антигистаминных препаратов первого поколения по данным контролируемых исследований и опубликованных отчетов. Поскольку в сообщениях о нежелательных явлениях был отмечен переход от «старых» препаратов к недавно лицензированным препаратам, то проводился анализ сообщений средств массовой информации США в период с 1996 по 2008 г. в отношении несчастных случаев и нежелательных явлений, повлекших летальный исход при применении Н1-антигистаминных препаратов первого поколения. Были получены неутешительные данные [9].
Ниже приведена краткая характеристика наиболее частых нарушений со стороны ЦНС при приеме Н1-антигистаминных препаратов первого поколения:
- нарушение функции ЦНС происходит при приеме даже самых малых доз Н1-антигистаминных препаратов первого поколения, рекомендованных производителем, например, при приеме 4 мг хлорфенирамина (хлорфенамина), 25 мг дифенгидрамина, 10 мг прометазина и 5 мг трипролидина [10, 11];
- влияние Н1-антигистаминных препаратов первого поколения на ЦНС аналогично воздействию алкоголя (этилового спирта) и седативных препаратов, например бензодиазепинов [12, 13, 14], а также усиливает их эффект;
- прием препарата перед сном не гарантирует прекращения или снижения выраженности функциональных нарушений в течение следующего дня, так как Н1-антигистаминные препараты первого поколения обладают длительным периодом полувыведения с синдромом абстиненции на следующее утро [12, 15, 16, 17, 18];
- некоторые пациенты особенно подвержены поражениям ЦНС. К ним относятся женщины, лица пожилого возраста, лица с низкой массой тела, лица с нарушениями функции печени или почек или с заболеваниями ЦНС в анамнезе [12, 13];
- толерантность к седативному эффекту или психомоторному нарушению, как подтверждено результатами некоторых исследований [12, 19], может наблюдаться не всегда [13, 20].
Необходимо также учитывать возможное неблагоприятное влияние АГС первого поколения на когнитивную сферу: способность к восприятию информации, внимание, образное мышление, память, аналитико-синтетические процессы, психомоторную деятельность, вероятностное прогнозирование, мелкую моторику – все это крайне актуально среди взрослой работоспособной популяции пациентов, а также в педиатрической практике. Любое изменение этих параметров ведет к развитию интеллектуальной недостаточности, снижает способность к обучению, проявляется социальной дезадаптацией и снижением качества жизни [21].
На основе современных представлений о безопасности и эффективности лекарственных препаратов были сформулированы требования к антигистаминным препаратам для лечения ряда аллергических заболеваний. EAACI (European Academy of Allergy and Clinical Immunology – Европейская академия аллергии и клинической иммунологии) в сотрудничестве с ARIA (Allergiс rhinitis and its impact on asthma initiative – инициатива «Аллергический ринит и его влияние на бронхиальную астму») предъявляет к Н1-антигистаминным средствам следующие фармакологические критерии и требования [22]:
- cпособность к селективной блокаде H1-рецепторов;
- способность оказывать быстрое противоаллергическое действие;
- быстрота наступления клинического эффекта;
- эффективность в течение 24 часов, позволяющая принимать препарат 1 раз в сутки;
- отсутствие тахифилаксии (развития толерантности);
- отсутствие клинически значимых взаимодействий с пищей, лекарственными препаратами, H1-антигистаминные средства не должны являться субстратами транспортных белков;
- отсутствие взаимодействия с системой цитохромов P4503A (CYP3A);
- отсутствие токсического эффекта (высокий уровень безопасности).
Несколько позже эти требования к АГС были дополнены критериями безопасности [23]:
- отсутствие седативного эффекта и влияния на познавательные и психомоторные функции;
- отсутствие атропиноподобного действия;
- не должны вызывать увеличения массы тела;
- отсутствие кардиотоксических эффектов.
Подводя итог, можно утверждать, что целый ряд особенностей АГС первого поколения крайне сужает показания к назначению антигистаминных препаратов первого поколения, сохраняя за ними преимущества лишь в ситуациях, требующих парентерального введения данных лекарственных средств. Обобщим негативные свойства АГС первого поколения:
- неполная связь с Н1-рецепторами, а значит, потребность в назначении высоких доз;
- кратковременный эффект, обусловленный коротким временем удерживания АГС первого поколения на рецепторе (кратность приема 2–3 раза в сутки);
- быстрое развитие явления тахифилаксии (снижение со временем терапевтического эффекта – необходимо чередование АГС разных групп каждые 2–3 недели);
- наличие широкого спектра серьезных побочных эффектов.
Кроме того, существует ряд абсолютных противопоказаний к назначению АГС первого поколения [24]:
- деятельность, требующая концентрации внимания;
- язвенная болезнь желудка и двенадцатиперстной кишки с явлениями стенозирования привратника;
- задержка мочеиспускания;
- совместное применение с антидепрессантами, снотворными препаратами, препаратами-ингибиторами моноаминоксидазы (МАО), противодиабетическими средствами, алкоголем.
АГС второго поколения в своем большинстве удовлетворяют требованиям EAACI/ARIA и являются препаратами выбора, согласно мнению экспертов, нашедшему отражение в современных консенсусах по лечению таких заболеваний, как аллергический ринит, различные формы крапивницы, атопический дерматит, некоторые виды бронхиальной астмы, легкие формы анафилаксии.
Одним из таких препаратов является дезлоратадин (оригинальный препарат Эриус) – активный метаболит лоратадина. Препарат обладает сходными фармакологическими свойствами, однако по активности превосходит лоратадин. Дезлоратадин ингибирует многие медиаторы аллергии, включая цитокины, хемокины, молекулы адгезии. Препарат назначается 1 раз в сутки, безопасен при нарушении функции печени. Прием пищи не оказывает влияния на всасывание данного АГС. Не вызывает сонливости и удлинения интервала QT на электрокардиограмме (ЭКГ).
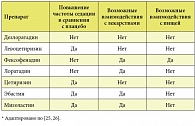
К сожалению, мы располагаем крайне скудным набором сравнительных рандомизированных исследований внутри подгруппы антигистаминных препаратов второго поколения и их активных метаболитов (табл.) [25, 26], результаты которых помогли бы четко указать на предпочтительное назначение того или иного препарата в определенных клинических ситуациях.
При приеме антигистаминных препаратов второго поколения в рекомендованных дозах седативный эффект практически отсутствует, что отличает их от АГС 1-го поколения. Дезлоратадин имеет лучший профиль безопасности в группе антигистаминных препаратов второго поколения с точки зрения частоты развития побочных эффектов, а также взаимодействия с пищей и лекарственными препаратами. Эффективность данного препарата не зависит от взаимодействия с пищей, он не метаболизируется системой цитохромов печени P450 3A4 или 2D6 (метаболизм в печени осуществляется неизвестной энзиматической системой), не взаимодействует с транспортной системой органических анионов (Organic Anion Transporter proteins, OATP). Это минимизирует потенциальные лекарственные взаимодействия и риск развития седативного эффекта. Такие препараты, как цетиризин, левоцетиризин, эбастин и мизоластин, способны вызывать незначительный седативный эффект, который может потенцировать побочные эффекты алкоголя в отношении психомоторной деятельности. Фексофенадин взаимодействует с кишечным P-гликопротеином и OATP, что снижает всасывание препарата. Биодоступность фексофенадина снижается при приеме антацидов, грейпфрутового, яблочного сока и жирной пищи, что требует от пациента дополнительных ограничений для достижения требуемой биодоступности, а значит, и клинического эффекта.
Лоратадин метаболизируется системой цитохромов печени P450 3A4 и в меньшей степени – 2D6, в связи с чем при одновременном приеме препаратов, которые метаболизируются этой системой (эритромицин, кетоконазол), возможно повышение концентрации лоратадина и его метаболита в плазме, но это повышение никак не проявляется клинически, в том числе по данным ЭКГ. Мизоластин метаболизируется системой цитохромов P450 3A4 и также имеет риск лекарственных взаимодействий. Кроме того, мизоластин противопоказан при серьезном нарушении функции печени и сердечно-сосудистых заболеваниях, так как удлиняет интервал QT.
Результаты современных сравнительных исследований антигистаминных препаратов второго поколения указывают на то, что антигистаминный эффект данных препаратов при назначении в терапевтических дозах приблизительно одинаков, но возможны некоторые различия в выраженности противовоспалительных и противоаллергических свойств. К примеру, у дезлоратадина присутствует уникальный механизм действия: он ингибирует как раннюю фазу аллергического воспаления, связанную с эффектами гистамина, триптазы, лейкотриенов и простагландинов, так и позднюю, которая поддерживается провоспалительными цитокинами, хемокинами и адгезивными молекулами, которые, в частности, участвуют в механизмах развития такого заболевания, как хроническая крапивница. Дезлоратадин обладает наиболее высокой антигистаминной активностью в группе Н1-АГС второго поколения [27, 28]. Он эффективно блокирует выделение целого ряда медиаторов из тучных клеток и базофилов [26, 29], например, гистамина, лейкотриена C4 и простагландина D2. Прослеживается также выраженная противовоспалительная активность в отношении ряда цитокинов: TNF-альфа (tumor necrosis factor-alpha – фактор некроза опухоли альфа), интерлейкинов (ИЛ) ИЛ-4, ИЛ-6, ИЛ-13 [30, 31], хемокинов RANTES (Regulated on Activation, Normal T-cell Expressed and Secreted – экспрессируемый и секретируемый нормальными T-клетками при активации) и ИЛ-8 [31, 32] и межклеточных молекул адгезии (Inter-Cellular Adhesion Molecule-1, ICAM-1) [33, 34, 35]. Противоаллергические и противовоспалительные эффекты дезлоратадина проявляются уже в наномолярных концентрациях.
В 2001 г. A.F. Daly и соавт. [36] представили систематический обзор влияния антигистаминных препаратов на назальную обструкцию. Анализ исследований показал, что дезлоратадин в дозе 5 мг 1 раз в сутки достоверно уменьшал заложенность носа во всех исследованиях (индекс заложенности носа уменьшался от 0,14 до 0,19 баллов (индекс заложенности носа оценивался по 4-балльной шкале – от «0» до «3»)). Эффект других антигистаминных препаратов в отношении заложенности носа не отличался от плацебо. На фоне лечения фексофенадином этот показатель колебался от +0,006 (увеличение) до -0,064 (снижение). При лечении цетиризином заложенность носа либо не уменьшалась, либо снижалась на 0,08. Таким образом, дезлоратадин – единственный антигистаминный препарат второго поколения, который продемонстрировал достоверное влияние на заложенность носа при аллергическом рините.
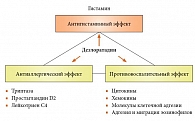
Можно утверждать, что дезлоратадин является в своем роде препаратом нового поколения, оказывая тройное воздействие на различных уровнях аллергического ответа (рис. 4) [37].
К неоспоримым преимуществам данного лекарственного средства можно также отнести быстроту развития клинического эффекта дезлоратадина, что подтверждается угнетением выраженности симптомов крапивницы уже после приема первой дозы: уменьшение зуда к концу первого дня и стойкое (до 24 часов) сохранение его действия [38].
Спорным вопросом остается терапевтическая тактика, требующая назначения доз, превышающих рекомендуемые, при лечении некоторых форм крапивницы у пациентов с недостаточным клиническим ответом. В согласительном документе Европейской академии аллергологии и клинической иммунологии, дерматологического подразделения группы GA2LEN, Европейского дерматологического форума (European Dermatology Forum, EDF) и Европейского союза медицинских специалистов (European Union of Medical Specialists, UEMS) учтена возможность использования высоких доз Н1-антигистаминных препаратов: «…при крапивнице необходимые дозы могут в 2–4 раза превышать обычные терапевтические». Если врач назначает бóльшую дозу, нежели предписано инструкцией, он обязан предупредить больного о возрастающем риске седативного эффекта и взаимодействии с другими препаратами, особенно, если они обладают седативным эффектом, таким образом, врач полностью берет на себя риск подобных рекомендаций. У пожилых больных с почечной дисфункцией или неврологическими нарушениями возможность появления седативного эффекта увеличивается. Другие авторы не рекомендуют превышение доз АГС, объясняя это возможным увеличением риска побочных явлений. Некоторые авторы говорят о возможности эмпирического назначения комбинаций антигистаминных препаратов первого и второго поколений в случае неудовлетворительного ответа на неседативные Н1-антигистаминные средства, но эта точка зрения не основывается на данных доказательной медицины ввиду отсутствия достаточного количества рандомизированных клинических исследований.
Безусловно, проблема выбора при назначении антигистаминных препаратов требует дальнейшего решения. Так, остаются открытыми вопросы безопасности назначения АГС в высоких дозах, создание доказательной базы эффективности комбинаций Н1- и Н2-гистаминоблокаторов, их применение при беременности и лактации, в группе пожилых пациентов и детей. На современном этапе развития науки имеющиеся на сегодняшний момент данные позволяют сделать вывод: основываясь на профиле безопасности и данных об эффективности АГС, единственным преимуществом антигистаминных препаратов первого поколения является наличие парентеральных форм, во всех остальных ситуациях в любом секторе терапии должно превалировать использование препаратов второго поколения.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.