количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
XXII Национальный конгресс по болезням органов дыхания: Ведение пациентов с бронхообструктивным синдромом
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Пульмонология и оториноларингология" №1 (10)
- Аннотация
- Статья
- Ссылки
Говоря о лечении пациентов с бронхообструктивным синдромом, докладчики подчеркнули, что комбинирование бронхолитических препаратов двух классов, например, бета-адреномиметика фенотерола и блокатора м-холинорецепторов ипратропия бромида в препарате Беродуал (компания «Берингер Ингельхайм»), позволяет использовать более низкие дозировки с высокой эффективностью и меньшими побочными эффектами при бронхиальной астме и ХОБЛ у взрослых, а также при лечении детей раннего возраста. При бронхообструктивном синдроме, с учетом нарушения мукоцилиарного клиренса в патогенезе, рекомендована муколитическая терапия, в частности амброксолом (препарат Лазолван), которая особенно востребована у детей раннего возраста в связи с узостью дыхательных путей.
Комплексное обсуждение актуальных аспектов диагностики и лечения пациентов с бронхообструктивным синдромом состоялось 24 октября 2012 г. в рамках XXII Национального конгресса по болезням органов дыхания. Известные пульмонологи – заведующий научно-клинической лабораторией пульмонологии НИМСИ МГМСУ, профессор К.А. Зыков, главный детский пульмонолог Минздрава РФ, профессор Ю.Л. Мизерницкий и профессор кафедры пропедевтики внутренних болезней лечебного факультета МГМСУ Г.Л. Юренев – выделили наиболее важные для практической деятельности пульмонологов, терапевтов и педиатров проблемы: преобладание острых респираторных вирусных заболеваний как причин бронхообструктивного синдрома у детей младшего возраста, частое латентное течение бронхообструкции при хронических обструктивных заболеваниях легких у взрослых, ошибки диагностики бронхообструкции и кашля.
Говоря о лечении пациентов с бронхообструктивным синдромом, докладчики подчеркнули, что комбинирование бронхолитических препаратов двух классов, например, бета-адреномиметика фенотерола и блокатора м-холинорецепторов ипратропия бромида в препарате Беродуал (компания «Берингер Ингельхайм»), позволяет использовать более низкие дозировки с высокой эффективностью и меньшими побочными эффектами при бронхиальной астме и ХОБЛ у взрослых, а также при лечении детей раннего возраста. При бронхообструктивном синдроме, с учетом нарушения мукоцилиарного клиренса в патогенезе, рекомендована муколитическая терапия, в частности амброксолом (препарат Лазолван), которая особенно востребована у детей раннего возраста в связи с узостью дыхательных путей.
Говоря о лечении пациентов с бронхообструктивным синдромом, докладчики подчеркнули, что комбинирование бронхолитических препаратов двух классов, например, бета-адреномиметика фенотерола и блокатора м-холинорецепторов ипратропия бромида в препарате Беродуал (компания «Берингер Ингельхайм»), позволяет использовать более низкие дозировки с высокой эффективностью и меньшими побочными эффектами при бронхиальной астме и ХОБЛ у взрослых, а также при лечении детей раннего возраста. При бронхообструктивном синдроме, с учетом нарушения мукоцилиарного клиренса в патогенезе, рекомендована муколитическая терапия, в частности амброксолом (препарат Лазолван), которая особенно востребована у детей раннего возраста в связи с узостью дыхательных путей.

Профессор Ю.Л. Мизерницкий

Профессор Г.Л. Юренев
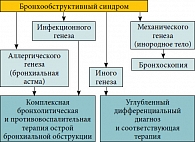
Рис. 1. Алгоритм дифференциального диагноза и подходы к терапии острой бронхиальной обструкции у детей

Таблица. Алгоритм ведения пациентов с ХОБЛ стабильного течения: рекомендации GOLD 2011*

Рис. 2. Алгоритм ведения пациентов с ХОБЛ: рекомендации GOLD 2007
В России принято характеризовать бронхообструктивный синдром как симптомокомплекс нарушения бронхиальной проходимости функционального или органического происхождения, проявляющийся кашлем, экспираторной одышкой и приступами удушья. Открывая симпозиум докладом «Кашель и бронхообструктивный синдром», профессор Кирилл Алексеевич ЗЫКОВ (доктор медицинских наук, лаборатория пульмонологии НИМСИ МГМСУ, лаборатория иммунопатологии сердечно-сосудистых заболеваний РКНПК) рассмотрел патогенез и классификацию бронхообструктивного синдрома. Механизмы бронхообструкции включают бронхоконстрикцию, образование слизистых пробок (из-за гиперсекреции и дискринии), отек бронхиальной стенки, ремоделирование бронхиальной стенки и перестройку воздухоносных путей в результате хронического воспаления, развитие эмфиземы при хронической обструктивной болезни легких (ХОБЛ).
Бронхообструкция может быть локальной (слизистой пробкой, инородным телом и др.) или генерализованной, как при хронических заболеваниях легких: бронхиальной астме, ХОБЛ и эмфиземе легких. Патогенез формирования обструкции при этих заболеваниях, объединенных в триаду хронических обструктивных заболеваний легких, принципиально различен, но у многих пациентов они перекрываются между собой, что реально представляет серьезную проблему в нашей практической деятельности. По течению выделяют острый и хронический бронхообструктивный синдром. Бронхообструктивный синдром может протекать латентно или с выраженной симптоматикой. «Ранняя диагностика бронхообструктивного синдрома дает нам возможность более эффективно лечить наших пациентов, – комментирует профессор К.А. Зыков. – Однако в клинической практике врачами чаще наблюдаются больные с III стадией ХОБЛ, у которых уже есть выраженная одышка, тогда как пациенты с более ранними стадиями заболевания редко обращаются к врачам». ХОБЛ обязательно протекает с наличием бронхообструктивного синдрома – это входит в определение заболевания, но не означает, что у больных ХОБЛ обязательно должны быть кашель, одышка или удушье в той или иной комбинации. 30% больных ХОБЛ I или II стадии с уже фиксированной бронхообструкцией попадают в бессимптомную фазу болезни. Это приводит к «недодиагностике» ХОБЛ в 50–88% случаев.
Говоря о бронхообструктивном синдроме, помимо бронхообструкции как таковой, которую нужно активно выявлять, существует еще второе слагаемое – кашель. Хотя этот симптом может быть и при необструктивных заболеваниях легких, кашель, особенно по ночам и ранним утром, позволяет заподозрить обратимую бронхообструкцию у пациентов и помочь в диагностике бронхиальной астмы, при которой хроническое воспаление вызывает гиперреактивность бронхов. При ХОБЛ персистирующее ограничение воздушного потока ассоциировано с воспалением в воздухоносных путях и легких в ответ на раздражающие частицы или газы (рекомендации GOLD 2011 (Global initiative for chronic Obstructive Lung Disease – Глобальная инициатива по ХОБЛ)). При ведении больного с кашлем важно учитывать, что существует очень много причин кашля, которые не связаны с изменениями легких и бронхов. Это и аллергические заболевания, и кардиологическая патология, и гастроэзофагеальная рефлюксная болезнь и др. Так, гастроэзофагеальная рефлюксная болезнь вызывает до 15–20% случаев хронического кашля.
Это состояние обязательно необходимо выявлять и корректировать у больных с кашлем. Также надо учитывать, что кашель может быть вызван приемом бета-блокаторов, ингибиторов ангиотензинпревращающего фермента. Среди внелегочных причин хронического кашля на первом месте стоит хронический ринит, вызывающий до 20–25% случаев хронического кашля. К легочным причинам кашля в первую очередь относятся хронический бронхит, ХОБЛ и бронхиальная астма. Каковы основные ошибки диагностики причин кашля? К ним докладчик отнес отсутствие диагностического поиска у курящих пациентов, игнорирование внелегочных причин кашля, изменение последовательности тестов (например, проведение мультиспиральной компьютерной томографии до функциональных тестов), отказ от фибробронхоскопии при неустановленной причине кашля, неучитывание приема лекарств и переоценка психогенного кашля. Нельзя игнорировать и то, что кашель может быть вызван несколькими причинами.
Хотя многие врачи применяют муколитические препараты при лечении больных ХОБЛ или бронхиальной астмой, в современных руководствах содержится мало информации о целесообразности муколитической терапии при этих заболеваниях, поскольку пока не хватает доказательной базы исследований. Рассматривая современные обоснования применения муколитических препаратов при борьбе с гиперсекрецией и дискринией, как компонентами бронхообструктивного синдрома, профессор К.А. Зыков отметил, что мукоцилиарный клиренс лежит в основе механической и биохимической противоинфекционной защиты бронхов. В качестве двух основных компонентов мукоцилиарного клиренса выделяют реснитчатый аппарат эпителия и секреторную систему воздухоносных путей. Механизмы нарушения клиренса – это повреждение мерцательного эпителия, повышение продукции секрета и повышение вязкости секрета. При тяжелом обострении бронхиальной астмы, как показали результаты электронной микроскопии биоптата слизистой бронхов, представленные профессором К.А. Зыковым, происходит повреждение эпителиоцитов, обнажение базальной мембраны.
Именно поэтому важно не допускать обострений и назначать препараты для коррекции мукоцилиарного клиренса. Только после купирования обострения бронхиальной астмы эпителий восстанавливается, начинает выполнять барьерную функцию, и восстанавливается мукоцилиарный клиренс. Говоря о связи прогноза заболевания с выраженностью бронхообструктивного синдрома и частотой обострений, докладчик привел результаты исследования P.R. Burgel и соавт. (2009), свидетельствующие о том, что выраженность хронического кашля и наличие мокроты являются факторами риска частых обострений (2 и более обострений на одного пациента в год отмечены у 55% и 22% пациентов с и без хронического кашля и наличием мокроты соответственно (p < 0,0001))1. Большое внимание в своем докладе профессор К.А. Зыков уделил принципам диагностики бронхообструктивного синдрома. Главное – выявить наличие бронхообструктивного синдрома, учитывая клинику и показатели функциональных тестов.
Однако это не так просто, поскольку пациент с бронхообструктивным синдромом не обязательно имеет четко очерченные жалобы. На следующем этапе оценивается выраженность бронхообструктивного синдрома, далее выявляется возможная этиология и предрасполагающие к хронизации факторы, в том числе аллергопатология, и факторы риска.
В ходе опроса пациента необходимо выявить наличие приступов удушья и их характеристики. Важно не пропустить такие «эквиваленты» удушья, как затрудненное дыхание с нарушением выдоха, ощущение «свистящего» дыхания, приступообразный надсадный непродуктивный кашель, ощущение одышки по ночам или ранним утром без видимых причин, динамическую одышку, возникающую периодически при резких запахах, усиление ее при физической нагрузке. Опрашивая больного, нужно уточнить наличие диагностических симптомов в аллергоанамнезе.
Ключевой метод выявления бронхообструкции – спирометрия. В исследовании T.L. Frank и соавт. (2006) было показано, что у 63,2% пациентов с факторами риска ХОБЛ (103 из 163 пациентов, у которых ХОБЛ не была заподозрена (отсутствовали записи в истории болезни)) данные спирометрии позволили диагностировать это заболевание2. На Западе для более полного охвата пациентов с кашлем и одышкой спирометрией в стандартах образования интернистов вводится обязательное обучение функциональным методам исследования, а врачам доступны карманные спирометры, которыми можно воспользоваться, не прибегая к услугам врачей кабинета функциональной диагностики. В лечении бронхообструктивного синдрома на первой позиции стоят бронхолитики. Но, как было показано еще в 1950–60-х гг., бесконтрольное применение высокодозовых неселективных адреномиметиков сопряжено с повышенным риском летальности3.
В этой связи профессор К.А. Зыков обратил внимание аудитории на то, что современные работы доказывают: хотя максимальную бронходилатацию можно достигнуть и монопрепаратами, взяв, например, один бета-адреномиметик или один антагонист м-холинорецепторов, комбинирование двух классов препаратов позволяет использовать более низкие дозировки с той же эффективностью и меньшими побочными эффектами4, причем как при бронхиальной астме, так и при хроническом бронхите5. Таким образом, следует опасаться увеличения дозировок, а не количества используемых классов препаратов. Для эффективности бронхолитической терапии очень важным представляется способ доставки препаратов в бронхи. Неправильное использование ингаляторов снижает контроль астмы. При использовании карманных ингаляторов частота ошибок у обученных пациентов достигает 30%. Профессор К.А. Зыков подчеркнул, что сразу после обучения больного технике использования ингалятора необходимо несколько раз проверить правильность его действий и осуществлять такую проверку как минимум раз в полгода.
Сейчас самыми распространенными средствами доставки бронхолитиков у взрослых являются дозированные карманные аэрозольные ингаляторы. Несмотря на очевидные преимущества (простота использования, компактность, портативность, быстрое дозирование и др.), дозированные аэрозольные ингаляторы подходят далеко не всем пациентам. Так, пожилые пациенты и дети не могут правильно координировать нажатие на клапан с медленным вдохом и задержать дыхание. Порошковые ингаляторы имеют свои преимущества (отсутствие пропеллента, активация вдохом, требуют адекватных усилий пациента), но способны доставить лишь небольшое количество препарата в периферические (малые) дыхательные пути. Для оценки эффективности терапии очень важен размер частиц препарата; а безопасность во многом зависит от степени абсорбции препарата, которая, в свою очередь, меняется в зависимости от размера частиц. Современные бесфреоновые мелкодисперсные аэрозоли содержат существенно более мелкие частицы, чем порошковые ингаляторы.
По сравнению с дозированными аэрозольными ингаляторами предыдущего поколения средство доставки бронхолитика Респимат характеризуется большей длительностью существования и меньшей скоростью облака аэрозоля6, более высокой степенью депозиции в легких7 и более высоким выходом фракций мелких частиц препарата8, что обеспечивает более эффективную доставку препарата в легкие. Можно сказать, что Респимат фактически представляет собой карманный небулайзер, который, в отличие от широко распространенных дозированных аэрозолей, практически не вызывает парадоксальный бронхоспазм.
Бронхообструктивный синдром в практике врача-педиатра
Бронхообструктивному синдрому у детей был посвящен доклад профессора Юрия Леонидовича МИЗЕРНИЦКОГО (д.м.н., главный детский пульмонолог Минздрава РФ, руководитель Детского научно-практического пульмонологического центра Минздрава РФ, заведующий отделением пульмонологии Московского НИИ педиатрии и детской хирургии Минздрава РФ). Профессор Ю.Л. Мизерницкий подчеркнул, что очень многие обсуждаемые позиции имеют разные акценты в педиатрии и в терапии. Так, в педиатрии, когда говорят о бронхообструктивном синдроме, чаще имеют в виду острое состояние, в отличие от терапии, где чаще приходится иметь дело с хроническими заболеваниями. У детей они тоже есть, но тем не менее для всех педиатров наиболее актуальна именно острая бронхиальная обструкция. Поскольку термин «бронхообструктивный синдром» собирательный и не может служить самостоятельным диагнозом, в каждом конкретном случае должен быть расшифрован ведущий механизм этой обструкции и уточнен диагноз, лежащий в ее основе.
Согласно разработанной Н.А. Геппе и соавт. рабочей классификации клинических форм бронхолегочных заболеваний у детей, самыми частыми этиологическими факторами, вызывающими бронхообструктивный синдром у детей первых лет жизни, являются острый обструктивный бронхит, бронхиолит и начальное проявление бронхиальной астмы. Возможны и другие причины, но на них приходится не более 5% всех бронхообструктивных заболеваний в практике педиатра9. Алгоритм дифференциальной диагностики бронхообструктивного синдрома (рис. 1) важен для определения подхода к лечению. Прежде всего, у детей надо отвергнуть механические причины обструкции, то есть аспирацию инородного тела, так как в этом случае требуется бронхоскопия для удаления инородного тела. В других случаях, будь то обструкция инфекционного генеза, когда на фоне респираторной вирусной инфекции по причине узких дыхательных путей и других особенностей детского организма развивается бронхиальная обструкция или бронхообструкция аллергического генеза, требуется комплексная бронхолитическая и противовоспалительная терапия.
А если она будет безуспешной и можно подозревать более редкий генез обструкции, потребуется углубленный дифференциальный диагноз. Вероятность обструкции чисто инфекционного генеза у детей уменьшается с возрастом, а вероятность аллергического заболевания (бронхиальной астмы) возрастает. У ребенка старше 4–5 лет инфекционный генез повторных бронхообструктивных эпизодов возможен только в качестве казуистики. Патофизиологические механизмы обструкции бронхов у маленького ребенка на фоне респираторной инфекции включают отек и инфильтрацию бронхиальной стенки вследствие вирусного воспаления, гиперсекрецию слизи и десквамацию реснитчатого эпителия, а также бронхоспазм, который развивается как под действием биологически активных веществ, выделяемых в ходе воспалительной реакции, так и нервно-рефлекторно при непосредственном воздействии вируса на нервные окончания и бета-2-адренорецепторы.
Каковы принципы терапии острой бронхиальной обструкции у маленького ребенка? Необходимы как можно более раннее начало лечения, адекватная регидратация и кислородная поддержка, основу терапии составляет бронхолитическое лечение. В ингаляционной терапии у детей, особенно в последние десятилетия, совершила переворот небулайзерная терапия. Небулайзерная техника «эволюционировала» от громоздких ультразвуковых аппаратов до компрессорных и портативных мембранных. Небулайзеры генерируют влажный аэрозоль с высокой респирабельной фракцией (доля фракции частиц диаметром 2–5 мкм превышает 50%) с прогнозируемым лечебным эффектом при минимальном участии пациента. Благодаря этим свойствам у детей как в остром состоянии, так и на выходе из него самыми востребованными остаются именно небулайзеры. Если возможность использовать небулайзер отсутствует, в педиатрии совершенно необходимо использование дыхательных приставок (спейсеров) для аэрозольных препаратов.
На сегодня бронхолитическим препаратом номер один у детей и в скорой помощи, и в стационаре, и в домашних условиях является препарат Беродуал – комбинация бета-2-агониста (фенотерола гидробромида) и холиноблокатора (ипратропия бромида). Эти компоненты влияют на различные механизмы бронхоконстрикции, а их сочетанное применение позволяет использовать преимущества обеих составляющих с меньшим риском побочных эффектов. Один миллилитр раствора для ингаляций содержит 20 капель Беродуала (в 1 капле содержится 25 мкг фенотерола и 12,5 мкг ипратропия бромида). Необходимую дозу препарата разводят физиологическим раствором и ингалируют через небулайзер. Детям до 6 лет на 1 ингаляцию назначают до 0,5 мл (10 капель) препарата, или 2 капли/кг массы тела; детям 6–14 лет – 0,5–1,0 мл (10–20 капель). Интервал между ингаляциями составляет 4–6 часов, соответственно, повторять такие ингаляции можно до 4 раз в сутки.
Глюкокортикостероидная терапия назначается в соответствии с тяжестью состояния ребенка. Если раньше речь шла только о пероральных стероидах, то сегодня применяются столь же эффективные, но более безопасные средства ингаляционной терапии. Препаратом выбора является суспензия будесонида через небулайзер, официально разрешенная к применению с возраста 6 месяцев. Важно, что можно сочетать будесонид с Беродуалом в одной ингаляции, и имеются подтверждения хорошего результата такого лечения. Так, по данным С.А. Царьковой, при использовании такой схемы лечения в условиях неотложной помощи у всех детей астматические проявления купировались на амбулаторном этапе10. Муколитическая терапия при обструкции бронхов у детей раннего и дошкольного возраста ввиду узости дыхательных путей совершенно необходима. Наличие бронхиальной обструкции всегда ухудшает эвакуацию мокроты и требует сочетанного с бронхолитиками назначения отхаркивающих средств и увлажнения дыхательных путей. При этом использование антигистаминных (I поколения) и атропиноподобных средств у детей нецелесообразно, так как эти препараты обладают «подсушивающим» слизистую оболочку эффектом и сгущают мокроту.
У детей старшего возраста мукоактивная терапия дискутабельна. Наиболее перспективными средствами, на взгляд экспертов, являются муколитические препараты на основе амброксола, в частности Лазолван, существенным преимуществом которого является возможность применения в ингаляциях через небулайзер. Препарат может применяться у детей с периода новорожденности. Будучи активным метаболитом бромгексина, амброксол эффективнее его и быстрее оказывает терапевтический эффект – начинает действовать уже через полчаса после приема, сохраняет свое действие в течение 6–12 часов, максимального эффекта достигает уже на 2–3-и сутки. Важно, что разжижение мокроты не сопровождается увеличением ее объема, а при одновременном назначении с антибиотиками достигается синергичный эффект. Механизмы действия амброксола очень разнообразны. Главное – это разжижение трахеобронхиального секрета за счет расщепления кислых мукополисахаридов. Кроме того, под воздействием препарата происходит усиление секреции гликопротеидов, активация движения ресничек мерцательного эпителия, повышение синтеза и секреции сурфактанта, торможение его распада. Амброксол оказывает также противовоспалительное действие, обладает антиоксидантными свойствами, а после курса лечения отмечается повышение уровня секреторного иммуноглобулина А. Недавно было описано местное обезболивающее действие препарата за счет ингибирования натриевых каналов в клеточных мембранах нервных волокон. В педиатрической практике важно, что лекарственные формы препарата рассчитаны на разные возрастные категории: помимо раствора для ингаляций Лазолван имеет формы сиропа для детей, пастилок для рассасывания, которые можно применять с 6 лет, и таблеток для взрослых.
Антибиотикотерапия при бронхообструктивном синдроме у детей ограничивается строгими показаниями (лихорадка выше 38 °С длительностью более 2–3 дней, выраженная интоксикация, невозможность исключить бактериальные осложнения, прежде всего пневмонию и бронхит), а также при затяжных не купирующихся в течение 12–24 часов обструктивных состояниях (астматическом статусе). Учитывая частоту провокации обструкции атипичными возбудителями (микоплазмами и хламидиями), а также частоту грибковой сенсибилизации, препаратами первого выбора становятся антибиотики макролидного ряда. Тактика дальнейшего наблюдения определяется диагнозом, который лежит в основе острой бронхиальной обструкции у ребенка. Дифференциальный диагноз при бронхообструктивном синдроме у детей по данным Американской ассоциации торакальной хирургии (American Association of Thoracic Surgery) включает более 150 нозологических форм. Если есть основания подозревать бронхиальную астму, ребенок должен получать базисную терапию. Для базисной терапии бронхиальной астмы у детей используется ряд препаратов: ингаляционные глюкокортикостероиды в качестве моно- и комбинированной с пролонгированными симптоматическими препаратами терапии, антилейкотриеновые препараты, кромоны, пролонгированные теофиллины, анти-IgE-антитела (омализумаб), системные пероральные глюкокортикостероиды. Однако для купирования и профилактики приступов и обострений бронхиальной астмы всегда «под рукой» должен быть лекарственный препарат бронхолитической направленности, короткодействующий бета-агонист, а еще лучше – комбинированный препарат Беродуал.
Бронхообструктивный синдром в практике врача-терапевта
В заключительном сообщении симпозиума профессор кафедры пропедевтики внутренних болезней лечебного факультета МГМСУ Георгий Леонидович ЮРЕНЕВ изложил свою позицию относительно подходов к диагностике и лечению бронхообструктивного синдрома у взрослых пациентов. Острый обструктивный синдром у взрослых чаще всего связан с острыми респираторными вирусными заболеваниями (ОРВИ), которые осложняются острым бронхитом, а острый бронхит на фоне ОРВИ в 60% случаев сопровождается синдромом бронхиальной обструкции. Правда, подавляющее большинство этих случаев представляют собой начальную обструкцию, а умеренная и тяжелая обструкция встречается значительно реже. Что касается хронической патологии, то при проведении дифференциальной диагностики следует помнить о том, что ХОБЛ и бронхиальная астма составляют 90% всех случаев хронической бронхиальной обструкции у взрослых. Другие заболевания, такие как бронхоэктатическая болезнь, муковисцидоз, облитерирующий бронхиолит, стеноз крупных дыхательных путей, карциноидный синдром, диагностируются значительно реже.
Бронхообструктивным синдромом могут осложниться и заболевания, которые первично поражают не органы дыхания, а органы пищеварения, например, гастроэзофагеальная рефлюксная болезнь, или сердечно-сосудистую систему с развитием хронической сердечной недостаточности. Говоря о механизмах обструкции, важно отметить, что есть механизмы необратимые (ремоделирование бронхов) и обратимые. Последние представляют наибольший интерес с практической точки зрения, потому что на них можно воздействовать лекарственными препаратами. Классическая триада обратимого механизма – бронхоспазм, сокращение гладкой мускулатуры бронхов, воспалительная отечность слизистой оболочки с гиперсекрецией слизи – определяет выбор лекарственного препарата: бронхолитиков, препаратов, оказывающих противоотечное действие, и мукоактивных препаратов. Ингаляционные глюкокортикостероиды уменьшают продукцию лейкотриенов, простагландинов, провоспалительных цитокинов, снижают проницаемость сосудов и за счет этого оказывают противоотечное действие. Из муколитиков, по наблюдениям докладчика и данным литературы, наиболее часто используются амброксол и N-ацетилцистеин. Применение амброксола наиболее целесообразно при бронхообструктивном синдроме с кашлем и вязкой мокротой.
В литературе есть данные об эффективном использовании амброксола при заболеваниях дыхательных путей с сухим кашлем: на фоне фарингита, благодаря местному анестезирующему эффекту, уменьшающему кашель11, и у больных острым бронхитом (ускорение выздоровления происходит при начале применения амброксола до появления мокроты)12. В нашем арсенале есть три класса бронхолитических препаратов: бета-агонисты, холинолитики и теофиллины. Есть препараты длительного и короткого действия. Бронхолитики короткого действия используются на начальных стадиях заболевания, при недостаточном эффекте базисной терапии, обострении хронического заболевания и как альтернатива препаратам длительного действия при их недоступности. Профессор Г.Л. Юренев представил вниманию аудитории вариант схемы лечения ХОБЛ, принятый GOLD в 2007 г. (рис. 2), а также последнюю схему лечения, рекомендованную GOLD в 2011 г. (табл.). Короткодействующие бронхолитики используются начиная с первой стадии ХОБЛ по потребности и в дальнейшем сохраняют свое значение на всех стадиях заболевания.
Начиная со второй стадии пациентам показана длительно действующая терапия, но в тех случаях, когда это лечение пациенту недоступно, использование короткодействующих бронхолитиков несколько раз в день не оставляет пациента без помощи. Согласно рекомендациям GOLD 2011, короткодействующие бета-агонисты и холинолитики являются средствами первой линии у пациентов группы А и показаны как средства альтернативного выбора пациентам групп В, С и D. При ступенчатой терапии бронхиальной астмы согласно рекомендациям GINA 2006–2011 короткодействующие бета-агонисты или комбинированные бронхолитики показаны по потребности на всех ступенях, на поздних ступенях рекомендуется добавление длительно действующих бета-агонистов. Высокой эффективностью и быстродействием в отношении симптомов бронхиальной обструкции обладают бета-2-агонисты. Они расслабляют гладкую мускулатуру бронхов, усиливают мукоцилиарный клиренс, купируют симптомы за 1–3, максимум 5 минут.
Но эти препараты не лишены достаточно большого количества побочных эффектов (тахикардия, нарушение ритма, иногда нарушения ритма бывают фатальными). Особенно это важно для групп риска, к которым относятся пожилые пациенты и пациенты с сопутствующей патологией сердечно-сосудистой системы. Современные низкодозовые селективные бета-2-агонисты не действуют на сердце, но при передозировке препараты преодолевают селективность и влияют на рецепторы сердца. У пожилых пациентов с возрастом уменьшается плотность бета-адренорецепторов, пациенты чаще используют ингаляторы и поэтому у них повышается риск нарушения ритма. Альтернативой короткодействующим бета-агонистам служат антихолинергические препараты. При хроническом бронхите и при ХОБЛ холинолитики по эффективности превосходят короткодействующие бета-агонисты, а при астме уступают им, являясь, однако, достаточно эффективными, чтобы при необходимости быть альтернативой. Антихолинергические препараты характеризуются более высоким профилем безопасности. Единственный их недостаток, особенно для астматиков, это медленное – в течение получаса – развитие эффекта.
Альтернативное использование антихолинергических препаратов при астме показано в случае неэффективности или плохой переносимости бета-агонистов, что может быть связано, с одной стороны, с длительным приемом длительно действующих бета-агонистов, а с другой стороны – с генетическим полиморфизмом (по данным европейских исследований, среди лиц европейской расы около 15% больных генетически предрасположены к недостаточной эффективности бета-агонистов). Если у пациента развился бронхоспазм на фоне приема бета-агонистов, его можно лечить только антихолинергическими препаратами, поскольку бета-адренорецепторы заблокированы. Среди других показаний к назначению антихолинергических препаратов отметим ночную астму, которая во многих случаях обусловлена повышенным тонусом блуждающего нерва; астму курильщиков, поскольку у них также повышен тонус блуждающего нерва; астму на фоне ХОБЛ.
Профессор Г.Л. Юренев подчеркнул значимость комбинированной бронхолитической терапии, включающей бета-агонист и антихолинергический препарат. «У нас есть в распоряжении препарат Беродуал, состоящий как раз из двух таких компонентов, – комментирует докладчик. – Важным его преимуществом является то, что доза бета-агониста 50 мкг в два раза меньше, чем в монопрепарате Беротеке, что обусловливает более высокую безопасность использования Беродуала. Оба компонента Беродуала удачно дополняют друг друга как в отношении скорости наступления эффекта и продолжительности эффекта, так и в отношении воздействия на мукоцилиарный клиренс». Во многих исследованиях было показано, что комбинированная терапия в большей мере улучшает функцию легких, чем монотерапия отдельными компонентами, в том числе это было показано и при обострении бронхиальной астмы13. В 2005 г. был опубликован крупный метаанализ 32 исследований, включавший более 3500 больных, который выявил при применении комбинированной бронхолитической терапии достоверно более высокий прирост объема форсированного выдоха за первую секунду (ОФВ1) – на 0,44 л – и снижение риска госпитализаций на 32%14. Подводя итог, профессор Г.Л. Юренев выделил основные преимущества бронхолитической терапии комбинацией холинолитика и бета-агониста:
- влияние на различные отделы дыхательных путей (холинорецепторы преимущественно локализованы в проксимальных отделах бронхов, а адренорецепторы – в дистальных отделах дыхательных путей);
- воздействие на два компонента бронхоконстрикции: на симпатические и парасимпатические механизмы;
- быстрое наступление эффекта и его бóльшая продолжительность;
- уменьшение выработки слизи без нарушения ее выведения из дыхательных путей;
- минимальный риск развития тахифилаксии;
- снижение риска госпитализаций;
- отсутствие кардиотоксического действия, в том числе у больных с сердечно-сосудистыми заболеваниями;
- низкая вероятность побочных эффектов и фатальных осложнений у всех категорий больных, включая детей и пожилых пациентов.
Заключение
Как отметил председатель симпозиума профессор К.А. Зыков, прошедшее обсуждение бронхообструктивного синдрома с позиций педиатра, терапевта и пульмонолога показало, что «бронхообструктивный синдром отнюдь не линейное понятие, каким мы его привыкли рассматривать», а правильный выбор препарата для лечения бронхообструкции и средства доставки этого препарата с учетом новых данных доказательной медицины позволит врачам улучшить качество лечения пациентов с бронхообструктивным синдромом.
1. Burgel P.R., Nesme-Meyer P., Chanez P. et al. Cough and sputum production are associated with frequent exacerbations and hospitalizations in COPD subjects // Chest. 2009. Vol. 135. № 4. P. 975–982.
2. Frank T.L., Hazell M.L., Linehan M.F. et al. The diagnostic accuracies of chronic obstructive pulmonary disease (COPD) in general practice: The results of the MAGIC (Manchester Airways Group Identifying COPD) study // Prim. Care Respir. J. 2006. Vol. 15. № 5. P. 286–293.
3. Inman W.H., Adelstein A.M. Rise and fall of asthma mortality in England and Wales in relation to use of pressurised aerosols // Lancet. 1969. Vol. 2. № 7615. P. 279–285.
4. Donohue J.F. Combination therapy for chronic obstructive pulmonary disease: clinical aspects // Proc. Am. Thorac. Soc. 2005. Vol. 2. № 4. P. 272–281.
5. Van Schayck C.P., Folgering H., Harbers H. et al. Effects of allergy and age on responses to salbutamol and ipratropium bromide in moderate asthma and chronic bronchitis // Thorax. 1991. Vol. 46. № 5. P. 355–359.
6. Hochrainer D., Hölz H., Kreher C. et al. Comparison of the aerosol velocity and spray duration of Respimat Soft Mist inhaler and pressurized metered dose inhalers // J. Aerosol. Med. 2005. Vol. 18. № 3. P. 273–282.
7. Newman S.P., Steed K.P., Reader S.J. et al. Efficient delivery to the lungs of flunisolide aerosol from a new portable hand-held multidose nebulizer // J. Pharm. Sci. 1996. Vol. 85. № 9. P. 960–964.
8. Zierenberg B. Optimizing the in vitro performance of Respimat // J. Aerosol. Med. 1999. Vol. 12. Suppl. 1. P. S19–S24.
9. Геппе Н.А., Розинова Н.Н., Волков И.К., Мизерницкий Ю.Л. Рабочая классификация основных клинических форм бронхолегочных заболеваний у детей // Трудный пациент. 2009. № 1–2. С. 35–39.
10. Царькова С.А., Абелевич М.М. Небулизированный будесонид (суспензия Пульмикорта) при острой обструкции дыхательных путей у детей // Педиатрическая фармакология. 2003. № 2. С. 36–39.
11. 11 Malerba M., Ragnoli B. Ambroxol in the 21st century: pharmacological and clinical update // Expert. Opin. Drug Metab. Toxicol. 2008. Vol. 4. № 8. P. 1119–1129.
12. Schulz M., Hämmerlein A., Hinkel U. et al. Safety and usage pattern of an over-the-counter ambroxol cough syrup: a community pharmacy-based cohort study // Int. J. Clin. Pharmacol. Ther. 2006. Vol. 44. № 9. P. 409–421.
13. Rodrigo G.J., Rodrigo C. First-line therapy for adult patients with acute asthma receiving a multiple-dose protocol of ipratropium bromide plus albuterol in the emergency department // Am. J. Respir. Crit. Care Med. 2000. Vol. 161. № 6. P. 1862–1868.
14. Rodrigo G.J., Castro-Rodriguez J.A. Anticholinergics in the treatment of children and adults with acute asthma: a systematic review with meta-analysis // Thorax. 2005. Vol. 60. № 9. P. 740–746.
Новости на тему
28.12.2023
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.