Ринобронхиальный синдром – новые возможности топической терапии
- Аннотация
- Статья
- Ссылки
- English
Для расширения возможностей консервативной терапии СПЗ с кашлем на фоне острого риносинусита легкого или среднетяжелого течения с применением комплексного назального спрея Полидекса с фенилэфрином на кафедре оториноларингологии Российского университета медицины было проведено клиническое исследование. Исследование показало быстрое купирование кашля и улучшение качества сна пациентов, сокращение кратности приема сосудосуживающих средств и ранний отказ от их применения, эффективное подавление роста патогенной микрофлоры на фоне применения спрея Полидекса с фенилэфрином.
Для расширения возможностей консервативной терапии СПЗ с кашлем на фоне острого риносинусита легкого или среднетяжелого течения с применением комплексного назального спрея Полидекса с фенилэфрином на кафедре оториноларингологии Российского университета медицины было проведено клиническое исследование. Исследование показало быстрое купирование кашля и улучшение качества сна пациентов, сокращение кратности приема сосудосуживающих средств и ранний отказ от их применения, эффективное подавление роста патогенной микрофлоры на фоне применения спрея Полидекса с фенилэфрином.
Введение
Заболевания лор-органов, которые сопровождаются синдромом постназального затека (СПЗ), относятся к частым причинам кашля (по данным ряда авторов, СПЗ является причиной кашля в 54% случаев) [1]. В большинстве случаев СПЗ не самостоятельная нозологическая форма. Этим термином обозначают воспалительные процессы верхних дыхательных путей (носоглотки, полости носа, околоносовых пазух), при которых отделяемое из полости носа стекает по задней стенке в гортанную часть глотки, где происходит механическая стимуляция афферентной части дуги кашлевого рефлекса, что и вызывает появление кашля.
Осведомленность врачей в отношении СПЗ очень важна, поскольку кашель при этом состоянии часто ошибочно принимают за проявления хронического бронхита.
Данный синдром является результатом нарушения работы регионарных экзокринных желез, продуцирующих слизь. Гиперпродукцию слизи могут провоцировать воспалительные реакции различной этиологии. Чаще всего это аллергические, бактериальные или вирусные риносинуситы, вазомоторные или медикаментозные риниты, риниты беременных, в детском возрасте – аденоидит. При исключении у пациента вышеперечисленных заболеваний и состояний и невозможности найти объективную причину возникновения СПЗ используется термин «идиопатический постназальный синдром».
СПЗ имеет особое эпидемиологическое значение в связи с тем, что, по данным ряда авторов, является причиной хронического кашля в 20–34% случаев [2–4]. А по официальной статистике западных стран, СПЗ выступает ведущей причиной хронического кашля с распространенностью 24–52% [5]. В свою очередь кашель – это одна из наиболее частых причин обращения к врачу. Чтобы понять патофизиологическую связь между СПЗ и кашлем, необходимо понять механизмы развития кашля.
Кашель является врожденным безусловным рефлексом, способствующим эвакуации крупных частиц и инородных тел, которые не могут быть удалены путем мукоцилиарного клиренса. Кашель при СПЗ появляется преимущественно ночью или утром. Это связано с тем, что ночью, во время сна, в горизонтальном положении отделяемое стекает в гортаноглотку, раздражает рефлексогенные зоны и вызывает кашель. Днем в вертикальном положении тела отделяемое также стекает в гортаноглотку, но проглатывается рефлекторно, почти не попадая на надгортанник и голосовые складки и не вызывая кашля [4, 6].
Патогенез кашля при СПЗ обусловлен тем, что отделяемое из полости носа, стекая по задней стенке глотки в трахеобронхиальное дерево, приводит к механической стимуляции афферентной части дуги кашлевого рефлекса [7, 8]. Также имеются результаты исследования, подтверждающие повышенную чувствительность задней стенки глотки к раздражающим факторам у пациентов, имеющих различные заболевания полости носа в совокупности с СПЗ. У этих пациентов обнаружены специальные рецепторы TRPV1, широко представленные на слизистой оболочке верхних и нижних дыхательных путей. Раздражение данных рецепторов приводит к достоверному увеличению частоты кашля у таких пациентов [5].
Считается, что в группе некурящих пациентов всех возрастов, не принимающих ингибиторы ангиотензинпревращающего фермента для лечения артериальной гипертензии и имеющих нормальную рентгенограмму грудной клетки, хронический кашель более чем в 90% случаев развивается на фоне трех имеющихся заболеваний: СПЗ, бронхиальной астмы, гастроэзофагеальной рефлюксной болезни [9, 10].
Помимо кашля клиническими проявлениями постназального затека могут быть одышка и хрипы в легких при аускультации, но у части пациентов кашель бывает единственным симптомом СПЗ [1, 2].Также пациенты могут предъявлять жалобы на ощущение скопления слизи в задних отделах полости носа и чувство стекания ее по задней стенке глотки. Данный симптом отмечается преимущественно в утренние часы и сопровождается ощущением дискомфорта в глотке. Могут наблюдаться явления фарингита, которые связаны со стеканием патологического секрета из полости носа или околоносовых пазух по задней стенке глотки. Еще одним проявлением СПЗ является частое отхождение слизистых сгустков оранжево-коричневого цвета. При мезофарингоскопии определяются слизистые тяжи по задней стенке глотки. Несколько реже можно обнаружить увеличение и гиперемию лимфоидных фолликулов задней стенки глотки [8].
Диагностика СПЗ, помимо сбора жалоб, включает эндоскопическое исследование носа и носоглотки, по результатам которого выявляется эндоскопически позитивный или эндоскопически негативный СПЗ [1, 3]. Характерными находками являются застойные скопления слизи в задних отделах полости носа (обычно на дне, под задними концами нижних носовых раковин), либо потоки густого секрета, который транспортируется из полости носа или из соустий околоносовых пазух в глотку, минуя заднюю поверхность мягкого неба или глоточные отверстия слуховых труб. В данном случае устанавливается эндоскопически позитивный СПЗ. При отсутствии патологических скоплений слизи синдром определяют как эндоскопически негативный [8].
Лечение СПЗ в настоящее время все еще представляет непростую задачу. В первую очередь лечебная тактика зависит от причины, вызвавшей СПЗ. В зависимости от этого могут быть использованы как консервативные, так и хирургические методы, направленные на лечение основного заболевания. Также крайне важно исключить воздействие этиологических факторов, способных приводить к возникновению данного синдрома, таких как профессиональные вредности, курение, заболевания нижних дыхательных путей или желудочно-кишечного тракта [7].
Цель исследования
Для оценки клинической эффективности, переносимости и безопасности препарата комплексного назального спрея Полидекса с фенилэфрином (Полидекса с ФЭ) у пациентов с кашлем на фоне острого риносинусита легкого или среднетяжелого течения с СПЗ проведено клиническое исследование. Пациенты были разделены на две группы – основную и контрольную, в каждой по 25 больных с острым риносинуситом легкого или среднетяжелого течения с СПЗ и кашлевым синдромом.
Материал и методы
Пациентам основной группы был назначен препарат Полидекса с ФЭ по одному впрыску в обе половины полости носа четыре раза в день в течение десяти дней, орошение изотоническим солевым раствором по две дозы в каждую половину полости носа три раза в день.
В контрольной группе лечение проводили мометазона фуроатом (инГКС) по две дозы в обе половины полости носа два раза в день в течение десяти дней, антисептик из группы протеината серебра по две-три капли в каждый носовой ход три раза в день в течение семи дней, орошение изотоническим солевым раствором по две дозы в каждую половину полости носа три раза в день. В обеих группах при необходимости было разрешено использовать местно сосудосуживающие препараты и системные жаропонижающие средства, анальгетики.
Всем пациентам, включенным в исследование, на первом визите проводилась цифровая диафаноскопия для исключения острого экссудативного риносинусита.
Для оценки общего самочувствия пациентов использовали ВАШ и Питтсбургский опросник определения качества сна. Больные оценивали общее самочувствие, количество эпизодов дневного и ночного кашля. Чтобы установить корреляцию между субъективными и объективными симптомами (гиперемия и отечность слизистой оболочки полости носа, отделяемое в полости носа), всем пациентам на всех визитах выполнялось эндоскопическое исследование полости носа.
Для анализа результатов исследования использовались методы описательной статистики.
Результаты
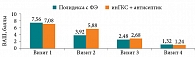
На фоне проводимого лечения положительная динамика общего самочувствия с учетом эпизодов дневного и ночного кашля по шкале ВАШ отмечена в обеих группах, однако в основной группе она была более выраженной в отношении всех симптомов уже ко второму визиту (третий день лечения). В контрольной группе явное улучшение больные отмечали только к третьему визиту (седьмой день лечения) (рис. 1).
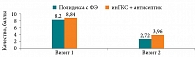
Все пациенты заполняли опросник по качеству сна (рис. 2). Данная анкета заполнялась дважды – на первом визите и на 14-й день при контрольном визите. Питтсбургский опросник определения качества сна (Pittsburgh Sleep Quality Index, PSQI) разработан D.J. Buysse и соавт. Для исследования была использована одобренная правообладателем невалидизированная русскоязычная версия. Данный опросник используется в качестве самодиагностики и позволяет оценить сон по семи различным компонентам, каждый из которых оценивается в диапазоне от 0 до 3 баллов. Путем суммирования семи составляющих баллов получается общий балл в диапазоне от 0 до 21, где более низкие баллы указывают на более здоровое качество сна. Согласно данным исследований, балл PSQI имеет диагностическую чувствительность 89,6% и специфичность 86,5% (p < 0,001) в оценке хорошего и плохого сна, положительно зарекомендовав себя в комплексном анализе качества сна. Данный опросник также позволяет дополнить информацию о динамике ночного кашля и составить более полную картину о самочувствии пациента.
По полученным в ходе исследования данным, у основной группы удалось быстрее достичь более низких значений по опроснику, что свидетельствует о более высоком качестве сна в этой группе по сравнению с контрольной. Поскольку пациенты на первом визите связывали плохой сон с выраженным кашлем, улучшенные показатели сна свидетельствуют в первую очередь об эффективности купирования ночного кашля.
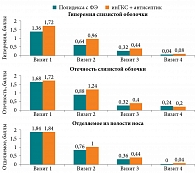
При объективном осмотре пациентов также было отмечено наличие изменений слизистой оболочки полости носа по балльной системе. Гиперемия оценивалась от 0 баллов (отсутствие признака) до 3 баллов (сильно выраженная гиперемия). Отечность слизистой оболочки оценивалась от 0 баллов (отсутствие признака) до 3 баллов (сильно выраженная отечность). Наличие слизистого отделяемого также оценивалось от 0 баллов (отсутствие признака) до 3 баллов (сильно выраженное).
Различия в купировании воспалительных изменений между группами были зарегистрированы уже ко второму визиту (3-й день терапии). В основной группе (с применением препарата Полидекса с ФЭ) эффект наступал раньше (рис. 3).
Также был проведен забор биоматериала со слизистой оболочки полости носа для определения спектра микрофлоры и ее чувствительности к антибиотикам перед началом терапии и на седьмой день лечения.
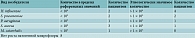
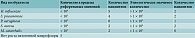
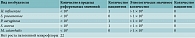
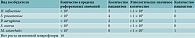
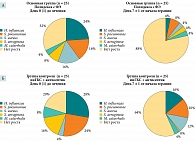
На первом визите в день 0 (1) получены следующие результаты микробиологического исследования в основной группе: Haemophilus influenzae (24%), Streptococcus pneumoniae (16%), Pseudomonas aeruginosa (8%), Staphylococcus aureus (16%), Moraxella catarrhalis (4%). Не было выявлено роста патогенной микрофлоры в 32% случаев (табл. 1).
В группе контроля: H. influenzae (28%), S. pneumoniae (24%), P. aeruginosa (4%), S. aureus (16%), M. catarrhalis (8%). Не было выявлено роста патогенной микрофлоры в 20% случаев (табл. 2).
На третьем визите в день 7 ± 1 от начала терапии выполнялся повторный забор отделяемого из полости носа. В основной группе высеивались: H. influenzae (4%), S. pneumoniae (0%), P. aeruginosa (4%), S. aureus (4%), M. catarrhalis (0%). При этом у всех пациентов патогенные возбудители высеивались в этиологически незначимых количествах. Не было выявлено роста патогенной микрофлоры в 88% случаев (табл. 3).
В группе контроля высеивались: H. influenzae (16%), S. pneumoniae (16%), P. aeruginosa (12%), S. aureus (0%), M. сatarrhalis (4%). У части (12%) пациентов патогены определялись в этиологически значимых количествах. Не было выявлено роста патогенной микрофлоры в 64% случаев (табл. 4).
Динамика результатов микробиологического исследования мазков из полости носа по группам между визитами отображена на рис. 4.
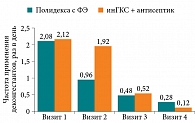
Также в обеих группах проводился контроль частоты и длительности использования сосудосуживающих капель (рис. 5). По дневникам пациентов была проанализирована частота и длительность применения деконгестантов. Сосудосуживающие препараты применялись один – три раза в день. В основной группе пациенты в более ранние сроки стали уменьшать применение деконгестантов и уже ко второму визиту часть пациентов от них отказалась. С третьего визита схожая положительная динамика отмечалась и в контрольной группе, сохраняясь в обеих группах до конца исследования.
В ходе исследования в обеих группах не было отмечено известных или вновь выявленных нежелательных явлений. Кроме того, следует отметить, что пациенты основной группы были более привержены лечению, поскольку кратность применения препарата и схема лечения оказалась более удобной и простой, тогда как в контрольной группе применялись два препарата с разной кратностью введения, из-за чего отмечены эпизоды нарушения режима: два пациента пропустили применение антисептика в последние дни терапии. Кроме того, два пациента из группы контроля жаловались на жжение при введении протеината серебра, которое купировалось самостоятельно.
Выводы
Анализ результатов сравнительного наблюдательного исследования, проведенного на клинических базах кафедры оториноларингологии Российского университета медицины Минздрава России, продемонстрировал эффективность комплексного назального спрея Полидекса с ФЭ в лечении пациентов с острым риносинуситом легкого или среднетяжелого течения с синдромом постназального затека.
У пациентов основной группы, получавших лекарственный препарат Полидекса с ФЭ, согласно полученным результатам, быстрее купировался кашель (уже ко второму визиту, в день 3 ± 1), чем у больных контрольной группы, где пациенты получали топический интраназальный глюкокортикостероид с антисептиком из группы протеината серебра.
Контрольное обследование показало также лучшую динамику качества сна по опроснику PSQI, у пациентов основной группы.
Тщательная оценка использования деконгестантов в обеих группах позволила выявить, что больные основной группы быстрее сокращали кратность приема сосудосуживающих средств и полностью отказывались от их применения: уже ко второму визиту девять (36%) больных не нуждались в препаратах для облегчения носового дыхания в сравнении с группой контроля, где все пациенты продолжали использовать деконгестанты.
Результаты исследования микрофлоры полости носа показали, что Полидекса с ФЭ эффективно подавляет рост патогенной микрофлоры. При повторном исследовании мазков на контрольном визите в день 7 ± 1 у 22 (88%) пациентов основной группы рост патогенной флоры не отмечен, среди остальных трех (12%) пациентов патогенная флора была в пределах референсных значений, этиологически незначимых.
В ходе исследования в группах сравнения не отмечено нежелательных явлений. Кроме того, пациенты основной группы были более привержены лечению, поскольку кратность применения препарата и схема лечения была более удобной и простой, тогда как в контрольной группе с применением двух препаратов с разной кратностью приема были отмечены нарушения режима и жалобы на преходящее жжение при введении протеината серебра.
Таким образом, в группе применения комплексного топического назального спрея Полидекса с ФЭ в лечении острого риносинусита легкого и среднетяжелого течения с синдромом постназального затека выздоровление наступало раньше в сравнении с группой контроля:
- быстрее (в день 3 ± 1) улучшалось самочувствие пациентов и разрешались объективные и субъективные симптомы острого риносинусита;
- раньше (в день 3 ± 1) купировался кашель, разрешались симптомы СПЗ;
- раньше улучшалось качество сна;
- снижалась частота дополнительного использования деконгестантов (в два раза ко второму визиту);
- эффективнее подавлялся рост патогенной микрофлоры.
Отмечается хороший профиль безопасности – отсутствие нежелательных явлений за весь период наблюдения в исследовании и высокая комплаентность.
Заключение
Комплексный топический антибактериальный назальный спрей Полидекса с фенилэфрином показал превосходящую клиническую эффективность и лучшую комплаентность в сравнении с интраназальным глюкокортикостероидом и антисептиком не только в лечении острого риносинусита легкого и среднетяжелого течения, но и в купировании симптомов постназального затека.
A.Yu. Ovchinnikov, N.A. Miroshnichenko, Yu.O. Nikolaeva, A.R. Umarov, A.V. Maslennikova
Russian University of Medicine
Contact person: Andrey Yu. Ovchinnikov, lorent1@mail.ru
Cough is the most common reason for contacting doctors of various specializations. The cause of cough in 54% of cases is «postnasal congestion syndrome» (PDS) caused by diseases of the ENT organs. Despite the fact that allergic and vasomotor rhinitis are the most common diseases of the upper respiratory tract (VDP), leading to the development of postnasal congestion syndrome, coughing can be accompanied by viral, bacterial and polypous rhinosinusitis. Cough in postnasal congestion syndrome worries the patient mainly at night and in the morning. This is due to the fact that at night, during sleep, in a horizontal position, the discharge flows into the larynx, irritates the reflexogenic zones and causes coughing. In the vertical position of the body, the discharge is reflexively swallowed and almost does not get on the epiglottis and vocal folds and does not cause coughing. Currently, the treatment of SDR is still a difficult task.
A clinical trial was conducted at the Department of Otorhinolaryngology of the Russian University of Medicine to expand the possibilities of conservative treatment of SPD with cough in the context of mild or moderate acute rhinosinusitis using a complex nasal spray Polydex with phenylephrine (Polydex with PHE). The study showed rapid relief of cough and improvement in the quality of sleep of patients, reduction in the frequency of taking vasoconstrictors and early withdrawal from their use, effective suppression of the growth of pathogenic microflora against the background of the use of Polydex spray with PE.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.