количество статей
7415
Загрузка...
Пожалуйста, авторизуйтесь:
Дабигатран против Варфарина у пациентов с искусственным клапаном сердца (результаты исследования RE-ALIGN)
Дабигатран против варфарина у пациентов с искусственным клапаном сердца (результаты исследования RE-ALIGN)
Предпосылки
В настоящее время антагонисты витамина К являются единственной доступной группой препаратов для лечения пациентов с механическими протезами клапанов сердца. Неадекватная степень антикоагуляции может привести как к тромботическим, так и к геморрагическим осложнениям. Кроме того, прием варфарина требует определенных ограничений в приеме алкоголя, продуктов питания и лекарственных препаратов, а также регулярного контроля МНО. Учитывая сложности пожизненного приема антагонистов витамина К, многие пациенты настаивают на имплантации биопротезов, хотя они более подвержены деградации, и значительно чаще требуют повторных операций по протезированию клапана.
Согласно результатам исследования RELY, дабигатран в дозе 300мг/сут оказался эффективнее варфарина в отношении предотвращения тромботических осложнений у пациентов с неклапанной мерцательной аритмией (при более благоприятном профиле безопасности).
В исследованиях на животных моделях дабигатран показал достаточно многообещающие результаты в отношении профилактики тромбоза клапана (рисунок 1).
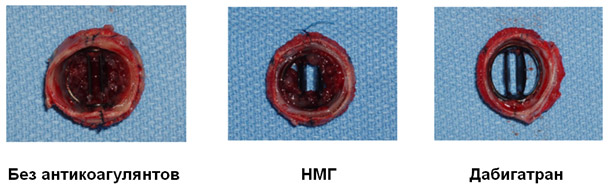
Рисунок 1. Тромбоз искусственных клапанов в зависимости от вида антикоагулянтной терапии (животные модели).
Цель данного исследования: изучить оптимальный режим дозирования дабигатрана у пациентов с двустворчатым механическим протезом клапана сердца (опираясь на фармакокинетическую модель из исследования RELY).
Методы
Исследование 2 фазы, открытое, проспективное, рандомизированное. Проводилось в 39 центрах 10 стран. Рассматривались 2 популяции пациентов: в первой (популяция А) пациентам выполнили протезирование клапана (аортального и/или митрального) не более 7 суток назад, вторым (популяция В) хирургическое вмешательство произвели как минимум 3 месяца назад.
Пациенты рандомизировались в соотношении 2:1 к приему дабигатрана или варфарина. Выбор дозы дабигатрана (150 мг, 220 мг или 300 мг дважды в день) основывался на исходной функции почек (соответственно, клиренс креатинина менее 70 мл/мин, 70-109 мл/мин и ≥110 мл/мин).
Кроме того, доза дабигатрана корректировалась таким образом, чтобы его концентрация в плазме не была ниже 50 нг/мл (с помощью прибора Hemoclot). Согласно исследованию RELY, такая (и большая) концентрация дабигатрана в плазме крови эффективна для предотвращения тромбозов. Если у принимающих максимальную дозу дабигатрана (300 мг 2 раза в день) не удавалось достичь требуемой концентрации, прием дабигатрана прекращали. Вообще, предполагалось подобрать такую дозу дабигатрана, при приеме которой минимальная концентрация препарата в плазме составила бы не менее 50 нг/мл более, чем у 90% пациентов.
Целевой диапазон МНО составлял 2-3 или 2,5-3,5 в зависимости от риска тромбоэмболических осложнений.
Первичная конечная точка – минимальная концентрация дабигатрана в плазме крови. Дополнительные конечные точки по эффективности и безопасности – инсульт, системная эмболия, транзиторная ишемическая атака (ТИА), тромбоз клапана, кровотечение, инфаркт миокарда (ИМ) и смерть. Клинические конечные точки анализировались «по намерению лечить» с использованием модели пропорционального риска Кокса.
Длительность наблюдения составила 12 недель. Предполагалось, что по окончании исследования участники могли быть по их желанию переведены на открытую терапию антагонистами витамина К, либо продолжить принимать исследуемые препараты в течение 84 месяцев в рамках исследования – продолжения RE-ALIGN-EX.
Результаты
Исследование было остановлено преждевременно на момент включения 252 пациентов в связи с большей частотой тромбоэмболических и геморрагических осложнений в группе дабигатрана.
Из 252 пациентов 168 были рандомизированы к приему дабигатрана, 84 –варфарина. По основным исходным характеристикам группы были сравнимы между собой. Большинство пациентов были из популяции А (199 пациентов). Протезирование аортального клапана выполнялось 172 пациентам (68%), митрального – 71 (28%), обоих – 9 (4%). У 79 пациентов риск тромбоэмболических осложнений был оценен как низкий, у остальных – как высокий.
В исследовании – продолжении приняли участие 99 пациентов, принимающих дабигатран, и 59 пациентов из группы варфарина. Суммарная длительность наблюдения в популяции А составила 143 дня в группе дабигатрана, 152 дня в группе варфарина, в популяции В - 136 и 143 дней, соответственно.
Исходная доза дабигатрана составила 150 мг у 15% пациентов, 220 мг –у 54%, 300 мг – у 31%. У 24% пациентов доза была впоследствии увеличена; у 8% препарат был отменен в связи с недостижением требуемой концентрации на максимальной дозе. Время пребывания концентрации дабигатрана более 50 нг/мл составило 86%, время пребывания МНО в целевом диапазоне на фоне приема варфарина – 49% и 51% популяциях А и В, соответственно. Концентрация дабигатрана первые 4 недели после рандомизации была ниже в популяции А, чем в популяции В.
Частота основных неблагоприятных событий представлена в таблице 1, а также на рисунках 1 и 2.
Таблица 1. Неблагоприятные события (отражающие эффективность и безопасность терапии) за все время наблюдения (включая исследование – продолжение RE-ALIGN-EX) в популяции «по намерению лечить».

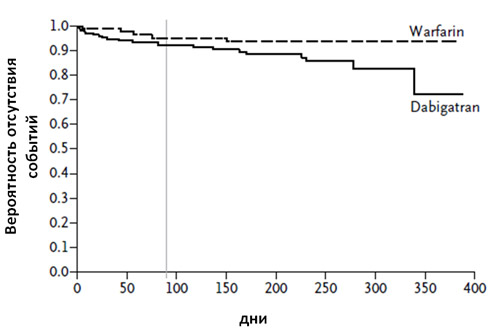
Рисунок 1. Кривая Каплана – Мейера, отражающая дожитие без неблагоприятных событий (инсульт, ТИА, СЭ, ИМ, смерть) в зависимости от терапии, р=0,24. (Вертикальная черта обозначает время начала исследования – продолжения).
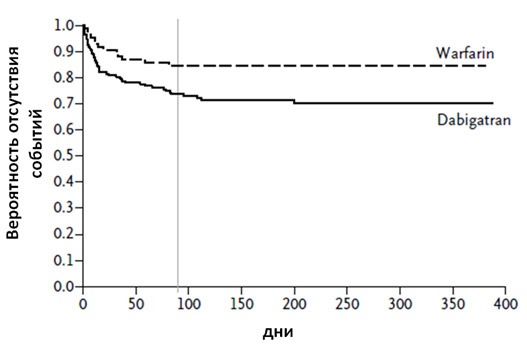
Рисунок 2. Кривая Каплана – Мейера, отражающая дожитие без развития кровотечений в зависимости от терапии, р=0,01. (Вертикальная черта обозначает время начала исследования – продолжения).
Больше тромбоэмболических событий на фоне приема дабигатрана произошло в популяции А. Кровотечения случались чаще на фоне приема дабигатрана в обеих популяциях. Большие кровотечения на фоне любого лечения происходили у пациентов, у которых рандомизация была выполнена через 1 неделю после операции. Все большие кровотечения являлись перикардиальными кровотечениями, произошедшими в течение 2 недель после операции.
При анализе пациентов «на лечении» частота неблагоприятных событий оказалась сопоставима. Не было выявлено связи между дозой дабигатрана и частотой ишемических и геморрагических осложнений.
Заключение и обсуждение
Применение дабигатрана у пациентов с механическими протезами клапана менее эффективно и безопасно, чем использование варфарина.
Причиной таких результатов может быть недостаточная доза дабигатрана, либо иной механизм действия, чем у варфарина.
В популяции А первые 4 недели после рандомизации концентрация дабигатрана была ниже, чем у тех же пациентов впоследствии. Низкая концентрация препарата могла быть причиной раннего формирования тромботических масс на клапане с последующими клиническими проявлениями. Однако тромбоэмболические события происходили и у пациентов с большей концентрацией дабигатрана, а также у пациентов популяции В, поэтому недостаточная концентрация препарата не может быть единственным достаточным объяснением этой клинической ситуации. Целевой уровень минимальной концентрации дабигатрана 50 нг/мл был выбран на основании результатов исследования RELY. Авторы не исключают, что более высокие значения целевой минимальной концентрации могли бы привести к снижению частоты ишемических событий. Правда, это могло бы привести к дальнейшему неприемлемому роста числа кровотечений, которые и так чаще происходят на фоне приема дабигатрана в прежней дозе. Возможно, более дробный прием дабигатрана (3 раза в день) без увеличения его суточной дозы мог бы привести к повышению минимальной концентрации и снижению пиковой концентрации, что, в свою очередь, могло бы стать основой для снижения частоты ишемических событий без увеличения числа кровотечений. Однако такой подход пока не тестировался.
Также причиной выявленных различий клинической эффективности варфарина и дабигатрана может быть разный механизм действия препаратов. В случае мерцательной аритмии тромб, в основном, формируется в ушке левого предсердий в условиях низкой скорости кровотока, низкого напряжения сдвига в стенке камеры сердца. Представляется, что в этих условиях генерация тромбина запускается стазом крови и эндотелиальной дисфункцией. У пациентов с протезированным механическим клапаном выработка тромбина происходит в ответ на высвобождение из повреждаемых во время операции структур тканевого фактора. Этот механизм частично объясняет высокий риск тромбоза в раннем послеоперационном периоде. Кроме того, происходит контактная активация коагуляции – тромбообразование в ответ на контакт крови с искусственными материалами протеза. Чаще тромбообразование происходит на опорном кольце протеза, которое подвергается эндотелизации лишь через несколько недель после имплантации. Поскольку варфарин ингибирует оба пути активации коагуляции – и контактный (путем ингибирования образования фактора IX), и связанный с высвобождением тканевого фактора (путем ингибирования образования фактора VII), а также ингибирует образование тромбина и X фактора, общих для обоих путей свертывания, он, по-видимому, оказывается эффективнее дабигатрана, ингибирующего только тромбин. Если контактная активация интенсивна, локальный уровень тромбина так высок, что концентрация дабигатрана в плазме оказывается недостаточной для предотвращения тромбообразования.
По материалам:
- RE-ALIGN: Dabigatraninpatientswithamechanicalheartvalve. Доклад на Европейском конгрессе кардиологов 2013. Авторы - Frans Van de Werf (Leuven, Belgium), Alec Vahanian (Paris, France).
- John W. Eikelboom, Stuart J. Connolly, Martina Brueckmann et al. Dabigatran versus Warfarin in Patients with Mechanical Heart Valves. September 1, 2013. DOI: 10.1056/NEJMoa1300615
Новости на тему
13.02.2025
14.05.2024
СТАТЬИ по теме
МЕРОПРИЯТИЯ по теме
НОВОСТИ этой компании
