количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Адъювантная терапия мышечно-неинвазивного рака мочевого пузыря
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Урология и Нефрология" №2
- Аннотация
- Статья
- Ссылки
В 2009 г. в России было выявлено 13 260 больных РМП (примерно 9,34 на 100 тыс. населения, средний возраст больных 67,0 лет) [1], общий прирост заболеваемости за последние 10 лет составил 22,57%, смертность от РМП в 2009 г. – 6933 человек.
К сожалению, выявляемость РМП на I стадии составляет не более 40%, несмотря на повсеместное распространение УЗИ, КТ и МРТ в лечебных учреждениях России.
Рак мочевого пузыря (РМП) занимает 8-е место в структуре онкологических заболеваний у мужчин и 18-е место – у женщин. Среди онкоурологических заболеваний РМП находится на втором месте после рака простаты.
В 2009 г. в России было выявлено 13 260 больных РМП (примерно 9,34 на 100 тыс. населения, средний возраст больных 67,0 лет) [1], общий прирост заболеваемости за последние 10 лет составил 22,57%, смертность от РМП в 2009 г. – 6933 человек.
К сожалению, выявляемость РМП на I стадии составляет не более 40%, несмотря на повсеместное распространение УЗИ, КТ и МРТ в лечебных учреждениях России.
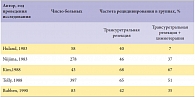
Таблица 1. Частота рецидивирования поверхностного рака мочевого пузыря при использовании Митомицина С в адъювантном режиме
- группа низкого риска: единичные опухоли TaG1 менее 3 см в диаметре;
- группа высокого риска: TaG1, множественные или часто рецидивирующие опухоли, Tis;
- группа умеренного риска: остальные поверхностные опухоли Ta-1, G1-2, множественные опухоли более 3 см в диаметре.
Адъювантная внутрипузырная химиотерапия (АВПХТ)
Препарат для внутриполостного лечения РМП должен обладать двумя основными свойствами: высокой противоопухолевой активностью по отношению к уротелиальному РМП и низкой системной и местной токсичностью. В настоящее время наиболее изученными и часто используемыми препаратами для ВХТ являются тиофосфамид, митомицин, доксорубицин, эпирубицин.
Тиофосфамид (Th iophosphamide)
Впервые сообщение о применении препарата как внутрипузырного агента при РМП принадлежит Jones и Swinney. Тиофосфамид обычно назначается в дозе 30–60 мг. Инстилляции препарата проводятся 1 раз в неделю в течение 6 недель. Лечение может быть продолжено до одного года с ежемесячной инстилляцией. При наличии симптомов острого цистита лечение должно быть приостановлено.
Доксорубицин (Doxorubicin)
Как внутрипузырный агент препарат используется в различных дозах от 30 до 100 мг. Схема введения: еженедельные инстилляции на протяжении 6–8 недель с внутрипузырной экспозицией 1–2 ч. Системные побочные реакции при внутрипузырном лечении выявляются редко и включают тошноту, рвоту, диарею (1,7%), повышение температуры тела (0,8%), аллергические реакции (0,3%). H. Akaza и соавт. [4], проанализировав результаты лечения более 600 больных, не выявили системных побочных эффектов при внутрипузырном назначении препарата. Местные побочные эффекты доксорубицина более выражены. При анализе 399 пациентов химический цистит был зарегистрирован у 28,8% больных. При применении высоких доз доксорубицина (8 еженедельных инстилляций по 100 мг) у 16% больных (7 из 44) отмечено уменьшение объема мочевого пузыря.
Эпирубицин (Epirubicin)
Препарат обычно вводится в дозе 30–80 мг. Схемы введения агента различны: одни авторы предлагают вводить ежедневно в течение 3 дней, затем делать перерыв 4 дня, далее – 3 ежедневных введения. Время экспозиции препарата в мочевом пузыре – 1–2 ч. М. Kuroda и соавт. оценили токсичность эпирубицина у 911 больных. У большинства пациентов была выполнена схема еженедельного введения препарата в дозе 50 мг. Проявлений системной токсичности зарегистрировано не было. Химический цистит был выявлен у 14% больных. Частота возникновения локальной токсичности зависит от дозы введенного препарата. При единственной инстилляции эпирубицина в дозе 80 мг циститы выявлены у 6,8% пациентов [5]. Также ряд авторов сообщают о минимальном количестве осложнений при внутрипузырной инстилляции препарата в дозе 30 мг еженедельно в течение 8 недель. В другом исследовании 43 пациентам были проведены 6 еженедельных инстилляций 50 мг эпирубицина. Лекарственный цистит был выявлен у 21% больных, срок наблюдения составил 2 года. Гематологической токсичности отмечено не было. Результат сравнительного исследования химиотерапевтических агентов показал большую эффективность и меньшую токсичность эпирубицина по сравнению с доксорубицином [6].
Митомицин (Mitomycin)
На сегодняшний день большое количество исследований посвящено использованию митомицина. Эффективность данного агента проверена при различных вариантах опухолей, в частности, при переходно-клеточном раке мочевого пузыря. Митомицин является антибиотиком, продуцируемым культурой грибов Streptomyces caespitosus, который после проникновения в клетку проявляет свойства би- и трифункционального алкилирующего агента, избирательно ингибируя синтез ДНК. В высоких концентрациях вызывает супрессию синтеза клеточной РНК и белка, главным образом в поздних (G1 и S) фазах митоза. Противопоказаниями к применению являются гиперчувствительность, тромбоцитопения, коагулопатия (в том числе тенденция к кровоточивости), беременность, кормление грудью, детский возраст. Ограничениями к применению являются нарушения функции костного мозга, печени, почек (уровень креатинина в сыворотке крови более 0,15 ммоль/л), предшествующее лечение цитотоксическими препаратами или лучевая терапия. Применение митомицина при некоторых инфекционных заболеваниях (ветряная оспа, опоясывающий герпес) может привести к тяжелым осложнениям.
Схемы лечения различны, доза может варьировать от 20 до 60 мг в 20–40 мл физиологического раствора еженедельно (до 8–10 доз). Оптимально однократное введение 20–40 мг препарата. Наиболее применимыми и хорошо изученными режимами введения являются внутрипузырная инстилляция препарата непосредственно после операции или в течение ближайших 24 часов, а также от 4 до 6 еженедельных инстилляций после операции. Длительность экспозиции химиопрепарата в полости мочевого пузыря составляет 1,5–2 часа. Целесообразность поддерживающей внутрипузырной химиотерапии (на протяжении 1–2 лет) является спорным вопросом, так как ряд исследований не показали значительного преимущества в частоте рецидивирования и длительности безрецидивного периода при использовании поддерживающей внутрипузырной химиотерапии [7, 8, 9].
Наиболее частыми побочными эффектами при внутрипузырном введении митомицина являются химический цистит и аллергические реакции. Характерный симптомокомплекс химического цистита включает учащенное мочеиспускание и боль. Эти симптомы проявляются в 6–41% случаев (в среднем в 15,8%). Митомицин имеет молекулярную массу, равную 329 D. Это обусловливает минимальную абсорбцию препарата из мочевого пузыря после инстилляций, что снижает системную токсичность. Лейкопения и тромбоцитопения выявляются только в 0,7% случаев. Известны случаи смертельного исхода от миелосупрессии при внутрипузырном введении 80 мг препарата непосредственно после ТУР мочевого пузыря. Аллергические реакции – везикулярные дерматиты рук, ног, генитальные дерматиты и более Митомицин имеет молекулярную массу, равную 329 D. Это обусловливает минимальную абсорбцию препарата из мочевого пузыря после инстилляций, что снижает системную токсичность. Лейкопения и тромбоцитопения выявляются только в 0,7% случаев. 41 ЭФ. Урология. 2/2011 Онкоурология широко распространенные высыпания – встречаются примерно в 9% случаев. Сморщивание мочевого пузыря наблюдается у 0,5% больных. В некоторых исследованиях отмечается бессимптомное образование кальцинатов в полости мочевого пузыря. В таблице 1 приведены данные о частоте рецидивирования поверхностного рака мочевого пузыря в контролируемых исследованиях при использовании митомицина в адъювантном режиме. Митомицин является перспективным химиотерапевтическим агентом, эффективность которого доказана в рандомизированных исследованиях.
Препарат Веро-митомицин (компания «Верофарм») является аналогом Митомицина С, выпускаемым в России. В исследование, проведенное проф. И.Г. Русаковым и соавт., были включены пациенты с мышечно-неинвазивным переходно-клеточным раком мочевого пузыря, с уровнем инвазии рТа, рТ1, степенью дифференцировки Gl–G2, ECOG 0 или 1, первичные опухоли были у 65,2%, рецидивные – у 34,8% пациентов, единичная опухоль была у 70% больных, множественные наблюдались у 30%. Уровень инвазии рТа отмечался у 42% больных, рТ1 – у 68; высокодифференцированный рак выявлен у 65,2% больных, умереннодифференцированный – у 34,8%. Рецидив рака после применения Веро-митамицина был выявлен в 39,1% случаев, прогрессирование опухолевого процесса (увеличение степени инвазии процесса из Та в Т1) – в 4,3%. Рецидивы развились через 12–16 месяцев. Осложнение в виде острого цистита выявлено в 8,7% (после 4 и 6 инстилляций препарата). Гематологической токсичности в исследовании отмечено не было [10].
Внутрипузырная иммунотерапия
С конца 80-х гг. ХХ века широко используется внутрипузырная иммунотерапия (ВИТ), основанная на применении рекомбинантных или нативных цитокинов. Наиболее хорошо изученными и широко применяемыми в практике являются рекомбинантные интерферон-альфа (ИФН-?) и интерлейкин-2 (ИЛ-2). Положительные результаты в виде увеличения безрецидивного периода были получены многими авторами при использовании высоких доз препаратов. Показана эффективность малых доз реальдирона и интрона А при длительной экспозиции препарата в мочевом пузыре. При ВИТ реальдироном рецидивы выявлены у 20% больных. Средний срок наблюдения составил 28,6 месяца. При использовании ИФН-? рецидивы возникли у 10% больных, срок наблюдения – 13,8 месяца [11]. Внутрипузырная БЦЖтерапия в адъювантном режиме, впервые предложенная Morales в 1976 г., обладает высокой эффективностью при поверхностных опухолях мочевого пузыря с высоким и средним риском развития рецидива и является методом выбора при проведении адъювантного лечения для данной категории больных.
Под воздействием живой вакцины происходит активация иммунокомпетентных клеток стенки мочевого пузыря с образованием БЦЖ активированных клеток-киллеров (ВАК-клетки). Минимальный срок, по истечении которого можно начинать лечение, – 2 недели. Доза БЦЖ для однократной инстилляции варьирует от 60 до 150 мг. Наиболее часто используется 6-недельный курс индукции, подразумевающий еженедельные инстилляции вакцины БЦЖ в мочевой пузырь. Через 2–3 месяца после инициального курса начинается проведение поддерживающей терапии, которая продолжается в виде ежемесячных инстилляций БЦЖ до 6 месяцев или более – до 1, 2, 3 лет. Осложнения БЦЖ-терапии обусловлены местным и системным действием вакцины. Более чем в 60% случаев выявляется цистит. Микроскопическая гематурия и пиурия присутствуют у пациентов на протяжении практически всего периода лечения. Лихорадка отмечается у четверти больных. Необходимо помнить о том, что не рекомендуется проводить очередную инстилляцию при наличии выраженных побочных реакций от предшествующего введения. Отсрочка на 1–3 недели от намеченного графика в данной ситуации не приведет к снижению эффективности лечения. Если последнюю инстилляцию больной перенес тяжело, необходимо рассмотреть вопрос о снижении дозы препарата на 1/2 или на 1/3 от начальной. Это позволяет снизить токсичность препарата на 20–30%, что подтверждается результатами различных исследований. В некоторых исследованиях утверждается, что подобное снижение дозы приводит к ухудшению выживаемости у больных с опухолями высокого риска, по данным других авторов – не влияет на прогноз заболевания. Особую опасность представляют системные токсические проявления БЦЖ-терапии. БЦЖ-сепсис возникает в 0,4% случаев и сопровождается быстрым нарастанием симптомов (высоким повышением температуры тела, болями в суставах, гипотонией) через 2 ч после инстилляции или травматичной катетеризации. Органоспецифическая манифестация может быть представлена эпидидимоорхитами, пневмонитами и гепатитами, которые возникают в 2–3% случаев и требуют госпитализации [12, 13].
Учитывая, что ВИТ с применением БЦЖ имеет высокую эффективность, в мире проводятся разнообразные исследования, направленные на снижение токсичности препарата. Это достигается следующими способами: 1) снижение дозы БЦЖ (до сверхнизких) и увеличение интервала между введениями; 2) комбинированная терапия с цитокинами; 3) совместное применение с внутрипузырными химиотерапевтическими агентами; 4) редукция курса лечения; 5) совместное использование БЦЖ и противотуберкулезных препаратов. Результаты рандомизированных исследований, в которых БЦЖ-вакцина сравнивалась по эффективности с тиофосфамидом, доксорубицином, продемонстрировали преимущество БЦЖ-терапии. Проведено 7 рандомизированных исследований по сравнению эффективности внутрипузырного лечения БЦЖ и Митомицином С [14, 15, 16]. Результаты показывают, что митомицин и БЦЖ могут применяться как внутрипузырные агенты первой линии при опухолях низкой и средней степеней злокачественности, но при наличии T1G3 или Tis предпочтение следует отдавать терапии с использованием БЦЖ. Юго-Западная онкологическая группа (SWOG) провела исследование по сравнению эффективности БЦЖ и доксорубицина: было выявлено 70% и 60% полных ответов соответственно; при наблюдении в течение 5 лет эти цифры уменьшились до 45% и 18%. Похожие цифры приводят P.U. Malmstom и соавт. при оценке 5-летней безрецидивной выживаемости: 55% и 26% при лечении БЦЖ и митомицином соответственно [3].
Метаанализ исследований, включавших 2749 пациентов со средней и низкой степенями дифференцировки опухоли [17], показал превосходство БЦЖ-терапии над терапией митомицином: безрецидивное течение в группе БЦЖ-терапии в течение первых 2 лет составило 61%, в группе митомицина – 53%. Однако токсический эффект, выявленный в результате сравнительных метаанализов рандомизированных исследований (n = 2820) [3] внутрипузырного применения митомицина и БЦЖ-терапии при мышечнонеинвазивном раке мочевого пузыря, показал:
- местная токсичность отмечалась у 30% пациентов, получавших митомицин, и у 44% пациентов после БЦЖ-терапии;
- в 12% и 19% случаев соответственно развились системные побочные эффекты, у 5% больных возникли тяжелые осложнения после БЦЖ-терапии;
- степень токсичности должна быть соизмерима с риском развития рецидива и прогрессии рака;
- проведение БЦЖ-терапии обосновано только у пациентов с высокой степенью риска.
Фотодинамическая терапия
Новым перспективным направлением терапии РМП является фотодинамическая терапия (ФДТ). Метод основан на селективном накоплении фотосенсибилизатора в опухолевых клетках с последующим их облучением лазером определенной длины, что приводит к их повреждению вследствие химических превращений фотосенсибилизатора. В России метод применяется сравнительно недавно. На сегодняшний день можно говорить о конкурентоспособности метода, его эффективность в предотвращении рецидивов поверхностного рака мочевого пузыря должны оценить последующие исследования. ФДТ по эффективности несколько уступает БЦЖ-терапии, но превосходит внутрипузырную химиотерапию. Важным преимуществом является возможность однократного облучения мочевого пузыря. По предварительным данным, применение фотодинамической терапии оправдано у пациентов с высокой и средней степенями риска [18].
Заключение
Адъювантная внутрипузырная БЦЖ-терапия обладает высокой эффективностью при поверхностных опухолях мочевого пузыря с высоким риском развития рецидива и является методом выбора при проведении адъювантного лечения данной категории больных. Адъювантная внутрипузырная химиотерапия является важным компонентом лечения мышечнонеинвазивного рака мочевого пузыря. ВХТ обладает высокой противорецидивной эффективностью у пациентов со средним и низким риском развития рецидива, имеет низкую частоту побочных эффектов при интравезикальном применении. Применение химиопрепаратов, в частности, Веро-митомицина, является менее токсичным методом профилактики рецидивов поверхностного рака мочевого пузыря в сравнении с БЦЖ-терапией.
1. Чиссов В.И. и др. Злокачественные новообразования в России в 2009 году (заболеваемость и смертность). М., 2011.
2. Van der Heijden A.G., Witjes J.A. Future strategies in the diagnosis, staging and treatment of bladder cancer // Curr. Opin. Urol. 2003. Vol. 13 (5). P. 389–395.
3. Malmstrom P.U., Sylvester R.J., Crawford D.E. et al. An individual patient data metaanalysis of the longterm outcome of randomized studies comparing intravesical Mitomycin C versus bacillus Calmette-Guerin for nonmuscleinvasive bladder cancer // J. European. Urol. Vol. 56. 2009. P. 247–256.
4. Akaza H. et al. Comparative analysis of shortterm and longterm prophylactic intravesical chemotherapy of superficial bladder cancer // Cancer Chemother. Pharmacol. 1987. Vol. 20. P. S91–S96.
5. Kuroda M., Niijima T. et al. Effect of prophylactic treatment with intravesical epirubicin on recurrence of superficial bladder cancer – The 6th Trial of the Japanese Urological Cancer Research Group (JUCRG): a randomized trial of intravesical epirubicin at dose of 20mg/40ml, 30mg/40ml, 40mg/40ml // Eur. Urol. 2004. Vol. 45. P. 600–605.
6. Ali-el-dein В. et al. Intravesical epirubicin versus doxorubicin for superficial bladder tumors (stages pTa and pTI): a randomized prospective study // J. Urol. 1997. Vol. 158 (I). P. 68–74.
7. Islam M.A., Bhuiyan Z.H., Shameem I.A. Intravesical adjuvant therapy using mitomycin C // Mymensingh Med. J. 2006. Vol. 15 (1). P. 40–44.
8. Divrik R.T., Yildirim U., Zorlu F., Ozen H. The effect of repeat transurethral resection on recurrence and progression rates in patients with T1 tumors of the bladder who received intravesical mitomycin: a prospective, randomized clinical trial // J. Urol. 2006. Vol. 175 (5). P. 1641–1644.
9. Gardmark T., Jahnson S., Wahlquist R., Wijkstrom H., Malmstrom P.U. Analysis of progression and survival after 10 years of a randomized prospective study comparing Mitomycin C and bacillus Calmette-Guerin in patients with highrisk bladder cancer // BJU Int. 2007. Vol. 99. P. 817–820.
10. Русаков И.Г., Быстров А.А., Теплов А.А., Перепечин Д.В. Адъювантная внутрипузырная химиотерапия Веро-митомицином. М.: МНИОИ им. П.А. Герцена, 2007.
11. Алексеев Б.Я. Внутрипузырная иммунотерапия поверхностного рака мочевого пузыря: Автореф. ... дис. канд. мед. наук. М., 1998.
12. Elmer A., Bermes U., Drath L., Buscher E., Viertel A. Sepsis and multiple organ failure after BCG-instillation for bladder cancer // Internist (Berl.). 2004. Vol. 45 (8). P. 935–939.
13. Soloway M.S., Masters S. Urothelial susceptibility to tumor cell implantation: influence of cauterization // Cancer. 1980. Vol. 46 (5). P.1158–1163.
14. Shelley M.D., Court J.B., Kynaston H., Wilt T.J., Coles B., Mason M. Intravesical bacillus Calmette-Guerin versus Mitomycin C for Ta and T1 bladder cancer // Cochrane Database Syst. Rev. 2003. Vol. (3). P. CD003231.
15. Jarvinen R., Kaasinen E., Sankila A., Rintala E. Longterm Efficacy of maintenance bacillus Calmette-Guerin versus maintenance Mitomycin C instillation therapy in frequently recurrent TaT1 tumours without Carcinoma in situ: a sub group analysis of the prospective, randomized finnbladder I study with a 20-year follow-up // J. European Urol. Vol. 56. 2009. P. 260–265.
16. Shelly M., Wilt T., Court J., Coles B., Kynaston H., Mason M. Intravesical bacillus Calmette-Guerin in superior to Mitimycin C in reducing tumour recurrence in high-risk superficial bladder cancer: a metaanalysis of randomized trials // BJU Int. 2004. Vol. 93. P. 485–490.
17. Bohle A., Joham D., Bock P.R. Intravesical bacillus Calmette-Guerin versus Mitomycin C for superficial bladder cancer: a formal meta-analysis of comparative studies on reccurence and toxicity // J. Urol. 2003. Vol. 169. P. 90–95.
18. Berger A.P. et al. Photodynamic therapy with intravesical instillation of 5-aminolevulinic acid for patients with recurrent superficial bladder cancer: a singlecenter study // Urology. 2003. Vol. 61 (2). P. 338–341.
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.