Дегидроэпиандростерон у мужчин: потенциальные физиологические эффекты с позиции доказательной медицины
- Аннотация
- Статья
- Ссылки
- English
Введение
Дегидроэпиандростерон (ДГЭА) и другие надпочечниковые андрогены были открыты в 1930–40-х гг. Долгое время им не придавалось существенного клинического значения в обеспечении андрогенного фона у мужчин, и они оставались практически не изученными вплоть до 1990-х гг., когда возник настоящий бум вокруг ДГЭА. Именно тогда появились работы, которые продемонстрировали, что назначение ДГЭА в физиологических (50 мг/сут) и фармакологических (200–400 мг/сут) дозах людям после 60 лет принципиально улучшает у них показатели качества жизни. В этой связи многие исследователи стали рассматривать ДГЭА как потенциальный антивозрастной гормон (гормон молодости). К настоящему времени опубликовано множество работ, посвященных физиологии, эндокринологии, клиническому применению ДГЭА. Однако пока, увы, нет однозначного ответа на главный вопрос о биологическом значении этого гормона в организме человека [1].
Сегодня продолжается активное изучение ДГЭА, и с каждым годом появляются все новые данные о важной роли надпочечниковых андрогенов (прежде всего ДГЭА) в обеспечении здоровья и долголетия человека. При этом интерес к ДГЭА особенно силен в США, где он классифицируется как пищевая добавка и продается без рецепта. В большинстве стран ДГЭА доступен только по рецепту врача [2]. В РФ препараты ДГЭА официально не зарегистрированы.
В статье обсуждаются физиологические функции ДГЭА по результатам преимущественно систематических обзоров и метаанализов, поскольку именно они составляют основу аналитической базы доказательной медицины.
Возрастная эндокринология дегидроэпиандростерона
К основным андрогенам, которые вырабатываются в сетчатой зоне коры надпочечников, относятся ДГЭА, его транспортная сульфатная форма ДГЭА-сульфат (ДГЭА-С) и андростендион [1]. В среднем ежедневно синтезируется 15–30 мг надпочечниковых андрогенов. Согласно одним источникам, эти стероидные гормоны не имеют каких-либо циркадианных (суточных) ритмов секреции, по другим данным, циркадианные ритмы секреции ДГЭА-С все же имеют место и пик концентрации ДГЭА-С приходится на ночное время. При этом не вызывает сомнений тот факт, что ДГЭА-С производится в надпочечниках только представителей отряда приматов (человека, высших и низших обезьян) [1].
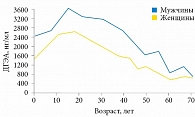
Секреция ДГЭА надпочечниками впервые повышается у детей в период адренархе в возрасте шести – восьми лет. Максимальный плазменный уровень циркулирующего в крови ДГЭА наблюдается между 20 и 30 годами, после чего его уровень у обоих полов начинает сокращаться примерно на 2% ежегодно. В итоге к 50 годам он уменьшается на 50%, к 70 годам – на 80%, к 90 годам – на 90% по отношению к возрасту 20–30 лет, что ассоциируется как с возрастным снижением устойчивости к стрессу, так и с нейродегенеративными, когнитивными и депрессивными нарушениями (рис. 1) [1, 3].
Ключевые эффекты дегидроэпиандростерона у мужчин с позиции доказательной медицины
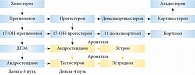
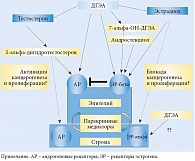
С момента открытия в 1930-х гг. и вплоть до 1990-х гг. ДГЭА и его транспортная сульфатная форма ДГЭА-С рассматривались у мужчин как слабые надпочечниковые андрогены. Их функциональный вклад в общий андрогенный фон считался клинически не значимым, в связи с чем физиологическая роль ДГЭА в мужском организме практически не изучалась [4, 5]. Долгое время считалось, что ДГЭА у мужчин выполняет исключительно функции прогормона (биохимического субстрата) в процессе синтеза тестостерона и далее эстрогенов, за что он и получил название «мать всех половых стероидных гормонов» (рис. 2) [6].
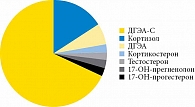
Однако современные исследования показали, что по концентрации в периферической крови среди всего спектра веществ стероидной структуры ДГЭА в норме уступает только холестерину, опережая прогестерон (своего предшественника) и кортизол – еще один важный гормон, который вырабатывается в клубочковой зоне коры надпочечников и отвечает за реализацию гормональных адаптационных механизмов организма к любой стрессовой реакции (гормон стресса). Так, концентрация ДГЭА в крови превышает содержание его конечных метаболитов: тестостерона у мужчин в 200–1000 раз, 17-бета-эстрадиола у женщин в 5000–25 000 раз (рис. 3) [1].
Как полагают исследователи, биологически подобное распределение ДГЭА и его метаболитов в крови у человека объясняется тем, что ДГЭА, будучи ключевым буферным гормоном стрессоустойчивости, представляет собой практически единственный естественный антиглюкокортикоидный гормон, противостоящий кортизолу – ключевому гормону стресса, приводящему к «синдрому обкрадывания» синтеза надпочечникового ДГЭА и тестикулярного тестостерона [7, 8].
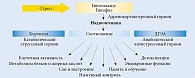
Соотношение «кортизол – ДГЭА» рассматривается как ключевой маркер устойчивости человека к стрессу. Для адекватной защиты от стресса ДГЭА, который характеризуется протективным эффектом по отношению к центральной нервной системе, всегда должен преобладать над кортизолом, который деструктивно влияет на гиппокамп [9, 10].
По данным некоторых исследований, низкий уровень ДГЭА в крови – одна из причин недостаточной стрессоустойчивости, нарастающей с возрастом, депрессии у подростков и пожилых людей, повышенной частоты суицидов, а снижение уровня циркулирующего ДГЭА и уменьшение соотношения «кортизол – ДГЭА» ассоциированы с ускоренным старением, депрессией, нарушениями памяти, синдромом хронической усталости, болезнью Альцгеймера (рис. 4) [8, 10].
В организме мужчин и женщин кроме традиционной выработки половых стероидных гормонов в половых железах (яичках и яичниках соответственно) есть и другой важный механизм обеспечения клеток периферических тканей необходимыми половыми гормонами – их самостоятельное производство «по требованию» из ДГЭА непосредственно внутри клеток некоторых органов и тканей, без участия системного кровотока и независимо от функциональной способности половых желез (яичек или яичников). Указанный механизм был открыт в 1988 г. канадским профессором Ф. Лабри и получил название интракринного периферического синтеза половых стероидных гормонов [11]. При этом типе гормональной клеточной регуляции половые стероидные гормоны образуются сразу внутри клеток и тут же оказывают соответствующее физиологическое действие [11]. Такой самостоятельный интракринный синтез половых стероидных гормонов происходит в клетках молочной и предстательной желез, головном мозге, мышечной ткани, коже, а у женщин еще и в эпителии влагалища. По мере старения гонад роль ДГЭА в обеспечении гормонозависимых клеток половыми стероидными гормонами за счет внутриклеточного интракринного синтеза возрастает. Так, именно из ДГЭА потенциально образуется до 35% тестостерона в периферических тканях у стареющих мужчин и до 80–100% тестостерона в гормонозависимых клетках у женщин в постменопаузе [12].
Поскольку ДГЭА является биохимическим субстратом для дальнейшего синтеза половых стероидных гормонов (тестостерона и эстрогенов) и подвергается интракринному метаболизму с образованием тестостерона и/или эстрадиола в клетках ряда органов и тканей, некоторые авторы предполагают, что дефицит ДГЭА у мужчин способен приводить к дефициту тестостерона и эстрогенов. Следовательно, назначение ДГЭА-заместительной терапии при возрастном дефиците ДГЭА может рассматриваться как физиологическая альтернатива заместительной терапии тестостероном у мужчин с возрастным дефицитом тестостерона [13, 14].
Однако с позиций доказательной медицины возможность использования ДГЭА-заместительной терапии изучена только у пожилых мужчин, что отражено в единственном доступном метаанализе 2013 г., охватившем результаты 25 клинических рандомизированных исследований (n = 1353) [15]. Средняя длительность терапии препаратами ДГЭА составила 36 недель. По данным метаанализа, ДГЭА-заместительная терапия у пожилых мужчин приводила к достоверному уменьшению жировой массы тела на фоне повышения уровней общего тестостерона и эстрадиола. Однако в мультивариационном регрессивном анализе связь между объемом жировой массы и уровнем ДГЭА не получила статистически значимого подтверждения. Достоверных эффектов ДГЭА-заместительной терапии в отношении липидного и углеводного обменов, костного метаболизма, сексуальной функции и качества жизни по сравнению с плацебо также не выявлено [15].
Тем не менее, согласно результатам исследований, накопленных к настоящему времени, ДГЭА можно рассматривать как самостоятельный полифункциональный гормон с достаточно широким спектром физиологических эффектов в организме, которые еще предстоит оценить с точки зрения доказательной медицины (рис. 5) [16].
Предстательная железа
С учетом описанных особенностей периферического метаболизма ДГЭА только 60% внутрипростатического 5-альфа-дигидротестостерона, ключевого андрогена предстательной железы, синтезируется из тестикулярного тестостерона, поступающего в железу из яичек с системным кровотоком, а 40% производится ими автономно (независимо от тестикулярного стероидогенеза) из тестостерона, синтезированного внутриклеточно из ДГЭА. При этом интракринный простатический синтез половых стероидных гормонов из ДГЭА выявлен как в железистом эпителии (тестостерон), так и в строме органа (эстрогены). Это объясняется тем, что ДГЭА, будучи биохимическим предшественником тестостерона, в строме простаты под влиянием стромальных ароматаз легко трансформируется в эстрогены [17].
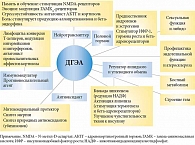
Согласно одной точке зрения, на фоне возрастного снижения уровня тестикулярного тестостерона предстательная железа, чтобы поддержать андрогенный гомеостаз, начинает активно использовать для синтеза 5-альфа-дигидротестостерона именно ДГЭА из крови. Дефицит ДГЭА, как и дефицит тестикулярного тестостерона, способен повышать активность 5-альфа-редуктазы, вызывающей простатическую пролиферацию [17]. Так сформировалась новая полигормональная эндокринно-аутокринно-интракринно-паракринная модель взаимодействия стромы и эпителия предстательной железы с учетом метаболизма в них ДГЭА. Это послужило основой для разработки рабочей гипотезы о том, что в патогенезе простатической пролиферации, характерной для доброкачественной гиперплазии предстательной железы и рака простаты, возрастной дефицит ДГЭА может играть столь же важную роль, как и возрастной дефицит тестикулярного тестостерона (рис. 6) [17].
Уникальность и сложность влияния ДГЭА на процессы пролиферации и воспаления в ткани предстательной железы состоят в том, что он является потенциальным субстратом как для синтеза тестостерона, так и (при необходимости) для трансформации в эстрогены за счет ароматазы стромы предстательной железы [18]. Роль эстрогенов в предстательной железе представляется достаточно сложной, поскольку зависит от локальных сигнальных механизмов, обеспечивающих баланс между эффектами двух типов рецепторов эстрогена – альфа и бета (в отличие от андрогенов, имеющих лишь один тип рецептора). Эстрогены вовлечены в локальную клеточную пролиферацию, воспаление и канцерогенез в предстательной железе путем, отличным от андрогенов. При этом рецепторы эстрогена альфа опосредуют неблагоприятные (негативные), а рецепторы эстрогена бета, соответственно, благоприятные (позитивные) эффекты в отношении воспаления, пролиферации и канцерогенеза в предстательной железе [18, 19].
Несмотря на известный факт о том, что возрастное снижение синтеза тестостерона у мужчин играет важную роль в патогенезе доброкачественной гиперплазии предстательной железы, существует гипотеза, согласно которой одним из гормональных механизмов простатической пролиферации может быть именно прогрессирующая с возрастом адреналовая недостаточность. Она сопровождается постепенным снижением синтеза прогестерона и особенно ДГЭА в надпочечниках, которые, будучи биохимическими предшественниками тестостерона, приводят к его дефициту. Вместе эти факторы, очевидно, запускают механизм активации 5-альфа-редуктазы, вызывающей простатическую железистую пролиферацию и гиперплазию предстательной железы [17, 20, 21].
Стресс
Различия в функционировании гипоталамо-гипофизарно-адренокортикальной системы у пациентов с посттравматическим стрессовым расстройством (ПТСР) и здоровых людей серьезно изучаются. Активация гипоталамо-гипофизарно-адренокортикальной системы приводит к выбросу в системный кровоток многих стероидных гормонов, включая ДГЭА, который метаболизируется в ДГЭА-С с выраженным антиглюкокортикоидным эффектом [22].
Чтобы выяснить, есть ли достоверные различия в базальных плазменных уровнях ДГЭА и ДГЭА-С на фоне ПТСР и без него, был проведен метаанализ, объединивший результаты ранее опубликованных исследований по этой теме. Были включены девять работ с данными об уровне ДГЭА (n = 486) и восемь работ с данными об уровне ДГЭА-С (n = 501). Анализы подгрупп для изучения связи между ПТСР и временем экспозиции травмы показали, что у пациентов с ПТСР по сравнению с контролем наблюдалась тенденция к более высокому уровню ДГЭА (k = 3, стандартизованная разность средних (СРС) = 1,12, 95%-ный доверительный интервал (ДИ) 0,03–2,52, Z = 1,91, p = 0,06) и достоверно более высокому уровню ДГЭА-С (k = 2, СРС = 0,76, 95% ДИ 0,38–1,13, Z = 3,94, p < 0,001). В группах контроля, подвергнутых травматическому воздействию, по сравнению с группами контроля без такового воздействия уровень ДГЭА был статистически значимо выше (k = 3, СРС = 0,66, 95% ДИ 0,33–0,99, Z = 3,88, p < 0,001, I2 = 86%). Авторы пришли к выводу, что воздействие травмы, независимо от дальнейшего развития ПТСР, увеличивает базальные уровни ДГЭА и ДГЭА-С, что объясняется проявлением универсальной реакции адаптации к стрессу и демонстрирует антистрессовые эффекты ДГЭА [22].
Метаанализ 2019 г. (108 исследований соответствующего качества, n = 6484) показал, что утренний и 24-часовой уровни кортизола в крови при ПТСР были достоверно ниже, чем в группе контроля (g = -0,21, 95% ДИ от -0,42 до -0,01 и g = -0,31, 95% ДИ от -0,60 до -0,03 соответственно). Значительный рост уровня кортизола наблюдался при ПТСР после пробуждения (g = 0,40, 95% ДИ 0,13–0,67) и в группе контроля без стрессового воздействия (g = 0,96, 95% ДИ 0,59–1,33). Вечерний уровень ДГЭА был достоверно выше при ПТСР, чем в группе контроля без стрессового воздействия (g = 0,58, 95% ДИ 0,17–0,99) [23].
Мышечная система
В свободном доступе удалось найти семь систематических обзоров и метаанализов, в которых тестировались десять фармакологических агентов для поддержания количества и качества мышечной массы: витамин D, комбинированный эстроген-гестагенный препарат, ДГЭА, гормон роста (соматотропин), рилизинг-гормон гормона роста, комбинация тестостерона и гормонов роста, инсулиноподобный фактор роста 1, сахароснижающий препарат пиоглитазон, тестостерон и ингибиторы ангиотензинпревращающего фермента. Важно отметить, что в немногих систематических обзорах или метаанализах четко указан исходный статус саркопении. В этой связи полученные результаты обобщены для пожилых людей в целом без уточнения эффекта при нормальной скелетной мускулатуре, предсаркопеническом состоянии или саркопении.
Так, прием витамина D благоприятно сказывался на мышечной силе и физической работоспособности у обоих полов, особенно у женщин с его низкими исходными значениями (< 25 нмоль/л в крови), причем редко вызывал побочные явления. Тестостерон оказывал достоверно сильное влияние на мышечную массу и от умеренного до минимального влияния на мышечную силу и/или физическую работоспособность (на результаты анализа повлияло включение мужчин с низким уровнем общего тестостерона в сыворотке крови (< 200–300 нг/дл)). Побочные явления на фоне его приема были редкими и умеренными. Для того чтобы рекомендовать другие фармакологические вмешательства при саркопении, доказательных данных, по мнению авторов метаанализа, явно недостаточно [24].
Костная система
Результаты последнего метаанализа свидетельствуют о том, что заместительная терапия ДГЭА может частично увеличить минеральную плотность костной ткани тазобедренного сустава и вертела лишь у женщин. Аналогичные результаты у мужчин не наблюдались. Для изучения клинически значимого влияния ДГЭА на минеральную плотность костной ткани необходимы дальнейшие доказательные исследования [25].
Нейропротекция и нейродегенерация
Несколько исследований подтвердили нейропротективные свойства ДГЭА и ДГЭА-С в различных экспериментальных моделях, включая модели мозговой ишемии, черепно-мозговой травмы, травмы спинного мозга, токсичности глутамата и нейродегенеративных заболеваний с точкой приложения эффектов в астроцитах головного мозга [26]. Поскольку астроциты отвечают за поддержание гомеостаза нервной ткани и контроль энергоснабжения нейронов, изменения астроцитарной функции связаны с повреждением нейронов и прогрессированием различных патологий [27, 28].
Сегодня известно, что ДГЭА – слабый андрогенный стероид, секретируемый не только корой надпочечников, но и тканью головного мозга, где он является посредником в биосинтезе андрогенов и эстрогенов [29].
По результатам кокрейновского обзора 2015 г., добавки ДГЭА не оказывают благоприятного влияния на когнитивные функции людей среднего или пожилого возраста без деменции. Однако ввиду особого общественного энтузиазма в отношении ДГЭА-заместительной терапии, особенно в США, и теоретически возможных пролонгированных нейропротективных эффектов ДГЭА авторы сочли целесообразным проведение в будущем высококачественных доказательных исследований эффектов ДГЭА, где прием добавок будет дольше (больше года), а число участников выше [30].
В клиническом рандомизированном исследовании с участием 225 мужчин и женщин среднего и пожилого возраста, которые в течение 12 месяцев принимали ДГЭА по 50 мг/сут, тоже не было выявлено никаких достоверных когнитивных преимуществ такой терапии по сравнению с плацебо [31].
Напротив, согласно данным метаанализа 2018 г., нейроактивные стероиды, включая тестостерон, ДГЭА и ДГЭА-С, могут играть важную роль в патофизиологии шизофрении. Метаанализ включал 34 исследования соответствующего качества, в которых приняли участие 1742 пациента и 1604 здоровых добровольца. Основной анализ выявил повышенные плазменные уровни ДГЭА-С у всех пациентов с шизофренией (95% ДИ 0,23–1,28, p = 0,005). У пациентов с первым эпизодом психоза уровни свободного тестостерона (95% ДИ 0,30–2,12, р = 0,009) и ДГЭА-С (95% ДИ 0,66–1,71, р < 0,001) были достоверно высоки. У больных с острым рецидивом шизофрении отмечался достоверно более высокий уровень общего тестостерона (95% ДИ 0,21–0,70, р < 0,001). При стабильной многоэпизодной шизофрении общий уровень тестостерона был увеличен у женщин (95% ДИ 0,33–0,80, p < 0,001) и снижен у мужчин (95% ДИ -1,07–0,18, p = 0,006). С учетом повышенных уровней биологически активного (свободного) тестостерона и ДГЭА-С у больных с первым эпизодом психоза можно предположить, что эти изменения могут быть ответом на стресс, который притупляется во время последующих обострений шизофрении. Различные изменения уровня общего тестостерона у мужчин и женщин со стабильной многоэпизодной шизофренией могут отражать индуцированные медикаментозно нарушения, вызванные влиянием антипсихотиков на пролактин [32].
Метаанализ 2019 г., включивший 31 доказательное исследование, не выявил статистически значимой связи между уровнем ДГЭА и болезнью Альцгеймера (СРС = 0,51, 95% ДИ от -0,44 до 1,45, Z = 1,06, p = 0,29). С другой стороны, более низкий уровень ДГЭА-С наблюдался именно у пациентов с болезнью Альцгеймера (СРС = -0,69, 95% ДИ от -1,17 до -0,22, Z = -2,84, p < 0,01). Авторы пришли к выводу, что снижение концентрации ДГЭА-С может быть важным показателем для болезни Альцгеймера, хотя вопрос о том, можно ли его использовать в качестве диагностического инструмента при данной патологии, требует дальнейшего изучения [33].
Депрессия
Такое психическое расстройство, как депрессия, затрагивает сегодня большую часть населения мира. ДГЭА издавна приписывали способность улучшать депрессивную симптоматику [29].
Метаанализ 2015 г. (десять клинических исследований «случай – контроль», 493 пациента с депрессией и 4003 здоровых добровольца) продемонстрировал более низкий уровень экспрессии белка ДГЭА-С у пациентов с депрессией (СРС = 0,17, 95% ДИ 0,06–0,27, p = 0,002). После стратификации по этнической принадлежности оказалось, что у кавказцев и азиатов не было низкого уровня экспрессии белка ДГЭА-С (р > 0,05). Тем не менее, по заключению авторов, повышение уровня экспрессии белка ДГЭА-С может коррелировать с биологической патофизиологией депрессии, в связи с чем определение уровня ДГЭА-С и дальнейшая ДГЭА-заместительная терапия могут способствовать эффективному лечению депрессии [34].
Последний метаанализ 2018 г. по этой теме основан на электронном поиске статей, опубликованных до июня 2018 г., по ключевым словам «дегидроэпиандростерон и депрессии» в базах данных Medline, Embase, Lilacs и Cochrane. Были включены только рандомизированные клинические исследования. Авторы отмечают значительный эффект лечения ДГЭА по сравнению с плацебо у больных с депрессией. Таким образом, ДГЭА-заместительная терапия может быть эффективной фармакологической альтернативой препаратам, традиционно используемым в лечении депрессии [35].
Иммунная система
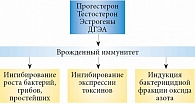
Многие исследования показали, что ДГЭА и ДГЭА-С связаны с различными аспектами иммунной системы и часто характеризуются как полезные и поддерживающие иммунокомпетентность гормоны (иммуномодуляторы) [36, 37]. Однако при ближайшем рассмотрении обнаруживается путаница в отношении модифицированных иммунологических компонентов, механизмов действия и его выраженности и даже в отношении того, имеют ли эти гормоны прямое влияние или их иммуномодулирующие эффекты опосредованы метаболитами и связями с другими гормонами и гормональными рецепторами. Кроме того, большая часть исследований проводилась на моделях грызунов с использованием высоких концентраций гормональных добавок. В результате они не всегда могут быть репрезентативными для эффектов этих гормонов в естественных концентрациях в циркулирующей крови или экстраполированы на физиологию человека. Тем не менее с учетом данных литературы, а также исследований, изучающих связь естественных циркулирующих уровней ДГЭА и ДГЭА-С и конкретных иммунологических компонентов и заболеваний, была высказана точка зрения, что ДГЭА оказывает достоверное позитивное дифференцированное действие на иммунную функцию человека, а его иммуномодулирующие эффекты зависят от уровня в крови других гормонов (рис. 7) [36].
Согласно результатам ряда доказательных исследований, ДГЭА может быть полезен как терапевтическое средство за счет способности уменьшать синтез провоспалительных цитокинов, в частности при заболеваниях с высоким уровнем системного хронического субклинического воспаления, например при ревматоидном артрите или вторичной гипофункции надпочечников [38–40].
Заключение
Как продемонстрировал проведенный обзор, доказательные исследования последних десятилетий позволили по-иному взглянуть на роль надпочечниковых андрогенов (прежде всего ДГЭА) как в норме, так и при ряде заболеваний и патологических состояний. ДГЭА уже не рассматривается исключительно как биохимический субстрат для дальнейшего синтеза в организме половых стероидных гормонов (тестостерона, эстрогенов). Исследования эндокринологии ДГЭА позволяют говорить о нем как о полифункциональном гормоне с широким спектром физиологических эффектов, многие из которых пока до конца не понятны и активно изучаются. Однако, опираясь на результаты имеющихся доказательных клинико-экспериментальных исследований, начатых в конце прошлого века и продолжающихся в настоящее время, можно утверждать, что у этого незаслуженно забытого гормона есть уникальные перспективы более активного клинического применения с целью профилактики и терапии ассоциированных с возрастом заболеваний. Вот почему, несмотря на противоречивые данные, изучение интракринологии и эффектов ДГЭА, несомненно, следует активно продолжать, поскольку это направление медицины имеет большое клиническое и научно-прикладное значение для обеспечения здоровья и активного долголетия современного человека.
I.A. Tyuzikov, PhD
Medical Center ‘Tandem-Plus’, Yaroslavl
Contact person: Igor A. Tyuzikov, phoenix-67@list.ru
The review article is devoted to the hormone dehydroepiandrosterone (DHEA) as a representative of the class of adrenal androgens, which are most rarely (in comparison with other hormones) mentioned in the domestic scientific literature, remaining insufficiently studied until now. From its discovery in the mid-twentieth century until its end, DHEA was considered solely as a biochemical starting substrate in the synthesis of testosterone and estrogens. However, studies that began in the 1990s and are still ongoing demonstrate broader physiological effects of DHEA in the human body. Based on systematic reviews and meta-analyses, the article examines the role of DHEA in certain diseases and pathological conditions of modern humans (stress, depression, neurodegeneration, etc.). Despite the contradictory nature of modern scientific publications on DHEA, it has been reliably confirmed the presence of such effects as anti-stress, antidepressant, immunomodulatory and a number of others, which are extremely necessary for a person to maintain health and active longevity.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.