Энцефалополирадикулоневрит у пациентки с болезнью Крона и синдромом Шегрена
- Аннотация
- Статья
- Ссылки
- English
В представленном исследовании описан клинический случай молодой женщины, у которой в течение одного года были последовательно диагностированы три иммуноопосредованных заболевания: синдром Шегрена, болезнь Крона и энцефалополирадикулоневрит. Особого внимания заслуживает развитие нейровоспалительного ответа с вовлечением центральной и периферической нервных систем на фоне сочетанного течения двух системных аутоиммунных патологий. Представлены клинико-анамнестические данные, результаты лабораторного и инструментального обследований, особенности терапии и динамики состояния. Проведен краткий патогенетический анализ возможных общих механизмов иммунной активации, лежащих в основе представленного сочетания патологий.
В представленном исследовании описан клинический случай молодой женщины, у которой в течение одного года были последовательно диагностированы три иммуноопосредованных заболевания: синдром Шегрена, болезнь Крона и энцефалополирадикулоневрит. Особого внимания заслуживает развитие нейровоспалительного ответа с вовлечением центральной и периферической нервных систем на фоне сочетанного течения двух системных аутоиммунных патологий. Представлены клинико-анамнестические данные, результаты лабораторного и инструментального обследований, особенности терапии и динамики состояния. Проведен краткий патогенетический анализ возможных общих механизмов иммунной активации, лежащих в основе представленного сочетания патологий.
Введение
В структуре внекишечных патологий неврологические проявления относительно редки, но при возникновении клинически значимы [1]. Поэтому в процессе ведения пациентов с воспалительными заболеваниями кишечника (ВЗК) должна сохраняться настороженность относительно потенциального развития нейропатических симптомов, что позволит обеспечить своевременную диагностику и адекватную терапию.
Среди неврологических симптомов ВЗК встречаются поражения как периферической, так и центральной нервной системы. Согласно статистическим данным, частота диагностирования ишемического инсульта при ВЗК может достигать 6,4%, среди пациентов моложе 17 лет – 20% [2]. Риск развития рассеянного склероза при ВЗК повышен примерно на 50% [2]. У 32–37% пациентов с ВЗК описаны изменения периферической нервной системы по типу мононевропатии, плексопатии, множественной мононевропатии, компрессионной невропатии, полиневропатии и краниальной невропатии [2]. Выраженность указанных симптомов не всегда связана с активностью кишечного воспаления [2].
В качестве патогенеза невропатий, ассоциированных с ВЗК, могут выступать несколько механизмов, включая изменение концентраций нейротрансмиттеров или собственных метаболитов мозга при особенностях микробиоты, что способно привести к нейродегенеративным процессам [3]. Известна роль влияния повышенной проницаемости кишечника и эндотоксемии, имеющей место при болезни Крона (БК), на гипоталамо-гипофизарную и вегетативную нервные системы: антигены, в большом количестве проникающие сквозь кишечную стенку в системный кровоток, модулируют иммунно-воспалительную реакцию организма больного с выделением провоспалительных цитокинов и возникновением системного ответа с возможной аутоиммунной атакой соединительных тканей организма [4]. Другими причинами появления неврологической симптоматики в данном случае могут послужить вторичные гематологические (гиперкоагуляция) и сосудистые патологии (васкулиты, тромбозы, тромбоэмболии сосудов головного мозга), иммунологические аномалии (сопутствующие аутоиммунные заболевания, хронические инфекционные процессы), побочные эффекты лекарственных препаратов, дефицит витаминов (В12, фолиевой кислоты), макро- и микронутриентов вследствие синдрома мальабсорбции, сопровождающего ВЗК [1, 3]. Стоит отметить, что при ВЗК значимо чаще, чем в популяции, встречаются аутоиммунный гепатит, первичный склерозирующий холангит, неалкогольная жировая болезнь печени, лекарственно-индуцированное поражение печени, тромбоз портальной и печеночной вен, абсцесс печени, амилоидоз печени и гранулематозный гепатит (а значит, и цирроз печени с печеночной энцефалопатией) [5].
Сочетание нескольких иммуновоспалительных заболеваний у одного пациента является редким, но клинически значимым феноменом и представляет собой важную клиническую проблему ввиду сложности диагностики, выбора лечебной тактики и прогностической неоднозначности. Чаще всего в рамках сочетанной аутоиммунной патологии наблюдаются комбинации органоспецифических заболеваний, таких как сахарный диабет 1-го типа, аутоиммунный тиреоидит и синдром Шегрена [6].
Менее типичным представляется одновременное или последовательное развитие сочетания воспалительных заболеваний кишечника и аутоиммунных поражений центральной и периферической нервных систем, особенно на фоне уже установленного системного аутоиммунного диагноза [7, 8].
Представленный клинический случай показывает уникальное сочетание болезни Крона, синдрома Шегрена и энцефалополирадикулоневрита, развившихся в течение года у пациентки молодого возраста.
Клинический случай
Пациентка А., 35 лет, поступила в гастроэнтерологическое отделение Республиканской клинической больницы (РКБ) Минздрава Чувашии 20.01.2023 г. с целью мониторинга состояния и уточнения тактики ведения в связи с ранее установленным диагнозом БК.
Из анамнеза жизни известно: росла и развивалась согласно возрасту, в 2017 г. перенесла кесарево сечение, эпидемиологический анамнез – без особенностей, вредных привычек не имеет. Наследственность по аллергическим, аутоиммунным заболеваниям не отягощена.
Из анамнеза заболевания: с 2018 г. стала отмечать появление сухости в глазах и во рту, с начала 2020 г. – появление периодических мелкоточечных высыпаний на ногах, самостоятельно купируемых, без участков остаточной гиперпигметации. В течение 2020 г. масса тела пациентки спонтанно снизилась на 17 кг (с 65 до 48 кг). Проконсультирована гематологом 31.07.2020 г. с диагнозом: «Вторичный васкулит (под вопросом). Железодефицитная анемия легкой степени тяжести».
30 декабря 2020 г. появилась боль в верхней части живота. 10 января 2021 г. пациентка обратилась к участковому терапевту, проведено двухнедельное лечение ингибитором протонной помпы (омепразол 20 мг по одной таблетке два раза в день) и полиферментными препаратами (микрокапсулированный панкреатин 10 000 Ед с каждым приемом пищи) с улучшением состояния. Во время лечения пациентка отметила повторное появление мелкоточечных высыпаний на ногах, была осмотрена гинекологом и инфекционистом, патологий не выявлено. По назначению ревматолога были проведены профильные исследования с результатами: антитела к экстрагируемому ядерному антигену 28.01.2021 г. − положительно, иммуноблот 28.01.2021 г. − SSA/Кщ-52 +++, SS − A (60 kДа) +++, SS В +++, антинуклеарный фактор 1 : 10 240 (< 1 : 160). От повторной консультации и лечения отказалась.
В конце января 2021 г. вновь появилась боль в верхней части живота, обратилась к гастроэнтерологу, терапевту, была направлена на консультацию хирурга, хирургической патологии на момент осмотра не выявлено.
10.03.2021 г. во время очередного приступа боли в эпигастральной области госпитализирована в хирургическое отделение Центральной районной больницы Алатырского района с диагнозом: «Хронический панкреатит. Геморрагический васкулит, хроническое течение с кожно-суставным и абдоминальным синдромами». На фоне терапии с 13 на 14 марта состояние ухудшилось: утром 14.03.2021 г. обнаружила слабость и онемение в левой и правой ногах и правой руке; с 15.03.2021 г. пациентка перестала ходить и двигаться; с 16.03.2021 г. зарегистрирована афазия. Переведена в РКБ Минздрава Чувашии для уточнения диагноза и дальнейшей тактики лечения.
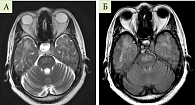
На магнитно-резонансной томограмме (МРТ) головного мозга (ГМ) пациентки с контрастным усилением от 16.03.2021 г.: обнаружены признаки диффузного объемного поражения моста (умеренное объемное увеличение моста, плотность его неоднородно повышена в Т2-, Т2-FLAIR-взвешенных изображениях (ВИ), после введения контраста выявляется его незначительное неравномерное накопление в мосту) (рис. 1).
В анализах ликвора изменений не выявлено. С 16.03.2021 г. начата терапия глюкокортикостероидами (ГКС) (солумедрол 500 мг № 6, с переходом на пероральный прием преднизолона 50 мг внутрь ежедневно с 23.03.2021 г.), коррекция нутритивного статуса (парентеральное питание с переходом на энтеральные методы коррекции), проведена коррекция нутритивного статуса. В общеклиническом и биохимическом анализах крови были отмечены: лейкоцитоз, ускорение скорости оседания эритроцитов до 44,00 мм/ч, гипокалиемия и повышение уровня С-реактивного белка до 11,3 г/л. В общем анализе мочи: протеинурия (1,77 г/л). Обращало на себя внимание увеличение концентрации фекального кальпротектина до 588,6 мкг/гр. В неврологическом статусе: выраженный тетрапарез, горизонтальный нистагм, небольшая гиперестезия по типу «удлиненных перчаток» и «гольф». С 25.03.2021 по 31.03.2021 г. получала эртапенем, с 30.03.2021 г. – ципрофлоксацин в стандартных дозах. Во время проведения антибактериальной терапии регистрировались подъемы температуры до 38,2 °С.
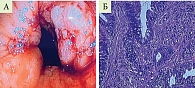
По результатам проведения фиброколоноскопии от 30.03.2021 г., заподозрен диагноз: «болезнь Крона; заболевание толстой кишки»; по заключению патоморфолога: солитарная язва кишечника с перифокальным воспалением высокой степени активности (рис. 2).
На фоне ГКС-терапии и коррекции нутритивного статуса отмечалась выраженная положительная неврологическая динамка: исчезновение нистагма, увеличение звучности голоса, увеличение мышечной силы конечностей. На МРТ ГМ от 26.03.2021 г.: уменьшение зоны перифокального отека и распространенности, контрастирование по периферии − менее четкое, местами менее интенсивное. Рекомендации к дальнейшему лечению включали продолжение приема ГКС, проведение повторной колоноскопии и МРТ ГМ с контрастированием через месяц. Выписана в удовлетворительном состоянии.
По заключению МРТ ГМ от 14.05.2021 г.: уменьшение сигнала перифокального отека в динамике от 26.03.2021 г., выраженное снижение интенсивности накопления контрастного вещества. Прием преднизолона 50 мг пациентка продолжила до июля 2021 г., затем доза постепенно была уменьшена до 30 мг (темп снижения – по 1/2 таблетки в две недели).
В связи с сохранением желудочно-кишечной симптоматики 11.06.2021 г. была проведена фиброколоноскопия, по результатам которой описана картина воспалительных изменений стенки, соответствующих среднетяжелой атаке БК в прямой кишке, ректосигмоидальном изгибе и в поперечно-ободочной кишке. Гастроэнтерологом по месту жительства диагноз подтвержден, назначена комплексная терапия азатиоприном (150 мг) и преднизолоном (20 мг) с положительным эффектом.
В связи с рецидивом кожного синдрома, а также учетом результатов ранее выполненных лабораторных тестов пациентка была госпитализирована и находилась на стационарном лечении с 01.02.2022 по 28.02.2022 г. в Научно-исследовательском институте (НИИ) ревматологии им. В.А. Hacoновой. Из заключения контрастной рентгенографии слюнной железы и протоков (сиалографии) от 07.02.2022 г.: выявлены признаки паренхиматозного паротита, сиалодохита. Из заключения ультразвукового исследования (УЗИ) слюнных желез от 09.02.2022 г.: лимфоузлы в околоушных слюнных железах увеличены; диффузно неоднородная структура слюнных желез; УЗ-признаки паренхиматозного сиаладенита (синдрома/болезни Шегрена). В условиях НИИ установлен диагноз: «болезнь Шегрена с поражением слезных желез (сухой кератоконъюнктивит, гиполакримия второй степени, эпителиопатия роговицы стадии III, микроэрозии), слюнных желез (хронический паренхиматозный паротит, ксеростомия стадии I, пришеечный кариес), иммунологической активностью (РФ+, высокопозитивные анти-Rо+, анти-Lа+, АНФ+), с внежелезистыми проявлениями в виде поражения центральной нервной системы (остаточные явления перенесенного энцефалополирадикулоневрита, атактический синдром смешанного генеза, мозжечково-сенситивная атаксия, двусторонний неврит зрительного нерва), суставов (артралгии), кожи (эритематозные высыпания)».
Заключение МРТ ГМ с внутривенным контрастированием от 10.02.2022 г.: при сравнении с исследованием от 16.03.2021 г. отмечается выраженная положительная динамика в виде уменьшения моста в размерах, отсутствия перифокальной реакции, замещения зоны патологической перестройки кистозным рубцом и отсутствием ее контрастирования, что позволяет включить в дифференциально-диагностический ряд демиелинизирующий процесс, нарушение мозгового кровообращения в бассейне вертебро-базиллярных артерий в анамнезе.
По результатам обследования рекомендована коррекция терапии основного заболевания с назначением препаратов: будесонид – 9 мг восемь недель с последующим использованием поддерживающей дозы в 6 мг длительно; преднизолон – 20 мг в сутки (выбрана тактика снижения дозы преднизолона по 1/4 таблетки в неделю до трех таблеток в сутки с последующим (через три месяца) решением вопроса о дальнейшем снижении дозы преднизолона).
27.02.2022 г. выполнено первое введение препарата ритуксимаб 1000 мг на 500 мл 0,9%-ного раствора NaCl с использованием премедикации дексаметазоном (16 мг внутривенно капельно) и хлорпирамином (20 мг внутривенно струйно) перед введением ритуксимаба без неблагоприятных лекарственных реакций после введения препарата. Через две недели произведено повторное введение ритуксимаба с последующей курацией пациента в Национальном медицинском исследовательском центре колопроктологии им. А.Н. Рыжих.
Следующая плановая госпитализация в РКБ Минздрава Чувашии ‒ 20.01.2023 г. По результатам фиброколоноскопии от 25.01.2023 г. выставлен диагноз: «Болезнь Крона в стадии ремиссии. Эритематозная колопатия». Заключение эзофагогастродуоденоскопии от 25.01.2023 г.: очаговый гастрит; дуоденит.
Проведено лечение с 20.01.2023 по 27.01.2023 г. в объеме: преднизолон 1,25 мг один раз в день, панкреатина микрогранулированного капсулированного 25 000 – 50 000 Ед, ингибитор протонной помпы в стандартной дозировке. Состояние на момент госпитализации удовлетворительное. По решению телемедицинской консультации пациентке выдано предписание для госпитализации в НИИ ревматологии им. В.А. Насоновой для повторного введения ритуксимаба.
Обсуждение
Представленный клинический случай демонстрирует редкий и показательный пример потенциальной взаимосвязанности иммуновоспалительных заболеваний, затрагивающих различные органы и системы, не ассоциированные между собой в традиционном понимании. Сочетание болезни Крона, синдрома Шегрена и энцефалополирадикулоневрита у одной пациентки в течение довольно ограниченного временного промежутка позволяет предположить наличие общего пускового механизма или перекрестных патогенетических каскадов.
Анализ возможных причин подобного сочетания симптомов дает возможность обобщения патогенетической картины для выявления наиболее перспективных векторов дальнейших исследований: персистирующее иммунное воспаление, нарушение гистогематических барьеров (в частности, гематоэнцефалического и кишечного), эндотелиальная дисфункция и активация врожденного и адаптивного иммунного ответов характеризуют все три патологических состояния у пациентки в представленном клиническом случае.
В современных исследованиях эндотелий рассматривают в качестве активного участника иммунорегуляции, отвечающего как за провоспалительные, так и за противовоспалительные механизмы [9, 10]. При аутоиммунных заболеваниях происходит фенотипическая трансформация эндотелиальных клеток в проинфламматорный тип, что способствует локализации воспаления, образованию самоподдерживающихся и самовоспроизводящихся иммунных «конгломератов» и, как следствие, поддержанию хронического воспаления.
В случае болезни Крона обнаруживаются признаки эндотелиальной активации и нарушенной васкуляризации в слизистой кишечника, особенно в фазе обострения [11].
Из этого следует, что эндотелиальная дисфункция может быть универсальным патогенетическим звеном, выступающим в качестве потенциального инициатора каскада иммуновоспаления в различных системах органов, являясь неким связующим механизмом, который присутствует в большинстве структур и тканей и регулирует практически все механизмы взаимодействия этих систем.
Описанный клинический случай дает основание предположить наличие общего клеточного или гуморального цитокинового каскада, который повлиял на развитие подобной картины у пациентки.
В настоящее время известно, что в болезни Крона и синдроме Шегрена задействованы клеточные пулы Th1/Th17. Болезнь Крона характеризуется активацией в основном Th1- и Th17-клеток с продукцией интерлейкина (ИЛ) 17, ИЛ‑22, а также фактора некроза опухоли α, ИЛ‑1β и ИЛ‑6. При синдроме Шегрена, в свою очередь, также наблюдается увеличение количества Th17-клеток и повышение уровней ИЛ‑17, ИЛ‑6 и ИЛ‑1β [12, 13].
Также имеются сведения, подтверждающие активацию сходного кинуренинового пути у пациентов с синдромом Шегрена и в моделях рассеянного склероза и экспериментального аутоиммунного энцефаломиелита [14, 15].
Остается открытым вопрос о возможном наличии конкретного молекулярного фактора или сигнального пути, обуславливающего сочетанную иммуновоспалительную патологию центральной нервной системы, желудочно-кишечного тракта и экзокринных желез. Дальнейшие исследования позволят расширить понимание формирования аутоиммунитета благодаря более обширной карте иммунорегуляции.
Клиническая значимость данного случая заключается не только в его редкости, но и в указании на необходимость понимания природы аутоиммунных заболеваний как проявлений единого патологического процесса, а не независимых нозологий. Углубление и расширение объема знаний о различных сочетаниях нозологий и, самое главное, о причинах подобного поведения иммунитета позволят создать ресурсы для предикции осложнений, более раннего выявления системной активности и индивидуализации терапии на основе понимания общих патофизиологических механизмов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Авторы заявляют об отсутствии источников внешнего финансирования при подготовке данной публикации.
Соблюдение этических принципов. Получено информированное согласие пациента на публикацию клинического случая.
L.V. Tarasova, PhD, A.A. Nikolaev, YU.V. Tsyganova, PhD, T.E. Stepashina
Chuvash State University, Cheboksary
Contact person: Larisa V. Tarasova, tlarisagast18@mail.ru
Immune-mediated diseases affecting multiple organ systems represent a significant diagnostic and therapeutic challenge. We present a clinical case of a young woman who was consecutively diagnosed with three immune-mediated conditions within one year: Sjogren's syndrome, Crohn’s disease, and encephalopolyradiculoneuritis. The case is notable for the development of neuroinflammatory involvement of both the central and peripheral nervous systems against the background of systemic autoimmune pathology. We provide clinical and anamnestic data, laboratory and instrumental findings, therapeutic interventions, and disease dynamics. A brief pathogenetic analysis of potential shared mechanisms of immune activation underlying this combination is presented.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.