Интравитреальное введение стероидного имплантата пациентам с лучевой ретинопатией при увеальной меланоме
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Поиск необходимых работ осуществлялся в базах данных PubMed и Scopus за период до 2025 г. включительно по ключевым словам: uveal melanoma (увеальная меланома), radiation maculopathy (лучевая макулопатия), steroid implant (стероидный имплантат), radiation therapy complications (осложнения лучевой терапии). Всего отобрано 16 статей.
Результаты. Проанализировав данные литературы, можно сделать вывод, что интравитреальное введение дексаметазонового имплантата на фоне развития лучевой ретинопатии при увеальной меланоме эффективно. Его введение ассоциируется со снижением высоты макулярного отека и улучшением показателей остроты зрения.
Заключение. Интравитреальное введение дексаметазонового имплантата является перспективным методом лечения лучевого макулярного отека, обеспечивающим снижение высоты макулярного отека и улучшение или стабилизацию зрительных функций.
Материал и методы. Поиск необходимых работ осуществлялся в базах данных PubMed и Scopus за период до 2025 г. включительно по ключевым словам: uveal melanoma (увеальная меланома), radiation maculopathy (лучевая макулопатия), steroid implant (стероидный имплантат), radiation therapy complications (осложнения лучевой терапии). Всего отобрано 16 статей.
Результаты. Проанализировав данные литературы, можно сделать вывод, что интравитреальное введение дексаметазонового имплантата на фоне развития лучевой ретинопатии при увеальной меланоме эффективно. Его введение ассоциируется со снижением высоты макулярного отека и улучшением показателей остроты зрения.
Заключение. Интравитреальное введение дексаметазонового имплантата является перспективным методом лечения лучевого макулярного отека, обеспечивающим снижение высоты макулярного отека и улучшение или стабилизацию зрительных функций.
Актуальность
Увеальная меланома (УМ) считается наиболее распространенной первичной злокачественной внутриглазной опухолью. Данное заболевание не только приводит к снижению зрительных функций, но и представляет угрозу для жизни пациентов из-за развития метастатической болезни [1]. Основными методами органосохраняющего лечения УМ являются лучевые технологии: брахитерапия (БТ), протонная терапия и стереотаксическая радиохирургия (СР) [2, 3]. Поскольку показатели выживаемости пациентов после энуклеации глаза и органосохраняющего лечения сопоставимы, последнее считается приоритетным в клинической практике [4].
Несмотря на высокую эффективность лучевой терапии (ЛТ) при УМ, ее применение ассоциируется с развитием осложнений, угрожающих зрению. ЛТ воздействует не только на злокачественные, но и на расположенные рядом здоровые клетки. Ионизирующее излучение повреждает ДНК клеток, после чего они утрачивают способность делиться и погибают. Однако повреждение ДНК может быть следствием прямого и непрямого (косвенного) действия излучения. Так формируется порочный круг: воспалительная реакция тканей, ишемия, изменение сосудов, кровоизлияние [5, 6]. Воспаление сосудистой оболочки, индуцированное ЛТ и опосредованное действием провоспалительных и проангиогенных цитокинов, приводит к повреждению сосудистого эндотелия и нарушению гематоретинального барьера. Как следствие, развивается отек сетчатки, что сопровождается снижением зрительных функций.
Лучевой макулярный отек (ЛМО) является наиболее частой причиной снижения зрения после ЛТ внутриглазных опухолей [7]. Данное состояние характеризуется накоплением жидкости в макулярной области сетчатки, что ведет к существенному ухудшению зрительных функций и снижению качества жизни пациентов [8]. Увеличение частоты выявляемости ЛМО в последние годы обусловлено как ростом числа пациентов, получивших лучевое лечение, так и совершенствованием методов диагностики офтальмологической патологии [9].
Особое внимание в лечении ЛМО, ассоциированного с воспалительными процессами, уделяется интравитреальному введению дексаметазона (ИВВД). Благодаря специализированной системе доставки действующего вещества достигается продолжительный терапевтический эффект. Снижая сосудистую проницаемость и подавляя экссудацию, ИВВД способствует улучшению зрительных функций [10].
Цель – проанализировать данные о частоте и особенностях развития лучевой ретинопатии у пациентов с УМ после ЛТ, а также оценить эффективность интравитреального введения имплантата дексаметазона для коррекции данного осложнения.
Первая линия лечения ЛМО дексаметазоновым имплантатом
Стероидные имплантаты обеспечивают пролонгированное высвобождение активного вещества, что позволяет поддерживать терапевтическую концентрацию стероидов в течение длительного времени и, соответственно, снижать кратность их введения.
В ряде исследований показано, что на фоне применения интравитреального триамцинолона ацетонида (ИТА) при ЛМО снижается высота ЛМО и увеличиваются показатели максимальной корригированной остроты зрения (МКОЗ). Однако эффект непродолжителен и требует повторного введения стероидов, что существенно увеличивает частоту побочных эффектов.
Первое упоминание об интравитреальном введении стероидов встречается в работе C.L. Shields и соавт. [11]. В проспективном нерандомизированном исследовании оценивали эффективность ИТА у 31 пациента с ЛМО после БТ на фоне УМ. Согласно результатам, на момент диагностики УМ большинство пациентов имели высокие показатели МКОЗ (в 90% случаев от 20/50 до 20/20). Средняя доза облучения на фовеолу составила 5,122 сГр (1,000–13,1000). ЛМО развился в среднем через 22 (6–96) месяца после лечения. После применения ИТА МКОЗ улучшилась или осталась стабильной у 20 (91%) пациентов через месяц и у 14 (45%) – через шесть месяцев. Авторы отметили, что ИВВД способно стабилизировать или улучшать МКОЗ у пациентов с ЛМО, хотя эффект может быть временным.
ИВВД применяют при манифестации ЛМО. Благодаря такой лекарственной форме эффект более продолжительный. При этом снижается частота не только инъекций, но и побочных эффектов.
S. Baillif и соавт. наблюдали пять пациентов с УМ после протонотерапии. Снижение центральной толщины макулы (ЦТМ) сопровождалось незначительным увеличением показателей МКОЗ. Авторы связали неудовлетворительные результаты с лучевым повреждением клеток сетчатки. Как следствие – низкие зрительные функции и отсутствие корреляции с хорошим анатомическим результатом [12].
В ретроспективном исследовании I. Koc и соавт. оценивали эффективность ИВВД у семи пациентов с лучевой макулопатией после стереотаксической ЛТ УМ. Трое из них ранее получали интравитреальные инъекции бевацизумаба (ИВИБ). Все пациенты отметили улучшение остроты зрения, а также значительное снижение отека сетчатки по данным оптической когерентной томографии (ОКТ). Исследование подтвердило, что ИВВД может быть эффективным средством контроля ЛМО [13].
В ряде работ интравитреальный имплантат флуоцинолона ацетонида (ИВИФА) применяли при ЛМО у пациентов с УМ после БТ. Так, в исследовании L. Zimmermann и соавт. анализировали эффективность ИВИФА у пациентов с ЛМО после ЛТ УМ. Пять пациентов, не ответивших на лечение триамцинолоном и стероидными имплантатами, получили ИВИФА. У всех пациентов отмечалось уменьшение высоты ЛМО, у 80% – улучшение остроты зрения. У одного пациента острота зрения осталась стабильной. Отсутствие побочных эффектов или осложнений и пролонгированное действие делают ИВИФА многообещающим вариантом лечения пациентов с ЛМО [14].
В литературе описан клинический случай применения стероидного имплантата при ЛМО после ЛТ УМ. F. Stringa и соавт. проанализировали данные 46-летней пациентки с ЛМО после протонотерапии УМ. Авторы оценивали МКОЗ и центральную толщину сетчатки (ЦТС) в течение 16 месяцев. ЛМО возник через 25 месяцев после протонной ЛТ. Перед инъекцией показатели МКОЗ составляли 6/12, а толщина нейроэпителия (НЭ) – 502 мкм. Через восемь месяцев МКОЗ улучшилась до 6/6 и оставалась стабильной, ЦТС составила 269 мкм. Исследование показало, что имплантат дексаметазона эффективно улучшает зрение и снижает ЦТС у пациентов с ЛМО на срок до 16 месяцев [15].
И.Е. Панова и соавт. провели ретроспективный анализ данных 28 пациентов с ЛМО после БТ УМ. Пациенты были разделены на две группы в зависимости от срока развития ЛМО после БТ – до девяти месяцев (n = 18) и свыше девяти месяцев (n = 10). Авторы зафиксировали статистически достоверную разницу между двумя группами по результатам ОКТ: при сроке до девяти месяцев чаще встречалась отслойка НЭ (p < 0,005), при сроке свыше девяти месяцев – гиперрефлективные очаги (p < 0,005), дезорганизация внутренних слоев сетчатки (p < 0,005) и нарушение зоны эллипсоида (p < 0,005). Всем пациентам выполнялось ИВВД. Эффективность инъекций определяли с учетом срока развития ЛМО после БТ. В первой группе наблюдался полный регресс, во второй – частичный. Авторы связали это с ведущей ролью воспалительного компонента в патогенезе ЛМО на ранних этапах его развития [16].
В.А. Яровая и соавт. провели статистический анализ эффективности использования дексаметазонового имплантата у 130 пациентов с ЛМО, развившимся после БТ УМ [17]. После применения ИВВД отмечалось улучшение функционального (p = 0,039) и анатомического результата (p < 0,001). Положительный эффект зафиксирован в 83 (64%) случаях. Тем не менее у 47 (36%) пациентов ИВВД не оказало должного эффекта, что требует дополнительных исследований. В клиническом исследовании представлен один из крупнейших на сегодняшний день отечественных опытов применения интравитреального дексаметазонового имплантата у пациентов с ЛМО, развившимся после ЛТ УМ. В исследование было включено 130 пациентов (130 глаз), что существенно превышает объемы выборок в большинстве ранее опубликованных работ по данной тематике. Авторы провели детальный клинико-инструментальный анализ с использованием ОКТ и стандартизированных показателей зрительных функций. Статистическая обработка выполнена с применением параметрических и непараметрических методов с предварительной оценкой нормальности распределения данных, что обеспечивает высокую достоверность полученных результатов. Показано статистически значимое снижение ЦТС и объема макулярного куба, а также улучшение и стабилизация МКОЗ после ИВВД.
Несмотря на явное преимущество стероидного имплантата в виде продолжительного действия, работ, посвященных лечению ЛМО, крайне мало. Кроме того, выборка пациентов немногочисленна. В шести проанализированных исследованиях применение интравитреальных стероидов продемонстрировало эффективность как в анатомическом, так и в функциональном результате у пациентов с ЛМО после ЛТ. И.Е. Панова и соавт., предпринявшие попытку провести статистический анализ, определили ОКТ-признаки, характерные для ЛМО в зависимости от срока его развития после БТ. Однако обоснование границы анализа в девять месяцев не представлено, как и статистический анализ в отношении эффективности стероидной терапии, что может быть связано с малой выборкой пациентов [16]. Исследование В.А. Яровой и соавт. с участием 130 пациентов, продемонстрировавшее клиническую эффективность ИВВД при ЛМО, является методологически обоснованной работой с достаточной выборкой пациентов и корректным статистическим анализом. Это означает, что полученные результаты имеют высокую доказательную ценность [17].
Стероиды при резистентных формах ЛМО
Ряд работ посвящен применению интравитреальных инъекций стероидов при неэффективности другой терапии или резистентности к ней. Так, J.M. Caminal и соавт. [18] назначали интравитреальные инъекции стероидного имплантата 12 пациентам с ЛМО, развившимся после БТ йодом-125 (I-125). У девяти пациентов наблюдалось развитие ЛМО, рефрактерного к проводимой терапии: двум из них ранее проводилась лазерная коагуляция сетчатки (ЛКС), другие два пациента получали анти-VEGF-терапию, пяти пациентам выполнена сочетанная ЛКС и анти-VEGF-терапия. Три пациента ранее не получали лечения. Снижение толщины НЭ было статистически достоверным (р = 0,016), в то время как улучшение показателей МКОЗ имело тенденцию к достоверности (р = 0,091). Между группами с первичным и вторичным введением стероидного имплантата разницы в статистической достоверности не установлено. В течение наблюдаемого периода у двух пациентов диагностирована стероид-ассоциированная катаракта, у одного пациента – повышение уровня внутриглазного давления (ВГД).
K.M. Bui и соавт. [19] опубликовали клинические случаи двух пациентов с ЛМО, устойчивым к интравитреальной анти-VEGF-терапии и ИТА. Применение стероидного имплантата у этих пациентов позволило добиться продолжительного анатомического результата. У одного пациента наблюдалось повышение зрительных функций. Применение ИТА ассоциировалось с резким повышением МКОЗ наряду со снижением высоты НЭ, однако эффект оказался непродолжительным, что потребовало ряда повторных инъекций. С увеличением частоты инъекций возрастает частота побочных эффектов стероидов – катаракта и офтальмогипертензия. По мнению авторов, преимущество стероидного имплантата с учетом лекарственной формы препарата, медленного высвобождения и продолжительного воздействия на сетчатку очевидно.
L. Tarmann и соавт. [20] сообщили о четырех пациентах, у которых развился ЛМО и при этом не было ответа на проводимую анти-VEGF-терапию. Во всех случаях наблюдали снижение высоты ЛМО. У двух пациентов улучшилось зрение. В одном случае отмечался побочный эффект в виде повышения уровня ВГД, который был купирован местными гипотензивными каплями. Однако выборка пациентов ограниченна, что указывает на необходимость проведения дополнительных исследований для подтверждения имеющихся результатов.
В исследовании S.J. Bakri и соавт. [21] рассматривался эффект лечения ИВИБ и ИТА при ЛМО. Исследование проводилось в формате клинических случаев. Были проанализированы данные пяти пациентов с ЛМО, получавших сначала анти-VEGF-терапию, затем ИТА. Согласно результатам, у первого пациента наблюдалось полное разрешение ЛМО после первых двух инъекций анти-VEGF-препаратов с уменьшением ЦТС с 340 до 243 и 284 мкм. Однако эффект снизился после дальнейших инъекций, и пациент был переведен на ИТА с положительным ответом. Средняя ЦТC после четырех инъекций ИТА составила 249 мкм, а зрение улучшилось на три строчки. У второго и третьего пациентов наблюдалась частичная реакция на анти-VEGF-препараты с уменьшением ЦТС, но без улучшения зрения. Второго пациента перевели на комбинацию анти-VEGF и ИТА, что привело к полному разрешению ЛМО. Четвертый и пятый пациенты не ответили на анти-VEGF-терапию, но хорошо отреагировали на ИТА с полным разрешением отека и стабилизацией/улучшением зрения. Авторы сделали вывод, что анти-VEGF-терапия и ИТА имеют нестабильный эффект в снижении высоты ЛМО. Анти-VEGF-терапия может уменьшать отек, но с течением времени развивается резистентность. ИТА оказался эффективным у трех из пяти пациентов, а на фоне применения комбинации анти-VEGF-терапии и ИТА полностью разрешился отек у одного пациента, что может быть обусловлено различными механизмами действия данных препаратов.
В исследовании R.I. Kaplan и соавт. [22] оценивалось влияние адъювантной терапии ИТА на ЛМО, устойчивый к применению бевацизумаба, у пациентов с УМ после БТ. Восемь пациентов (восемь глаз), не реагировавших на бевацизумаб, получили инъекции ИТА с интервалом от четырех до 16 недель. Результаты показали, что острота зрения оставалась стабильной или улучшилась у 100% пациентов через три месяца, у 88% – через шесть и девять месяцев, у 75% – через 12 месяцев. ЦТС уменьшилась с 417 до 339 мкм через месяц. Авторы отметили, что ИТА эффективен в сохранении зрения и уменьшении ЛМО, устойчивого к анти-VEGF-препаратам, у пациентов с УМ. Эту закономерность авторы объясняют различными свойствами препаратов. В частности, анти-VEGF-препарат подавляет VEGF, тем самым увеличивая активность других цитокинов [10]. ИТА в силу антицитокиновых свойств снижает уровень VEGF, который вырабатывается в условиях гипоксии. Кроме того, ИТА способствует восстановлению целостности гематоретинального барьера, увеличивая количество плотных соединений, что уменьшает выход жидкости из сосудов в межклеточное пространство. ИТА также повышает уровень аденозина, что способствует снижению осмотического набухания клеток Мюллера [22].
В ретроспективном исследовании N.V. Shah и соавт. [23] рассматривались данные пациентов с ЛМО после БТ с использованием I-125 для лечения УМ. Из 186 пациентов с ЛМО после БТ при УМ 25 (13%) получали комбинированную терапию ИТА и ИВИБ. В среднем пациенты получили две инъекции ИТА (1–6) и 8,8 ИВИБ (1–26) в течение 30 месяцев (от 10 до 54 месяцев). Средний срок развития ЛМО у этих пациентов составил 14,5 месяца. Состояние ЦТС оценивали с помощью спектральной ОКТ с интервалами 2–4 месяца после БТ. Лечение ИВИБ начиналось при первых признаках ЛМО, а ИТА назначали в случае недостаточного эффекта от анти-VEGF-терапии. Текущее исследование показало, что у пациентов с резистентным ЛМО, часто не поддающимся лечению анти-VEGF-препаратами, инъекции ИТА могут быть эффективны. При использовании комбинированного лечения у трети пациентов улучшилась МКОЗ до 20/50, у большинства пациентов МКОЗ оставалась стабильной. Однако существует группа пациентов, у которых, несмотря на анатомическое улучшение, МКОЗ не увеличивается.
Ряд исследований показывают эффективность интравитреальных стероидов у пациентов с ЛМО при резистентности к aнти-VEGF-препаратам. Из шести опубликованных работ статистический анализ представлен лишь в исследовании J.M. Caminal и соавт. [18], в котором было достоверно доказано уменьшение толщины центральной зоны сетчатки (р = 0,016). Увеличение показателей МКОЗ имело тенденцию к достоверности (р = 0,091). Отсутствие статистического анализа в других работах может быть связано с недостаточной для статистики выборкой пациентов, что подчеркивает важность оценки эффективности и безопасности при проведении большого клинического исследования.
Сравнительный анализ анти-VEGF-терапии и стероидного имплантата
Ряд работ посвящен сравнению эффективности анти-VEGF-терапии и стероидного имплантата. Так, R. Parrozzani и соавт. [24] сравнивали регрессию экссудативной отслойки сетчатки у 96 пациентов после лечения УМ БТ I-125, а также безопасность терапии. Пациенты были поровну разделены на три группы – анти-VEGF-терапии, ИТА и контрольную (инъекции не проводились). Статистически достоверная разница в анатомическом результате наблюдалась между группами ИТА и анти-VEGF-терапии (р = 0,0007), а также между группой ИТА и контрольной группой (р = 0,0001). И в том и в другом случае наилучший результат наблюдался в группе ИТА. В течение всего периода наблюдения у семи из 96 пациентов развилась вторичная неоваскулярная глаукома (три случая в контрольной группе, три – в группе анти-VEGF-терапии и один – в группе ИТА). У 11 пациентов выявлены метастазы в течение 27 ± 6 месяцев после БТ. Не зарегистрировано ни одного случая продолженного роста. Несмотря на эффективность интравитреальных инъекций стероидов, зафиксированы побочные эффекты – стероид-ассоциированная катаракта у четырех из 32 пациентов. Офтальмогипертензия не зарегистрирована.
В ретроспективном исследовании I. Seibel и соавт. [25] также оценивались клинические исходы у 78 пациентов, получавших ИВИБ (n = 38), ИТА (n = 35), стероидные имплантаты (n = 5) для лечения лучевой макулопатии после протонотерапии. Результаты показали, что во всех группах статистически достоверно снизилась ЦТМ (р = 0,01, р = 0,0034, р = 0,049 соответственно). Статистически достоверной разницы в эффективности лечения между группами не зарегистрировано. В частности, не обнаружено значимых различий в показателях МКОЗ на момент манифестации (р = 0,530), перед инъекцией (р = 0,780), через четыре недели после последней инъекции (р = 0,871) и на последнем визите (р = 0,792). Анатомический результат также не показал статистически значимых межгрупповых различий (р = 0,757).
В одном из исследований A. Russo и соавт. [26] показано, что применение интравитреального ранибизумаба (восемь пациентов) и ИВВД (восемь пациентов) при ЛМО после БТ привело к положительному анатомическому и функциональному результатам. Показано, что при использовании интравитреального стероидного имплантата требовалось меньшее количество инъекций для достижения необходимого эффекта.
Представленные исследования, посвященные сравнительной оценке эффективности интравитреальной анти-VEGF-терапии и ИВВД, продемонстрировали, что на фоне применения этих препаратов снижается высота НЭ и увеличиваются функциональные показатели. Во многих исследованиях не зафиксировано статистически достоверной разницы в эффективности данных препаратов [25, 26]. На различия указали R. Parrozzani и соавт. [24], которые лучший анатомический результат наблюдали в группе инъекций стероидов (р = 0,0007), но не в группе анти-VEGF-терапии. Между тем небольшая выборка пациентов в рассмотренных исследованиях делает статистический анализ ограниченным.
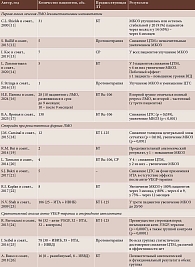
Краткая характеристика исследований, посвященных терапии ЛМО и вошедших в анализ, представлена в таблице.
Заключение
Лучевой макулярный отек является основной причиной снижения зрительных функций у пациентов после органосохраняющего лечения УМ и представляет собой одно из наиболее тяжелых и клинически значимых постлучевых осложнений. ЛМО существенно ухудшает качество жизни пациентов и требует своевременного патогенетически обоснованного лечения.
Как показывает анализ опубликованных исследований, интравитреальное введение дексаметазонового имплантата рассматривается в качестве перспективного метода лечения ЛМО, обеспечивающего редукцию макулярного отека и улучшение или стабилизацию зрительных функций. Вместе с тем доказательная база метода остается ограниченной ввиду малочисленности выборок, отсутствия стандартизированных критериев оценки эффективности и в ряде случаев недостаточного статистического анализа.
В связи с этим особую значимость приобретают работы, выполненные на репрезентативном клиническом материале с применением корректных статистических методов и позволяющие объективно оценить эффективность и безопасность интравитреального введения дексаметазонового имплантата у пациентов с ЛМО после лучевой терапии УМ. Результаты таких исследований служат основой для перехода от эмпирического применения препарата к разработке клинически обоснованных алгоритмов лечения.
Несмотря на возрастающий интерес к использованию стероидных имплантатов при ЛМО, в настоящее время отсутствуют единые рекомендации по срокам, режимам и показаниям к их применению, а также данные о долгосрочных анатомо-функциональных результатах на больших выборках пациентов. Это указывает на необходимость дальнейших проспективных исследований, направленных на выявление факторов риска развития ЛМО, предикторов эффективности терапии и оптимизацию тактики ведения пациентов.
Таким образом, дальнейшее накопление клинических данных и проведение методологически выверенных исследований – две важные составляющие формирования доказательной базы и внедрения интравитреального введения дексаметазонового имплантата в стандарты лечения ЛМО у пациентов с УМ.
E.O. Malakshinova, V.A. Yarovaya, PhD, A.A. Yarovoy, PhD, S.V. Zhidkov
Interdisciplinary Scientific and Technical Complex ‘Eye Microsurgery’ named after Academician S.N. Fedorov
Contact person: Ekaterina O. Malakshinova, ekaterinamalakshinova@yandex.ru
The aim is to analyze data on the development of radiation retinopathy in patients with uveal melanoma after radiation therapy and the effectiveness of intravitreal administration of dexamethasone implant.
Material and methods. The search for the necessary work was carried out in the PubMed and Scopus databases for the period up to and including 2025 using the keywords: uveal melanoma, radiation maculopathy, steroid implant, radiation therapy complications. A total of 16 articles were selected.
Results. After analyzing the literature data, it can be concluded that intravitreal administration of dexamethasone implant against the background of the development of radiation retinopathy in uveal melanoma is effective. The introduction of such an implant is associated with a decrease in the height of macular edema and an improvement in visual acuity.
Conclusion. Intravitreal injection of dexamethasone implant is a promising method of treatment of radial macular edema, providing a reduction in the height of macular edema and improvement or stabilization of visual functions.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.