количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Использование Вигамокса в лечении микробных кератитов, явившихся следствием осложнений при ношении контактных линз
Эффективная фармакотерапия. Офтальмология. №1
- Аннотация
- Статья
- Ссылки
Любой подозрительный роговичный инфильтрат следует лечить как микробный кератит (пока не будет доказана его неинфекционная природа), поскольку задержка в лечении микробного кератита существенно ухудшает течение болезни. Согласно данным зарубежных и отечественных исследований, при микробном кератите препаратами первого выбора являются антисептики в комбинации с фторхинолонами 4-го поколения. Для оценки эффективности и безопасности препарата Вигамокс (моксифлоксацина гидрохлорид) было проведено исследование с участием 58 амбулаторных пациентов (102 глаза) с различными клиническими проявлениями синдрома «красного глаза» в возрасте от 14 до 48 лет. В качестве антимикробной терапии использовали пиклоксидин (Витабакт 0,05%), антибактериальной – Вигамокс. Препараты применяли по следующей схеме: а) первый этап (начальная терапия) – в течение первых 48 часов оба препарата закапывали каждый час (с перерывом на ночь); б) второй этап – инстилляции обоих препаратов 4 раза в сутки в течение 5–7 дней (в зависимости от клинического течения). Показано, что Вигамокс хорошо переносится и безопасен в применении. Препарат обладает достаточным антимикробным эффектом, легко комбинируется с другими препаратами.
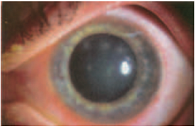
Рис. 1. Передние стромальные инфильтраты при акантамебном кератите

Рис. 2. Периневральные инфильтраты при акантамебном кератите
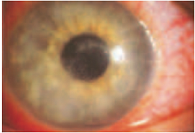
Рис. 3. Эпителиальные изменения и псевдодревовидные дефекты при акантамебном кератите
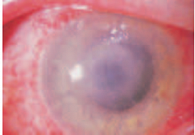
Рис. 4. Кольцо инфильтрата при акантамебном кератите
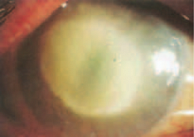
Рис. 5. Выраженная стадия акантамебного кератита
Среди пациентов с внезапно возникшим так называемым синдромом «красного глаза» преобладают больные с глазной инфекцией. В целом воспалительные поражения глаз инфекционной и реже неинфекционной природы относятся к числу наиболее распространенных заболеваний. Эпидемиологические данные свидетельствуют: в Российской Федерации в структуре обратившихся на амбулаторный прием лидируют больные с воспалительными поражениями глаз – 40,2%, или около 16 млн человек в год [1]. С воспалительными заболеваниями связано до 80% случаев временной нетрудоспособности, до 50% – госпитализаций, до 10–30% – слепоты [2].
Наиболее частым местом глазной инфекции является конъюнктива (конъюнктивит), а наиболее серьезным – поражение роговицы (кератит, язва роговицы) и внутренних оболочек глаза (эндофтальмит). По расчетным данным, среди общего числа больных с воспалительными заболеваниями глаз 66,7% составляют больные с конъюнктивитами, 23,3% – с блефаритами. На кератиты приходится 4,2% случаев воспалительных заболеваний глаз, на увеиты, хориоретиниты, невриты – до 5,8%, однако именно эти заболевания опасны такими грозными последствиями, как частичная или полная потеря зрения.
Вне зависимости от причинного фактора для кератита (воспаление роговой оболочки) характерны следующие клинические признаки: 1) симптомы раздражения роговицы (слезотечение, светобоязнь, блефароспазм, иногда боль в глазу); 2) наличие перикорнеальной гиперемии или смешанной, сочетающейся с покраснением конъюнктивы; 3) помутнение роговицы, сопровождающееся нарушением прозрачности, зеркальности, блеска роговицы.
При ношении контактных линз могут возникать осложнения, связанные с механическим повреждением роговицы, токсико-аллергическими и гипоксическими реакциями, инфекционными заболеваниями. Дефекты эпителия, часто возникающие у носителей контактных линз, способствуют распространению инфекции [3, 4, 5]. В этом случае речь может идти не только о потере зрения, но и о потере глаза как органа. В свое время на силикон-гидрогелевые контактные линзы возлагались большие надежды в плане снижения риска микробных кератитов. Первоначально предполагалось: благодаря тому, что такие контактные линзы пропускают кислород в значительно более высокой степени, чем линзы предыдущего поколения, удастся устранить гипоксию роговицы и тем самым свести к минимуму инфекционные заболевания, вызванные ношением контактных линз. Согласно данным разных авторов, вероятность развития микробных кератитов при ношении силикон-гидрогелевых линз в непрерывном режиме варьирует в диапазоне от 19,3 случая до 100–125 случаев на 10 000 носителей линз [6]. Массовое распространение силикон-гидрогелевых контактных линз не только не уменьшило количество микробных кератитов, а наоборот, в несколько раз повысило риск развития последних. Причина – в широком использовании контактных линз в режиме непрерывного ношения (в течение 30 суток не снимая).
Среди глазных инфекций, ассоциированных с ношением контактных линз, наиболее распространены следующие клинические формы: инфильтративный кератит, периферийная язва и микробный кератит.
Инфильтративный кератит – воспалительная реакция, развивающаяся у пользователей мягкими контактными линзами. В зависимости от этиологии она может наблюдаться на одном глазу или на обоих, симптомы могут отсутствовать или проявляться в виде слабой или средней боли. В больном глазу наблюдаются небольшие (менее 1 мм) инфильтраты на передней строме роговицы, без чрезмерных повреждений эпителия, с диффузной инфильтрацией от средне-периферийной зоны до периферии. Конъюнктива диффузно инъецирована. Инфильтративный кератит может быть вызван прокрашиванием роговицы (из-за несовместимости раствора с материалом контактной линзы), слишком плотной посадкой линзы или стафилококковой гиперчувствительностью (на линзе могут скапливаться грамположительные бактерии). При инфильтративном кератите применяется следующая тактика – пациенту достаточно прекратить ношение контактных линз и провести паллиативное лечение до полного устранения признаков и симптомов заболевания. Затем пациент может продолжить носить контактные линзы.
Периферийная язва – это роговичный инфильтрат, наиболее часто встречающийся у пациентов, носящих контактные линзы в расширенном или непрерывном режиме. Бульбарная инъекция обычно ограничена пределами квадранта, примыкающего к инфильтрату. Такая язва, скорее всего, появится в том случае, если на линзах пациента скапливаются микробы или биопленка, а эпителий роговицы поврежден. Основными возбудителями бактериальных язв роговицы (более 80% всех случаев) являются: Staphylococcus, Streptococcus, Pneumococcus, Pseudomonas aeruginosa, реже встречаются Escherichia coli, Neisseria, Proteus vulgaris, Moraxella. Периферийная язва не представляет угрозы для зрения, проходит сама по себе после того, как пациент прекращает носить контактные линзы, хотя на месте фокального инфильтрата формируется шрам. Поскольку симптомы периферийной язвы исчезают достаточно быстро после снятия линзы, необходимость в местном офтальмологическом лечении возникает очень редко. Такой корнеальный инфильтрат кажется незначительным по сравнению с куда более опасным микробным кератитом, однако по клиническим проявлениям может его напоминать. Если есть сомнения, особенно в том случае, когда нельзя тщательно осмотреть пациента, следует руководствоваться консервативным подходом и назначить антибактериальное лечение. На начальном этапе предпочтение следует отдать Вигамоксу в виде монтерами.
Микробные кератиты: клиника, диагностика, лечение
Бактериальный кератит – одно из самых серьезных осложнений при ношении контактных линз. Более чем в половине случаев заболевание вызвано синегнойной палочкой (Pseudomonas aeruginosa). Гипоксия, связанная с ношением контактных линз, может нарушать целостность эпителия роговицы, замедлять заживление повреждений и повышать микробное связывание, что может вызвать у пациента предрасположенность к инфекции.
Пациенты с бактериальным кератитом ощущают умеренную или сильную боль, светобоязнь, жалуются на покраснение глаз и слизисто-гнойные выделения. Осмотр на щелевой лампе покажет на строме фокальный инфильтрат неправильной формы, по размеру превышающий 1 мм. Он может находиться в центральной, средне-периферийной или периферийной зоне роговицы наряду с диффузной инфильтрацией и поверхностным дефектом эпителия. В диагностике кератитов новые перспективы открывает конфокальная прижизненная микроскопия роговицы [7].
Как было сказано выше, признаки и симптомы раннего бактериального кератита могут отчасти напоминать тяжелую периферийную язву роговицы. Однако, в отличие от нее, отказ от ношения линз не принесет облегчения; а без надлежащей антимикробной терапии (например, Вигамокс (3 раза в сутки) в сочетании с Витабактом 0,05% (4 раза в сутки)) состояние пациентов стремительно ухудшается.
Акантамебный кератит является самым тяжелым из возможных осложнений ношения контактных линз. В 70–85% случаев заболевание возникает у пациентов, использующих контактные линзы независимо от их типа (жесткие или мягкие). Возбудитель заболевания Acanthamoeba – простейший микроорганизм, принадлежащий к роду амебы, – обитает в почве, пресной и морской воде и других местах. При неблагоприятных условиях подвижная акантамеба (трофозоид) принимает форму неподвижной цисты. В таком состоянии она может существовать до 1 года [8].
Acanthamoeba проникает в роговицу в результате ее микротравм. Это происходит при нарушении правил гигиены; промывании линз и контейнеров для их хранения водопроводной водой, использовании растворов, не содержащих консервантов; купании (не снимая линз) в загрязненных водоемах и бассейнах.
Заболевание отличается медленным развитием и первоначально может быть принято за герпетический кератит. Пациент жалуется на ухудшение зрения, возникающее из-за образования хейза в центральной или парацентральной зоне. При прогрессировании процесса развивается кольцевой инфильтрат, появляется острая боль, не соответствующая клинической картине заболевания и вызванная внедрением трофозоида в периневральное пространство ткани роговицы. В дальнейшем нередко отмечаются задний увеит и эндофтальмит, что значительно осложняет течение заболевания и в некоторых случаях заканчивается потерей глаза.
Сходная клиническая картина наблюдается при поражении роговицы амебами рода Vahlkampfia и Hartmanella.
Для заболевания характерно длительное хроническое течение. Нередко акантамебный кератит осложняется вторичной бактериальной или герпесвирусной инфекцией. Он плохо поддается лечению и может привести к развитию десцеметоцеле и прободению роговицы. Акантамебному кератиту не свойственно спонтанное заживление.
Назовем клинические признаки акантамебного кератита в порядке их проявления [9]:
лимбит, периневральные инфильтраты (радиальный кератоневрит) (рис. 1) и мелкие неоднородные инфильтраты передних слоев стромы (рис. 2) обнаруживают в течение первых 4 недель от начала заболевания;
эпителий роговицы может оставаться интактным либо поражаться по типу точечного или псевдодревовидного кератита (рис. 3);
постепенное расширение и слияние инфильтратов ведет к формированию центрального или парацентрального кольцевидных абсцессов (рис. 4);
по периферии кольцевидного абсцесса наблюдают отдельные мелкие белесые инфильтраты;
медленно прогрессирующее истончение стромы роговицы (рис. 5), склерит и в конечном итоге – формирование десцеметоцеле.
Для диагностики акантамебного кератита важны сведения о ношении мягких контактных линз, выраженном стойком болевом синдроме, отрицательных результатах посевов на бактерии, вирусы и грибки (дифференциальная диагностика с герпетическим и грибковым кератитом) и устойчивости к обычной антибактериальной терапии. Для доказательства наличия акантамебы часть контактной линзы помещают в термостат на кровяной агар с Е. coli. Амеба переваривает бактерии, и вокруг материала линзы будет оставаться пустое пространство [10]. Для подтверждения диагноза также может быть использован метод полимеразной цепной реакции.
Пациент с акантамебным кератитом нуждается в лечении и непрерывном наблюдении. Рекомендуется назначение антибактериальных препаратов широкого спектра действия, противогрибковых и антисептических препаратов, содержащих хлоргексидин или полигексаметилена бигуанид. Однако кератит, вызванный акантамебой, может трудно поддаваться лечению, поскольку некоторые инфекционные акантамебы устойчивы к лекарственным препаратам. В тяжелых случаях акантамебный кератит требует пересадки роговицы (кератопластика).
При бактериальных язвах роговицы в лечении оправдано субконъюнктивальное введение аминогликозидных антибиотиков, особенно при начальной терапии тяжелых кератитов. Общая терапия необходима при вовлечении в процесс склеры и наличии перфорации роговицы. Лечение акантамебного кератита включает назначение следующих глазных капель в виде моно- или комбинированной терапии:
Вигамокс (моксифлоксацин) – 3 раза в день (можно каждые 4 часа в зависимости от клинического течения);
Витабакт 0,05% (пиклоксидина гидрохлорид 500 мкг) каждые 3–4 часа;
стероиды местного действия можно использовать для регуляции длительного воспалительного процесса, но их применение должно быть ограничено перед прекращением антиамебной терапии. В зарубежной практике настойчиво рекомендуют применять хлоргексидин диглюконат, комбинацию пропамидина с полигексаметилена бигуанидом [4] или сочетание моксифлоксацина и дибромопропамидина [5].
Циклоплегики (например, тропикамид 3 раза в день) необходимы для предотвращения образования синехий и для уменьшения болевого синдрома.
Начальная терапия микробного кератита (в первые 48 часов) проводится без учета результатов бактериоскопии мазка с конъюнктивы и бактериологического исследования посева содержимого конъюнктивальной полости. Решение об изменении первоначальной терапии принимается с учетом следующих факторов: клинический ответ на предварительное лечение, результаты микробиологических исследований, а также исследований устойчивости к антибактериальным агентам и чувствительности in vitro к антибиотикам. Так, если тесты на чувствительность микрофлоры роговицы указывают на более низкую эффективность антибиотика, назначенного на первом этапе, по сравнению с другим антибактериальным препаратом, медикамент может быть заменен. Если бактериологическое исследование показало, что посев стерилен, может быть сделан вывод о неинфекционном поражении роговицы. В этом случае антибиотики могут быть отменены и начата кортикостероидная или другой вид терапии.
Для оценки динамики лечения используют исследование с помощью щелевой лампы и схемы роговиц, где указаны размеры эпителиального дефекта, стромального инфильтрата, реакция со стороны передней камеры глаза, вовлечение в процесс стромы.
При наступлении улучшения со стороны стромального инфильтрата (выражается в уменьшении плотности, появлении четкости краев, уменьшении размеров и глубины инфильтрата) через 48–72 часа можно снизить частоту антибактериальной терапии. Однако следует помнить, что ранняя отмена или уменьшение частоты инстилляций местных препаратов недопустимы при лечении язв роговицы.
В случае отрицательной динамики язвы роговицы на фоне антибактериальной терапии следует заподозрить грибковый, амебный, герпетический кератит или кератит, вызванный другими организмами, которые не дали роста при посеве на имеющиеся культуры. Необходимо провести повторный соскоб с роговицы и посев на культуру. Решение о прекращении антибактериальной терапии должно приниматься через 24 часа после постановки нового диагноза.
Ухудшение клинической картины может быть вызвано токсичностью концентрированного антибиотика.
Если заболевание не поддается лечению или является самоиндуцирующимся, необходима госпитализация.
При отрицательных результатах исследования повторного соскоба или биопсии на микрофлору следует предположить неинфекционную природу заболевания. Антибактериальная терапия должна быть прекращена и назначены кортикостероиды или другие препараты.
Как было сказано выше, признаки и симптомы раннего микробного кератита могут отчасти напоминать тяжелую периферийную язву роговицы. Однако, в отличие от нее, отказ от ношения линз не принесет облегчения. Более того, без надлежащей антимикробной терапии состояние пациентов стремительно ухудшается. Поскольку задержка в лечении микробного кератита значительно ухудшит течение болезни, любую подозрительную язву роговицы нужно лечить как микробный кератит, пока не будет доказано обратное.
Вопросы профилактики акантамебного кератита
Установлена высокая устойчивость амеб к воздействию химических и физических факторов, что значительно затрудняет решение вопроса профилактики вызываемых ими заболеваний. Цисты акантамеб сохраняют жизнеспособность после 30-минутного воздействия 20° метилового или 70° этилового спирта, 5%-ного раствора лизола, 10%-ного – формалина. Акантамебы устойчивы к 24-часовому действию брома в концентрации 1 мг/мл. Йод (5 мкг/мл) и йодоформ (5 мкг/м) при 24-часовом контакте не губительны для акантамеб. В воде при 4 °С цисты акантамеб сохраняют жизнеспособность и, что еще важнее, вирулентность в течение периода от нескольких месяцев до 10 лет [10].
Обеззараживание воды в отношении этой группы микроорганизмов удается достигнуть хлорированием. Однако необходимые концентрации хлора значительно превышают обычно применяемые для обеззараживания воды от возбудителей бактериальных инфекций. Только при концентрации в воде остаточного хлора 2,2 мг/л и более чем двухчасовом контакте погибают все амебы.
В последние годы появились интересные сведения о том, что ряд бактерий, включая патогенные, могут быть проглочены акантамебами. Поскольку акантамебы могут выживать и сохранять способность к выживанию и размножению при таких концентрациях свободного и избыточного хлора, которые губительны для патогенных бактерий, акантамебы предохраняют проглоченные бактерии от воздействия дезинфектантов, играя существенную роль в возникновении инфекционных заболеваний. Показано, что такие бактерии, как Salmonella, Yersinia, Shigella sonnei, Legionella и другие, могут быть высеяны в культуру из обработанных хлором простейших. Более того, оказывается, что акантамебы способны «оживлять» жизнеспособные, но «некультивируемые» клетки легионеллы в культивируемую и инфекционную форму, а Mycobacterium avium паразитирует на внешних стенках цист акантамебы-полифага и может расти на продуктах, выделяемых этим организмом. Попадание в организм человека амебы, содержащей легионеллы, может привести к проникновению большого количества патогенных микроорганизмов, которые не только адаптированы к паразитированию в амебах, но еще и идеально приспособлены к паразитированию в альвеолярных макрофагах. В результате развивается так называемая болезнь легионеров [11].
Собственный опыт лечения микробных кератитов
Нами было проведено исследование, целью которого являлась оценка эффективности и безопасности применения препарата Вигамокс (моксифлоксацина гидрохлорид) у пациентов с синдромом «красного глаза», вызванного ношением контактных линз (постоянным или временным). Моксифлоксацин (Вигамокс, компания Alcon) является фторхинолоном 4-го поколения, высокоэффективным в отношении целого ряда грамположительных и грамотрицательных бактерий, атипичных микроорганизмов и анаэробов. Помимо широкого спектра действия отличительной особенностью моксифлоксацина является способность проникать во все среды глаза, то есть именно туда, где необходим антибактериальный эффект препарата.
Исследование проведено с участием 58 амбулаторных пациентов (102 глаза) с различными клиническими проявлениями синдрома «красного глаза» в возрасте от 14 до 48 лет. Все пациенты пользовались мягкими контактными линзами как средствами коррекции зрения. Постоянно носили контактные линзы 26 человек, периодически – 22 человека. Из-за частых рецидивов воспаления глаз 10 человек пользуются контактными линзами редко.
Всем пациентам проводили стандартное комплексное обследование, включавшее визометрию, биомикроскопию, флюоресцеиновую пробу (инстилляция одной капли 0,5%-ного раствора флюоресцеина в конъюнктивальный мешок) с последующим осмотром роговицы с помощью щелевой лампы при любом подозрении на нарушение поверхности роговицы. Наиболее часто диагностировались язвы роговицы, реже – кератиты. У включенных в исследование пациентов были диагностированы следующие клинические формы глазных инфекций: роговичные инфильтраты (35 человек), в том числе периферийная язва (9 человек); микробный кератит (23 человек), в том числе бактериальный (19 человек) и акантамебный кератит (4 человека).
Все пациенты в качестве местной терапии получали антибактериальный препарат Вигамокс 3–4 раза в день, дополнительно (или в качестве монотерапии) противомикробную терапию препаратом Витабакт. В течение первых 48 часов препараты закапывали каждый час (с перерывом на ночь). Далее препараты применяли 4 раза в сутки в течение 5–7 дней (в зависимости от клинического течения заболевания). Осмотр пациентов проводился ежедневно (биомикроскопия).
В группе пациентов с роговичным инфильтратом (35 человек) уже на 2-е сутки лечения отмечена положительная динамика: уменьшилось количество инфильтратов, выраженность перикорнеальной инъекции стала слабее. У пациентов этой группы терапия Вигамоксом была прекращена и назначены инстилляции Витабакта (пиклоксидина гидрохлорид 500 мкг) 3–4 раза в день в течение 4–5 дней. У всех пациентов с роговичным инфильтратом заболевание закончилось выздоровлением в течение 5 дней. У 9 человек с периферийной язвой диагноз подтвердился после первых суток лечения – симптомы полностью исчезли после отказа от ношения мягких контактных линз. Тем не менее у всех пациентов терапия Витабактом была продолжена в течение 5–7 дней (инстилляции 4–6 раз в сутки). Осмотр пациентов данной группы проводился 1 раз в 3 дня – рецидивов отмечено не было. На месте язвы у 5 человек сформировался нежный рубец.
Из 23 человек с подозрением на микробный кератит диагноз подтвердился у 14 пациентов: у 11 человек был выявлен стафилококк, у 3 человек – стрептококк. У остальных пациентов из этой группы (9 человек) возбудитель не был выявлен, однако на фоне проводимой антибактериальной терапии наблюдалась отрицательная динамика, что дало основания заподозрить грибковый, амебный, герпетический кератит или кератит, вызванный другими организмами, которые не дали роста при посеве на имеющиеся культуры. Этим пациентам была изменена терапия: Вигамокс сочетали с кортикостероидами, иммуномодуляторами и циклоплегиками. Динамика у пациентов данной группы была слабо положительной. При биомикроскопии у 4 пациентов обнаружился кольцевидный инфильтрат, жалобы усилились, появилась острая боль – признаки акантамебного кератита. Пациентам был назначен Вигамокс (6 раз в сутки), Витабакт (каждые 2 часа), тропикамид 1% (2–3 раза в день), Максидекс (2 раза в день) – местно в течение 7–10 дней. В связи с подозрением на амебную этиологию заболевания всех 4 пациентов госпитализировали на 7–8 суток в глазное отделение, где диагноз «акантамебный кератит» был подтвержден. У остальных 5 человек из группы с подозрением на микробный кератит динамика была слабо положительной, но стабильной. Пациенты в госпитализации не нуждались, при обследовании (биомикроскопия) очаги не имели характера акантамебного кератита, роговичный синдром был не ярко выражен. Пациентам этой подгруппы была назначена комбинированная терапия: Вигамокс (каждый час в первые сутки, потом – через 2–3 часа), Витабакт (6 раз в сутки с третьего дня лечения) и Максидекс (2 раза в сутки с 4–5-го дня лечения). Лечение пациентов этой подгруппы (с подозрением на акантамебный кератит в начале заболевания) продолжалось до 14 дней в амбулаторных условиях и привело к исчезновению всех симптомов заболевания.
Таким образом, проведенное нами исследование подтверждает целесообразность назначения Вигамокса на ранних стадиях заболевания в целях своевременного купирования кинических проявлений и предотвращения развития его осложнений. Препарат отлично переносится пациентами. Вигамокс хорошо сочетается и комбинируется с другими препаратами. Осложнений и побочных эффектов на фоне терапии Вигамоксом не наблюдалось. По субъективным оценкам пациентов переносимость препарата Вигамокс оценена как отличная.
Заключение
Доказанная в ходе зарубежных и отечественных исследований эффективность Вигамокса существенно повлияла на методы лечения микробного кератита.
На начальном этапе, когда клинический диагноз кератита не подтвержден лабораторными методами, пациенту следует немедленно назначить антибиотик широкого спектра действия. Во всем мире в этих случаях применяют фторхинолоны нового поколения (в том числе моксифлоксацин (Вигамокс, Alcon)), которые воздействуют как на грамположительные, так и на грамотрицательные бактерии [12]. Поскольку действие этого антибактериального препарата зависит от концентрации, пациенту следует назначить начальную дозу каждые 15 минут. Если пациенту был поставлен точный диагноз по результатам микробиологического исследования, режим лечения может меняться в зависимости от того, какие именно микроорганизмы вызвали заболевание, и от его клинического течения. В заключение подчеркнем: в последние несколько лет новые подходы к лечению микробного кератита позволили изменить прогноз у пациентов с этим заболеванием. Определяя равновесие между эффективностью и безопасностью терапии, преимуществами и рисками, необходимо стремиться к тому, чтобы в итоге выигрывал пациент.
1. Южаков А.М., Травкин А.Г., Киселева О.А. и др. Статистический анализ глазной заболеваемости и инвалидности по РСФСР // Вестник офтальмологии. 1991. No 2. С. 5–7.
2. Майчук Ю.Ф. Терапия инфекционных заболеваний глаз // Офтальмологический журнал. 1996. No 4. С. 193–199.
3. Mathers W.D., Sutphin J.E. // Experimental eye research. 1998. Vol. 67. P. S83.
4. Varga J.H., Wolf T.C., Jensen H.G. et al. Combined treatment of Acanthamoeba keratitis with propamidine, neomycin, and polyhexamethylene biguanide // Am. J. Ophthalmol. 1993. Vol. 115. No 4. P. 466–470.
5. Hargrave S., McCulley J., Husseim Z.M. et al. // American Academy of Ophthalm. Meeting. San Francisco, 1997. P. 152.
6. Морган Ф. Соблюдение рекомендаций как фактор снижения рис- ка кератита // Современная оптометрия. 2008. No 4. С. 8–11.
7. Майчук Ю.Ф., Вахова Е.С. Глазные мази «Эубетал» и «Колбиоцин» в лечении хламидийных конъюнктивитов // Вестник офтальмоло- гии. 1998. No 2. С. 32–34.
8. Майчук Ю.Ф. Паразитарные заболевания глаз. М., 1988. 287 с.
9. Акантамебный кератит – следствие ношения контактных линз // http://ophthalmolog.com.ua/obrazovanie/rycovodstva-po- ophtalmologii/194-akantamyobnyj-keratit.html.
10. Mедицинский портал www.glazamed.ru.
11. Podolsky M.L. // Ophthalmol. World News. 1995. Vol. 1. No 9. P. 20–21.
12. DeNaeyer G.W. Осложнения, связанные с ношением контак- тных линз: диагностика и оказание помощи // www.svetlinz. ru/?idp=8&idts=8&ids=128
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.