Методы интервенционной медицины в лечении неспецифической люмбоишалгии, обусловленной дисфункцией крестцово-подвздошного сочленения
- Аннотация
- Статья
- Ссылки
- English
В статье представлены результаты исследования, выполненного с целью определения основного источника боли при неспецифической люмбоишалгии для дальнейшего лечения с использованием малоинвазивных манипуляций, оценкой их эффективности и безопасности. Был обследован 51 пациент (36 женщин и 15 мужчин, средний возраст 56,4 ± 2,1 года) с дисфункцией КПС. Первая группа получала консервативное лечение – периартикулярные блокады с местными анестетиками и глюкокортикостероидами. Вторая группа пролечена в условиях нейрохирургического отделения методом радиочастотной денервации КПС.
Дифференцированный подход в оценке основного источника боли при хронической люмбоишалгии, обусловленной дисфункцией КПС, с проведением нейроортопедического обследования, подтверждением диагноза периартикулярной блокадой и таргетным воздействием с помощью методов интервенционной медицины обеспечил хороший результат, который согласуется с данными литературы: уменьшение болевого синдрома, повышение трудоспособности, качества жизни и психоэмоционального статуса.
В статье представлены результаты исследования, выполненного с целью определения основного источника боли при неспецифической люмбоишалгии для дальнейшего лечения с использованием малоинвазивных манипуляций, оценкой их эффективности и безопасности. Был обследован 51 пациент (36 женщин и 15 мужчин, средний возраст 56,4 ± 2,1 года) с дисфункцией КПС. Первая группа получала консервативное лечение – периартикулярные блокады с местными анестетиками и глюкокортикостероидами. Вторая группа пролечена в условиях нейрохирургического отделения методом радиочастотной денервации КПС.
Дифференцированный подход в оценке основного источника боли при хронической люмбоишалгии, обусловленной дисфункцией КПС, с проведением нейроортопедического обследования, подтверждением диагноза периартикулярной блокадой и таргетным воздействием с помощью методов интервенционной медицины обеспечил хороший результат, который согласуется с данными литературы: уменьшение болевого синдрома, повышение трудоспособности, качества жизни и психоэмоционального статуса.

Введение
В настоящее время боль в спине принято рассматривать в рамках предложенной G. Waddell в 1987 г. биопсихосоциальной модели, в которой выделяют биологическую (анатомические источники боли), а также психологическую и социальную (способствуют возникновению и поддержанию боли) составляющие. В соответствии с современной классификацией – диагностической триадой боли в спине подразделяются:
- на неспецифические (скелетно-мышечные);
- связанные с серьезной патологией (опухолями, травмами, инфекциями и др.);
- вызванные компрессионной радикулопатией.
Наиболее часто (в 85% случаев) в клинической практике встречается неспецифическая (скелетно-мышечная, механическая) боль [1–4]. Группа пациентов с неспецифической болью в спине неоднородна, что определяет необходимость в дифференцированном поэтапном лечении с учетом основного патогенетического механизма (ноцицептивного, невропатического или психогенного) [5–8].
Применение диагностической триады для установления биологической составляющей боли в спине достаточно для врача общей практики. Однако в условиях специализированного отделения у пациентов с затянувшимся и рецидивирующим болевым синдромом определение основного источника боли – принципиальная задача для выбора тактики лечения с использованием блокад, мануальной терапии, а при необходимости нейрохирургического вмешательства.
Согласно данным, полученным с помощью малоинвазивных диагностических процедур, неспецифическая боль в 25–42% случаев имела дискогенную природу, в 18–45% – фасеточный характер и в 15–30% случаев боль локализовалась в крестцово-подвздошном сочленении (КПС), при этом мышечный фактор не упоминался [9, 10]. Таким образом, КПС – один из наиболее частых источников боли при неспецифической люмбоишалгии [11].
На базе клиники нервных болезней им. А.Я. Кожевникова проведено исследование с целью определения основного источника боли при неспецифической люмбалгии/люмбоишалгии для дальнейшей терапии с использованием малоинвазивных манипуляций, оценкой их эффективности и безопасности.
Материал и методы
Был обследован и пролечен 51 пациент, у которого основным источником боли при неспецифической люмбалгии/люмбоишалгии была дисфункция КПС, из них 36 женщин и 15 мужчин (средний возраст 56,4 ± 2,1 года). Пациенты разделены на две группы. Пациенты первой группы получали консервативное лечение – периартикулярные блокады с местными анестетиками и глюкокортикостероидами. Пациентам второй группы в условиях нейрохирургического отделения выполнена радиочастотная денервация КПС.
Основной источник боли устанавливался с помощью нейроортопедического обследования, проводимого независимо двумя экспертами. Клинические тесты подтверждались данными нейровизуализации и диагностическими блокадами (диагностически значимым считалось уменьшение боли на 70%). В исследование не включались пациенты со специфической болью в спине, корешковыми синдромами, широко распространенной болью в спине, фибромиалгией.
Для оценки интенсивности болевого синдрома использовали Визуальную аналоговую шкалу (ВАШ), степени нарушения жизнедеятельности – опросник Освестри (Oswestry Disability Index – ODI). Для выявления сопутствующих тревожных и/или депрессивных расстройств применяли Госпитальную шкалу тревоги и депрессии (Hospital Anxiety and Depression Scale – HADS), выявления и оценки невропатического компонента боли – Диагностический вопросник невропатической боли (Douleur Neuropathique 4 Questions – DN4). Качество жизни определялось по Краткой форме оценки здоровья (12-Item Short-Form Health Survey – SF-12). Состояние пациентов наблюдалось в динамике: повторная оценка перечисленных показателей осуществлялась через три месяца после лечения. Кроме того, с помощью Шкалы риска хронизации боли (Keele STarT Back Screening Tool – SBST) оценивался риск неблагоприятного исхода для выбора последующей тактики лечения уже на ранних стадиях заболевания.
Полученные данные статистически обрабатывались в программе SPSS Statistics V22, рассчитывались средние показатели, параметрический парный t-критерий Стьюдента, непараметрический критерий Манна – Уитни, проводился корреляционный анализ с использованием коэффициента Спирмена.
Результаты
В целом средний уровень боли по ВАШ при поступлении составил 6,7 ± 0,24 см, через три месяца после курса лечения он достоверно уменьшился до 3,6 ± 0,36 см (p < 0,0001). В 71% случаев через три месяца отмечалось уменьшение боли на 50% и более. Невропатический компонент боли по шкале DN4 (свыше 4 баллов) имел место в среднем у 29,4% пациентов в отсутствие клинических признаков радикулопатии. Показатель нетрудоспособности по ODI после лечения снизился с 42,94 ± 2,50 до 28,98 ± 3,03 балла (p < 0,001). Уровень тревоги по шкале HADS до лечения в среднем составил 7,3 ± 0,58 балла, а депрессии – 6,0 ± 0,48 балла, причем тревога/депрессия субклинического и клинического уровня обнаруживалась у 47% респондентов. Изначально у пациентов были снижены и физический (33,36 ± 1,17 балла), и психологический (41,95 ± 1,40 балла) аспекты качества жизни по шкале SF-12. Согласно SBST, высокий риск хронизации наблюдался в 29,4% случаев, средний – в 39,6%, низкий – в 31% случаев. Проведенный анализ выявил статистически достоверную выраженную положительную корреляцию риска хронизации боли по SBST и степени нарушения жизнедеятельности по ODI (коэффициент корреляции Спирмена 0,685, p < 0,01) и отрицательную корреляцию с параметрами качества жизни по SF-12 (коэффициент корреляции Спирмена -0,553, p < 0,01), как физической, так и психологической составляющей (коэффициент корреляции Спирмена -0,600, p < 0,01).
Пациентам первой группы (32 пациента, из них 23 женщины и девять мужчин, средний возраст 51,75 ± 2,6 года) выполнялись периартикулярные блокады КПС раствором местного анестетика и глюкокортикостероида. Выраженность боли по ВАШ статистически значимо уменьшилась после лечения в среднем на 61,4%, при этом у 80% пациентов через три месяца боль уменьшилась на 50% и более. 21,8% пациентов испытывали невропатическую боль (по шкале DN4). После лечения уровень тревожности достоверно снизился на 35%, депрессии – на 39,7%. Степень нарушения трудоспособности по ODI достоверно уменьшилась на 43% (p < 0,001). Улучшились показатели качества жизни (по SF-12): физическая составляющая – на 23% (p < 0,001), психологическая – на 8,5% (p < 0,01).
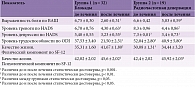
Пациентам второй группы (19 пациентов, из них 13 женщин и шесть мужчин, средний возраст 64,1 ± 2,8 года) выполнена радиочастотная денервация КПС. Невропатическими болями страдали 40,1% больных. Уровень боли после лечения по ВАШ уменьшился на 23% (p < 0,05). Через три месяца снижение боли по ВАШ на 50% и более от изначального уровня отметили 46% пациентов. После лечения уровень тревожности достоверно снизился на 46%, депрессии – на 53,4%. Степень нарушения жизнедеятельности после лечения достоверно уменьшилась на 22% (p < 0,05). Не было отмечено статистически достоверного улучшения физической составляющей качества жизни (p = 0,174). Психологическая составляющая улучшилась на 8,3% (p < 0,05) (табл. 1).
По некоторым параметрам группы статистически достоверно отличались (p < 0,05). Так, во второй группе были достоверно выше средний возраст, уровень депрессии, степень нарушения жизнедеятельности, частота обнаружения невропатической боли и хуже физическая составляющая качества жизни.
Обсуждение
В нашем исследовании наиболее частым источником боли при неспецифической люмбоишалгии было КПС – 42%, в 23% – фасеточные суставы, в 17% – патология диска. Полученные данные согласуются с результатами M.J. DePalma и соавт. 2012 г. о преобладании патологии КПС в старших возрастных категориях [9, 10].
КПС – своеобразный сустав: частично типичный синовиальный (диартроз – передние 30–50% сочленения), а частично неподвижный хрящевой синостоз. Основная функция КПС опорная: поддержка верхней части тела и уменьшение нагрузки при ходьбе. Объем движений в КПС ограничен, оно укреплено связками: передней и задней крестцово-подвздошными, крестцово-остистой, крестцово-бугорной и межостистой. Связки ограничивают движение в суставе при ходьбе. КПС взаимодействует с мышцами и фасциями, в том числе грудопоясничной фасцией, большой ягодичной, грушевидной мышцами и широчайшей мышцей спины [12]. По мнению W. King и соавт., правильнее говорить не о КПС, а о крестцово-подвздошном комплексе, который включает собственно сустав и поддерживающие его связки, при этом каждый из элементов может быть источником боли [13].
Иннервация КПС сложна, в иммуногистохимических исследованиях выявлены ноцицепторы в суставной капсуле, связках и в меньшей степени в субхондральной кости. Предполагается, что повреждение любой из этих структур может вызвать боль. Типичный паттерн боли был изучен в экспериментах на здоровых добровольцах при растяжении капсулы и раздражении связок. Задняя поверхность сустава лучше изучена и выступает в качестве основного объекта интервенционных методов лечения (блокад, денервации). Она иннервируется в основном из дорзальных ветвей корешков S1–S3, иногда имеется дополнительная иннервация от корешков L5 и S4. Иннервация вентральной поверхности сустава сложнее, в большинстве исследований описывается участие вентральных ветвей L5–S2 и, возможно, L4, обсуждается иннервация от ветвей верхнего ягодичного и запирательного нервов [12].
Термин «дисфункция» подразумевает дегенеративные изменения КПС в отсутствие специфических факторов поражения (опухолей, переломов, септического или аутоиммунного воспаления и т.п.). Дисфункция КПС возникает при комбинации неадекватной осевой нагрузки и вращения и характеризуется изменением подвижности в суставе (блокированием сустава или микронестабильностью), что ведет к неадекватному стрессовому распределению нагрузки на окружающие ткани (капсулу, связки, мышцы, кости) [14]. В то же время в исследованиях с применением рентгеновской стереофотометрии не установлена связь между развитием болевого синдрома и объемом движения в суставе [15]. Кроме того, КПС может быть зоной отраженной боли при поясничных грыжах диска, заболеваниях органов малого таза (прежде всего гинекологической патологии).
Среди факторов, предрасполагающих к развитию боли в КПС, выделяют возраст (чаще у пожилых лиц и молодых спортсменов), асимметрию длины ног, аномалии строения, походки и биомеханики, сколиоз, длительное напряжение/травмы (например, бег трусцой), беременность, предшествующие операции на позвоночнике (особенно спондилодез). В 40–50% случаев развитие боли связано с конкретным провоцирующим фактором, часто боли в КПС возникают в результате дорожно-транспортных происшествий, падений, после повторяющихся нагрузок и при беременности [16, 17].
При проспективном наблюдении в течение шести месяцев у 70% пациентов, перенесших радиочастотную денервацию фасеточных суставов, развились боли, связанные с дисфункцией КПС. По мнению авторов, это могло быть вызвано недостаточной диагностикой этих состояний или скрытыми причинами боли («дремлющий источник боли») [18].
Для дисфункции КПС типично усиление боли при вставании из положения сидя, наклонах, длительном сидении или стоянии. В блокированном КПС нарушается подвижность подвздошной кости относительно крестца, что проверяется попеременным надавливанием на крестец и подвздошную кость пациента, лежащего на животе. Характерна болезненность при пальпации КПС с воспроизведением типичного паттерна боли. Не происходит опускания задней верхней ости при поднятии ноги в положении стоя на стороне блока КПС. Симптомов выпадения не наблюдается, пациенты отмечают усиление болевых ощущений при проведении трех или более провокационных тестов на сжатие или растяжение этого сустава [14, 19].
Радиологическое исследование не имеет большой диагностической информативности и показано только при наличии «красных флажков». Ряд методов диагностической визуализации применялся для изучения боли в КПС. Компьютерная томография – быстрый способ диагностики, который считается золотым стандартом выявления костной патологии. По данным ретроспективного исследования H. Elgafy и соавт. (n = 112), чувствительность компьютерной томографии составляет лишь 57,5%, а специфичность – 69% при использовании диагностических блокад в качестве стандарта [20]. Радиоизотопное сканирование костей в сравнении с блокадами анестетиками также продемонстрировало низкую чувствительность. C.W. Slipman и соавт. установили 100%-ную специфичность, но только 13%-ную чувствительность для радионуклидного исследования (n = 50) [21]. J. Maignе и соавт. сообщили о 46,1%-ной чувствительности и 89,5%-ной специфичности этого метода (n = 32) [22]. Таким образом, низкие значения чувствительности не позволяют рекомендовать радионуклидные методы исследования для скрининга при боли в КПС. Сообщается, что магнитно-резонансная томография эффективна в обнаружении спондилоартропатий уже на ранней стадии с чувствительностью, превышающей 90%, но не имеющей пользы для диагностики невоспалительных состояний [23].
Стандарт для подтверждения диагноза – блокады с введением малых объемов местных анестетиков. Подтверждением роли КПС в развитии боли служит исчезновение или существенное уменьшение боли (по данным разных авторов, на 50% и более) после блокады сустава растворами местных анестетиков [24].
Согласно данным литературы, среди внутрисуставных причин боли в КПС чаще остальных встречаются дисфункция (артрозо-артрит) и спондилоартропатии [12]. В настоящее исследование не включались пациенты со сподилоартропатией (на основании критериев Berlin). Среди внесуставных источников боли лидируют повреждения связок и мышц, а также энтезопатии. В настоящем исследовании 46% пациентов отмечали появление боли после физической (динамической и статической) нагрузки, но в большинстве случаев явная причина не установлена.
Односторонняя боль наблюдалась в 86% случаев, что согласуется с литературными данными о, как правило, одностороннем латерализованном характере боли в проекции КПС. Наиболее специфична для поражения КПС так называемая зона Fortin размером приблизительно 3 × 10 см, которая располагается непосредственно книзу от задней верхней подвздошной ости [25].
Дисфункция КПС часто имитирует корешковые поражения. Клинические наблюдения и артрографические исследования на здоровых добровольцах показали, что в 94% случаев болевые ощущения иррадиируют в область ягодиц, в 72% случаев – в нижнепоясничную область, в 50% случаев боль распространялась по задней поверхности бедра, включая 28% с иррадиацией боли ниже колена и 12% с иррадиацией до стопы. У 14% пациентов боль распространяется в паховую область, у 6% – в верхние отделы поясничной области, у 2% – в живот [25, 26]. По данным D. Kurosawa и соавт., 46,5% пациентов с дисфункцией КПС (преимущественно верхней части сустава) жаловались на боли, иррадиирующие в пах, что значительно превышало встречаемость паховых болей у пациентов с другими причинами люмбоишалгии [27]. Среди обследованных нами пациентов в 92% случаев отмечались боли, иррадиирующие в ягодичную область, в 68% случаев – распространение боли по задней поверхности бедра, в 41% – по наружной поверхности бедра, в 18% случаев боли отдавали в паховую область и низ живота. В 8% случаев имели место «длинные» боли до уровня голеностопного сустава и пальцев. Вместе с тем четкой корешковой симптоматики не определялось, данные магнитно-резонансной томографии исключали дискорадикулярный конфликт и боли регрессировали после блокады КПС. Каждый пациент был обследован двумя независимыми экспертами, с дальнейшим подтверждением диагноза с помощью блокад. Основные тесты приведены в табл. 2 [14].
Отношение к применению провокационных тестов в диагностике дисфункции КПС неоднозначно. Р. Dreyfuss и соавт. отмечали ненадежность истории заболевания и диагностических тестов при боли в КПС, подтвержденной положительным ответом на блокаду в качестве эталонного стандарта [28]. В других исследованиях отмечена информативность батареи провокационных тестов для выявления боли в КПС. В слепом исследовании оценки валидности клинического тестирования М. Laslett и соавт. установили, что три из шести провокационных тестов имели 94%-ную чувствительность и 78%-ную специфичность в прогнозировании положительного ответа на однократную диагностическую блокаду КПС [29]. По данным P. van der Wurff и соавт., чувствительность и специфичность трех положительных из пяти провокационных тестов составили 85 и 79% соответственно (в качестве диагностического стандарта использовалась двойная диагностическая блокада) [30]. Считается, что для идентификации боли в КПС провокационные тесты надежнее тестов измерения объема движений [30]. Таким образом, наличие трех или более положительных провокационных тестов представляется достаточно чувствительным и специфичным для определения пациентов, которые положительно ответят на диагностические блокады КПС [31].
В настоящее время для оценки информативности тестов в диагностике заболевания применяется коэффициент отношения правдоподобия (Likelihood Ratios, КОП). Положительный КОП, равный +1, имеет недостаточную диагностическую ценность. КОП от +2 до +5 считается небольшим, но иногда важным, от +5 до +10 – средним, но обычно достоверным. Значение КОП больше +10 – абсолютно достоверный признак заболевания. В систематическом обзоре K.M. Szadek и соавт. пришли к выводу, что три положительных провокационных теста имели значимую диагностическую ценность (КОП +17,16) для подтверждения боли в КПС с использованием в качестве эталонного стандарта двойной положительной блокады [31]. Этот критерий применялся в данной работе. Совпадение источника боли в виде дисфункции КПС при оценке двумя экспертами, владеющими навыками нейроортопедического обследования, достигало 90%. Клиническое обследование подтверждалось диагностической блокадой КПС. В нашем исследовании значимым считалось уменьшение боли на 70%, что обеспечило 90%-ную чувствительность и 85%-ную специфичность этого теста. Учитывая роль связочно-суставного комплекса в развитии боли, препараты вводились периартикулярно. Считается, что блокады без нейровизуализационного контроля связаны с высокой частотой ложноположительных ответов, а использование контролируемых блокад повышает вероятность ложноотрицательных результатов, но не влияет на результаты лечения. Проведение блокад имеет и прогностическое значение. По данным B.J. Schneider и соавт., у пациентов с отсутствием быстрого эффекта на блокаду не отмечалось улучшения симптоматики в отдаленном периоде и при повторных блокадах [32].
В нашем исследовании почти треть пациентов с дисфункцией КПС испытывали невропатическую боль в отсутствие клинических признаков радикулопатии. В соответствии с классическими представлениями патология КПС должна проявляться ноцицептивной болью, однако возникновение невропатической боли в группе пациентов со скелетно-мышечной болью – достаточно известный факт. Невропатический компонент боли в спине не только встречается при классической радикулопатии, но и нередко обнаруживается наряду с периферическими ноцицептивными источниками. При этом в качестве ведущего механизма развития невропатической боли рассматриваются процессы нейропластичности на различных уровнях соматосенсорной системы, основанные на структурных, функциональных и нейрохимических изменениях. При повреждении в пояснично-крестцовом отделе происходит выделение медиаторов воспаления, приводящее к сенситизации периферических ноцицепторов (и первичной гипералгезии). Существенные нейропластические изменения происходят и на уровне заднего рога спинного мозга. Продолжающаяся болевая афферентация от поясничной области вносит вклад в феномен центральной сенситизации нейронов заднего рога, основанной на повышении возбудимости клеточной мембраны и синаптической эффективности. Кроме того, у пациентов с болью в спине описана дисфункция нисходящих модулирующих ингибиторных путей, начинающихся в стволе мозга (например, в околоводопроводном сером веществе), что приводит к усилению и приумножению афферентной импульсации. Из сенсорных афферентных волокон выделяются медиаторы, активирующие микроглию и астроциты, которые в свою очередь формируют длительную гиперчувствительность проекционных нейронов. Нейропластические изменения развиваются и на церебральном уровне. У пациентов с болью в спине показано расширение площади представительства поясничной области в первичной соматосенсорной коре. Обсуждается уменьшение плотности кортикального серого вещества. Описаны значимые нейрохимические изменения в дорзолатеральной префронтальной, передней поясной и орбитофронтальной коре, таламусе, причем их выраженность коррелировала с продолжительностью боли в пояснице. Описанные механизмы способствуют формированию невропатического компонента боли в спине даже при отсутствии клинических признаков радикулопатии [33–36]. E. Murakami и соавт. выявили, что боль, иррадиирующая в ногу, с невропатическим компонентом, не соответствующим дерматомному распределению, встречается у 60% пациентов с дисфункцией КПС преимущественно при поражении задней сакроилеальной связки [37].
Один из основных показателей эффективности лечения – сохранение трудоспособности [38]. В настоящем исследовании нетрудоспособность оценивалась по ODI. Исходно у пациентов отмечался высокий уровень нетрудоспособности, который после лечения уменьшился в среднем на 35%, достигнув умеренной степени.
При оценке качества жизни по шкале SF-12 наблюдалось существенное ухудшение как физического, так и психологического компонентов и у пациентов с хронической болью, обусловленной дисфункцией КПС.
Шкала SBST достаточно широко используется в мировой практике для определения тактики лечения и рекомендуется несколькими руководствами по ведению пациентов с поясничной болью [38, 39]. В нашей работе мы впервые в России применили эту шкалу. У пациентов преобладал высокий и средний риск хронизации (суммарно 69%), что оправдывает мультидисциплинарное лечение в условиях специализированного стационара с дополнительным подключением психологических и физических методов. Со всеми пациентами проведена беседа по поводу доброкачественной природы болевого синдрома, их двигательного стереотипа, необходимости активизации и занятий лечебной физической культурой в виде ходьбы. Результат по SBST статистически достоверно коррелировал с параметрами степени нарушения жизнедеятельности, определяемой по ODI (p < 0,01), и достоверно отрицательно – с параметрами качества жизни по SF-12 (p < 0,01). В то же время не получено статистически достоверной корреляции данных SBST с уменьшением боли на 50% в конце наблюдения. Таким образом, SBST информативна и проста в использовании, что позволяет применять ее для отбора пациентов, нуждающихся в дополнительном лечении, вместе с тем шкала не имеет прогностического значения для определения исхода болевого синдрома.
У пациентов наблюдалась высокая частота тревожности/депрессии субклинического и клинического уровня (47%), что согласуется с данными литературы о высокой распространенности тревожно-депрессивных нарушений при хронической неспецифической поясничной боли [40].
В большинстве руководств пациентам с неспецифической болью в спине рекомендуется участвовать в образовательных программах, сохранять активность, заниматься гимнастикой. Им показаны психотерапевтические методики (например, когнитивно-поведенческая терапия), мануальная терапия и нестероидные противовоспалительные препараты (НПВП) в качестве препаратов первой линии [1–4].
Согласно рекомендациям Американской академии медицины боли (American Academy of Pain Medicine) по диагностике и лечению синдрома КПС у пожилых лиц (2016), пациенты должны быть информированы о том, что сочетание физических упражнений, нормализация двигательного стереотипа и медикаментозная терапия могут уменьшить боль на 30% в течение шести недель и улучшить повседневную деятельность. Медикаментозная терапия включает короткий курс НПВП, трамадол при интенсивной боли, местные средства (пластырь с лидокаином). Показана гимнастика, особенно направленная на укрепление мышц, приводящих бедро, которая включают упражнения лежа на боку, упражнения на сопротивление и поддержание равновесия [11].
В Кохрановском обзоре была подтверждена эффективность НПВП в уменьшении выраженности болевого синдрома и степени дизабилитации при хронической боли в поясничной области. При этом как селективные, так и неселективные НПВП сравнимы по эффективности [41]. Однако селективные ингибиторы циклооксигеназы 2 в меньшей степени негативно влияют на желудочно-кишечный тракт. Среди селективных препаратов в лечении скелетно-мышечной боли хорошо зарекомендовал себя мелоксикам (Мовалис).
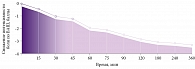
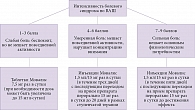
Мелоксикам (Мовалис) обладает сбалансированной селективностью в отношении циклооксигеназы 2, что подтверждено с помощью различных стандартных методов in vitro и in vivo и объясняет высокий профиль его гастроинтестинальной безопасности. В доклинических исследованиях на классических моделях острого и хронического воспаления установлено, что мелоксикам оказывает яркое противовоспалительное, обезболивающее и антипиретическое действие. Мелоксикам изучен более чем в 230 клинических исследованиях, в которых принимали участие свыше 30 000 пациентов. Лечебный эффект мелоксикама, назначаемого внутрь, 7,5 мг/сут при остеоартрозе и 15 мг/сут при хронических воспалительных заболеваниях (ревматоидном артрите или анкилозирующем спондилите) не уступает таковому традиционных НПВП, а по гастроинтестинальной переносимости мелоксикам превосходит эти препараты. Данные основных контролируемых исследований свидетельствуют о сходной эффективности, но более высокой безопасности мелоксикама по сравнению с диклофенаком, пироксикамом и напроксеном. В отличие от большинства НПВП Мовалис не подавляет агрегацию тромбоцитов [42]. В экспериментальных работах установлен хондропротективный эффект мелоксикама в виде торможения апоптоза хондроцитов и увеличения синтеза матриксного компонента [43]. Недавно было установлено, что мелоксикам также подавляет продукцию простагландина Е2, блокируя микросомальную простагландин-Е2-синтетазу 1, что усиливает его противовоспалительный эффект [44]. Внутримышечное введение обеспечивает более быстрое терапевтическое действие. Облегчение боли наступает уже через 15 минут после инъекций Мовалиса, а статистически значимый (р < 0,01) терапевтический эффект развивается через 30 минут (рис. 1) [45]. С учетом фармакокинетических характеристик Мовалиса можно предложить схему назначения препарата в зависимости от уровня интенсивности боли по ВАШ (рис. 2).
При недостаточной эффективности консервативного лечения обсуждаются интервенционные методы лечения, включая лечебные блокады и радиочастотную денервацию [8]. Диагностические и лечебные блокады широко используются при боли в области поясницы, причем в последние годы все чаще. Количество различных вариантов блокад, оплаченных в системе Medicare, возросло с 1 450 495 в 2000 г. до 4 815 673 в 2011 г. [46]. В то же время в мире нет единого мнения о целесообразности применения интервенционных методов лечения неспецифической боли в спине. Например, Американское общество по изучению боли (American Pain Society) и Национальный институт здравоохранения и усовершенствования медицинского обслуживания Великобритании (National Institute for Health and Care Excellence, 2016) не рекомендуют использование блокад и малоинвазивных нейрохирургических вмешательств, включая различные варианты радиочастотной денервации [2, 39, 47]. В свою очередь Американское общество интервенционных методов лечения боли (American Society of Interventional Pain Physicians) опубликовало несколько систематических обзоров и клинические рекомендации с доказательством эффективности и безопасности этих методов лечения [48].
Как внутри-, так и внесуставное введение глюкокортикостероидов может обеспечить кратковременное облегчение у пациентов с активным воспалением, но длительный эффект этих препаратов остается недоказанным. В систематическом обзоре D. Kennedy и соавт. оценили эффективность лечения дисфункции КПС методом блокад под рентгенологическим контролем: проанализировано 50 работ, отобрано два рандомизированных плацебоконтролируемых исследования и одно крупное обсервационное. Сделан вывод об эффективности блокад в лечении синдрома КПС (уровень доказательности В) [49]. В других работах подтверждена эффективность как интра-, так и периартикулярных блокад [12, 48].
При сравнении эффективности периартикулярных (n = 58) и интраартикулярных (n = 55) блокад КПС в уменьшении боли (0,5 мл бупивакаина + 20 мг триамцинолона) регистрировалось достоверное снижение выраженности боли, без статистической разницы между ними [50]. Сравнение влияния периартикулярных и интраартикулярных блокад КПС показало достоверное улучшение трудоспособности при периартикулярных инъекциях (по шкале Японской ортопедической ассоциации) – 96 и 62% соответственно. Сделан вывод, что периартикулярные блокады эффективнее и проще в плане технического выполнения и могут быть рекомендованы в качестве метода лечения дисфункции КПС [51]. В нашем исследовании продемонстрирована высокая эффективность периартикулярных блокад с использованием местного анестетика и глюкокортикостероида в трехмесячном периоде наблюдения. Отмечено достоверное снижение выраженности болевого синдрома, степени нарушения жизнедеятельности, тревожно-депрессивных нарушений, а также улучшение качества жизни. Показана высокая безопасность данного метода лечения, не зарегистрировано ни одного серьезного побочного эффекта.
У пациентов со значительным, но кратковременным облегчением боли после блокад в КПС радиочастотная аблация нижнепоясничных дорзальных ветвей и латеральных ветвей S1–S3(4) может обеспечить облегчение боли продолжительностью до года. Денервация – малоинвазивное оперативное вмешательство, позволяющее осуществить деструкцию нервных окончаний с целью быстрого уменьшения болевого синдрома. Радиочастотная денервация основана на принципе термокоагуляции. Этот метод используется уже много лет, он высокоэффективен, имеет широкий спектр показаний, практически лишен осложнений. Высокочастотная невротомия проводится в стерильных условиях, под контролем рентгеноскопии или компьютерной томографии. Радиочастотная денервация осуществляется через микропрокол с минимальной травматизацией прилегающих и обрабатываемых тканей [52]. Эффективность этого способа лечения дискутируется в литературе. В обзоре J. Juch и соавт. не установлена эффективность радиочастотной деструкции в сравнении со стандартным лечением [53]. А L. Leggett и соавт. отмечают эффективность метода, способствовавшего уменьшению боли [54].
По данным L. Manchikanti и соавт., в лечении дисфункции КПС эффективны внутрисуставные и периартикулярные блокады (уровень С), а также радиочастотная деструкция с охлаждаемым электродом (уровень В) [48]. В голландском руководстве по применению инвазивных методик лечения боли в спине отмечено, что при неэффективности консервативной терапии дисфункции КПС могут быть рекомендованы блокады с глюкокортикостероидами. В случае неэффективности блокад с глюкокортикостероидами показана радиочастотная деструкция [8].
В нашем исследовании была продемонстрирована эффективность (по всем оцениваемым параметрам) радиочастотной деструкции КПС. Этот метод хотя и уступал в эффективности блокадам, но разница не достигала статистической достоверности. Необходимо отметить, что состояние пациентов второй группы (получивших лечение радиочастотной деструкцией) изначально было тяжелее по целому ряду параметров. Кроме того, большинство больных этой группы раньше получали лечение блокадами с недостаточным эффектом. Таким образом, мы поддерживаем терапевтический подход, предложенный в голландском руководстве (2015) [8].
Заключение
Дифференцированный подход в оценке основного источника боли у пациентов, страдающих хронической люмбоишалгией, обусловленной дисфункцией КПС, с проведением нейроортопедического обследования, подтверждением диагноза периартикулярной блокадой и дальнейшим таргетным воздействием с помощью методов интервенционной медицины, обеспечил высокую эффективность лечения. Отмечено уменьшение болевого синдром, повышение трудоспособности и качества жизни, психоэмоционального статуса. Полученные результаты согласуются с данными литературы. При дисфункции КПС почти в трети случаев имел место невропатический компонент боли без явлений радикулопатии. Шкала SBST информативна и проста в использовании, что позволяет применять ее в отборе пациентов, нуждающихся в дополнительном лечении, но она не имеет прогностического значения для определения исхода болевого синдрома.
A.V. Kavelina, A.I. Isaykin, M.A. Ivanova
I.M. Sechenov First Moscow State Medical University
Contact person: Aleksey Ivanovich Isaykin, alexisa68@mail.ru
The group of patients with non-specific back pain is heterogeneous, which requires a differentiated approach to treatment. One of the most common sources of pain in nonspecific lumbar ischialgia is the sacroiliac joint (SIJ). Three or more positive provocative tests allow you to diagnose pain in the SIJ with sufficient accuracy.
Diagnostic blockade with local anesthetics is recognized as the gold standard of diagnostics. Treatment is started in accordance with the general principles set out in the international guidelines for the management of patients with non-specific back pain. The most preferred is the multi-modal approach. Among of medical drugs the priorities have non-steroidal anti-inflammatory drugs, including meloxicam.
Provided the results of the study performed to determine the main source of pain in nonspecific lumbar ischialgia for further treatment using minimally invasive procedures, the assessment of their effectiveness and safety. 51 patients (36 women and 15 men, mean age 56.4 ± 2.1 years) with SIJ dysfunction were examined. The first group received conservative treatment in the form of periarticular blockades with local anesthetics and glucocorticoids. The second group was treated in neurosurgical department by the method of radiofrequency denervation of SIJ.
A differentiated approach in assessing the primary source of pain in patients with chronic lumbar ischialgia due to dysfunction of SIJ, with neuro orthopedic survey, confirmation of the diagnosis, periarticular blockade and targeted impact with the use of interventional medicine methods has provided good results, which corresponds to data reported in the literature: reduction in pain, increase of ability, quality of life and psychosocial status.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.