Неалкогольная жировая болезнь печени у коморбидных пациентов: опыт терапии с использованием Тиотриазолина
- Аннотация
- Статья
- Ссылки
- English


Введение, эпидемиология, актуальность
Хронические болезни печени представляют достаточно разнородную группу заболеваний, однако большинство из них объединяют длительное бессимптомное течение и необратимость процессов фиброзирования, что, несомненно, можно отнести к важнейшим медицинским проблемам XXI в. [1, 2].
В целом за последние 20 лет отмечается значительный рост частоты всех заболеваний печени, а неалкогольная жировая болезнь печени (НАЖБП) приобретает поистине грандиозные масштабы. По данным популяционных исследований, распространенность НАЖБП в развитых странах (РФ, страны Европы, США) составляет около 30% населения, в развивающихся странах этот показатель составляет около 10%, что связано в первую очередь с особенностями питания и образом жизни [3].
Российские исследования, проведенные под руководством профессора В.Т. Ивашкина, продемонстрировали результаты, схожие с общемировыми: среди пациентов, обратившихся к терапевту, 27% имели неалкогольную жировую болезнь печени, большинство (около 80%) – на стадии стеатоза, 16% – на стадии стеатогепатита и около 3% – на стадии цирроза печени [4]. Все это говорит о высокой распространенности НАЖБП (в том числе на стадии продвинутого фиброза печени), а также о недостаточном внимании к данной проблеме на уровне первичного звена терапевтической помощи.
В США среди наиболее частых причин цитолитического синдрома у амбулаторных пациентов названа НАЖБП [5]. В 2004 г. опубликованы интересные результаты: целенаправленно обследовано 2287 пациентов семейного врача, в результате чего у 34% выявлена НАЖБП, в подавляющем числе случаев сочетающаяся с метаболическим синдромом [3]. Метаболический синдром включает в себя артериальную гипертонию, дислипидемию, ожирение, нарушения углеводного обмена. В последние годы НАЖБП уже рассматривают как компонент метаболического синдрома, так как в большом проценте случаев данные патологии сочетаются.
При наличии метаболического синдрома и особенно сахарного диабета 2 типа пациент относится к группе высокого риска кардиоваскулярных осложнений (риск 4), кроме того, в течение длительного времени считалось, что НАЖБП сама по себе также является фактором риска сердечно-сосудистой смерти, и исследования последнего десятилетия эту гипотезу подтвердили [6]. Так, одной из множества иллюстраций, подтверждающих независимый вклад НАЖБП в развитие заболеваний коронарных артерий, может служить наблюдение, представленное в 2016 г. группой ученых под руководством N. Perera: в анализ включено 120 пациентов с НАЖБП на доцирротической стадии, не имеющих других установленных факторов риска сердечно-сосудистых осложнений и не злоупотребляющих алкоголем. Все пациенты проходили лечение в госпитале Коломбо по поводу острого коронарного синдрома, 56 из них имели НАЖБП. Для оценки риска летального исхода и развития острого инфаркта миокарда на этапе стационарного лечения и в последующие шесть месяцев использовалась шкала GRACE: по результатам, пациенты с НАЖБП более старшего возраста имели более высокий риск смертности, нежели больные без НАЖБП [7].
Определение, патогенез
Неалкогольная жировая болезнь печени представляет собой гетерогенную группу патологических состояний этого органа, начиная от стеатоза без признаков воспалительной реакции до активного стеатогепатита с выраженными синдромами цитолиза и холестаза, прогрессированием фибротических изменений вплоть до цирроза и гепатоцеллюлярной карциномы.
Формирование неалкогольного стеатогепатита следует считать важной составляющей в развитии болезни: доказано, что именно некровоспалительная реакция активизирует процессы фиброгенеза, приводя к продвинутому фиброзу и циррозу печени [8].
Несмотря на неугасающий интерес исследователей к проблеме НАЖБП, до сегодняшнего дня патогенез данного заболевания полностью не раскрыт. Несомненно, что в основе развития НАЖБП лежат нарушения обменных процессов. Хотя единой теории патогенеза не существует, одним из основополагающих механизмов большинство исследователей признают развитие инсулинорезистентности [9].
Развитие заболевания можно условно разделить на два этапа: отложение в клетках печени липидов в виде жировых вакуолей (стеатоз) и воспалительная реакция с гибелью гепатоцитов и фиброгенезом (стеатогепатит). Течение и скорость прогрессирования фибротических изменений индивидуальны и в каждом конкретном случае могут существенно различаться в зависимости от множества факторов (генетических особенностей, образа жизни, сопутствующей патологии, приема алкоголя и др.) [10].
Лечение
Для многих заболеваний печени до настоящего времени не разработана этиотропная терапия. В ее отсутствие патологический процесс прогрессирует, идут процессы фиброзирования, что потенциально может привести к инвалидизации и смерти пациента. В подобных ситуациях перед практическими врачами встает задача патогенетической терапии, что достигается назначением препаратов группы гепатопротекторов, использование которых не теряет своей актуальности [11].
Важно отметить, что большая часть терапевтических агентов, используемых в гепатологии, имеет в своей основе воздействие на то или иное звено патогенеза, будь то иммуносупрессивная терапия в лечении аутоиммунных заболеваний печени, антиоксидантная терапия при алкогольном поражении печени или лечение НАЖБП.
Неалкогольная жировая болезнь печени крайне сложна для терапии ввиду многофакторности ее развития и целого комплекса взаимосвязанных метаболических нарушений, который лежит в ее основе. Поэтому поиск универсального эффективного терапевтического агента пока представляет собой нерешенную задачу, а использование любого лекарственного препарата в лечении НАЖБП будет оправдано, если имеются положительные эффекты в отношении хотя бы одного отдельно взятого звена патогенеза.
В течение многих лет лечение различных заболеваний печени трудно представить без использования гепатопротекторов. Многие российские и зарубежные исследователи подтвердили эффективность ряда терапевтических агентов в лечении хронических заболеваний печени: это цитокины, антиоксиданты, метаболические препараты и др. Даже в случае проведения этиотропной терапии, когда это возможно, использование гепатопротекторов в качестве вспомогательной терапии существенно улучшает исходы и прогноз [12].
НАЖБП занимает особое место в группе хронических заболеваний печени и находится на стыке специальностей в первую очередь за счет многогранности патогенеза и взаимосвязи с метаболическим синдромом. Отсутствие возможности этиотропной терапии диктует необходимость применения патогенетических средств: коррекции инсулинорезистентности при ее наличии, воздействия на окислительные процессы в гепатоцитах и др. Эффекты гепатопротекторов могут быть направлены на препятствие деструкции мембраны гепатоцитов, восстановление структуры и функций клеток, подавление процессов перекисного окисления липидов и нормализацию метаболизма в клетке.
До настоящего времени не разработаны единые критерии и схемы лечения неалкогольной жировой болезни печени: эффективность традиционно применяемых и новых лекарственных агентов продолжает активно исследоваться, в том числе в повседневной клинической практике [13].
В патогенезе НАЖБП одним из потенциально корригируемых звеньев является развитие оксидативного стресса, воздействие на который стало возможным с использованием группы антиоксидантных препаратов, среди которых относительно недавно стал активно использоваться в гепатологии Тиотриазолин (морфолиний-метил-триазолил-тиоацетат).
Многочисленные эффекты препарата обусловлены особым химическим строением: в его структуре присутствует тиольная группа, за счет которой препарат имеет выраженную восстанавливающую способность и является акцептором электронов от нестойкой активной формы кислорода. Данные свойства реализуются в виде блокировки окислительного стресса не только на ранней стадии, но и на более поздних этапах [14].
Таким образом, препарат обладает мембраностабилизирующим эффектом, который обусловлен его антиоксидантными свойствами: клеточные мембраны остаются способными к сохранению своих физико-химических свойств (нормальный трансмембранный потенциал, проницаемость и др.), за счет чего осуществляется жизнедеятельность клетки. Тиотриазолин активирует лактатдегидрогеназу и пируваткиназу, ферменты малат-аспартатного челночного механизма, что активизирует аэробный и анаэробный пути окисления глюкозы, вследствие чего восстанавливается макроэргический пул и снижается лактат-ацидоз в гепатоцитах даже при развитии гипоксии. Иными словами, Тиотриазолин за счет антиоксидантных эффектов препятствует гибели гепатоцитов, замедляет прогрессирование жирового гепатоза, тормозит развитие некровоспалительной реакции и стимулирует процессы регенерации. Кроме того, препарат обладает рядом положительных эффектов в отношении состава и качества желчи: Тиотриазолин способствует увеличению образования и секреции желчи, нормализации ее состава [15].
К настоящему времени препарат уже показал свою эффективность в комплексной терапии хронических вирусных гепатитов, алкогольной болезни печени и ряда других.
Особого внимания требуют коморбидные пациенты, имеющие заболевание печени и патологию сердечно-сосудистой системы. В группе пациентов с НАЖБП таких больных больше 50%, ведь патогенез данного заболевания неразрывно связан с метаболическими нарушениями, обусловливающими повышенный риск коронарных осложнений: это дислипидемия, гипергликемия (нарушение толерантности к углеводам и сахарный диабет), ожирение. Лечение таких пациентов должно быть комплексным, и группа антиоксидантных препаратов обоснованно занимает свое место в терапии.
Так, еще в 1996 г. в базе PubMed были опубликованы результаты исследования, в котором изучалось влияние Тиотриазолина на эффективность антиангинальной терапии у возрастных пациентов. Для оценки эффективности терапии использовались инструментальные (электрокардиограмма, функциональные пробы) и лабораторные методы. В результате было показано, что включение Тиотриазолина в комплексную антиангинальную терапию у больных ишемической болезнью сердца (ИБС) в старшей возрастной группе повышало ее эффективность [16].
Комплексный подход к терапии инфаркта миокарда у пациентов с НАЖБП представлен в журнале «Медицина неотложных состояний» в 2017 г.: исследовались эффекты Тиотриазолина в сочетании с фосфолипидами. Исследование включало 47 пациентов с острым Q-образующим инфарктом миокарда и наличием сопутствующего неалкогольного стеатогепатита. Пациенты были разделены на три группы: 16 человек получали только стандартную антиишемическую терапию, 16 – в сочетании с Тиотриазолином и 15 – с Тиотриазолином и эссенциальными фосфолипидами. Оценка состояния и результатов функциональных проб проводилась до и после трехнедельной терапии. В результате было показано, что использование комплексной терапии с включением в стандартную схему Тиотриазолина и эссенциальных фосфолипидов способствовало более выраженному увеличению биоэлектрических потенциалов миокарда и лучшей регенерации кардиомиоцитов по периферии зоны инфаркта [17]. Таким образом, использование Тиотриазолина усиливает положительные эффекты стандартной терапии. Кроме того, назначение статинов у данной группы пациентов существенно ограничено показателями цитолиза, поэтому применение гепатопротекторов расширяет возможности антиангинальной и гиполипидемической терапии.
Наше исследование посвящено вопросам эффективности и безопасности Тиотриазолина у коморбидных пациентов с НАЖБП. Целью явилось оценить клиническую и лабораторную картину до и после курса терапии с использованием Тиотриазолина.
Материал и методы
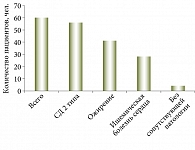
В условиях стационара отделения заболеваний печени Московского клинического научно-практического центра им. А.С. Логинова комплексно обследовано 60 пациентов с неалкогольной жировой болезнью печени, из них 38 (63%) женщин, 22 (37%) мужчины. Средний возраст обследуемых составлял 55,2 ± 6,1 года.
Сопутствующую патологию сердечно-сосудистой системы имели 28 человек (ишемическая болезнь сердца: стенокардия напряжения, атеросклеротический кардиосклероз), сахарный диабет – 56 человек и ожирение – 41 (рисунок).
Всем больным проводились оценка клинического и биохимического анализов крови, липидного спектра, ультразвуковое исследование, оценка степени фиброза печени методом эластометрии до и после курса терапии, а также комплексное обследование перед началом исследования для исключения возможных других этиологических факторов заболевания печени (исключение вирусных гепатитов, аутоиммунных заболеваний печени, болезней накопления, опросники САGE и AUDIT-C для исключения алкогольного гепатита).
В условиях стационара пациенты получали Тиотриазолин в дозе 100 мг внутривенно капельно в течение пяти дней с последующим переходом на пероральный прием по 200 мг три раза в сутки в течение двух недель.
Результаты
Общая характеристика и результаты обследования пациентов до начала терапии представлены в табл. 1 и 2.
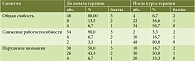
Клиническая картина заболевания представлена различными проявлениями астенического синдрома (общая слабость, снижение работоспособности, нарушение внимания). Динамика клинических проявлений до и после курса лечения представлена в табл. 3.
Таким образом, по завершении курса терапии большинство пациентов отметили снижение проявлений астенического синдрома в виде уменьшения общей слабости, повышения работоспособности и концентрации внимания.
Пациенты с клиническими проявлениями ИБС (стенокардия напряжения) отметили повышение толерантности к физической нагрузке, снижение частоты ангинозных приступов за время лечения.
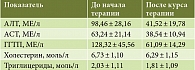
Важно отметить и динамику лабораторных проб: снижение выраженности синдрома цитолиза и уменьшение уровня гамма-глутамилтранспептидазы. Следует отдельно остановиться на улучшении показателей липидного профиля, что важно для пациентов с сопутствующей ИБС (табл. 4).
Обсуждение результатов и выводы
Наш собственный опыт применения Тиотриазолина в терапии НАЖБП свидетельствует о его эффективности, что выражается в четкой положительной динамике показателей синдрома цитолиза, снижении уровня общего холестерина и триглицеридов, а также клиническом улучшении состояния пациентов. Отдельно следует остановиться на вопросах безопасности: за время терапии и дальнейшего амбулаторного наблюдения нежелательных явлений при приеме Тиотриазолина у пациентов не наблюдалось.
Важным представляется и наличие кардиопротективного эффекта, что позволяет рассматривать применение Тиотриазолина не только у больных НАЖБП, но и у коморбидных пациентов с сопутствующей ИБС в дополнение к стандартной антиангинальной и гиполипидемической терапии.
Несмотря на активное применение классической антиангинальной терапии, большая часть пациентов с клиническими проявлениями ИБС имеют неудовлетворительное качество жизни, что проявляется ограничением привычной физической активности, а также болевыми приступами. Кардиопротективное лечение в этой ситуации позволит улучшить качество жизни больного. Кардиопротекторы представляют собой достаточно разнородную группу препаратов, в которой особое место занимают метаболические средства. Самым быстрым источником энергии является глюкоза, которая утилизируется путем аэробного гликолиза, однако в условиях ишемии миокарда утилизация глюкозы идет по менее эффективному анаэробному пути. Для вступления глюкозы в цикл Кребса и образования аденозинтрифосфата требуется присутствие пирувата. На это звено успешно воздействует Тиотриазолин, который активирует образование пирувата, что является несомненным преимуществом препарата [18].
Таким образом, за счет своих кардио- и гепатопротекторных свойств, а также положительного влияния на показатели липидного профиля Тиотриазолин можно с уверенностью назвать универсальным препаратом для группы коморбидных пациентов с НАЖБП.
A.V. Polukhina, Ye.V. Vinnitskaya, D.S. Bordin, Yu.G. Sandler
A.S. Loginov Moscow Clinical Scientific and Practical
Contact person: Yelena Vladimirovna Vinnitskaya, e.vinnitskaya@mknc.ru
The article describes the pathogenesis and possible methods of therapy of nonalcoholic fatty liver disease, including in the group of comorbid patients. The mechanisms of Thiotriazoline action in NAFLD patients are examined. We present clinical cases of a positive impact of Thiotriazoline in NAFLD patients.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.