Неалкогольные стеатогепатит: лечение с позиций доказательной медицины
- Аннотация
- Статья
- Ссылки
Неалкогольная жировая болезнь печени (НАЖБП) – заболевание, ассоциированное с метаболическими расстройствами, не обусловленными воздействием алкоголя. Заболевание имеет несколько морфологических форм (стадий): печеночный стеатоз, стеатогепатит, стеатогепатит с фиброзом, цирроз печени.
Неалкогольный стеатогепатит (НАСГ) – самостоятельная нозологическая единица, для которой характерны повышение активности ферментов печени в крови, морфологические изменения в биоптате печени, подобные изменениям при алкогольном гепатите – жировая дистрофия и воспалительная реакция.
Неалкогольная жировая болезнь печени (НАЖБП) – заболевание, ассоциированное с метаболическими расстройствами, не обусловленными воздействием алкоголя. Заболевание имеет несколько морфологических форм (стадий): печеночный стеатоз, стеатогепатит, стеатогепатит с фиброзом, цирроз печени.
Неалкогольный стеатогепатит (НАСГ) – самостоятельная нозологическая единица, для которой характерны повышение активности ферментов печени в крови, морфологические изменения в биоптате печени, подобные изменениям при алкогольном гепатите – жировая дистрофия и воспалительная реакция.

Эпидемиология
НАЖБП встречается в популяции приблизительно у 20–40% населения, при этом у 15–20% больных НАЖБП выявляется цирротическая стадия [52, 63]. В США заболевание поражает до 30% всей популяции [45]. Эпидемиологическое исследование в России, включающее почти 31 тыс. человек, показало, что 27% пациентов, посещающих терапевта, имеют НАЖБП. В районах Сибири частота НАЖБП достигает 31,6% [8, 10]. Частота НАЖБП в Европе составляет 10–15% всех хронических заболеваний печени. Интересно, что 60–80% всех криптогенных циррозов выявляются у пациентов с НАЖБП [55]. Необходимо отметить, что в 10% случаев показанием для трансплантации печени является НАЖБП.
НАЖБП развивается преимущественно в возрасте старше 45 лет, у женщин в 3 раза чаще, чем у мужчин, хотя в последние годы отмечается обратная тенденция. Так, например, в США НАЖБП наблюдается в 3-5 раз чаще у мужчин, что связано с большей распространенностью ожирения.
Большинство авторов рассматривают следующие стадии этого заболевания:
- жиросодержащая печень;
- печени;
- стеатогепатит (НАСГ);
- печени («жировой цирроз печени») [58,82].
Этиология НАЖБП
НАЖБП представляет собой многофакторное заболевание, развивающееся в результате воздействия целого ряда факторов риска: абдоминального ожирения (объем талии более 94 см у мужчин и 80 см у женщин); повышения уровней триглицеридов в крови более 1,7 ммоль/л, холестерина со снижением содержания липопротеидов высокой плотности; повышения артериального давления более 130/85 мм; нарушения толерантности к глюкозе, длительной гипергликемии (сахарный диабет 2 типа); повышения уровня мочевой кислоты в моче более 0,4 ммоль/л и, самое главное, инсулинорезистентности [18, 30, 50]. У пациентов с ожирением НАЖБП встречается в 40–90%, а при индексе массы тела выше 30 – более чем в 90% случаев [15, 23, 74]. Важную роль в развитии НАЖБП играют такие генетические факторы, как полиморфизм генов, реглирующих окисление жирных кислот, равновесие окислительных процессов в клетке и экспрессию фактора некроза опухоли-альфа (ФНО-α) [22].
Патогенез НАСГ
В настоящее время общепринятой моделью патогенеза НАСГ является теория двух «толчков». Развитие стеатоза (первичный толчок) происходит в результате последовательных процессов: инсулинорезистентность, стимуляция липолиза и повышение транспорта свободных жирных кислот в печень, угнетение их окисления в митохондриях с накоплением триглицеридов и снижением экскреции жиров гепатоцитом. Оксидативный стресс (второй толчок – multi-hit) возникает в результате образования продуктов перекисного окисления липидов (ПОЛ) (свободные жирные кислоты являются субстратом для перекисного окисления липидов) и реактивных форм кислорода и цитокинов (ФНО-α, интерлейкина 6 (ИЛ-6) и др.) [17, 35, 36, 58, 82].
ПОЛ сопровождается набуханием митохондрий, ломкостью лизосом, нарушением целостности клеточных мембран, коллагенообразованием, что приводит к некрозу гепатоцитов и развитию воспалительной клеточной инфильтрации – происходит формирование неалкогольного стеатогепатита. Кроме того, продукты ПОЛ, некроз гепатоцитов, ФНО-α, ИЛ-6 вызывают активацию звездчатых клеток, что сопровождается избыточной продукцией соединительной ткани с развитием фиброза, а при длительном персистировании процесса – цирроза печени [17].
Клиническая картина НАСГ
Для неалкогольного стеатогепатита, как правило, не характерна яркая клиническая картина. Возможно наличие астенического синдрома, дискомфорта в правом подреберье, гепатомегалии примерно у 50–75% пациентов. На поздних стадиях появляется клиника цирротической стадии с синдромом портальной гипертензии и печеночно-клеточной недостаточности.
Диагностика НАСГ
Для диагностики НАСГ необходимо исключить злоупотребление алкоголем в анамнезе, хронический вирусный гепатит, метаболические заболевания печени (болезнь Вильсона, гемохроматоз), аутоиммунные болезни печени, лекарственный гепатит. Диагноз НАСГ – это диагноз исключения [21]. При этом нужно учитывать тот факт, что в клинической практике мы нередко сталкиваемся с гепатитами смешанной этиологии, например, НАСГ и вирусный гепатит, НАСГ и алкогольный гепатит, НАСГ и вирусно-алкогольный гепатит и прочие. Что касается биохимических изменений, то они носят неспецифический характер. Умеренный цитолиз регистрируется у 50–90% больных, соотношение АСТ/АЛТ, как правило, всегда менее 1. В последнее время для больных хроническими заболеваниями печени в клинической практике рекомендуются новые нормы АЛТ и АСТ: 30 U/L для мужчин и 17 U/L для женщин. Билирубин в норме или умеренно повышен, возможно умеренное повышение щелочной фосфатазы и ГГТП. Нередко одновременно с повышением уровня АЛТ определяется дислипопротеидемия и нарушения углеводного обмена [51].
Некоторые специалисты используют различные индексы для определения риска НАСГ. Например, индекс HAIR (Hypertension, ALT, Insulin Resistance) включает гипертензию, повышение АЛТ и инсулинорезистентность [37]. Индекс ВААТ (BMI, Age, ALT, Triglycerides) включает индекс массы тела (ИМТ) выше 28, возраст старше 50 лет, уровень AЛT более 2 норм, повышение уровня триглицеридов [74, 82]. J.-H. Lee предложил NAFDL-индекс, который рассчитывается по формуле: у = 8 * АЛТ/АСТ + величина ИМТ. При значении индекса менее 31 диагноз НАЖБП маловероятен, если величина y выше 36 – вероятность диагноза более 90%. Специфичность индекса NAFDL составляет 91,2%. [57].
Инструментальная диагностика включает УЗИ брюшной полости (УЗ-признаками НАЖБП являются гиперэхогенность печени и гепатомегалия), компьютерную и магнитно-резонансную томографию [67]. Чувствительность УЗИ и магнитно-резонансной томографии для диагностики НАЖБП составляет 45% и 90,9%, специфичность – 90% и 94% соответственно [80]. Неинвазивными методами оценки активности воспалительных изменений и фиброза в печени являются фиброскан, фибротест и актитест [28].
Тем не менее «золотым стандартом» диагностики НАЖБП остается биопсия печени. Гистологическая картина в печени при этом заболевании характеризуется крупнокапельной жировой дистрофией в 3-й зоне (центролобулярно). Позднее появляются признаки гепатита, фиброза, нередко – цирроза печени. Оценка гистологической активности и фиброза проводится по E. Brunt [31]. Необходимо отметить, что при алкогольном и неалкогольном гепатите морфологическая картина идентична. Однако, учитывая инвазивность метода и риск осложнений, предпочтение следует отдавать неинвазивным методам обследования.
Лечение НАСГ
В настоящее время не существует стандартной схемы лечения НАЖБП, основанной на доказательной базе [2, 9]. Стандарты лечения этого заболевания разработаны только для стран азиатско-тихоокеанского региона [40].
Ведение пациентов необходимо начинать с общих рекомендаций по режиму питания и физической активности, особенно на фоне ожирения и сахарного диабета. В настоящее время общепризнано, что начинать лечение следует с немедикаментозных мероприятий – исключения алкоголя, отмены гепатотоксичных лекарств, гиполипидемической диеты.
Основой патогенетического лечения НАЖБП являются меры, направленные на преодоление инсулинорезистентности [7, 21, 69]. Многочисленные клинические исследования доказывают, что физические нагрузки способствуют увеличению чувствительности рецепторов к инсулину, а физические упражнения не менее 1 часа в день в сочетании с диетой приводят к достоверно значимому улучшению биохимических и гистологических показателей [23, 33, 49, 72]. Снижение веса на 500–1000 г в неделю сопровождается положительной динамикой клинико-лабораторных показателей, снижением инсулинорезистентности, уровня IgА и степени стеатоза в печени [21, 37, 46, 50]. Слишком быстрая потеря веса, в свою очередь, приводит к ухудшению течения заболевания. В европейских клиниках пациенту со стеатозом печени или НАСГ с минимальной активностью первоначально рекомендуют только немедикаментозные методы лечения. Вопрос о назначении медикаментозной терапии решается на последующих визитах при достижении целевого веса. Стандарты ведения пациентов с НАСГ в странах тихоокеанско-азиатского региона в качестве первой ступени терапии также рекомендуют только немедикаментозные мероприятия – диету, увеличение физической активности, снижение веса. При повышении холестерина назначают статины, возможно также проведение бариатрических операций. Вторая ступень терапии включает лекарственные средства – инсулиносенситайзеры, гепатопротекторы и антиоксиданты (витамин Е, бетаин, урсодезоксихолевая кислота, пентоксифиллин) [40].
При выборе медикаментозной терапии следует учитывать многофакторную природу заболевания. Если диета и физические упражнения не дают результата, назначают препараты для снижения веса – орлистат (блокатор панкреатической липазы). Его эффективность подтверждается результатами плацебо-контролируемого слепого рандомизированного исследования по лечению пациентов НАСГ в течение 6 месяцев, в ходе которого наблюдалось уменьшение цитолиза, уменьшение стеатоза и фиброза в печени [46].
Поскольку инсулинорезистентность является главным патогенетическим звеном в развитии НАЖБП [15, 21, 65], для ее преодоления используют инсулиносенситайзеры метформин и тиазолидиндионы. К сожалению, среди терапевтов широко распространено мнение, что эти препараты нужно рекомендовать только при лечении сахарного диабета. Клинические исследования по изучению эффективности метформина (Сиофора) при НАСГ показали, что использование препарата в дозе 1,5–2 г/кг/сут в течение 6–12 месяцев приводит к уменьшению инсулинорезистентности, снижению аппетита, гликемии, синтеза липидов в печени, усилению окисления жирных кислот, уменьшению уровня триглицеридов, ФНО-α, улучшению биохимической и гистологической картины (снижение стеатоза и фиброза) [32, 81]. Применение метформина по 1,5 г/кг/сут в течение 4 месяцев приводит к уменьшению инсулинорезистентности и цитолитического синдрома [66]. Повторная пункционная биопсия у пациентов, получавших метформин в дозе 2 г в сутки в течение 1 года в рамках рандомизированного исследования, продемонстрировала значительное уменьшение жировой инфильтрации, некровоспалительной активности, а также фиброзных изменений печени [32, 70]. Таким образом, метформин эффективен при НАСГ, в том числе и у пациентов без сахарного диабета [79].
В плацебоконтролируемом исследовании PIVENS, а также ряде других, был продемонстрирован противовоспалительный и метаболический эффект пиоглитазона, на фоне терапии которым происходило уменьшение инсулинорезистентности, синтеза жирных кислот в гепатоцитах, воспаления, улучшение гистологической картины печени [29, 42, 73].
Положительные эффекты розиглитазона были продемострированы в рандомизированном плацебоконтролируемом исследовании FLIRT-2, где регистрировалось уменьшение инсулинорезистентности, уровня трансаминаз, улучшение гистологической картины печени [29, 71, 75].
При неэффективности немедикаментозных методов лечения дислипопротеидемии при НАСГ рекомендуется применение статинов [60]. При этом следует учитывать их гепатотоксическое действие. Статины не назначаются при цитолизе более 2 норм, лучше одновременно с гепатопротекторами и под контролем печеночных тестов. В ряде плацебоконтролируемых слепых клинических исследований продемонстрирована безопасность и эффективность аторвастатина [38, 47, 53].
Определенный интерес для лечения НАСГ представляют препараты с противовоспалительным действием. Результаты ряда исследований показали, что пентоксифиллин при НАСГ подавляет воспалительный процесс в печени, снижает уровень ФНО-α, ИЛ-6, ИЛ-8, замедляет процессы фиброгенеза и улучшает микроциркуляцию в печени [20]. Однако исследования эффективности инфликсимаба (моноклональные антитела к ФНО-α) не подтвердили эффективность и безопасность препарата при НАСГ.
Учитывая полифакторный генез НАСГ, помимо коррекции инсулинорезистентности и липидного обмена показано назначение антиоксидантов и гепатопротекторов.
Большинство специалистов считают, что антиоксиданты являются неотъемлемой частью лечения НАСГ [15, 21, 69]. Плацебоконтролируемое исследование по применению витамина Е в дозе 300–800 мг/сут в течение 12 месяцев показало, что при этом варианте терапии происходит уменьшение фиброза в печени при НАСГ [44]. В клиническом исследовании по лечению НАСГ A.J. Sanyal был получен более значимый клинический эффект при сочетании витамина Е с пиоглитазоном по сравнению с монотерапией витамином Е [78].
Перспективными для лечения данной патологии являются препараты альфа-липоевой кислоты (Берлитион, Тиогамма, Эспа-липон), которые снижают уровень холестерина, глюкозы, обладают антиоксидантными свойствами, являясь «ловушкой» для свободных радикалов [16]. Рандомизированное клиническое исследование с применением альфа-липоевой кислоты в комбинации с витамином Е при НАСГ продемонстрировало снижение уровня трансаминаз, ФНО-α, липопротеидов низкой плотности и триглицеридов [26]. Зафиксирован также положительный эффект назначения альфа-липоевой кислоты в комбинации с метформином: было отмечено улучшение клинических характеристик, показателей липидного и углеводного обменов, уменьшение УЗИ-признаков стеатоза и гистологической картины печени [3, 12, 62].
Существует положительный опыт по коррекции микробиоценоза кишечника при НАСГ, клинические рандомизированные исследования по применению пробиотиков при НАСГ [62].
На сегодняшний день накоплен большой опыт применения эссенциальных фосфолипидов (Эссенциале Н, Эссливер, Фосфоглив), силимарина (Гепабене, Легалон) при НАСГ [1, 9]. К основным эффектам препаратов относят мембраностабилизирующее, антиоксидантное, детоксицирующее, антифибротическое действие.
При этом наибольшее количество клинических исследований посвящено оценке эффективности препаратов урсодеоксихолевой кислоты (УДХК). Известно, что УДХК обладает антиоксидантным, мембранстабилизирующим, цитопротективным, антиапоптотическим, иммуномодулирующим, антифибротическим, холеретическим действием и с успехом может применяться при стеатогепатите [19, 61]. На фоне лечения стандартными дозами УДХК у больных НАСГ происходит достоверное улучшение биохимических показателей [77]. Плацебоконтролируемые мультицентровые исследования по изучению эффективности высокодозного (23–28 мг/кг) режима применения УДХК, в свою очередь, не показали преимуществ над стандартными дозировками [59, 77].
Кроме того, в ряде работ было показано снижение уровня N-терминального пептида проколлагена 3 типа и металлопротеиназ в сыворотке крови и улучшение гистологической картины печени при лечении УДХК [35, 48], однако другими авторами не отмечен четкий положительный эффект УДХК в отношении гистологической динамики [53, 56]. Получены данные о высокой эффективности применения УДХК при НАСГ в комбинации с симвастатином в течение 6 месяцев терапии [11]. Рандомизированное исследование показало эффективность УДХК в комбинации с пентоксифиллином при НАСГ в виде уменьшения цитолитического синдрома и фиброза на начальных стадиях заболевания [35].
Перспективным направлением терапии НАСГ является применение L-орнитина-L-аспартата (Гепа-Мерц). Гепа-Мерц – детоксикант, обеспечивающий связывание аммиака, регулирует обмен в гепатоцитах. Препарат, синтезированный в 1960-х гг. в Японии как средство детоксикации при отравлении аммиаком, в последующем использовался для лечения печеночной энцефалопатии. Основной причиной развития энцефалопатии является повышение концентрации аммиака в крови, применение Гепа-Мерц приводит к увеличению активности ферментов цикла обезвреживания аммиака в печени и мышцах, повышает толерантность к белку.
В настоящее время доказаны также гепатопротективные свойства препарата [2, 14, 41]. В многоцентровом нерандомизированном проспективном когортном исследовании, включающем 1167 больных с хроническими заболеваниями печени (в том числе 648 больных с НАСГ), показана эффективность и хорошая переносимость Гепа-Мерц [41]. В ряде клинических исследований показана высокая эффективность этого лекарственного средства, улучшение биохимических показателей печени при НАСГ [2, 14, 34]. К его основным гепатопротективным свойствам относят способность повышать энергетический ресурс митохондрий гепатоцитов, анаболический эффект (увеличение синтеза белка), уменьшение дистрофии гепатоцитов, повышение их устойчивости к повреждающим агентам (включая активные формы кислорода), мембраностабилизирующее и антиоксидантное действие [2, 13, 54].
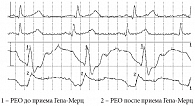
Наши исследования показали, что гепатопротективные свойства Гепа-Мерц обусловлены, в том числе его положительным воздействием на порто-печеночную гемодинамику. Методом полигепатографии было выявлено влияние препарата на пресинусоидальный и на синусоидальный кровоток1 (рис. 1) [4, 5, 6].
В 2010 г. Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова
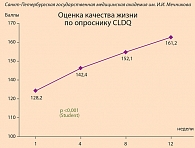
участвовала в многоцентровом нерандомизированном клиническом исследовании, целью которого была оценка терапевтической эффективности (гепатопротективный эффект и влияние на качество жизни) и переносимости препарата L-oрнитин-L-аспартат (Гепа-Мерц) у пациентов с неалкогольным стеатогепатитом. Клиническое исследование проводилось в 18 центрах, обследовано 289 пациентов. Диагноз был установлен по анамнестическим, клинико-биохимическим данным и УЗИ; критериями исключения были наличие хронического вирусного, алкогольного, аутоиммунного и лекарственного гепатита. Пациенты получали Гепа-Мерц перорально по 1 пакету гранулята (3 г активного вещества) 3 раза в день после еды в течение 3 месяцев. В исследовании было выделено 4 базовых точки-визита (1, 4, 8 и 12-я неделя лечения). Критериями оценки эффективности лечения являлись динамика биохимических показателей крови (АЛТ, АСТ, щелочная фосфатаза, билирубин, общий белок, альбумин, глюкоза, креатинин, мочевина) (рис. 2), динамика клинической симптоматики (астенический, диспептический и болевой синдромы), динамика времени выполнения теста связи чисел (ТСЧ), показателей качества жизни (по опроснику CDLQ, в баллах). Анализ эффективности лечения показал, что к 12-й неделе терапии достоверно уменьшался астенический, диспептический и болевой (р = 0,007) синдромы (рис. 2), снижалась активность АЛТ, АСТ (р = 0,029) и гамма-глутамилтранспептидазы (ГГТП) (р = 0,003), уменьшилось время выполнения теста связи чисел с 41,9 до 36,4 (р = 0,018). Показатели качества жизни повысились с 128,2 до 161,2 баллов (р < 0,001). Таким образом, лечение пациентов НАСГ с включением Гепа-Мерц на протяжении 3 месяцев способствовало значимому улучшению клинико- биохимических показателей и демонстрировало хорошую переносимость препарата (рис. 3). L-орнитин-L-аспартат (Гепа-Мерц) может быть рекомендован для лечения пациентов с неалкогольным стеатогепатом. В дальнейшем необходимо планировать клинические исследования эффективности Гепа-Мерц у пациентов с НАСГ с проведением биопсии печени для оценки гистологической динамики).
Таким образом, многочисленные клинические исследования, посвященные лечению НАСГ, показали эффективность снижения веса, диеты, физических нагрузок, применения статинов (аторвастатина), орлистата, инсулиносенситайзеров (метформина и глитазонов), антиоксидантов-гепатопротекторов (витамин Е, альфа-липоевая кислота, УДХК, L-орнитин-L-аспартата).
Перспективы лечения НАСГ
Продолжается изучение новых звеньев патогенеза стеатогепатита в качестве новых терапевтических мишеней. Примерами являются открытие регуляторной молекулы microRNA, обнаруженной в периферической жировой ткани больных НАСГ [39], гамма-рецептора пролифератора-активатора пероксисом PPAR–gamma, регулирующего накопление липидов и метаболизм глюкозы [68], митохондриального протеин-регулятора HINT2 [24], регулятора инсулинорезистентности KLF6 (Kruppel like factor) [27, 43], селективных ингибиторов апоптоза GS-9450 и TRO 19622 (2-я фаза клинических исследований) [76]. Перспективно использование римонабанта – селективного антагониста рецепторов каннабиноидов СВ1, препарат снижает липогенез, повышает уровень адипонектина, улучшает липидный профиль [25].
Необходим дальнейший поиск подходов к диагностике и лечению НАЖБП.
1 Метод лечения запатентован, патент № 2286773
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.