Недержание мочи при напряжении и α1-адреноблокаторы: теоретическое обоснование концепции консервативной терапии
- Аннотация
- Статья
- Ссылки
Долгое время α1-адреноблокаторы рассматривались только с одной позиции, основанной на данных нейроанатомии. Поскольку в шейке мочевого пузыря и в проксимальной уретре расположено большое количество α-адренорецепторов, то назначение препаратов из данной группы лекарственных средств (ЛС) должно усиливать или вызывать недержание мочи у женщин. Соответственно назначение α1-адреноблокаторов считается обоснованным лишь в случаях повышенного сопротивления шейки мочевого пузыря. Второе направление применения этой группы ЛС ограничивается коррекцией императивных расстройств мочеиспускания. Исследование, проведенное для установления достоверной терапевтической эффективности теразозина (1), показало что статистически достоверной разницы между плацебо и препаратом нет. Так как оценка в основной и группе сравнения проводилась по шкале IPSS, доказать эффективность применения α-блокатора не удалось. С другой стороны, клинические наблюдения использования доксазозина, показывали, что при его назначении возникало недержание мочи (2, 3). Рекомендации, последовавшие за этими случаями, носили однозначный характер и сводились к тому, что следует очень осторожно относиться к α1-адреноблокаторам и внимательно вести больных в случае назначения.
Развитие концепции улучшения органного кровообращения при назначении α1-адреноблокаторов, нашло свое отражение в том, что с конца прошлого века препараты этой группы стали рассматриваться не только как средства для уменьшения динамической обструкции шейки мочевого пузыря, но и как мощные сосудистые препараты (5, 6). Комбинация с витаминами и производными никотиновой кислоты оказалась весьма удачной и нашла свое применение для лечения нестабильного детрузора и недержания мочи у женщин (6, 7, 8).
Следует особо отметить, что в специальной литературе мало источников, отражающих результаты применения α1-адреноблокаторов для лечения недержания мочи у женщин. Именно этому вопросу посвящено наше исследование.
Материал и методы
Под нашим наблюдением находились 34 женщины с комбинированной формой недержания мочи, клиническая картина расстройств мочеиспускания у которых была обусловлена преимущественно стрессовым компонентом (недержание мочи при напряжении, НМПН). Средний возраст в группе наблюдения – 51 год (от 22 до 76 лет).
Обследование перед началом терапии включало 3-суточный урофлоуметрический мониторинг, УЗИ, лабораторную диагностику. Консультации смежных специалистов выполнялись по показаниям (невролог, кардиолог, гинеколог). Оценка выраженности недержания мочи проводилась с помощью таблицы, представленной в работе (8), полученные данные обрабатывались с помощью программного обеспечения УРОВЕСТ и пакета программ MS Office 97. Дизайн исследования был предварительно одобрен этическим комитетом ВГМУ.
После заполнения таблиц оценки недержания мочи и выполнения объема предварительного обследования, назначался курс терапии, в который входил α1-адреноблокатор теразозин (Сетегис, фармацевтическая фирма «ЭГИС») в возрастающей дозировке 1 мг 1 раз на ночь 2 недели, затем 2 мг на ночь 6 недель и последние 4 недели по 5 мг на ночь однократно, пикамилон 50 мг трехкратно в сутки и витамины группы В. Периодические осмотры выполнялись каждые 2 недели, а в конце курса терапии повторяли домашний урофлоумониторинг. Количественную оценку выраженности недержания мочи с помощью таблицы рассчитывали только после отмены терапии не ранее чем через 4 недели. За это время исчезали побочные эффекты и у части пациенток происходило восстановление механизма удержания мочи.
Результаты
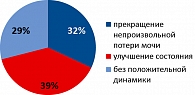
Нами отмечено, что после назначения α1-адреноблокаторов, а также после повышения дозировки при титровании ЛС, происходило усиление недержания мочи. Поскольку все пациентки были предупреждены о возможных побочных явлениях и в частности об этой особенности, случаев отмены препаратов нами не отмечено. Вместе с этим, после окончания курса терапии и обработки результатов в катамнезе, стало очевидным, что на консервативном лечении положительная динамика была отмечена далеко не у всех больных. Из группы были выделены три подгруппы: 11 случаев полного прекращения непроизвольной потери мочи, 13 случаев существенного улучшения состояния и 10 случаев, когда существенной динамики отмечено не было (рисунок 1).
Как следует из диаграммы, представленной на рисунке 1, у каждой третьей больной результата в виде восстановления или улучшения механизма удержания мочи не получено, но у 71% пациенток отмечен положительный эффект. В процессе терапии достаточно интересно проявлялся побочный эффект α1-адреноблокаторов. Так у пациенток, которые теряли ранее мочу при чихании и кашле, появилось постоянное подтекание мочи без какой-либо причины или физического напряжения. Вместе с этим при чихании и кашле, наоборот, потери мочи не отмечалось. Наиболее часто такое явление наблюдалось на малых дозировках теразозина, 0,5 или 1 мг в сутки. При увеличении дозы до 2 мг и более, возникало недержание мочи без какой-либо дифференцировки условий инконтиненции. Данное наблюдение есть наглядная демонстрация того, что в малой концентрации α1-адреноблокатора возникает улучшение периферического кровообращения, но блокада α-рецепторов шейки мочевого пузыря остается невыраженной. Однако при увеличении дозировки все больший удельный вес приобретает локальный, «уроселективный» эффект, который и скрывает основной лечебный.
На период назначения препарата или увеличения дозировок, особенно минимальных, пациентки отмечали усиление недержания мочи. Далее при ведении пациенток на дозах 2-4 и более мг в сутки выраженность инконтиненции или вообще не менялась, или менялась несущественно. В любом случае, качество жизни во время консервативной терапии не улучшалось, а в каждом четвертом случае даже ухудшалось. Вероятно, это обстоятельство не позволило рассматривать данный вид терапии как успешный при каком-либо широком назначении без предварительного отбора и титрования препарата.
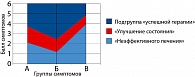
Обращает на себя внимание тот факт, что все пациентки, у которых недержание мочи исчезло, изначально имели относительно невысокий балл во всех группах симптомов (соответственно 1, 2 и 4 группы симптомов по таблице). Этот уровень статистически значимо отличался от уровня соответствующих групп симптомов тех пациенток, у которых после отмены лечения выраженность недержания мочи осталось на исходном уровне. На диаграмме (рисунок 2) можно отметить своеобразный коридор, отмеченный цифрой «2», разделяющий подгруппы «1» (успешная терапия) и «3» (неэффективного лечения).
Неэффективная, или малоэффективная терапия чаще наблюдалась у пациенток старше 50 лет. Нами установлено, что средний возраст в подгруппе с хорошими результатами (включая тех пациенток, у которых недержание мочи устранено), составил 49 лет, тогда как в подгруппе «без успеха лечения», средний возраст 58 лет.
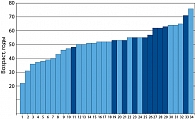
Но на представленной на рисунке 3 диаграмме можно заметить еще один интересный факт. Наиболее многочисленная возрастная подгруппа пациенток, участвовавших в исследовании, включала 15 случаев в возрасте от 50 до 60 лет, далее следовали 8 случаев старше 60. Две подгруппы – до 40 и от 40 до 50 лет – всего в сумме составили 11 случаев. Явно заметен фактор возраста в развитии такого заболевания, как недержание мочи.
Неприятной особенностью данного варианта терапии является то, что в период назначения α1-адреноблокаторов недержание мочи у женщин усиливается, соответственно качество жизни существенно снижается, особенно при невыраженной инконтиненции, наблюдаемой в начальной стадии заболевания. В связи с этим нами было рекомендовано пациенткам использовать специально разработанные прокладки MoliMed (Hartmann), позволяющие нейтрализовать нежелательный побочный эффект назначения лекарственных средств.
Результаты клинического наблюдения в катамнезе убедительно показали, что использование теразозина (Сетегис) позволяет восстановить механизм удержания мочи, частично или в ряде случаев полностью, при этом также устранить и другие расстройства мочеиспускания. Изменения выраженности инконтиненции были обнаружены только после отмены терапии.
Обсуждение
Системный анализ клинических данных, полученных при ведении женщин с расстройствами мочеиспускания, показал весьма интересную особенность. Вместе с уменьшением поллакиурии и выраженности императивов, уменьшается и стрессовый компонент недержания мочи. В ранее опубликованной работе (7) есть указание на сравнительно высокую эффективность терапии α1-адреноблокаторами. Второе исследование, прямым образом относящееся к оценке вышеуказанного клинического эффекта, более определенно указывает на сосудистый механизм действия ЛС (8).
Вместе с этим, очень важно обратить внимание на некоторые особенности терапии α1-адреноблокаторами. Во-первых, лечебный эффект возникает не сразу, а только через некоторое время, чаще через несколько недель, но иногда и через 2-3 месяца. Например, в сравнении с действием М-холинолитика, который непосредственно блокируя рецепторы детрузора, меняет клиническую симптоматику расстройств мочеиспускания практически на первой неделе приема, в нашем случае динамика оказывается часто малозаметной и что важно, медленной. Вторая особенность заключается в том, что клинический эффект возникает не всегда, а в ряде случаев оказывается нестойким. Побочный эффект ЛС, а именно усиление недержания мочи, маскирует лечебный. Мало того, нами отмечены случаи, когда усиление инконтиненции на препаратах предшествует ее исчезновению.
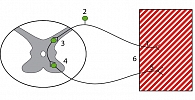
Эффекты назначения α1-адреноблокаторов у женщин были продемонстрированы в ранее проведенном исследовании (9), однако механизм действия ЛС предполагался строго локальный, на мышцы тазового дна и сфинктера. Проведенные в дальнейшем наблюдения и анализ побочных эффектов показал, что α1-адреноблокаторы действуют опосредованно через центры, расположенные в спинном и головном мозге (10, 11). В данном случае интерес представляет нейрофизиологическая модель, отражающая достаточно сложный механизм такого взаимодействия, вместе с этим позволяющая объяснить вышеописанные эффекты консервативной терапии. Известно, что управление тазовым дном осуществляется через нейроны, располагающиеся в поясничном утолщении спинного мозга, а, следовательно, и трофические функции и тонус сфинктера прямым образом зависят от функции самого нейрона. При ухудшении кровообращения, например, вследствие ишемии поясничного утолщения, будет страдать механизм удержания мочи. Расположение артерий, питающих спинной мозг, определяет сам характер патологии. В литературе есть ряд весьма интересных работ (Zulch K.I. (1954), Jellinger K., Neumaer E. (1962), Мотавкин П.А., (1962, 1974)), прямо указывающих на данную особенность в отношении нарушения функций органов, находящихся в «сфере интересов» управляющих ядер спинного мозга на уровне L1-S5. В частности Gorbin J.L. (1961) весьма обоснованно полагает, что наиболее ранимыми являются зоны утолщений спинного мозга. Доказанный факт, что при ишемии в первую очередь наступает гибель нейронов в области промежуточной и аксиальной зон передних рогов, что соответствует терминальным ветвям передней спинальной артерии.
Согласно современным представлениям, трехнейронная дуга обеспечивает автоматизм срабатывания механизма удержания мочи следующим образом. При растяжении мышцы, например вследствие повышения внутрибрюшного давления, замыкается рефлекторная дуга, что приводит к сокращению мышцы (срабатывает так называемый миотатический рефлекс «растяжения»). Тонус мышцы резко возрастает, а после снятия нагрузки возвращается в исходное состояние. Автоматизм позволяет полностью исключить участие структур головного мозга в данном процессе контроля. В случае повреждения одного из нейронов, рефлекторная дуга перестает нормально работать. При этом или происходит запаздывание реакции или вообще ответ оказывается неэффективным, в любом варианте происходит непроизвольная потеря мочи.
При поражении периферического нейрона, например при травме полового нерва во время родов, также нарушается рефлекторная дуга. Но в отличие от вышеприведенного механизма, периферическая ветвь нейрона может восстановиться, а при гибели ядра – уже нет. Этим можно объяснить обратный регресс симптоматики недержания мочи в ряде случаев. Нейропатия полового нерва, вне зависимости от вызывающей ее причины, закономерно должна приводить к инконтиненции. Коррекция α1-адреноблокаторами при этом не всегда позволяет восстановить функцию нерва, если не устранен фактор, приводящий к повреждению.
Рассматривая вышеприведенную нейрофизиологическую модель, становится понятна роль консервативной терапии стрессового недержания мочи. Казалось бы, α1-адреноблокаторы должны всегда менять клиническую симптоматику недержания мочи и весьма существенно, поскольку точка приложения ЛС находится в поясничном утолщении, или более определенно, в бассейне радикулярных артерий. α1-адреноблокаторы опосредованно действуют на мотонейроны через систему кровообращения. Однако именно это обстоятельство на самом деле отражает медленную динамику симптомов непроизвольной потери мочи.
Клиническая симптоматика не может меняться быстро отчасти из-за того, что механизм действия α1-адреноблокатора действительно сосудистый, или даже более точно, нейрососудистый, и после улучшения кровообращения поясничного утолщения требуется время для трансформации эффекта – усиления сократительной способности и координации мышц поперечнополосатого сфинктера. В свою очередь, мускулатура не может мгновенно изменить свои свойства, ей также требуется время на восстановление возникших ранее трофических нарушений. И еще одно обстоятельство – пожалуй, самое главное. Лечебный эффект будет значимым, если мотонейроны поясничного утолщения еще способны отреагировать на улучшение гемодинамики, другими словами если в них не произошло необратимых дистрофических процессов. Именно в этом случае восстановление функциональной активности нейронов позволит запустить механизм удержания мочи. И немаловажно также и то, что предел изменения кровообращения самого поясничного утолщения также существует, а, следовательно, ишемия в принципе не может быть устранена полностью. Исполнительный орган, в данном случае, мышцы тазового дна, имея трофические повреждения, вследствие длительного существования в условиях гипоксии и денервации, также может не отреагировать на терапию быстро и значимо.
Если все эти факторы суммировать, то становится понятным, почему α1-адреноблокаторы, в принципе не могут быть эффективны у всех, вне зависимости от степени выраженности инконтиненции.
А с другой стороны, появляется возможность относительно раннего назначения препаратов этой группы для предотвращения дальнейшего развития недержания мочи, устранения имеющегося или уменьшения его выраженности. С этой точки зрения трудно найти альтернативу патогенетической терапии α1-адреноблокаторами, и совершенно точно, что ни ЗГТ, ни М-холинолитики, не могут считаться препаратами для лечения НМПН.
Как показало исследование, у α1-адреноблокаторов есть интересная особенность. Как указывалось выше, препараты этой группы сами по себе способны вызывать недержание мочи за счет блокады адренорецепторов шейки мочевого пузыря, но проявляется это несколько своеобразно. На фоне приема, особенно в начале терапии или при увеличении дозировки, возникает усиление инконтиненции, что проявляется самостоятельным подтеканием мочи даже вне какой-либо физической нагрузки, или усиление непроизвольной потери при минимальной физической активности. Данный побочный эффект в ряде случаев самостоятельно исчезает еще во время лечения, но чаще только на 2-3 сутки после отмены α-блокаторов. Поэтому оценивать эффективность терапии становится сложным, или вообще невозможным, пока применяются препараты, а действительный терапевтический эффект можно оценить лишь спустя некоторое время, в пределах 6-8 недель после прекращения терапии.
Именно это обстоятельство было отмечено в ранее проводимых клинических исследованиях, что собственно и послужило если не основной, то наиболее существенной из всех остальных, причиной ограничения на применение α1-адреноблокаторов у женщин (12). Адренорецепторная блокада шейки мочевого пузыря, в данном случае как побочный эффект, не позволила широко использовать ЛС в клинической практике терапии инконтиненции. Вместе с тем, ориентированность на так называемую «уроселективность», стало естественной основой использования α-блокаторов при обструктивном мочеиспускании у женщин.
Однако столь существенный побочный эффект назначения α1-адреноблокаторов, как усиление недержания мочи, в нашем исследовании удалось скомпенсировать использованием специальных средств защиты, а именно прокладками MoliMed, что позволило пациенткам вести активный образ жизни и не отменять терапию, проводимую довольно длительный период.
Следует отметить, что сама по себе технология лечения, предусматривающая устранение инконтиненции только после отмены α1-адреноблоаторов, весьма необычна и требует не только времени, но и методик неинвазивного клинико-уродинамического мониторинга.
На основании наших наблюдений представляется вполне допустимым представление нейрофизиологической модели недержания мочи. Для объяснения основного звена патогенеза недержания мочи при напряжении можно предложить нейрососудистую теорию ишемии поясничного утолщения. Схема патогенеза выглядит следующим образом: ишемия поясничного утолщения спинного мозга как следствие нарушения кровообращения в бассейне артерии Адамкевича или Депрош-Готтерона приводит к нарушению, а в ряде случаев и к гибели нейронов, управляющих мышцами тазового дна, постепенно приводя к атрофии поперечнополосатых мышц сфинктера и нарушению связочного аппарата. Если устранить ишемию нейронов S2-S5 сегментов спинного мозга, процесс поражения тазового дна, возможно, остановить и частично восстановить тонус поперечнополосатого сфинктера. По результатам исследования получено два патента РФ на консервативную терапию стрессового недержания мочи и устранению ишемии спинного мозга.
Выводы
Назначение α1-адреноблокатора теразозина (Сетегис) в режиме титрования, в комбинации с лекарственными средствами сосудистой терапии, позволяет улучшить механизм удержания мочи и в ряде случаев полностью устранить недержание. Наиболее эффективно поддаются консервативной терапии пациентки с невыраженной клинической симптоматикой инконтиненции.
Длительность терапии должна составлять период не менее 6-8 недель, оценка результатов терапии может быть проведена только после отмены консервативной терапии в катамнезе не менее 4 недель.
Нейрофизиологическая модель патогенетического механизма недержания мочи при напряжении позволяет объяснить клинические эффекты назначения α1-адреноблокаторов с позиции существования хронической ишемии поясничного утолщения. При условии восстановления функции соответствующих управляющих структур спинного мозга происходит устранение инконтиненции.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.