Неврологические осложнения сахарного диабета
- Аннотация
- Статья
- Ссылки
Гипергликемия, вне зависимости от вызвавшей ее причины, будь то недостаточность продукции инсулина или инсулинорезистентность, является основным патогенетическим фактором поражения нервной системы при сахарном диабете (СД). В основе такого поражения лежит активация альтернативных путей распада глюкозы (пентозофосфатного цикла), окислительный стресс и угнетение процессов обмена энергии в нервных тканях, что приводит к неуклонно прогрессирующему поражению тонких и толстых волокон (по типу дегенерации осевых цилиндров аксонов с последующей демиелинизацией). Самой распространенной формой поражения нервной системы при СД является дистальная симметричная сенсорно-моторная полиневропатия (диабетическая полиневропатия, ДПН).
На момент установления диагноза сахарного диабета ДПН выявляется у 8% больных, через 20 лет болезни – более чем у 40%, а через 25 лет – примерно у 50% пациентов, причем речь идет лишь о случаях с наличием клинической симптоматики [1–3]. Если учитывать еще и бессимптомные формы этого заболевания, то в популяции больных СД 1 типа ДПН встречается в 54% случаев, а при СД 2 типа – в 45%. Тем не менее почти у половины больных СД неврологические осложнения не развиваются. По мнению ряда исследователей, это связано с различным уровнем генетически детерминированной экспрессии антиоксидантных ферментов (супероксиддисмутазы, поли(АДФ-рибоза)-полимеразы и др.). Таким образом, у одних «устойчивость» к окислительному стрессу выше, а у других естественная антиоксидантная защита слабее, в этом случае ДПН развивается раньше и протекает тяжелее [4, 5].
ДПН обычно начинается как генерализованная бессимптомная дисфункция периферических нервных волокон. Самым распространенным ранним нарушением является снижение скорости проведения возбуждения по нерву и уменьшение реакции сердечного ритма на гипервентиляцию или пробу Вальсальвы. Первыми клиническими признаками, развивающимися параллельно или последовательно с вышеуказанными изменениями, могут быть снижение или отсутствие ахилловых рефлексов и уменьшение или потеря вибрационной чувствительности на больших пальцах стоп. По мере прогрессирования заболевания развивается снижение всех видов чувствительности (преимущественно температурной, болевой и вибрационной, позднее присоединяется снижение тактильного и суставно-мышечного чувства) на стопах и голенях, снижение сухожильных рефлексов, вегетативные нарушения и парез в стопах и голенях. Через некоторое время в отсутствие патогенетической терапии добавляются чувствительные и двигательные нарушения в кистях. Субъективные симптомы у пациентов могут появиться при любой степени неврологических и электрофизиологических нарушений, а могут не появиться вообще.
Выделяют негативные и позитивные симптомы, отражающие функциональную недостаточность периферических нервов. К негативным симптомам относят снижение чувствительности, сенситивную атаксию, гипорефлексию, мышечную слабость и атрофию, вегетативные нарушения (импотенцию, гастропарез, ортостатическую гипотензию). К позитивным симптомам – парестезии («мурашки», покалывание), чувство стянутости, онемение, боль (стреляющую, жгучую, саднящую, глубокую ноющую), аллодинию, болезненность при пальпации конечностей в зоне «носков» и «перчаток» (статическую гипералгезию) и крампи (болезненные судороги, чаще в икроножных мышцах) [2]. Следует учитывать, что около 10% поражений периферической нервной системы при СД имеют недиабетическую этиологию (наследственные, алкогольные, иммунные и др.) – в этих случаях патогенетическая терапия ДПН может быть недостаточно эффективной [2, 3]. Учитывая это, диагноз ДПН может быть установлен с известной степенью точности при наличии следующих критериев:
- пациент страдает сахарным диабетом, диагностированным в соответствии с установленными критериями;
- сахарный диабет вызвал продолжительную хроническую гипергликемию (этот пункт зачастую невозможно отследить, ввиду того что пациенты с впервые выявленным СД могут годами и десятилетиями до установления диагноза не проверять уровень глюкозы в крови);
- у пациента имеется преимущественно дистальная симметричная сенсомоторная полиневропатия нижних конечностей;
- другие причины неврологических заболеваний и сенсомоторных полиневропатий, а также другие формы диабетической невропатии исключены;
- диабетическая ретинопатия или нефропатия приблизительно соответствуют по степени тяжести полиневропатии.
Отдельного внимания заслуживает проблема вегетативной невропатии при СД. В популяции больных СД 1 типа достоверная вегетативная невропатия выявляется у 8,5%, а вероятная – у 16,8% больных, а при СД 2 типа достоверная вегетативная невропатия имеет место у 12,2%, а вероятная – у 22,1% больных. Сердечно-сосудистые осложнения вегетативной невропатии являются одними из главных причин инвалидизации и летальных исходов у больных СД. Наличие у больных СД признаков вегетативной невропатии увеличивает риск развития диабетической стопы и связанных с ней осложнений, но главное – с момента появления клинической симптоматики вегетативной невропатии ожидаемая смертность в течение следующих 5 лет составляет 50%. Экспериментально подтвержденная связь между предрасположенностью к летальным аритмиям и признаками повышенной симпатической или пониженной парасимпатической активности инициировала изучение количественных показателей вегетативной активности для ранней диагностики вегетативной невропатии.
В настоящее время выявлена существенная взаимосвязь между состоянием вегетативной нервной системы и смертностью от сердечно-сосудистых заболеваний, включая внезапную смерть. Показано, что факторами риска развития вегетативной невропатии являются длительное течение СД, плохой контроль уровня гликемии и мужской пол больных. Основными клиническими проявлениями сердечно-сосудистой вегетативной невропатии являются: постоянная умеренная тахикардия и фиксированный пульс, ортостатическая гипотензия, безболевая ишемия и инфаркт миокарда, снижение циркадных влияний на вегетативную функцию, повышение риска возникновения сердечных аритмий вследствие увеличения симпатических влияний, диабетическая кардиомиопатия и нарушение функции миокарда, осложнения при анестезии и операциях в виде неожиданной остановки дыхания и сердцебиения. Развитие тахикардии в начале заболевания связано с поражением блуждающего нерва при относительном преобладании активности симпатического отдела вегетативной нервной системы. По мере прогрессирования вегетативной невропатии снижается активность и симпатического отдела, что может сопровождаться исчезновением тахикардии. На этой стадии отмечается отсутствие тахикардии, а в ответ на функциональные пробы и эмоциональный стресс выявляется так называемое «денервированное сердце» [6].
Безболевая ишемия или безболевой инфаркт миокарда регистрируется в 45–65% случаев СД с вегетативной невропатией по сравнению с 4% пациентов с СД без признаков вегетативной невропатии. Отсутствие характерных клинических признаков нарастающей ишемии является фактором риска развития инфаркта миокарда и внезапной смерти. Механизм развития безболевой ишемии комплексный. В его основе лежит дисфункция кардиальных афферентных нервных волокон и измененный порог болевой чувствительности. Показано, что кардиальная форма автономной невропатии является четким прогностическим критерием безболевой ишемии миокарда. Наличие сердечно-сосудистой вегетативной невропатии является прогностически неблагоприятным признаком в отношении развития терморегуляторных и судомоторных нарушений, мочеполовых расстройств и других осложнений СД, например, диабетической ретинопатии. Наиболее характерными признаками сердечно-сосудистой вегетативной невропатии на электрокардиограмме являются дисперсия интервала ST, удлинение интервала QT, инверсия положительного зубца Т, псевдокоронарный подъем сегмента ST. Однако эти изменения появляются на поздних стадиях заболевания, когда терапия вегетативной невропатии уже малоэффективна [6]. Для проведения начальной диагностики вегетативной невропатии наиболее широкое распространение получил метод 5 стандартных тестов по D. Ewing [7]:
- Изменение частоты сердечных сокращений (ЧСС) при медленном глубоком дыхании (6 дыхательных движений в минуту). Наблюдаемое в норме ускорение ЧСС на вдохе и урежение на выдохе исчезает по мере прогрессирования недостаточности парасимпатической иннервации сердца. Разница между минимальной и максимальной ЧСС в 10 ударов и менее свидетельствует о нарушении парасимпатической иннервации сердца (норма > 15).
- Тест Вальсальвы. При повышении внутрилегочного давления (пациент натуживается – дыхание в мундштук, соединенный с манометром, с целью поддержания давления в спирометре на уровне 40 мм рт. ст. в течение 10–15 сек) в норме ЧСС увеличивается с последующей компенсаторной брадикардией. При нарушении парасимпатической регуляции сердечной деятельности этот феномен выпадает. Отношение величины максимального R-R интервала в первые 20 сек после пробы к минимальному интервалу R-R во время пробы менее 1,20 свидетельствует о наличии у больного вегетативной невропатии.
- Тест Шелонга (ортостатическая проба). Пациент спокойно лежит на спине в течение 10 мин, после чего измеряется артериальное давление. Затем пациент встает, и артериальное давление измеряется на 2, 4, 6, 8 и 10-й минутах. Снижение артериального давления на 30 мм рт. ст. и более считается патологическим и свидетельствует о вегетативной невропатии с нарушением симпатической иннервации (норма < 10 мм рт. ст.).
- Тест 30:15. Тест основан на учащении ЧСС при вставании с максимальным значением к 15-му удару с последующим урежением ритма с минимальным значением к 30-му удару. Отношение 15-го R-R интервала к 30-му с момента начала вставания при ортопробе ниже 1,0 является диагностическим критерием вегетативной невропатии (норма > 1,04).
- Проба с изометрической нагрузкой. При сжатии динамометра в течение 3 мин до 1/3 максимальной силы руки отмечается подъем диастолического артериального давления (ДАД). Повышение ДАД менее чем на 10 мм рт. ст. говорит о вегетативной невропатии с недостаточной симпатической иннервацией (норма > 16 мм рт. ст.).
Использование данных тестов является «золотым стандартом» диагностики вегетативной невропатии, поскольку позволяют выявить раннее, субклиническое поражение вегетативной нервной системы. Для более точной оценки степени поражения вегетативной нервной системы может использоваться усовершенствованный вариант диагностики вегетативной невропатии – количественное вегетативное тестирование. В его основе лежит методика регистрации и оценки высокочастотных дыхательных колебаний сердечного ритма, представляющая собой исследование вариабельности ритма сердца, выполняемое синхронно глубокому дыханию частотой 6 дыхательных циклов в минуту. При такой частоте дыхания в наибольшей степени стимулируется блуждающий нерв, поэтому проба используется для оценки реактивности парасимпатического отдела вегетативной нервной системы. Количественно оценивается разница между максимальной и минимальной ЧСС во время дыхательного цикла или экспираторно-инспираторное отношение [6].
Проявления вегетативной невропатии затрагивают оба эфферентных звена вегетативной нервной системы – симпатические и парасимпатические нервные волокна, однако, учитывая более раннее и более значимое поражение парасимпатических нервных волокон при СД, количественную оценку состояния вегетативной нервной системы при диабетической вегетативной невропатии целесообразно проводить именно по низкочастотному компоненту вариабельности сердечного ритма. Обладая высокой чувствительностью и селективностью, методика количественного вегетативного тестирования позволяет диагностировать вегетативную невропатию уже на доклиническом этапе и количественно определять степень вегетативного дефицита, что особенно важно для контроля эффективности лечения.
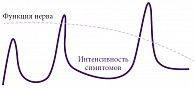
Количественное вегетативное тестирование может использоваться для раннего выявления дисфункции тонких волокон при ДПН наряду с такими современными методами объективной диагностики, как конфокальная микроскопия, биопсия кожи с подсчетом плотности интраэпидермальных волокон и контактные тепловые (или лазерные) вызванные потенциалы [1, 6]. По оценкам разных авторов, невропатический болевой синдром при ДПН встречается примерно в 20% случаев, приводя к выраженному снижению качества жизни больных и их социальной дезадаптации. Главная особенность болевой формы ДПН – флуктуация симптомов на фоне медленно прогрессирующего поражения нервных волокон [2]. При этом важно учесть, что вовлечение различных типов волокон в патологический процесс происходит с разной скоростью (рис.).
Интенсивная базовая (противодиабетическая) терапия и профилактика артериальной гипертонии, хотя и позволяют замедлить развитие таких осложнений СД, как нефропатия и ретинопатия (исследования Diabetes Control and Complications Trial (DCCT), United Kingdom Prospective Diabetes Study (UKPDS), The Steno Diabetes Study, Action to Control CardiОvascular Risk in Diabetes (ACCORD)), однако остаются все же недостаточно эффективными в плане предупреждения ДПН [8]. В то же время имеющиеся на сегодняшний день средства для терапии боли при ДПН (например, антиконвульсанты, трициклические антидепрессанты, местные анестетики) продемонстрировали воздействие только на отдельные симптомы ДНП. Кроме того, их интенсивное и длительное применение связано с рядом побочных эффектов: холинолитических и адреномиметических (антидепрессанты), седативных (антиконвульсанты), кардиотоксических (анестетики), что накладывает ограничения на их применение, особенно у больных преклонного возраста с большим количеством заболеваний (а такие пациенты составляют большинство больных ДПН).
Изолированное лечение боли, без восстановления функции периферических нервных волокон (патогенетической терапии), в конечном итоге приводит к усугублению вегетативно-трофических расстройств в конечностях, формированию «диабетической стопы», трофических язв, которые при инфицировании могут быть причиной ампутаций конечности [2, 3, 9, 10]. Кроме того, у 80% больных ДПН боль не является основным симптомом, и показаний к проведению терапии анальгетиками нет. Таким образом, актуальной является патогенетическая терапия, непосредственно ингибирующая патогенное действие гипергликемии и окислительного стресса на нервную ткань. Подобные средства характеризуются одновременным уменьшением тяжести всех основных проявлений ДПН – как снижением выраженности ее симптомов, так и улучшением клинических/физиологических показателей функции пораженных нервов. Основные требования, предъявляемые к патогенетической терапии ДПН, были сформулированы в итоговом документе-консенсусе международной конференции в г. Сент-Пол (США) в 1995 г. Было установлено, что лекарственный препарат может считаться патогенетическим, если он:
- по своему механизму непосредственно воздействует на патогенез ДПН;
- приводит к улучшению основных симптомов ДПН;
- улучшает функциональные показатели как толстых миелинизированных, так и тонких немиелинизированных волокон.
В последние десятилетия предпринимались многочисленные попытки доказательства эффективности различных препаратов для патогенетического лечения ДПН. Целый ряд субстанций (фактор роста нерва, ацетилкарнитин, миоинозитол, ингибиторы альдозоредуктазы, ингибиторы протеинкиназы С, витамин Е и др.), положительно зарекомендовавших себя в исследованиях доклинической и ранней клинической (I и II) фазы, не подтвердили своей эффективности на больших популяциях пациентов. По всей вероятности, причиной отрицательных результатов при проведении исследований третьей фазы была не столько недостаточная эффективность исследованных препаратов, сколько побочные эффекты терапии [3, 10]. В настоящее время роль окислительного стресса в развитии ДПН считается одной из ведущих [4, 5]. Естественным в связи с этим выглядит применение для патогенетического лечения ДПН препаратов, обладающих антиоксидантным действием, которые доказали как эффективность, так и безопасность в ходе целого ряда двойных слепых рандомизированных плацебоконтролируемых исследований.
Окислительным стрессом называется процесс повреждения клетки в результате действия свободных радикалов – реактивных форм кислорода. Большинство реактивных форм кислорода постоянно образуются в клетке – около 5% потребляемого тканями кислорода превращается в свободные радикалы, но в норме их уровень невелик. Клетка либо заменяет поврежденные молекулы, либо инактивирует их с помощью антиоксидантной системы (восстановленный глутатион, витамины С и Е, коэнзим Q10, нейтрализующие короткоживущие свободные радикалы реактивных форм кислорода, превращая их в долгоживущие или стабильные радикалы, в которых неспаренный электрон делокализован – окисленный глутатион, аскорбат-радикал, токофероксил-радикал, радикалы коэнзима Q10). Таким образом, реактивные формы кислорода, образующиеся в качестве побочных продуктов нормального клеточного метаболизма в дыхательной цепи митохондрий, а также других цитоплазматических реакций, не вызывают повреждения клетки. Однако уровень реактивных форм кислорода, превышающий защитные возможности клетки, вызывает серьезные клеточные нарушения (например, истощение аденозинтрифосфата) и в результате ведет к разрушению клетки. Одна из наименее реактивных форм кислорода – супероксид – превращается в более агрессивные (гидроксильный радикал и т.п.), что может вызвать окисление и разрушение многих клеточных компонентов – белков и липидов мембран, ДНК.
Эффект окислительного стресса зависит от силы его выраженности. При небольших нарушениях клетки могут вернуться в исходное состояние. Более выраженный стресс вызывает клеточную смерть. Клетки могут погибнуть в результате апоптоза, когда внутреннее содержимое клетки успевает деградировать до нетоксичных продуктов распада, или в результате некроза, когда клеточная мембрана разрушается и содержимое клетки высвобождается в межклеточное пространство, что может в результате повредить окружающие клетки и ткани. Тем не менее в некоторых случаях окислительный стресс играет роль защитного механизма. Иммунная система использует его для борьбы с антигенами, а некоторые реактивные формы кислорода служат посредниками (первичными мессенджерами) в передаче сигнала [4].
Различные органы и ткани в разной степени подвержены действию реактивных форм кислорода и демонстрируют различную устойчивость в процессе реализации окислительного стресса. Наиболее устойчивы к нему клетки кожи (это вполне объяснимо, ведь кератиноциты живут в пограничных условиях, в которых доступ кислорода из воздуха практически не ограничен), а наименее – нейроны головного и спинного мозга. Именно поэтому окислительный стресс является причиной или важным компонентом многих патологических состояний центральной и периферической нервной систем, таких как ДПН, алкогольная полиневропатия, радикулопатия и компрессионно-ишемические мононевропатии и плексопатии, ишемическое повреждение головного мозга, нейродегенеративные заболевания, а также является одной из составляющих процесса старения. В условиях окислительного стресса угнетается синтез оксида азота (NO) – основного регулятора расслабления сосудистой стенки – и активируется ядерный фактор (NF-kB), инициирующий выделение субстанций, которые ухудшают кровоток, например, эндотелина-1 [4, 5]. В этой связи помимо лечения ДПН особенно важно проведение профилактики ишемической болезни мозга у пациентов, страдающих СД 2 типа, у которых когнитивные расстройства наблюдаются вдвое чаще, чем в общей популяции.
Исследование ACCORD, в котором изучали влияние строгого контроля гликемии (цель HbA1c ≤ 6,5%) на риск развития сердечно-сосудистых нарушений у 10 251 пациента на протяжении 40 месяцев, не показало снижения риска развития сердечно-сосудистых заболеваний у больных, получавших интенсивную гипогликемическую терапию. Более того, смертность в группе, получавшей интенсивную сахароснижающую терапию, повысилась почти в 2 раза, что может объясняться учащением развития гипогликемических состояний, усугубляющихся наличием у больных периферической вегетативной недостаточности. Именно поэтому гипогликемическая ветвь исследования ACCORD была остановлена досрочно. Еще более пессимистичные результаты в отношении этиотропной терапии получены в подисследовании ACCORD-MIND (Memory In Diabetes), в которое были включены 2977 пациентов из основного исследования ACCORD. Этим больным проводилось динамическое исследование когнитивных функций и магнитно-резонансная томография головного мозга с измерением плотности серого и белого вещества в динамике.
Показано прогрессирующее снижение когнитивных функций по шкале Digit Symbol Substitution Test (DSST), а также снижение объема вещества мозга с незначительным повышением гиперинтенсивности сигнала от белого вещества у пациентов, получавших интенсивную сахароснижающую терапию [4, 11]. Полученные данные коррелируют с современными представлениями о том, что гипогликемия наряду с ишемией головного мозга способна вызывать каскад биохимических реакций, приводящих к апоптозу нервных клеток, одним из основных патогенетических механизмов которого является окислительный стресс. Именно поэтому применение антиоксидантов у больных СД является патогенетически обоснованным методом профилактики и лечения поражения периферической и центральной нервной систем [3, 4, 5, 9, 10].
Первое место среди антиоксидантов, использующихся для патогенетического лечения ДПН, сегодня занимает альфа-липоевая (тиоктовая) кислота – естественный липофильный антиоксидант. Клиническая эффективность и безопасность тиоктовой кислоты у больных ДПН была доказана в 9 двойных слепых плацебоконтролируемых исследованиях и подтверждена в одном метаанализе. В исследованиях был использован инновационный, оригинальный препарат тиоктовой кислоты – Тиоктацид® 600 Т для внутривенных инфузий и Тиоктацид® БВ в форме таблеток быстрого высвобождения (производитель «Меда Фармасьютикалс Швейцария ГМбХ») [3, 9, 10].
Тиоктацид® 600 Т является трометамоловой солью тиоктовой кислоты, что в сравнении с обычными препаратами-дженериками тиоктовой кислоты на основе этилендиаминовой соли обеспечивает Тиоктациду выраженные преимущества в виде улучшения местной переносимости (в том числе и безболезненность введения), а также отсутствия опасности тромбофлебитов [3, 9]. При внутривенной инфузии биодоступность тиоктовой кислоты максимальна, при пероральном приеме возможны существенные внутри- и межиндивидуальные различия по уровню действующего вещества в плазме крови. Так, при одинаковой дозе препарата колебания его концентрации у одного и того же человека могут достигать 30%. Благодаря хорошему профилю безопасности, переносимости и высокому терапевтическому индексу вариабельность абсорбции не опасна для здоровья пациентов, однако ведет к тому, что терапевтически эффективный уровень в плазме может не достигаться, и у части больных не будет ответа на лечение при приеме обычной формы таблетированной тиоктовой кислоты [10]. Для решения этой проблемы была разработана специальная пероральная форма тиоктовой кислоты – форма быстрого высвобождения с низкой вариабельностью абсорбции – Тиоктацид® БВ (быстрого высвобождения).
Достижение пиковой концентрации тиоктовой кислоты в плазме крови достигается уже через 30 мин после приема внутрь препарата Тиоктацид® БВ, что обеспечивает гарантированное поступление тиоктовой кислоты в нервную ткань, по сравнению с обычными таблетками тиоктовой кислоты препаратов-дженериков. Это, в свою очередь, обеспечивает высокую эффективность Тиоктацида БВ в отношении симптомов невропатии и невропатического дефицита и, следовательно, способствует снижению риска развития диабетических язв и синдрома диабетической стопы [10]. Следует обратить внимание на то, что таблетированные дженерики тиоктовой кислоты создаются с применением старых технологий, не предусматривающих форм быстрого высвобождения, поэтому результаты клинических исследований с Тиоктацидом БВ не могут быть экстраполированы на другие дженерические аналоги тиоктовой кислоты.
Иногда начало патогенетической терапии приводит к усилению болевого синдрома вследствие усиления периферической афферентации по регенерирующим нервным волокнам. При этом болевой синдром при монотерапии альфа-липоевой кислотой регрессирует медленнее, чем при симптоматической терапии трициклическими антидепрессантами, селективными ингибиторами обратного захвата серотонина и норадреналина или антиконвульсантами, поэтому при выраженном невропатическом болевом синдроме в начале лечения ДПН целесообразно назначение комбинированной терапии Тиоктацидом и анальгетиками [2]. Наличие у больных ДПН вегетативно-трофических нарушений (например, трофических язв) оправдывает добавление к комбинированному лечению препаратов, способствующих регенерации тканей (Солкосерил 1000 мг в/в капельно 5–10 дней, далее 200 мг в/м 10–20 дней), а при сопутствующей макроангиопатии и ретинопатии – фибратов (Трайкор 150 мг/сут). Наличие ортостатической гипотензии, встречающейся при вегетативной невропатии у 1–3,4% больных СД, может ограничить применение трициклических антидепрессантов и потребовать проведения симптоматической терапии.
Для терапии ортостатической гипотензии используют минералокортикоиды (флудрокортизона ацетат в дозе 0,1–1 мг/сут). К препаратам второго ряда, применяемым в качестве дополнительной терапии вегетативной невропатии при неэффективности флудрокортизона или в качестве монотерапии при невозможности его назначения, относят симпатомиметики (эфедрин, фенилпропаноламин, фенилэфрин, мапротилин, аторвастатин, тирамин, мидодрин, клонидин, иохимбин, DL-дигидроксифенилсерин) [4]. Синтетические аналоги вазопрессина (десмопрессина ацетат, лизин-вазопрессин), эритропоэтин, кофеин и ингибиторы циклооксигеназы (индометацин, флурбипрофен, ибупрофен, напроксен) являются дополнительными препаратами, не используемыми в качестве монотерапии. Существуют также нефармакологические методы лечения ортостатической гипотензии:
- медленное, постепенное изменение положения тела;
- избегание напряжения, натуживания и изометрических упражнений;
- использование компенсаторных физических упражнений;
- отмена гипотензивных лекарственных средств;
- сон на кровати с приподнятым головным концом;
- диета с высоким содержанием натрия (поваренной соли);
- специально разработанные комбинезоны, сдавливающие нижнюю часть тела.
Таким образом, основным требованием к патогенетическому лечению является уменьшение симптомов ДПН на фоне улучшения функциональных показателей периферических нервов; контроль эффективности терапии должен включать в себя как оценку симптомов и клинических проявлений ДПН, так и измерение объективных параметров функций нервов – электронейромиографию, количественное сенсорное и вегетативное тестирование. Подчеркнем, что лечение этого весьма распространенного заболевания наиболее эффективно на ранних стадиях, поэтому для сохранения нормального качества жизни больных СД требуется регулярное (1 раз в год) неврологическое обследование и как можно более раннее назначение патогенетической терапии тиоктовой кислотой (Тиоктацид® 600 Т, Тиоктацид® БВ).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.