Эффективность и безопасность инсулина деглудек у детей и подростков с сахарным диабетом 1 типа: клинический опыт
- Аннотация
- Статья
- Ссылки
- English
Основные положения. Двое пациентов с СД 1 типа исходно получали инсулин гларгин 100 ЕД/мл один раз в сутки и инсулин детемир два раза в сутки соответственно, затем их перевели на инсулин деглудек. Получавший инсулин гларгин 100 ЕД/мл был переведен на инсулин деглудек без снижения дозы, а получавший инсулин детемир – на инсулин деглудек в дозе 90% от предыдущей дозы инсулина.
Для оценки состояния больных до и после перевода на инсулин деглудек использовали непрерывный мониторинг уровня глюкозы. Кроме того, до перевода и через 9 и 12 недель после перевода у первого и второго больного соответственно определяли уровень гликированного гемоглобина (HbA1c).
У пациента, перешедшего с инсулина детемир на инсулин деглудек, не было выявлено существенных различий в показателях уровня глюкозы в крови до и после смены терапии. У пациента, ранее получавшего инсулин гларгин 100 ЕД/мл, уровень глюкозы в крови имел тенденцию к снижению после перехода на инсулин деглудек.
Общая суточная доза инсулина и общая суточная доза базального инсулина значительно снизились у больного, исходно получавшего инсулин детемир. У пациента, исходно получавшего инсулин гларгин 100 ЕД/мл, наметилась тенденция к снижению общей суточной дозы инсулина и общей суточной дозы базального инсулина.
Существенных различий уровня HbA1c у пациентов до и после перевода на инсулин деглудек не отмечено.
Заключение. У пациентов с СД 1 типа, получавших лечение инсулином гларгин 100 ЕД/мл или инсулином детемир, с помощью назначения однократной инъекции в сутки и более низких доз инсулина деглудек возможно достижение сопоставимого гликемического контроля при снижении вариабельности гликемии и меньшей частоте гипогликемических эпизодов.
Основные положения. Двое пациентов с СД 1 типа исходно получали инсулин гларгин 100 ЕД/мл один раз в сутки и инсулин детемир два раза в сутки соответственно, затем их перевели на инсулин деглудек. Получавший инсулин гларгин 100 ЕД/мл был переведен на инсулин деглудек без снижения дозы, а получавший инсулин детемир – на инсулин деглудек в дозе 90% от предыдущей дозы инсулина.
Для оценки состояния больных до и после перевода на инсулин деглудек использовали непрерывный мониторинг уровня глюкозы. Кроме того, до перевода и через 9 и 12 недель после перевода у первого и второго больного соответственно определяли уровень гликированного гемоглобина (HbA1c).
У пациента, перешедшего с инсулина детемир на инсулин деглудек, не было выявлено существенных различий в показателях уровня глюкозы в крови до и после смены терапии. У пациента, ранее получавшего инсулин гларгин 100 ЕД/мл, уровень глюкозы в крови имел тенденцию к снижению после перехода на инсулин деглудек.
Общая суточная доза инсулина и общая суточная доза базального инсулина значительно снизились у больного, исходно получавшего инсулин детемир. У пациента, исходно получавшего инсулин гларгин 100 ЕД/мл, наметилась тенденция к снижению общей суточной дозы инсулина и общей суточной дозы базального инсулина.
Существенных различий уровня HbA1c у пациентов до и после перевода на инсулин деглудек не отмечено.
Заключение. У пациентов с СД 1 типа, получавших лечение инсулином гларгин 100 ЕД/мл или инсулином детемир, с помощью назначения однократной инъекции в сутки и более низких доз инсулина деглудек возможно достижение сопоставимого гликемического контроля при снижении вариабельности гликемии и меньшей частоте гипогликемических эпизодов.








Введение
Сахарный диабет (СД) 1 типа характеризуется абсолютным дефицитом секреции инсулина, именно поэтому основой его лечения является базис-болюсная инсулинотерапия [1].
Физиологическая секреция инсулина поджелудочной железой состоит из двух фаз: первая фаза – быстрое высвобождение инсулина в ответ на прием пищи, вторая фаза – медленная, базальная секреция инсулина, которая играет роль в регулировании высвобождения глюкозы печенью в режиме голодания ночью и между приемами пищи [2]. Пациентам с СД 1 типа часто требуется многократная ежедневная инъекционная терапия с использованием инсулина короткого действия для дополнительной коррекции базальной дозы инсулина среднего или длительного действия [2]. Таковая не только обеспечивает достижение строгого гликемического контроля, но и предотвращает прогрессирование микрососудистых заболеваний [3].
При добавлении инсулина средней продолжительности действия к многократной ежедневной инъекционной терапии могут возникать проблемы, связанные с резким повышением уровня инсулина в крови и недостаточной продолжительностью действия, что может привести к ночной гипогликемии и повышению уровня глюкозы в крови в ранние утренние часы [4].
Для устранения недостатков препаратов инсулина средней продолжительности действия и достижения более физиологичного базального уровня инсулина были разработаны препараты инсулина длительного действия, такие как инсулин гларгин 100 ЕД/мл и инсулин детемир [5–7]. Установлено, что данные препараты в отличие от препаратов инсулина средней продолжительности действия снижали риск ночной гипогликемии, а также улучшали гликемический контроль [8–15].
Инсулин деглудек (компания Novo Nordisk, Дания) является базальным аналогом человеческого инсулина сверхдлительного действия. После введения инсулина деглудек в подкожно-жировую клетчатку формируется подкожное депо мультигексамерных цепочек, из которого в дальнейшем происходит непрерывное и пролонгированное высвобождение мономеров инсулина деглудек от концов цепочек в кровоток. Происходит также связывание инсулина деглудек с альбумином крови, что дополнительно замедляет его распределение в тканях и выведение из организма, усиливая пролонгированный эффект. Это обеспечивает инсулину деглудек сверхдлительный и плоский профиль действия и, как следствие, стабильный сахароснижающий эффект [16].
В настоящей статье представлены клинические случаи использования инсулина деглудек, демонстрирующие его большую эффективность по сравнению с применением инсулина гларгин 100 ЕД/мл или инсулина детемир при интенсифицированной инсулинотерапии у детей с СД 1 типа.
Клинический случай 1
Мальчик пяти лет с диагнозом СД 1 типа, поставленным полтора года назад, получал инсулин детемир в дозе 2 ЕД в 08.00, в дозе 2 ЕД в 21.00 и сверхбыстродействующий инсулин аспарт около 6 ЕД/сут.
Масса тела ребенка – 19,1 кг, рост – 111 см, коэффициент стандартного отклонения (Standard Deviation Score – SDS) массы тела – +0,23. Развитие среднее гармоничное, первая стадия полового развития по шкале Таннера.
Уровень гликированного гемоглобина (HbA1с), измеряемый с помощью системы Control-to-Range, до начала перевода ребенка на инсулин деглудек достигал 7,2%.
Общая суточная доза инсулина составляла 0,5 ЕД/кг, соотношение базального инсулина и общего суточного количества инсулина – 33%.
До начала перевода на инсулин деглудек в качестве болюсного инсулина пациент получал сверхбыстродействующий инсулин аспарт перед приемом пищи в дозе, установленной путем подсчета углеводов, и эта доза оставалась неизменной на протяжении всего периода наблюдения.
С помощью системы FreeStyle Libre 2 проводили непрерывный мониторинг уровня глюкозы (НМГ).
Непрерывная оценка уровня глюкозы в крови была начата до перевода на инсулин деглудек, когда ребенок еще использовал инсулин детемир, и продолжалась в течение трех дней после его перехода на инсулин деглудек до того момента, как уровень в крови стал стабилен.
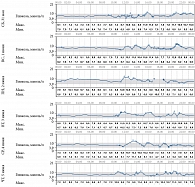
При введении инсулина детемир дважды в день в 8.00 и 21.00 развивалась ночная гипогликемия, определяемая как уровень глюкозы в крови менее 3,9 ммоль/л в период с 00.00 до 06.00, согласно данным НМГ (рис. 1).
При снижении дозы инсулина детемир до 1 ЕД в 21.00 у ребенка отмечалась гипергликемия в ночные часы (рис. 2).
В дневные часы наблюдалась высокая вариабельность уровня глюкозы в крови: как гипогликемия, так и гипергликемия, что было связано с неточным подсчетом хлебных единиц.
На период смены базального инсулина была назначена диета, которая на 55–60% состояла из углеводов, на 15–20% – из белков, на 20–25% – из жиров.
Согласно инструкции по применению инсулина деглудек, при переводе на него пациента, ранее получавшего базальный инсулин два раза в день, препарат назначается один раз в день в начальной дозе, составляющей 80–90% от общей дозы.
Титрация дозы инсулина деглудек в течение 12 недель проводилась с ориентиром на уровень глюкозы в плазме натощак. При уровне, равном или менее 4,4 ммоль/л, дозу снижали на 10–20% в день, при уровне 4,5–8,5 ммоль/л дозу не изменяли, при уровне 8,5–11,0 ммоль/л дозу увеличивали на 10% в день, или на 0,5 ЕД в день, при уровне, равном или превышающем 11,1 ммоль/л, дозу увеличивали на 10–20% в день, или на 1 ЕД в день.
Уровень HbA1c измеряли непосредственно перед переходом на терапию инсулином деглудек и через 12 недель после перехода. Отмечено, что через 12 недель уровень HbA1c снизился с 7,2 до 6,8%.
После начала терапии инсулином деглудек 3 ЕД однократно в 21:00 у ребенка уже в первые трое суток не была отмечена ночная гипогликемия (рис. 3).
Через 12 недель после перехода с инсулина детемир на инсулин деглудек в течение 14 дней проводился НМГ (рис. 4). Вариабельность уровня глюкозы в крови на фоне получения инсулина детемир составляла 55,8%, после перевода на инсулин деглудек – 17,8% (рис. 5).
Таким образом, после перехода на инсулин деглудек показатель вариабельности гликемии значительно снизился.
Клинический случай 2
Девочка 12 лет с СД 1 типа в течение четырех лет. Пациентка получала инсулин гларгин 100 ЕД/мл в дозе 13 ЕД/сут в 21.00, а также сверхбыстродействующий инсулин аспарт в дозе около 18 ЕД/сут.
Масса тела девочки – 44 кг, рост – 150 см, SDS массы тела – -0,46, SDS роста – +0,11. Развитие среднее гармоничное, третья стадия полового развития по шкале Таннера.
Уровень HbA1c до начала перевода ребенка на инсулин деглудек достигал 7,1%. Через 9 недель после перевода на инсулин деглудек уровень HbA1c снизился до 6,8%.
Общая суточная доза инсулина составляла 0,7 ЕД/кг, соотношение базального инсулина и общего суточного количества инсулина – 42%.
Непрерывный мониторинг глюкозы проводился с использованием системы FreeStyle Libre 2.
При введении инсулина гларгин 100 ЕД/мл в 21.00 в ночные часы развивалась гипергликемия, а в дневные – гипогликемия (рис. 6).
Подростка перевели на инсулин деглудек в той же дозе, исходя из принципа «единица на единицу» (13 ЕД в 21.00). После перехода на инсулин деглудек у ребенка уже в первые трое суток не были отмечены эпизоды ночной гипергликемии, однако сохранялись эпизоды гипогликемии в дневное и вечернее время (рис. 7). Через 9 недель после смены терапии дневные гипогликемии и гипергликемии не отмечались (рис. 8).
Через 9 недель после перехода с инсулина гларгин 100 ЕД/мл на инсулин деглудек проводился повторный НМГ в течение 14 дней. Вариабельность уровня глюкозы в крови при применении инсулина гларгин 100 ЕД/мл составляла 41%, после перевода на инсулин деглудек – 29,2% (рис. 9), что свидетельствует о снижении вариабельности гликемии.
Обсуждение
Аналоги инсулина длительного действия, такие как инсулин гларгин 100 ЕД/мл и инсулин детемир, могут обеспечивать до 24 часов действия при введении один или два раза в день. Однако из-за особенностей действия их следует вводить в одно и то же время каждый день, чтобы избежать периодов инсулиновой недостаточности [17]. Поскольку у детей всех возрастов часто бывает нестабильный распорядок дня, может быть полезен базовый режим, обеспечивающий большую гибкость во времени введения инсулина.
В сравнительных исследованиях инсулина деглудек с инсулином гларгин 100 ЕД/мл или инсулином детемир был установлен сопоставимый гликемический контроль на фоне применения этих препаратов, однако частота ночной гипогликемии была ниже при применении инсулина деглудек [18–23].
В исследовании T. Heise и соавт. показано, что инсулин деглудек характеризуется значительно более предсказуемым влиянием на уровень глюкозы в крови, чем инсулин гларгин 100 ЕД/мл [24]. Однако в предыдущих исследованиях не проводили оценку изменения уровня глюкозы в крови и не сравнивали дозы инсулина сразу после перехода на инсулин деглудек.
В приведенных нами клинических примерах продемонстрировано, как меняются колебания уровня глюкозы и дозы инсулина сразу после перехода с инсулина гларгин 100 ЕД/мл или инсулина детемир на инсулин деглудек.
Согласно данным НМГ, были обнаружены изменения уровня гликемии в ночное время (с 00.00 до 06.00) и частоты гипогликемии при переходе с инсулина гларгин 100 ЕД/мл на инсулин деглудек. У пациентки, получавшей инсулин гларгин 100 ЕД/мл один раз в сутки, переход на инсулин деглудек осуществлялся с использованием той же дозы и времени введения, что и до перехода, при этом уровень глюкозы в крови демонстрировал тенденцию к снижению в течение нескольких дней после начала терапии инсулином деглудек. У пациента, получавшего инсулин детемир два раза в день, лечение было начато со сниженной на 10% дозы инсулина деглудек по сравнению с дозой инсулина детемир.
Согласно данным НМГ, у мальчика были выявлены существенные изменения среднего уровня глюкозы в крови, вариабельности и количества ночных гипогликемий, что, вероятно, связано с более предсказуемым и устойчивым профилем действия инсулина деглудек, а также с малым возрастом пациента, высокой индивидуальной чувствительностью к инсулину и нестабильностью действия инсулина детемир в дневные часы.
Возможно, имел место остаточный эффект терапии инсулином гларгин 100 ЕД/мл или инсулином детемир, введенными непосредственно перед переходом на инсулин деглудек, поскольку период полувыведения инсулина гларгин 100 ЕД/мл составляет примерно 12 часов, продолжительность действия – около 24 часов, в то время как период полувыведения инсулина детемир составляет около 8–10 часов, а продолжительность действия – также около 24 часов. Необходимо отметить, что продолжительность действия этих инсулинов увеличивается в зависимости от дозы [25]. Однако в приведенных нами клинических примерах НМГ проводили через три дня после перехода на инсулин деглудек, и маловероятно, что эффект от применения инсулина гларгин 100 ЕД/мл или инсулина детемир сохранялся до третьего дня. Нельзя исключить предположение, что инсулин деглудек оказывает более сильное сахароснижающее действие по сравнению с той же дозой инсулинов гларгин 100 ЕД/мл или детемир.
При сравнении инсулина деглудек с инсулином гларгин 100 ЕД/мл у взрослых пациентов с СД 1 типа в течение 52 недель S. Heller и соавт. установили, что средние значения суточной дозы инсулина были значительно ниже в группе инсулина деглудек по сравнению с группой инсулина гларгин 100 ЕД/мл [26].
В нашем клиническом примере у девочки-подростка доза инсулина также снизилась спустя 9 недель терапии.
Полученные нами результаты позволяют предположить, что у пациентов, которые уже достигли удовлетворительного гликемического контроля с более низким уровнем глюкозы в плазме натощак и легкой гипогликемией, переход на инсулин деглудек следует начинать с более низкой дозы, чем при использовании других базальных инсулинов, чтобы избежать эпизодов гипогликемии. Аналогичный подход рекомендуется применять у пациентов, получающих базальный инсулин дважды в день. В то же время в некоторых исследованиях продемонстрировано, что суточные дозы инсулина были схожими при использовании инсулина деглудек и инсулина гларгин 100 ЕД/мл или инсулина детемир [27, 28].
При использовании в качестве базального инсулина гларгин 100 ЕД/мл или инсулина детемир, вводимых один раз в день, нередко наблюдаются значительные суточные колебания уровня глюкозы в крови из-за феномена утренней зари или эффекта Сомоджи [29]. Сообщалось, что у таких пациентов гликемический контроль можно улучшить, разделив дозу базального инсулина и вводя его дважды в день [30, 31].
Наш клинический пример перехода с инсулина гларгин 100 ЕД/мл показывает, что переход с однократного введения инсулина длительного действия на однократное введение инсулина деглудек может обеспечить гликемический контроль и помочь избежать феномена утренней зари.
Заключение
У пациентов с СД 1 типа с минимальной эндогенной секрецией инсулина стабильная заместительная терапия базальным инсулином необходима для достижения хорошего гликемического контроля, хотя в некоторых исследованиях сообщалось, что многим таким больным обычные препараты инсулина длительного действия необходимо вводить дважды в день [30, 31]. Результаты приведенных нами клинических примеров свидетельствуют о том, что аналогичного гликемического контроля можно достичь, переводя больных на инсулин деглудек, вводимый один раз в день, при этом снижаются общая суточная доза инсулина, вариабельность гликемии и частота гипогликемий.
E.S. Malysheva, PhD, T.A. Nekrasova, MD, PhD, I.G. Pochinka, MD, PhD, A.O. Marinina
Privolzhsky Research Medical University
Contact person: Ekaterina S. Malysheva, kayash3@yandex.ru
Aim – to assess changes taking place in basal insulin dose and blood glucose profile during basic-bolus therapy of type 1 diabetes mellitus (DM) in children when they are transferred from basal insulin glargine 100 U/ml or insulin detemir to insulin degludec.
Key points. Two patients with type 1 DM had initially received insulin glargine 100 U/ml once a day and insulin detemir twice a day, respectively; then they were switched to insulin degludec. The patient receiving insulin glargine was switched to insulin degludec without dose reduction, and the other one, receiving insulin detemir, was switched to insulin degludec at 90% dose of the previous insulin dose.
Continuous glucose monitoring was made to assess the patients’ state before and after switching to insulin degludec. In addition, before the transfer and 9 and 12 weeks after it glycated hemoglobin (HbA1c) level was tested in the first and second patients, respectively.
The patient, who had been switched from insulin detemir to insulin degludec, had no significant difference in blood glucose levels before and after therapy change. In the patient, who had previously received insulin glargine 100 U/ml, blood glucose levels demonstrated a tendency to decreasing after switching to insulin degludec.
The total daily dose of insulin and the total daily dose of basal insulin decreased significantly in the patient initially receiving insulin detemir. The total daily dose of insulin and the total daily dose of basal insulin in the patient who had initially received insulin glargine 100 U/ml demonstrated a tendency to decreasing.
There were no significant differences in HbA1c levels in patients before and after switching to insulin degludec.
Conclusion. A single injection per day and lower doses of insulin degludec can produce a similar glycemic control with reduced glycemic variability and lower incidence of hypoglycemic episodes in patients with type 1 diabetes mellitus previously treated with insulin glargine 100 U/ml or insulin detemir.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.