Особенности церебральной венозной гемодинамики при хронических нарушениях мозгового кровообращения
- Аннотация
- Статья
- Ссылки
- English
Введение
Важную роль в патогенезе цереброваскулярной патологии, в особенности на ранних этапах ее формирования, играют нарушения венозного кровообращения. Различные причины, затрудняющие отток венозной крови из полости черепа (механическое сдавление венозных сосудов, застойная сердечная недостаточность и т.д.), приводят к переполнению сосудистого русла головного мозга кровью и повышению внутричерепного давления [1]. Естественной компенсаторной реакцией церебральных артерий в данных условиях является их констрикция [2], направленная на уменьшение притока крови в полость черепа и соответственно снижение внутричерепного давления [3], а также улучшение венозного оттока (полноценный отток возможен только в том случае, если давление в венах выше внутричерепного давления). Когда указанные изменения развиваются на фоне неполноценности мозговых артерий (приобретенных или врожденных их сужении и окклюзии), могут возникнуть острая регионарная церебральная ишемия и очаговый неврологический дефицит.
Очевидно, что адекватная оценка церебральной гемодинамики, в частности ее венозного компонента, должна учитывать возможность компенсаторного оттока крови не только по поперечным, сигмовидным синусам и яремным венам, но и позвоночным сплетениям [4]. В то же время более точно разграничить зоны поступления крови в венозные коллекторы не всегда возможно вследствие высокой индивидуальной вариабельности расположения мелких анастомозов как внутри венозных систем, так и между ними [5]. В целом, несмотря на очевидный прогресс нейровизуализации, особенности венозной гемодинамики при различных патологических процессах в головном мозге менее изучены, чем особенности артериальной [6]. Роль венозной дисгемии в формировании неврологического дефицита фактически не выявлена, а клинические и диагностические методы сравнительно ограничены. Вышеизложенное подтверждает актуальность настоящего исследования.
Материал и методы
Анализ базы данных шестилетнего наблюдения за 833 больными с различными формами цереброваскулярной патологии позволил выделить 241 случай с верифицированным диагнозом нарушений венозного кровообращения головного мозга. Помимо неврологического осмотра проводились ультразвуковая допплерография экстракраниальных и транскраниальная допплерография интракраниальных сосудов головного мозга. Для подтверждения диагноза венозной дисгемии выполняли магнитно-резонансную венографию брахиоцефальных вен и венозных синусов головного мозга и ультразвуковое дуплексное сканирование внутренних яремных вен с цветовым картированием кровотока.
Для изучения гемодинамики в интракраниальных артериях и венах использовалась транскраниальная допплерография на аппарате Nicolet Companion датчиком 2MHz по стандартной методике. Определяли среднюю линейную скорость кровотока, пульсационный индекс Gosling и индекс резистивности Pourcelot во внутренней сонной артерии (область сифона), передних, средних и задних мозговых артериях, интракраниальных сегментах вертебральных и базилярной артерий, а также в базальных венах Розенталя и прямом синусе. Для исследования кровотока в указанных сосудах применялись три основных доступа: транстемпоральный (для локации средней, передней, задней мозговых артерий и вен Розенталя), трансорбитальный (для изучения сифона внутренней сонной артерии и кавернозного синуса) и трансокципитальный (для локации позвоночной, базилярной артерий и прямого синуса).
Состояние цереброваскулярной реактивности оценивалось с помощью гипокапнической пробы с форсированным (в течение одной минуты) дыханием и гиперкапнической пробы с задержкой дыхания на одну минуту (для восстановления нормального газового баланса они осуществлялись с интервалом 15 минут). Для выявления допплерографически латентного снижения компенсаторных возможностей коллатерального венозного кровообращения проводилась антиортостатическая проба, то есть нагрузка, заключающаяся в изменении положения головы (наклон вниз примерно на 30–45°).
Магнитно-резонансная томография выполнялась на аппарате Siemens Magnetom Viva резистивным магнитом, напряженность магнитного поля – 0,2 Т. Сканирование головного мозга осуществлялось в аксиальной, сагиттальной и коронарной проекциях с толщиной среза от 4 мм. ОценивалисьТ1-, Т2-взвешенные изображения SE, TSE и FLAIR режимов. Магнитно-резонансную ангиографию и магнитно-резонансную венографию также проводили на магнитно-резонансном томографе Magnetom Viva с помощью градиентных последовательностей с уменьшенным углом вектора намагниченности. После получения пакета срезов в режиме ангиографии выполнялась реконструкция по методике 2D time-of-flight. Изучались магистральные артерии шеи и артерии виллизиева круга, состояние сагиттального, поперечных и сигмовидных синусов, синусный сток и внутренние яремные вены. Для оценки ликвородинамики интенсивность сигнала от пульсации ликвора в сильвиевом водопроводе сравнивали с интенсивностью сигнала в боковых желудочках на том же уровне.
Материал статистически обрабатывали на персональном компьютере с использованием стандартных программ (SPSS 9.0). Для сравнения различий между непарными выборками применялся критерий Стьюдента. Результаты считались достоверными при р < 0,05.
Результаты
В генезе неврологических проявлений цереброваскулярной патологии большое внимание в последнее время уделяется сочетанным расстройствам артериального и венозного компонентов мозгового кровотока, поэтому транскраниальная допплерография была использована для регистрации кровотока не только в интракраниальных артериях, но и в венозной системе головного мозга [7]. О состоянии венозного кровотока предлагается судить по состоянию кровотока в прямом синусе (локация через затылочное окно), базальной вене Розенталя (локация через височное окно) и кавернозном синусе (орбитальное окно) [2]. Считается, что затрудненный венозный отток по поперечному и сигмовидному синусам может способствовать снижению скорости перфузии в структурах мозжечка и базальных отделах височной доли больших полушарий мозга с соответствующими клиническими проявлениями [8]. Основной недостаток метода – возможность ошибки измерения линейной скорости кровотока из-за «слепого» направления локации с возможными вариациями угла инсонации.
Транскраниальное дуплексное сканирование – самый «молодой» среди методов ультразвуковой визуализации [9], который сочетает возможность визуализации образований головного мозга в В-режиме и цветового изображения (картограммы) потоков крови в крупных интракраниальных сосудах, полученного в результате компьютерной обработки допплеровского сдвига частот, или энергии движущихся частиц в режиме реального времени [10]. По данным некоторых авторов, качество изображения мало зависит от угла и практически не зависит от скорости и направления потока, в связи с чем чувствительность и разрешающая способность данного метода выше, чем у обычной транскраниальной допплерографии [11]. Для визуализации сосудистых структур при транскраниальном сканировании предпочтительно использовать режим энергетического цветового кодирования. Значительно улучшает качество визуализации применение эхоконтрастных препаратов, при этом частота визуализации основных интракраниальных артерий приближается к 100%. Основное ограничение метода – наличие и выраженность ультразвуковых окон, прежде всего темпорального.
На основании комплексного мультисистемного обследования больные с церебральной венозной дисгемией (средний возраст 55 ± 12,5 года) [12] были распределены в три клинические группы:
- первая (n = 54) – с явлениями венозного застоя (клинически соответствовало гипертензивному синдрому);
- вторая (n = 91) – с венозной энцефалопатией (клинически проявилось псевдотуморозным синдромом и дисциркуляторной энцефалопатией);
- третья (n = 35) – с острыми расстройствами мозгового венозного кровообращения.
Контрольная группа состояла из 23 человек с дисциркуляторной энцефалопатией первой степени артериального генеза.
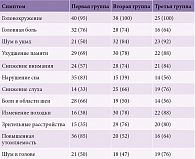
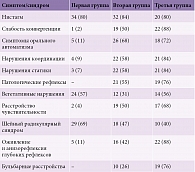
Во всех группах самыми частыми были жалобы на головокружение, головную боль, снижение слуха и др. (табл. 1) на фоне определенной неврологической симптоматики (табл. 2). Частота и распределение жалоб в клинических группах коррелировали со степенью нарушения венозного оттока из полости черепа: повышение давления во внутреннем ухе, в частности в лабиринте, является причиной стойких головокружений, вестибулярных расстройств, нейросенсорной тугоухости.
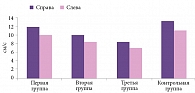
При изучении состояния кровотока по яремным венам установлено, что его скорость у больных первой группы была в среднем на 10% ниже, чем в контрольной группе (рис. 1). При этом, как и в контрольной группе, скорость кровотока по правой яремной вене на 10–15% превышала скорость кровотока по левой. У больных второй группы регистрировались еще меньшие значения кровотока по яремным венам, которые оказались на 18–20% ниже, чем в контрольной группе, и ниже, чем в первой группе. В третьей группе скорость кровотока по яремным венам также оказалась ниже на 25–30%, чем в группе контроля (р < 0,05). При этом достоверные отличия по сравнению с пациентами первой и второй групп отсутствовали.
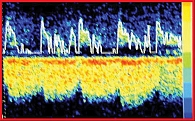
В отличие от пациентов первой группы у больных второй группы антиортостатическая проба не выполнялась, поскольку дальнейшее затруднение венозного оттока у них обнаруживалось уже при обычной инсонации вен. При этом отмечалось значительное возрастание линейной скорости кровотока по глубокой венозной системе на фоне выраженного уменьшения индекса пульсации (рис. 2).
В третьей группе прослеживались две тенденции в изменении венозной циркуляции. В большинстве случаев (n = 17, 68%) линейная скорость кровотока по базальным венам Розенталя и прямому синусу при прогрессирующем снижении индекса пульсации не нарастала. У восьми пациентов допплерографическая картина инсонации интракраниальных вен была аналогична изменениям у больных второй группы (рис. 3). При анализе вышеизложенного можно судить о корреляции нарушений ауторегуляции венозной системы кровообращения, с одной стороны, и выраженности клинической симптоматики, с другой.
Обсуждение результатов
Полученные данные свидетельствуют о том, что затруднение венозного оттока по основным путям (через мостиковые вены и венозные лакуны, вену Галена и прямой синус) компенсируется ускорением венозного оттока по глубоким венозным магистралям. Несмотря на то что у больных первой группы не было значимого увеличения максимальной систолической скорости кровотока, недостаточное возрастание скорости кровотока по вене Розенталя при антиортостатической пробе свидетельствовало о допплерографически латентном снижении компенсаторных возможностей коллатерального венозного кровообращения. Во второй группе прогрессирующее затруднение венозного оттока становилось явным и выражалось как в ускорении кровотока, так и в снижении индекса пульсации. У больных третьей группы в большинстве случаев наблюдалось отсутствие нарастания максимальной систолической скорости кровотока на фоне резкого снижения индекса пульсации, что отражало практически исчерпанные компенсаторные возможности коллатерального венозного кровообращения.
Интракраниальная венозная гемодинамика наряду с ликвородинамикой – стабилизирующий фактор внутричерепного давления [13, 14]. В области задней черепной ямки сочетанное физиологическое функционирование продольных, сагиттальных синусов, прямого синуса, большой цистерны и твердых оболочек мозга способствует оттоку венозной крови по яремным венам и ликвора к субарахноидальному пространству спинного мозга [15, 16]. Сбоем этого механизма можно объяснить частоту головных болей при аномалиях развития задней черепной ямки [17], в том числе при атрофии структур мозжечка (megacysterna magna) и гипоплазии большой цистерны мозга (аномалия Арнольда – Киари). Таким образом, важную роль в развитии церебральной венозной дисциркуляции играет затруднение гемо- и ликвородинамики вследствие препятствия как всасыванию спинномозговой жидкости, так и венозному дренажу всего внутричерепного пространства [18], особенно если имеется аномалия развития венозной системы (гипоплазия или аплазия венозных синусов и др.).
Современные методы нейровизуализации позволяют своевременно обнаруживать и достоверно оценивать компенсаторные возможности мозгового (венозного) кровообращения, что важно как для прогноза прогредиентности течения заболевания, так и для выбора адекватной тактики лечения пациентов с церебральной венозной дисгемией.
I. Verulashvili1, M. Beraia2, M. Kortushvili3
New Vision University, Tbilisi
Research Institute of Medical Radiology of the Georgian Academy of Sciences, Tbilisi
Tbilisi State Medical University
Contact person: Ivane Verulashvili, ivan_verulashvili@yahoo.com
On-time diagnosis of brain’s venous blood circulation disturbances plays an important role in the management of cerebral vascular pathology. The goal of this work was to correlate the clinical and structural-functional data of cerebral venous dishaemia (neurology investigation, doppler ultrasound and neuroimaging of 241 patients). Summing up the results of correlate comparison we consider, that sonography of cerebral vessels, supporting by data of clinical and neuroimaging investigation can detect arterial or venous disturbances of blood circulation and thus allow maintaining adequate treatment options.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.