Оценка эффективности лечения эндокринной офтальмопатии на основе пульс-терапии метилпреднизолоном
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить клиническую эффективность и безопасность разработанной схемы лечения активной стадии ЭОП на основе пульс-терапии метилпреднизолоном в комбинации с парабульбарным введением бетаметазона, симптоматическим лечением и физиотерапевтическими процедурами.
Материал и методы. В проспективном контролируемом нерандомизированном исследовании участвовало 80 пациентов с активной стадией ЭОП (легкой, средней и тяжелой степени), ранее не получавших специфического лечения. Всем пациентам выполнялась пульс-терапия метилпреднизолоном по авторской схеме (ступенчатое снижение дозы с 750 до 125 мг при двукратном введении через день) в комплексе с парабульбарными инъекциями бетаметазона, инстилляциями противовоспалительных средств, эндоназальным электрофорезом и магнитотерапией. Эффективность оценивали по динамике остроты зрения, уровня внутриглазного давления (ВГД), клинической активности (CAS), степени экзофтальма, ширины глазной щели, а также толщины экстраокулярных мышц (по данным В-сканирования). Статистическую обработку данных осуществляли с помощью критерия Уилкоксона.
Результаты. На фоне лечения зарегистрировано статистически значимое снижение активности воспалительного процесса по шкале CAS (p < 0,0001), снижение выраженности экзофтальма (p < 0,0001) и ширины глазной щели (p < 0,0001), повышение остроты зрения (p = 0,005), а также уменьшение толщины экстраокулярных мышц (p < 0,0001). Клинически значимого повышения уровня ВГД не отмечалось. За период последующего наблюдения (6–35 месяцев, медиана – 18,8 месяца) рецидивов заболевания не зафиксировано.
Выводы. Предложенная схема эффективна и безопасна. Ее применение позволяет в короткий срок достичь стойкой стабилизации патологического процесса, перевести заболевание в неактивную фазу и обеспечить надежную профилактику рецидивов.
Цель – оценить клиническую эффективность и безопасность разработанной схемы лечения активной стадии ЭОП на основе пульс-терапии метилпреднизолоном в комбинации с парабульбарным введением бетаметазона, симптоматическим лечением и физиотерапевтическими процедурами.
Материал и методы. В проспективном контролируемом нерандомизированном исследовании участвовало 80 пациентов с активной стадией ЭОП (легкой, средней и тяжелой степени), ранее не получавших специфического лечения. Всем пациентам выполнялась пульс-терапия метилпреднизолоном по авторской схеме (ступенчатое снижение дозы с 750 до 125 мг при двукратном введении через день) в комплексе с парабульбарными инъекциями бетаметазона, инстилляциями противовоспалительных средств, эндоназальным электрофорезом и магнитотерапией. Эффективность оценивали по динамике остроты зрения, уровня внутриглазного давления (ВГД), клинической активности (CAS), степени экзофтальма, ширины глазной щели, а также толщины экстраокулярных мышц (по данным В-сканирования). Статистическую обработку данных осуществляли с помощью критерия Уилкоксона.
Результаты. На фоне лечения зарегистрировано статистически значимое снижение активности воспалительного процесса по шкале CAS (p < 0,0001), снижение выраженности экзофтальма (p < 0,0001) и ширины глазной щели (p < 0,0001), повышение остроты зрения (p = 0,005), а также уменьшение толщины экстраокулярных мышц (p < 0,0001). Клинически значимого повышения уровня ВГД не отмечалось. За период последующего наблюдения (6–35 месяцев, медиана – 18,8 месяца) рецидивов заболевания не зафиксировано.
Выводы. Предложенная схема эффективна и безопасна. Ее применение позволяет в короткий срок достичь стойкой стабилизации патологического процесса, перевести заболевание в неактивную фазу и обеспечить надежную профилактику рецидивов.


Введение
Эндокринная офтальмопатия (ЭОП), также известная как офтальмопатия Грейвса, представляет собой аутоиммунное заболевание орбиты, обычно ассоциированное с патологией щитовидной железы, в частности с диффузным токсическим зобом. Актуальность проблемы обусловлена не только ростом заболеваемости, но и значительным снижением качества жизни пациентов, вплоть до риска потери зрения при тяжелых формах патологии.
Известно несколько классификаций ЭОП. В отечественной литературе выделяют три клинические формы: тиреотоксический экзофтальм, отечный экзофтальм и эндокринную миопатию [1], а также три стадии в зависимости от выраженности процесса: компенсацию, субкомпенсацию и декомпенсацию [1]. В мире наиболее распространены классификации, оценивающие тяжесть (NOSPECS, No symptoms or signs, Only signs, Soft tissue symptoms and signs, Proptosis, Extraocular muscle involvement, Corneal involvement and Sight loss due to optic neuropathy, 1969, 1977) и активность заболевания (CAS, Clinical Activity Score, 1989) [2–6]. ЭОП считается неактивной при сумме баллов по шкале CAS 1–2 и активной – при 3 и более баллах (CAS ≥ 3/7 или CAS ≥ 4/10).
Таким образом, общепризнанные классификации ЭОП описывают:
- характер патологического процесса (формы ЭОП);
- степень клинических проявлений (стадии ЭОП);
- динамику патологического процесса (активность по CAS и тяжесть по NOSPECS).
Для оценки тяжести в клинической практике применяют классификацию, рекомендованную Европейской группой по офтальмопатии Грейвса (European Group on Graves' Orbitopathy, EUGOGO). В ней предусмотрено три степени ЭОП – легкая, средняя и тяжелая (угрожающая потерей зрения) [2, 3].
Золотым стандартом лечения ЭОП средней и тяжелой степени являются глюкокортикостероиды (ГКС), в частности пульс-терапия. Эффективность метода подтверждена в многочисленных исследованиях [7–11]. В России широкое применение получила схема пульс-терапии, предложенная А.Ф. Бровкиной. Согласно данной методике, лечение начинается с внутривенного введения 1000 мг метилпреднизолона ежедневно в течение трех дней в стационаре с последующим постепенным снижением дозы каждые 7–10 дней. Курсовая доза составляет 5625 мг за 109–110 дней (около 3,5 месяца) [1]. Тем не менее ведение пациентов по данной схеме затруднено из-за невозможности длительного амбулаторного лечения по месту жительства. Отсутствие четкой преемственности между стационарным и амбулаторным звеном нередко приводит к тому, что пациенты остаются недолеченными.
В литературе описаны различные вариации схем пульс-терапии ГКС, например:
- введение ГКС из расчета 15 мг/кг массы тела на четыре цикла, затем по 7,5 мг/кг на следующие четыре цикла. Каждый цикл состоит из двух введений через день с двухнедельным интервалом [12];
- введение 500 мг в течение трех последовательных дней с дальнейшим переходом на пероральный прием преднизолона (0,7 мг/кг/сут в течение четырех недель) и постепенным снижением дозы на 5 мг каждую неделю [13];
- ежедневное внутривенное введение метилпреднизолона по 1 г на протяжении трех дней [14];
- использование комбинации внутривенных инфузий (по 500 мг через 48 часов) и перорального приема преднизолона (40 мг/сут) с постепенным снижением дозы, затем два раза по 500 мг через 48 часов [15].
Между тем описанные схемы не всегда позволяют достигать стойкой стабилизации процесса в короткий срок, что стимулирует поиск новых подходов к терапии. Остается дискутабельным вопрос о тактике ведения пациентов на разных стадиях заболевания, а также вопрос о целесообразности лечения пациентов с неактивной стадией ЭОП и активной ЭОП легкой степени [16–19]. Патофизиологические механизмы, лежащие в основе заболевания, такие как окислительный стресс и тканевая гипоксия, не всегда адекватно корригируются стандартными схемами терапии [20].
Таким образом, актуальность настоящего исследования обусловлена необходимостью поиска и оценки новых, эффективных и безопасных схем лечения активной ЭОП, направленных на достижение стойкой стабилизации заболевания в более короткие сроки и улучшение прогноза пациентов.
Цель – оценить клиническую эффективность и безопасность разработанной схемы лечения активной стадии ЭОП, основанной на пульс-терапии метилпреднизолоном в комбинации с парабульбарными инъекциями бетаметазона, симптоматическим лечением и физиотерапией.
Материал и методы
Изначально в проспективное контролируемое нерандомизированное исследование планировалось включить 156 пациентов. После применения критериев включения и исключения итоговая выборка составила 80 человек, не получавших ранее лечения по поводу ЭОП и обратившихся в ФГАУ НМИЦ «МНТК „Микрохирургия глаза“ им. академика С.Н. Федорова» Минздрава России в период 2022–2025 гг.
Возраст пациентов варьировал от 31 до 70 лет (медиана – 57 лет). Женщин насчитывалось 45 (56,25%), мужчин – 35 (43,75%).
Распределение участников исследования по степени тяжести ЭОП выглядело следующим образом: легкая степень зафиксирована у 15 (18,75%) пациентов, средняя – у 45 (56,25%), тяжелая – у 20 (25%). Миогенный вариант наблюдался у 4 (5%) пациентов, смешанный – у 72 (90%), эндокринная миопатия – у 2 (2,5%) и липогенный вариант – у 2 (2,5%). Подавляющее большинство пациентов (77 (96,25%)) страдали диффузным токсическим зобом. Аутоиммунный тиреоидит диагностирован у 3 (3,75%) больных, что соответствует данным литературы.
Всем пациентам трижды выполнялся контроль биохимических показателей крови: до начала лечения, после его окончания, а также через месяц после завершения курса.
Критерии включения в исследование:
- подтвержденный диагноз ЭОП в активной стадии (CAS ≥ 3) легкой, средней или тяжелой степени тяжести согласно классификации EUGOGO;
- компенсированное состояние патологии щитовидной железы (уровень тиреоидных гормонов в пределах референсных значений на момент включения);
- подписанное информированное согласие на участие в исследовании.
Критерии исключения из исследования:
- тяжелая сопутствующая соматическая патология (в том числе неконтролируемый сахарный диабет, хроническая сердечная недостаточность III–IV функционального класса по NYHA (New York Heart Association), декомпенсированные заболевания печени: гепатиты, цирроз, гепатоз);
- противопоказания к назначению ГКС или физиотерапии (включая онкологические заболевания в активной фазе, острые неврологические расстройства);
- предшествующее специфическое лечение ЭОП (кроме терапии синдрома сухого глаза);
- беременность и лактация;
- психические расстройства (по заключению невролога/психиатра).
Эффективность терапии оценивали в динамике исходно (до начала лечения) и непосредственно после завершения курса.
Всем пациентам проводили стандартное офтальмологическое обследование, включавшее визометрию, пневмотонометрию, периметрию, биомикроскопию, офтальмоскопию в условиях медикаментозного мидриаза.
До начала лечения острота зрения без коррекции варьировала от 0,1 до 0,7 для правого глаза (OD) (Ме – 0,5) и от 0,2 до 0,8 – для левого (OS) (Ме – 0,5). С коррекцией показатели составили: 0,8–1,0 (Ме – 1,0) для OD, 0,7–1,0 (Ме – 0,9) для OS.
Исходный уровень внутриглазного давления (ВГД) находился в пределах 17–20 (Ме – 19) мм рт. ст. для OD и 18–21 (Ме – 19,5) мм рт. ст. для OS.
Для оценки динамики субъективных жалоб использовали стандартизированный опрос, который на каждом визите проводил один и тот же врач-офтальмолог. Цель опроса – выявить и оценить следующие симптомы:
- боль в глазах и периорбитальной области;
- ощущение инородного тела в глазу;
- сухость, слезотечение;
- светобоязнь;
- зрительное утомление;
- затуманивание зрения;
- двоение (диплопия).
При наличии диплопии уточнялись ее частота и характер (горизонтальная, вертикальная, косая) на основании описаний пациента.
Активность ЭОП определяли по шкале CAS, рекомендованной EUGOGO. Учитывали семь клинических признаков (наличие – 1 балл, отсутствие – 0 баллов). Активным считалось заболевание при сумме баллов по CAS ≥ 3.
При первичном обследовании частота встречаемости признаков активности распределилась следующим образом:
- спонтанная ретробульбарная боль – 14 (17,5%);
- боль при движении глаз – 36 (45%);
- покраснение (эритема) век – 1 (1,25%);
- покраснение конъюнктивы – 77 (96,25%);
- отек век – 80 (100%);
- отек конъюнктивы (хемоз) – 68 (85%);
- воспаление и отек полулунной складки – 75 (93,75%).
Ширина глазной щели составила 19–21 (Ме – 20) мм для OD, 18–21 (Ме – 20) мм для OS.
Степень экзофтальма определяли экзофтальмометром Гертеля (Hertel exophthalmometer) с точностью измерения до 0,5 мм. Измерения проводили от латерального края костной стенки орбиты до передней поверхности роговицы.
До начала лечения величина экзофтальма составила для OD 22–24 (Me – 23) мм, для OS 21–25 (Me – 23) мм.
Величину ретракции верхнего века измеряли в миллиметрах с помощью миллиметровой линейки. Определяли расстояние от верхнего лимба роговицы до края верхнего века при взгляде пациента прямо (в положении первичного взгляда).
Подвижность глазных яблок исследовали с помощью периметра Гольдмана (Goldmann perimeter). Оценивали амплитуду движений в градусах по восьми основным направлениям взгляда. Регистрировали ограничение подвижности в каждом направлении.
Толщина экстраокулярных мышц оценивалась по данным В-сканирования:
- OD: 5,2–7,3 (Ме – 6,5) мм для верхней мышцы, 5,3–7,6 (Ме – 5,9) мм для внутренней, 4,2–5,8 (Ме – 4,5) мм для наружной, 4,9–6,7 (Ме – 5,6) мм для нижней;
- OS: 5,2–7,0 (Ме – 5,9) мм, 5,1–6,8 (Ме – 5,9) мм, 4,3–6,0 (Ме – 5,1) мм и 5,3–6,9 (Ме – 6,2) мм соответственно.
Все пациенты в условиях стационара получали пульс-терапию метилпреднизолоном по авторской схеме, разработанной в НМИЦ «МНТК „Микрохирургия глаза“ им. академика С.Н. Федорова» [21] и предусматривающей внутривенное капельное введение метилпреднизолона (двукратно с однодневным интервалом) в последовательно снижающихся дозах: 750, 500, 250 и 125 мг.
В дни между инфузиями метилпреднизолона пациентам внутримышечно вводили 1,0 мл фуросемида. На фоне системной пульс-терапии проводили курс парабульбарных инъекций бетаметазона (1,0 мл) № 3 с интервалом 5–7 дней.
В целях гастропротекции все пациенты принимали ингибитор протонной помпы омепразол 20 мг два раза в сутки. Коррекция электролитных нарушений предусматривала назначение калия аспарагината и магния аспарагината (по 175 мг каждого) по одной таблетке три раза в день.
Пульс-терапия дополнялась инстилляциями следующих групп препаратов (кратность указана в течение всего периода стационарного лечения):
- противовоспалительные средства: дексаметазон 0,1% четыре раза в день, бромфенак 0,09% один раз в день;
- корнеопротекторы (репаранты): препарат на основе гликозаминогликанов (баларпан 0,05%) четыре раза в день, декспантенол 5% (гель) два раза в день;
- антиоксидант: эмоксипин (метилэтилпиридинол) 1% четыре раза в день.
Всем пациентам на фоне медикаментозной терапии проводили курс физиотерапевтических процедур:
- эндоназальный электрофорез с 0,1%-ным раствором дексаметазона (4 мг/мл, 1,0 мл на процедуру). Курс предусматривал десять ежедневных сеансов;
- магнитотерапия (десять процедур) в реверсивном режиме с частотой 50 Гц и временем реверса 10 секунд. Воздействие осуществляли последовательно на три зоны проекции зрительного анализатора: область глазного яблока, височную и затылочную области. Продолжительность процедуры – 15 минут.
После завершения стационарного этапа лечения назначали пероральный прием преднизолона по убывающей схеме. Начальная доза – 10 мг/сут (две таблетки по 5 мг). Дозу еженедельно уменьшали на 2,5 мг (0,5 таблетки). Длительность курса составила один месяц, суммарная курсовая доза – 192,5 мг.
Результаты
После завершения курса, а также через месяц оценивали биохимические показатели крови: уровни аланин- и аспартатаминотрансферазы, билирубина общего, относительное содержание лимфоцитов, абсолютное количество лейкоцитов.
Непосредственно по окончании курса терапии у части пациентов регистрировались отклонения указанных показателей, не превышавшие 5% верхней границы референсных значений. Однако во время обследования через 4–6 месяцев указанные показатели находились в пределах нормативных значений, что свидетельствовало о благоприятном профиле безопасности проведенного лечения.
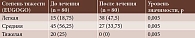
На момент завершения курса лечения легкая степень ЭОП имела место у 38 (47,5%) пациентов, средняя – у 27 (33,75%). Тяжелая степень ЭОП не зарегистрирована ни у одного пациента (p = 0,005) (табл. 1).
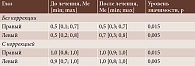
По окончании лечения острота зрения без коррекции составила для OD 0,3–0,7 (Ме – 0,5), для OS 0,3–0,9 (Ме – 0,7), с коррекцией – 0,9–1,0 (Ме – 1,0) и 0,8–1,0 (Ме – 1,0) соответственно. Повышение остроты зрения было статистически значимым как для OD (p = 0,015), так и для OS (p = 0,005) (табл. 2).
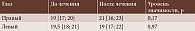
Уровень ВГД составил: OD – 16–23 (Ме – 21) мм рт. ст. (p = 0,17), OS – 17–22 (Ме – 19) мм рт. ст. (табл. 3).
Уровень ВГД у всех пациентов не превышал 24 мм рт. ст. Ни в одном случае не потребовалось назначения дополнительной гипотензивной терапии. Сравнительный анализ не выявил статистически значимого повышения уровня ВГД на фоне лечения: различия показателей до и после терапии оказались незначимыми (p = 0,97). Полученные данные свидетельствуют об отсутствии клинически значимого влияния предложенной схемы пульс-терапии на уровень ВГД.
На фоне лечения зарегистрировано статистически значимое снижение индекса CAS, отражающего активность воспалительного процесса при ЭОП (p < 0,0001). Спонтанная ретробульбарная боль, боль при движении глаз, покраснение век и конъюнктивы не зафиксированы ни в одном случае. Отек век отмечался у 12 (15%) пациентов, отек конъюнктивы (хемоз) – у 4 (5%), воспаление и отек полулунной складки – у 3 (3,75%) (табл. 4).
По завершении курса стационарного лечения ширина глазной щели составила 16–18 (Me – 18) мм для OD и 16–19 (Me – 18) мм для OS. Полученные данные свидетельствуют о статистически значимом уменьшении ширины глазной щели по сравнению с исходными показателями (p < 0,0001).
Кроме того, отмечалось статистически значимое снижение выстояния глазного яблока, что подтверждено данными экзофтальмометрии: 18–21 (Ме – 20) для OD и 18–21 (Ме – 21) для OS (p < 0,0001) (табл. 5).
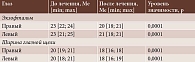
Курс консервативной терапии ЭОП продемонстрировал высокую эффективность, что подтверждено объективными данными ультразвукового сканирования (В-режим). Зарегистрировано статистически значимое уменьшение толщины экстраокулярных мышц (p < 0,0001), свидетельствующее о регрессе воспалительно-отечного процесса в орбите (табл. 6). После лечения толщина экстраокулярных мышц составила:
- правый глаз: верхняя мышца – 4,9–6,4 (Me – 5,5) мм, внутренняя – 4,9–6,8 (Me – 5,8) мм, наружная – 4,0–4,9 (Me – 4,2) мм, нижняя – 4,7–5,3 (Me – 5,1) мм;
- левый глаз: 4,5–5,8 (Me – 5,1) мм, 4,7–6,1 (Me – 5,4) мм, 4,0–5,2 (Me – 4,5) мм, 4,9–6,2 (Me – 5,3) мм соответственно.
Срок динамического наблюдения пациентов после лечения составил 6–35 (Me – 18,8) месяцев. За весь период наблюдения рецидивов заболевания не зарегистрировано ни в одном случае. У 37 пациентов со сроком наблюдения 24 месяца и более констатирована стойкая стабилизация процесса.
Обсуждение
Проведенное исследование было направлено на оценку клинической эффективности и безопасности схемы лечения активной стадии ЭОП средней и тяжелой степени. Предложенный протокол включал пульс-терапию метилпреднизолоном в комбинации с парабульбарными инъекциями бетаметазона, симптоматическим лечением и физиотерапевтическими процедурами.
Полученные результаты свидетельствуют о выраженном клиническом эффекте предложенного модифицированного протокола консервативной терапии.
Ключевым функциональным исходом стало статистически значимое повышение как некорригированной (p = 0,015 для OD, p = 0,005 для OS), так и максимальной корригированной остроты зрения (до 0,8–1,0). Показано, что примененная терапевтическая стратегия была направлена не только на купирование воспалительного процесса, но и на сохранение и восстановление зрительных функций.
Одной из потенциальных проблем системной терапии ГКС является риск повышения уровня ВГД и развития стероид-индуцированной глаукомы. В настоящем исследовании лечение не привело к статистически значимому увеличению уровня ВГД (p = 0,97). Более того, у всех пациентов по завершении курса этот показатель не превышал 24 мм рт. ст., что позволило избежать назначения дополнительной гипотензивной терапии. Данный аспект представляется крайне важным для общей оценки безопасности предложенного протокола и расширяет возможности его клинического применения, в том числе у пациентов с предрасположенностью к офтальмогипертензии. Вместе с тем у данной категории пациентов необходим более тщательный контроль за показателями ВГД.
Интегральным показателем эффективности терапии ЭОП служит смещение степени тяжести заболевания в сторону более легких форм. В исследовании к моменту завершения лечения не зарегистрировано ни одного случая тяжелой ЭОП, тогда как легкая степень имела место у 38 (47,5%) пациентов, средняя – у 27 (33,75%). Выявленные изменения носят статистически значимый характер (p = 0,005).
Предложенная терапевтическая стратегия позволила не только купировать активное воспаление, но и предотвратить прогрессирование заболевания до стадий, угрожающих потерей зрения. Достигнутый результат согласуется с основными целями лечения ЭОП – переводом заболевания в неактивную (стабильную) фазу и минимизацией риска развития клинически значимых осложнений, к которым относятся оптическая нейропатия, выраженный кератит и язва роговицы.
Шкала клинической активности (CAS) служит золотым стандартом для оценки остроты воспалительного процесса в орбите. Продемонстрированное в нашем исследовании статистически высокодостоверное снижение CAS (p < 0,0001) служит прямым доказательством эффективности терапии в отношении воздействия на ключевое патогенетическое звено ЭОП. Особенно показательно исчезновение таких субъективных и объективных признаков, как спонтанная и двигательная ретробульбарная боль, гиперемия век и конъюнктивы. Сохранение незначительного отека век (15%) и хемоза (5%) может объясняться остаточными явлениями после мощного воспалительного процесса, требующими более длительного времени для полного разрешения.
Высокодостоверное уменьшение толщины всех экстраокулярных мышц (p < 0,0001) для обоих глаз служит прямым инструментальным подтверждением разрешения воспалительного отека и инфильтрации. Учитывая доступность, скорость проведения, возможность многократного применения и практически полное отсутствие абсолютных противопоказаний для проведения, ультразвуковое исследование можно рассматривать в качестве не только диагностического, но и важнейшего мониторингового инструмента, позволяющего объективно оценивать ответ на терапию.
Полученные результаты целесообразно сопоставить с данными исследования О.И. Виноградской и соавт. [22], в котором оценивалась эффективность двух режимов пульс-терапии метилпреднизолоном у пациентов с активной ЭОП. В первой группе пациентам вводили по 1000 мг метилпреднизолона пять дней подряд (суммарная доза 5000 мг), во второй – по 1000 мг один раз в неделю в течение пяти недель (суммарная доза 5000 мг). Исходное значение по шкале CAS в группах составляло 4 [3; 5] и 4 [4; 4] балла, экзофтальм – 21,5 [19; 25] и 20 [19; 21] мм соответственно. Через 12 недель наблюдения в первой группе показатель CAS снизился до 2 [0; 4] баллов, во второй – до 2 [0; 3] баллов, экзофтальм – до 20 [16; 28] и 18 [15; 25] мм соответственно [22].
В зарубежном исследовании K.K.H. Lai и соавт. [23] обращает на себя внимание разница в протоколах и результатах. Авторы сравнивали две схемы внутривенного введения метилпреднизолона – шести- и 12-недельную. В группе с более интенсивным шестинедельным режимом (суммарная доза 4,5 г) снижение показателя по CAS составило 2,1 балла, а регресс экзофтальма – 0,8 мм за 12 недель наблюдения [23].
Данные, полученные S.M. Young и соавт. [24], указывают на то, что даже при использовании стандартизированных протоколов EUGOGO только у 65% пациентов наблюдается хороший ответ на пульс-терапию, тогда как у 31,7% – частичный, а у 3,3% эффект отсутствует. Высокий процент неполного ответа диктует необходимость поиска методов, направленных на улучшение результатов лечения.
Полученные в нашем исследовании данные коррелируют с данными мировой литературы об эффективности пульс-терапии при ЭОП. Однако применение такой схемы консервативного лечения ассоциируется с достижением выраженного клинического эффекта от лечения и стабилизации заболевания в более короткий срок, а также с сокращением частоты рецидивов.
Проведение курса лечения в условиях стационара позволяет:
- своевременно оценивать динамику заболевания и при необходимости корректировать терапию;
- обеспечивать полноту курса, исключая необходимость в дополнительных внутривенных инфузиях ГКС по месту жительства и, как следствие, предотвращая риск незавершенного лечения.
После завершения интенсивной внутривенной пульс-терапии сохраняется риск реактивации аутоиммунного процесса, поскольку резкая отмена ГКС способна спровоцировать синдром отмены и обострение ЭОП. Пролонгированный пероральный прием препарата позволяет плавно снижать его концентрацию в крови, давая возможность гипоталамо-гипофизарно-надпочечниковой системе адаптироваться и тем самым обеспечивая устойчивый противовоспалительный эффект [1, 25].
Проведенный анализ подтверждает, что включение локальных инъекций и физиотерапии в схему системной глюкокортикоидной терапии соответствует современным требованиям комплексного подхода к лечению активной ЭОП и способствует достижению выраженного контроля над воспалительным процессом в мягких тканях орбиты [26].
Усиленный клинический ответ объясняется двойным механизмом действия: системные ГКС купируют общие аутоиммунные реакции, тогда как локальное введение бетаметазона создает высокую концентрацию противовоспалительного агента непосредственно в орбитальных тканях, воздействуя на местные патофизиологические процессы в обход системных ограничений [22]. Дополнительное применение физиотерапии улучшает микроциркуляцию и фармакокинетику ГКС, что в совокупности обеспечивает устойчивое подавление воспаления и выражается в значимом клиническом улучшении.
Заключение
Эндокринная офтальмопатия представляет собой не только медицинскую, но и значимую социально-экономическую проблему, поскольку нередко поражает лиц молодого и среднего трудоспособного возраста. Для них стремительное развитие таких симптомов, как экзофтальм, диплопия, боль и риск потери зрения, становится причиной не только физических страданий, но и вынужденной социальной изоляции, профессиональных ограничений и снижения качества жизни. В связи с этим разработка эффективных, быстродействующих и безопасных терапевтических стратегий приобретает особую актуальность.
Лечение ЭОП направлено на быстрое купирование активного воспаления, достижение стойкого регресса симптомов, перевод заболевания в неактивную стадию в максимально короткий срок и минимизацию остаточных клинических и косметических проявлений.
Существующие схемы пульс-терапии нередко создают дополнительные трудности в достижении этих целей. Такие схемы нередко продолжительны (до нескольких месяцев), требуют длительного амбулаторного наблюдения и сложной логистики между стационаром и поликлиникой. Как следствие – прерывание лечения, снижение приверженности терапии и неполная или неустойчивая ремиссия.
Ключевым преимуществом предлагаемого подхода является его направленность на быструю и устойчивую стабилизацию процесса, что особенно важно для молодых активных пациентов. Перевод заболевания в неактивную стадию в сжатые сроки минимизирует период нетрудоспособности, снижает психологическую нагрузку и позволяет пациентам вернуться к привычному образу жизни, уменьшая зависимость от длительного амбулаторного долечивания. Безопасность метода (отсутствует значимое влияние на уровень ВГД и контролируемые системные эффекты) делает его применимым для широкого круга пациентов.
Таким образом, данный подход в терапии ЭОП обеспечивает не только стабильное подавление воспаления, но и выраженный регресс клинических симптомов и объективных признаков заболевания, улучшая функциональное состояние органа зрения и качество жизни пациентов.
Раннее начало и адекватное проведение пульс-терапии метилпреднизолоном остаются критически важными для предотвращения необратимых изменений – компрессионной оптической нейропатии и стойкого ограничения подвижности глазных яблок.
I.V. Potykun, A.A. Yarovoy, PhD, A.S. Levykina, S.S. Kleyankina, PhD, D.P. Volodin, PhD
Interdisciplinary Scientific and Technical Complex ‘Eye Microsurgery’ named after Academician S.N. Fedorov
Contact person: Il'ya V. Potykun, ferlj120598@yandex.ru
Relevance. Endocrine ophthalmopathy (EOP) is an autoimmune disease associated with a high risk of vision loss. Existing pulse therapy regimens are often prolonged in time, which makes it difficult to implement them on an outpatient basis and does not always allow achieving stable remission. In this regard, it is necessary to develop new, more effective and safer methods.
The aim is to evaluate the clinical efficacy and safety of the developed treatment regimen for the active stage of EOP based on pulse therapy with methylprednisolone in combination with parabulbar administration of betamethasone, symptomatic therapy and physiotherapy.
Material and methods. A prospective, controlled, non-randomized study involved 80 patients with active stage EOP (mild, moderate, and severe) who had not previously received specific treatment. All patients underwent pulse therapy with methylprednisolone according to the author's scheme (stepwise dose reduction from 750 to 125 mg with double administration every other day) in combination with parabulbar injections of betamethasone, instillations, endonasal electrophoresis and magnetic therapy. The effectiveness was assessed by the dynamics of visual acuity, the level of intraocular pressure (IOP), clinical activity (CAS), the degree of exophthalmos, the width of the ocular fissure, as well as the thickness of the extraocular muscles (according to B-scan data). Statistical data processing was performed using the Wilcoxon criterion.
Results. During treatment, there was a statistically significant decrease in the activity of the inflammatory process on the CAS scale (p < 0.0001), a decrease in the severity of exophthalmos (p < 0.0001) and the width of the ocular fissure (p < 0.0001), an increase in visual acuity (p = 0.005), as well as a decrease in the thickness of the extraocular muscles (p < 0.0001). There was no clinically significant increase in IOP levels. During the follow-up period (6–35 months, median – 18.8 months), no recurrence of the disease was recorded.
Conclusions. The proposed scheme is effective and safe. Its use makes it possible to achieve stable stabilization of the pathological process in a short time, transfer the disease to an inactive phase and ensure reliable prevention of relapses.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.