Постменопаузальная гиперандрогения
- Аннотация
- Статья
- Ссылки
- English
В статье рассмотрен клинический случай пациентки с текоматозом яичников.
В статье рассмотрен клинический случай пациентки с текоматозом яичников.
Введение
Гиперандрогения – группа эндокринных нарушений вследствие избыточного количества андрогенов или повышенной чувствительности к ним [1]. В организме женщины андрогены синтезируются тека-клетками яичников, корой надпочечников и периферическими тканями. К основным андрогенам относятся дегидроэпиандростерон (ДГЭА), 90% продукции которого приходится на надпочечники, дегидроэпиандростерона сульфат (ДГЭА-С), образующийся только в надпочечниках, андростендион и тестостерон, вырабатываемые как в надпочечниках, так и в яичниках, а также дигидротестостерон, являющийся продуктом конверсии тестостерона в периферических тканях.
Главным андрогеном считается тестостерон, синтез которого в организме женщин происходит в яичниках, надпочечниках и жировой ткани [2]. Посредством ароматазы тестостерон переходит в эстрадиол, а посредством 5-α-редуктазы – в дигидротестостерон. Основное количество циркулирующего тестостерона находится в связанном с белками состоянии. Так, 30–35% связывается с альбумином, а 60–70% – с глобулином, связывающим половые гормоны (ГСПГ) [1, 3]. Поскольку связывание тестостерона с альбумином довольно слабое, свободная и связанная с альбумином фракции определяются как биодоступный тестостерон. На содержание активной (свободной) фракции тестостерона помимо его продукции влияет уровень ГСПГ.
В период менопаузы происходит истощение фолликулов и снижение выработки тестостерона тека-клетками яичников. При этом повышается синтез тестостерона стромальными клетками из-за усиленной стимуляции лютеинизирующим гормоном. В результате выработка андрогенов яичниками в менопаузе остается примерно на том же уровне. Однако на фоне снижения продукции эстрогенов яичниками снижается уровень ГСПГ, что в конечном итоге обусловливает относительное преобладание андрогенов [4–6]. Поэтому в данный период жизни женщин помимо типично менопаузальных могут появиться андрогензависимые симптомы, например усиленный рост волос на лице, истончение волос из-за относительного избытка андрогенов [7].
Таким образом, к развитию гиперандрогении в постменопаузе может приводить снижение концентрации ГСПГ (с повышением фракции свободного тестостерона), избыточный синтез андрогенов (в яичниках или надпочечниках), снижение активности ароматазы (с подавлением конверсии тестостерона в эстрадиол), повышение активности 5-α-редуктазы (с усилением конверсии тестостерона в дигидротестостерон) [4, 5, 8].
Клиническая картина гиперандрогении представлена гирсутизмом, акне, андрогенной алопецией или симптомами вирилизации.
Гирсутизм проявляется усиленным ростом терминальных волос на верхней губе, подбородке, груди, верхней и нижней части спины, животе выше и ниже пупка, плечах, бедрах. Его выраженность определяется по шкале Ферримана – Голлвея. Каждая из девяти андрогензависимых зон оценивается от нуля до четырех баллов в зависимости от полного отсутствия волос или выраженного их роста по мужскому типу. Степень гирсутизма обусловлена этнической принадлежностью. Патология диагностируется при сумме баллов ≥ 6–8 (по некоторым данным, при сумме баллов ≥ 4–6). Сумма от 8 до 15 баллов характерна для легкой степени гирсутизма, от 16 до 25 баллов – для умеренной степени, более 25 баллов – для выраженного (тяжелого) гирсутизма [1, 9–11].
Развитие акне связывают с повышенным уровнем андрогенов. На данный момент времени общепринятой системы оценки акне не существует [8].
Появление андрогенной алопеции в лобно-теменной области объясняют влиянием 5-α-редуктазы в волосяных фолликулах и повышенным уровнем дигидротестостерона [12]. Для оценки степени алопеции используется шкала Людвига.
К симптомам вирилизации относят увеличение клитора (> 1,5 × 2,5 см) [13], барифонию (огрубение голоса) и атрофию молочных желез [14].
Наиболее распространенной причиной абсолютного избытка андрогенов в постменопаузе считается синдром поликистозных яичников, проявляющийся легкими или умеренными симптомами гиперандрогении без вирилизации [15]. Наличие в анамнезе менструальных нарушений или поликистозных яичников наряду с уровнем тестостерона в сыворотке менее 2 нмоль/л чаще всего подтверждает этот наиболее вероятный диагноз [16, 17].
Легкие симптомы гиперандрогении у пациенток в период менопаузы могут быть вызваны относительным избытком андрогенов, что связано с переходом к менопаузе. Однако прогрессирование гирсутизма или нарастание симптомов вирилизации должны вызвать настороженность в отношении развития гипертекоза яичников, а также андроген-секретирующей опухоли яичников или надпочечников [18].
Для гипертекоза яичников характерен повышенный синтез тестостерона (> 5 нмоль/л) лютеинизированными тека-клетками яичников, при этом уровень остальных андрогенов остается в пределах референса [15, 19]. Андроген-секретирующие опухоли яичников (опухоли из клеток Сертоли, Сертоли – Лейдига, Лейдиг-клеточные опухоли) – андробластомы – секретируют андрогены, а текомы и гранулезно-клеточные опухоли – эстрогены и иногда андрогены [15]. Андробластомы сопровождаются повышением уровня тестостерона более 5 нмоль/л, а также повышенным уровнем андростендиона и 17-гидроксипрогестерона (17-OHP). Гранулезно-клеточные опухоли обычно вырабатывают эстрадиол и/или тестостерон, а также антимюллеров гормон и ингибин В [20–22]. Андроген-секретирующие опухоли надпочечников встречаются реже, проявляются симптомами вирилизации с повышением уровня надпочечниковых андрогенов – ДГЭА и ДГЭА-С, а также тестостерона и кортизола, что требует исключения гиперкортицизма [15]. При этом все андроген-секретирующие опухоли характеризуются быстро нарастающими симптомами вирилизации и нуждаются в оперативном лечении.
Клинический случай
Пациентка 64 лет обратилась к эндокринологу с жалобами на охриплость, огрубение голоса, избыточный рост волос над верхней губой, на подбородке, груди и животе, в лобковой области, на наружных половых органах, предплечьях, внутренней поверхности бедер, коленях и голенях. Впервые изменение тембра голоса и избыточный рост волос над верхней губой отметила в 59 лет. Далее присоединился усиленный рост жестких пигментированных волос на подбородке, туловище, верхних и нижних конечностях. Пациентка была осмотрена врачом-гинекологом, клиторомегалии не выявлено.
При осмотре рост составлял 167 см, вес – 64 кг, индекс массы тела – 22,9 кг/м2. Кожные покровы физиологической окраски, чистые. Выявлены гирсутизм умеренной степени (19 баллов по шкале Ферримана – Голлвея) и алопеция в лобно-теменной области.
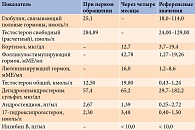
При гормональном исследовании обнаружено изолированное повышение уровня тестостерона (> 5 нмоль/л) на фоне незначительного увеличения уровня 17-OHP и нормальных показателей андростендиона, ДГЭА-С и ингибина В (таблица).
На следующем этапе были проведены инструментальные исследования.
Согласно результатам ультразвукового исследования (УЗИ) органов малого таза, матка имеет четкие, неровные контуры, положение anteversion-flexio, размер – 32 × 23 × 36 мм, форма грушевидная. Миометрий: структура неоднородная, из передней стенки, ближе ко дну, исходит субсерозный миоматозный узел размером 8,2 × 7,9 мм. Эндометрий: гиперэхогенный, линейный, каждый слой до 1,0–1,4 мм, контуры четкие, ровные. Шейка матки: длина – 36 мм, цервикальный канал расширен до 4 мм анэхогенным содержимым. Эндоцервикс утолщен, слабо гиперэхогенный, складчатый, с единичными сигналами кровотока при цветовом допплеровском картировании (ЦДК). Правый яичник: контуры четкие, ровные, положение обычное, размер – 25 × 12 × 16 мм, объем – 2,51 см3. Структура неравномерно уплотнена, с нечеткими участками сниженной эхогенности диаметром до 7 мм, единичные сигналы кровотока при ЦДК. Левый яичник: контуры четкие, ровные, положение обычное, размер – 21 × 20 × 19 мм, объем – 4,17 см3. Структура неравномерно уплотнена, с нечеткими участками сниженной эхогенности диаметром до 9 мм, единичные сигналы кровотока при ЦДК. Позадиматочное пространство: свободной жидкости не выявлено.
Заключение: УЗИ-признаки инволютивных изменений органов малого таза, серозоцервикса, эндоцервицита (под вопросом). Объем яичников не соответствует сроку постменопаузы (после десяти лет менопаузы объем яичника составляет около 1,5 см3).
Согласно результатам УЗИ надпочечников: в проекции патологических образований достоверно не обнаружено.
Компьютерная томография забрюшинного пространства с внутривенным контрастированием выявила липому поджелудочной железы, кисты почек, гиперденсное содержимое левой почки – конкремент.
Магнитно-резонансная томография (МРТ) органов малого таза. Матка: положение anteversion-flexio, размер – 42 × 42 × 29 мм, полость матки не деформирована. Эндометрий: толщина – 1,5 мм, структура негомогенная. Миометрий: структура неоднородная, субсерозно по переднему контуру визуализируется четко очерченное образование гомогенной структуры размером 10 × 9 × 7 мм. Шейка матки: длина – 23 мм, эндоцервикс диффузно утолщен до 7 мм (по заднему контуру), строма содержит единичные кисты до 2 мм, цервикальный канал не расширен. Влагалище: без структурных изменений.
Яичники: однородной структуры, справа размер – 20 × 18 × 24 мм, объем – 4,32 см3, слева размер – 25 × 24 × 27 мм, объем – 8,1 см3.
Заключение: МРТ-картина лейомиомы тела матки, гиперплазии шейки матки, инволютивных изменений матки и яичников.
С учетом жалоб, клинических и лабораторных данных в пользу гиперандрогении, повышения уровня тестостерона более 5 нмоль/л, двустороннего увеличения размера яичников, не соответствующего сроку постменопаузы, отсутствия образований в яичниках и надпочечниках был установлен диагноз: клинико-лабораторная гиперандрогенемия, текоматоз яичников.
Пациентке рекомендовано хирургическое лечение.
Заключение
В представленном клиническом случае проводился поиск причин, вызвавших клиническую и лабораторную гиперандрогению. Прежде всего исключались андроген-секретирующие опухоли яичников и надпочечников, ятрогенные формы гиперандрогении, вызванные приемом препаратов тестостерона.
Анализ данных литературы показал, что гипертекоз яичников проявляется медленным развитием тяжелых симптомов гиперандрогении у женщин в пери- или постменопаузе, его распространенность в период постменопаузы составляет 9,3% [15]. Гипертекоз яичников необходимо дифференцировать с андроген-секретирующими опухолями как надпочечников, так и яичников. Для подтверждения диагноза рекомендовано гистологическое исследование. В среднем объем яичников в постменопаузе составляет 2,20 ± 0,01 см3, но не более 5,0 см3. При текоматозе объем яичников может достигать 10 см3 [23–25].
У пациенток с гиперандрогенией подход к лечению во многом зависит от тяжести ее проявлений. При обнаружении опухоли яичника или тяжелого гипертекоза показана двусторонняя овариоэктомия.
F.V. Valeeva, PhD, Prof., Yu.U. Sharipova, PhD, Z.R. Alimetova, PhD, G.R. Gazizova, PhD
Kazan State Medical University
LiLC ‘Samson’
Contact person: Zulfiya R. Alimetova, alzurg@mail.ru
Postmenopausal hyperandrogenism is a condition caused by an increased androgen content due to endogenous overproduction or excessive external intake during postmenopause. The appearance of symptoms of severe virilization and hirsutism during this period most often indicates an increase in their synthesis in the ovaries or adrenal glands associated with androgen-producing tumors or ovarian tecomatosis.
The article presents a clinical case of a patient with ovarian tecomatosis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.