Оценка эффективности трансдермальной системы ЕВРА в лечении дисфункции яичников у девочек
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В проспективном рандомизированном контролируемом исследовании, проведенном в отделении гинекологии Российской детской клинической больницы (март – август 2025 г.), участвовало 120 девочек в возрасте от 12 лет до 17 лет 11 месяцев 29 дней с клинически и лабораторно подтвержденной ДЯ (нарушения менструального цикла, гиперандрогения, изменения соотношения лютеинизирующего (ЛГ) и фолликулостимулирующего (ФСГ) гормонов, повышенный уровень андрогенов). Пациентки в соотношении 1:1 были рандомизированы в группу ЕВРА (трансдермальный пластырь ЕВРА, смена еженедельно) и контрольную группу (стандартизированная циклическая витаминотерапия).
Результаты. Исходные характеристики пациенток обеих групп были сопоставимы по возрасту и продолжительности менструального цикла: в контрольной группе – 15,3 ± 1,7 года и 67,2 ± 25,3 дня, в группе ЕВРА – 15,1 ± 1,9 года и 65,5 ± 22,1 дня соответственно. Через шесть месяцев регулярный цикл (21–45 дней) наблюдался у 91,7% пациенток группы ЕВРА и 36,7% пациенток группы контроля (p < 0,001). Средняя продолжительность цикла нормализовалась до 28,4 ± 1,2 дня в группе ЕВРА и 44,5 ± 12,4 дня в контрольной группе (p < 0,001). В отличие от группы контроля в группе ЕВРА отмечались гормональные улучшения: снижение уровня свободного тестостерона (с 3,1 ± 0,9 до 2,5 ± 0,8 нг/дл; p < 0,01) и дегидроэпиандростерон-сульфата (с 280,5 ± 65,2 до 210,3 ± 50,1 мкг/дл; p < 0,001), нормализация ЛГ/ФСГ
(с 1,5 ± 0,6 до 1,2 ± 0,4; p < 0,05). В группе ЕВРА улучшились симптомы гиперандрогении: тяжесть акне снизилась на 28% (с 8,2 ± 2,5 до 6,5 ± 2,0; p < 0,01). В группе контроля зафиксированы минимальные изменения. Баллы по опроснику PGQoL возросли с 55,6 ± 8,2 до 78,9 ± 10,1 в группе ЕВРА (p < 0,001) и с 56,1 ± 7,9 до 65,3 ± 9,5 в контрольной группе (p < 0,01 между группами).
Серьезных нежелательных явлений (НЯ) не зарегистрировано. Легкие местные кожные реакции (зуд, покраснение) у 9 (15%) пациенток группы ЕВРА не потребовали прекращения терапии. Общие системные НЯ (головная боль у 3 (5%) пациенток и тошнота у 1 (1,7%) пациентки) также не повлекли за собой прекращения терапии. В контрольной группе общие НЯ отмечались в 5 (8,3%) случаях, при этом местные реакции отсутствовали.
Выводы. Трансдермальная система ЕВРА превосходит циклическую витаминотерапию в лечении девочек-подростков с ДЯ, существенно улучшая регулярность цикла, гормональный баланс, симптомы гиперандрогении и качество жизни при благоприятном профиле безопасности и высокой удовлетворенности. Удобство применения (еженедельно) делает трансдермальный пластырь ЕВРА эффективной альтернативой циклической витаминотерапии в детской гинекологии.
Материал и методы. В проспективном рандомизированном контролируемом исследовании, проведенном в отделении гинекологии Российской детской клинической больницы (март – август 2025 г.), участвовало 120 девочек в возрасте от 12 лет до 17 лет 11 месяцев 29 дней с клинически и лабораторно подтвержденной ДЯ (нарушения менструального цикла, гиперандрогения, изменения соотношения лютеинизирующего (ЛГ) и фолликулостимулирующего (ФСГ) гормонов, повышенный уровень андрогенов). Пациентки в соотношении 1:1 были рандомизированы в группу ЕВРА (трансдермальный пластырь ЕВРА, смена еженедельно) и контрольную группу (стандартизированная циклическая витаминотерапия).
Результаты. Исходные характеристики пациенток обеих групп были сопоставимы по возрасту и продолжительности менструального цикла: в контрольной группе – 15,3 ± 1,7 года и 67,2 ± 25,3 дня, в группе ЕВРА – 15,1 ± 1,9 года и 65,5 ± 22,1 дня соответственно. Через шесть месяцев регулярный цикл (21–45 дней) наблюдался у 91,7% пациенток группы ЕВРА и 36,7% пациенток группы контроля (p < 0,001). Средняя продолжительность цикла нормализовалась до 28,4 ± 1,2 дня в группе ЕВРА и 44,5 ± 12,4 дня в контрольной группе (p < 0,001). В отличие от группы контроля в группе ЕВРА отмечались гормональные улучшения: снижение уровня свободного тестостерона (с 3,1 ± 0,9 до 2,5 ± 0,8 нг/дл; p < 0,01) и дегидроэпиандростерон-сульфата (с 280,5 ± 65,2 до 210,3 ± 50,1 мкг/дл; p < 0,001), нормализация ЛГ/ФСГ
(с 1,5 ± 0,6 до 1,2 ± 0,4; p < 0,05). В группе ЕВРА улучшились симптомы гиперандрогении: тяжесть акне снизилась на 28% (с 8,2 ± 2,5 до 6,5 ± 2,0; p < 0,01). В группе контроля зафиксированы минимальные изменения. Баллы по опроснику PGQoL возросли с 55,6 ± 8,2 до 78,9 ± 10,1 в группе ЕВРА (p < 0,001) и с 56,1 ± 7,9 до 65,3 ± 9,5 в контрольной группе (p < 0,01 между группами).
Серьезных нежелательных явлений (НЯ) не зарегистрировано. Легкие местные кожные реакции (зуд, покраснение) у 9 (15%) пациенток группы ЕВРА не потребовали прекращения терапии. Общие системные НЯ (головная боль у 3 (5%) пациенток и тошнота у 1 (1,7%) пациентки) также не повлекли за собой прекращения терапии. В контрольной группе общие НЯ отмечались в 5 (8,3%) случаях, при этом местные реакции отсутствовали.
Выводы. Трансдермальная система ЕВРА превосходит циклическую витаминотерапию в лечении девочек-подростков с ДЯ, существенно улучшая регулярность цикла, гормональный баланс, симптомы гиперандрогении и качество жизни при благоприятном профиле безопасности и высокой удовлетворенности. Удобство применения (еженедельно) делает трансдермальный пластырь ЕВРА эффективной альтернативой циклической витаминотерапии в детской гинекологии.


Введение
В современной России на фоне общего улучшения демографических показателей, таких как рождаемость и продолжительность жизни, наблюдается парадоксальная тенденция к ухудшению здоровья подрастающего поколения, включая детей, подростков, и женщин репродуктивного возраста. Инициированное Указом Президента РФ от 29 мая 2017 г. № 240 «десятилетие детства» (2018–2027) подчеркивает стратегическую важность поддержки материнства и детства как фундаментального элемента развития общества. В ближайшие годы репродуктивного возраста достигнут около 11,6 млн российских девушек, что определит их ключевую роль в будущем воспроизводстве населения. Поддержание и укрепление соматического и репродуктивного здоровья представительниц этой группы становится приоритетной задачей, ведь именно они составляют тот золотой фонд, от которого зависит здоровье последующих поколений [1].
Одной из ключевых причин нарушений репродуктивной функции и развития заболеваний является гиперандрогения, распространенность которой среди девочек и женщин репродуктивного возраста колеблется от 4 до 18% [2].
Выявление данной эндокринной патологии затруднено, особенно в пубертатном периоде, когда границы между физиологической нормой и патологическими изменениями размыты [3]. Дополнительные трудности создает возможность более ранней манифестации гиперандрогении у некоторых пациенток, а также особенности клинической картины синдрома поликистозных яичников, симптомы которого в подростковом возрасте могут имитировать типичные проявления пубертата [4].
Клинические признаки гиперандрогении, в частности гирсутизм и нарушения менструального цикла, возникают на разных этапах развития, а их коррекция нередко сопряжена с определенными трудностями. Недостаточное внимание к комплексному изучению изменений в организме при гиперпродукции андрогенов, включая нейроэндокринные и психохарактерологические дисфункции, а также особенности фолликулогенеза, препятствует разработке оптимальных подходов к диагностике и терапии у подростков [5, 6].
Несмотря на повсеместное распространение, циклическая витаминотерапия остается малоэффективной в коррекции гиперандрогенных состояний у подростков. Исследования показывают, что лишь у незначительной части пациенток после такого лечения менструальный цикл становится регулярным. Это ставит под сомнение целесообразность применения данного вида терапии в качестве основного [7]. В связи с этим особого внимания заслуживают трансдермальные гормональные системы, такие как ЕВРА (этинилэстрадиол + норэлгестромин). Удобство их применения (пластыри наклеивают один раз в неделю) значительно повышает приверженность пациенток лечению. По данным клинических наблюдений, приверженность терапии трансдермальными системами может превышать 89%, что делает ее перспективной альтернативой для юных пациенток, нуждающихся в длительном и эффективном контроле гиперандрогенных состояний [8–10].
Цель – сравнить эффективность трансдермальной системы ЕВРА и стандартной терапии в коррекции симптомов дисфункции яичников (ДЯ) у девочек, а также оценить влияние таких методов на качество жизни.
Материал и методы
Проспективное рандомизированное контролируемое исследование проводилось на базе отделения гинекологии Российской детской клинической больницы – филиала ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России в период с марта по август 2025 г. В исследование было включено 120 девочек в возрасте от 12 лет до 17 лет 11 месяцев 29 дней с диагнозом ДЯ, установленным на основании клинических проявлений (нарушения менструального цикла, гиперандрогения) и данных лабораторного исследования (нарушение соотношения лютеинизирующего (ЛГ) и фолликулостимулирующего (ФСГ) гормонов, повышенный уровень андрогенов).
Критериями включения были:
- возраст от 12 лет до 17 лет 11 месяцев 29 дней;
- наличие клинически значимых симптомов ДЯ, требующих медикаментозного лечения;
- подтвержденные гормональные отклонения, соответствующие диагнозу ДЯ;
- возможность регулярного амбулаторного наблюдения в течение шести месяцев;
- получение письменного информированного согласия от родителей/опекунов, а также от самой пациентки, достигшей 15-летнего возраста.
Критерии исключения:
- беременность или подозрение на беременность;
- наличие других эндокринных заболеваний (например, сахарного диабета, заболеваний щитовидной железы), требующих специфической терапии;
- аллергические реакции или повышенная чувствительность к компонентам трансдермальной системы ЕВРА или стандартной витаминотерапии;
- прием гормональных препаратов (включая комбинированные оральные контрацептивы, прогестины, антиандрогены) в течение шести месяцев, предшествовавших включению в исследование, либо необходимость их приема в рамках стандартной терапии (определялась протоколом).
После подписания информированного согласия и проведения скринингового обследования пациентки, соответствовавшие критериям включения, в соотношении 1:1 были рандомизированы в две группы – основную (трансдермальная система ЕВРА) и контрольную (циклическая витаминотерапия) – с использованием централизованной компьютерной генерации случайных чисел. Период наблюдения составил шесть месяцев.
Пациентки основной группы применяли трансдермальную систему ЕВРА в соответствии с протоколом исследования. Режим применения (частота смены пластыря, доза, место аппликации) был стандартизирован и детально описан в протоколе.
Пациентки контрольной группы получали циклическую витаминотерапию, назначенную врачом-гинекологом в соответствии с действующими клиническими рекомендациями в качестве метода вспомогательной терапии для девочек с ДЯ. Состав, доза и схема применения витаминных комплексов были стандартизированы в рамках протокола исследования.
Первичными конечными точками служили:
- регулярность менструального цикла. Оценивались частота наступления менструаций, регулярность цикла (соотношение количества циклов продолжительностью 21–45 дней к общему числу циклов за период наблюдения) и его длительность;
- гормональный профиль. Определялись уровни ФСГ, ЛГ, эстрадиола, прогестерона, свободного тестостерона, дегидроэпиандростерон-сульфата (ДГЭА-С) в сыворотке крови;
- симптомы гиперандрогении. Анализировалась динамика проявлений, таких как акне (согласно глобальной системе классификации акне – Global Acne Grading System, GAGS), гирсутизм (шкала Ферримана – Голлвея).
Вторичные конечные точки:
- качество жизни. Оценивалось с использованием валидированного опросника Pediatric Gynecology Quality of Life Questionnaire (PGQoL), адаптированного для подростков, до начала терапии и после шести месяцев лечения;
- безопасность. Регистрировались все нежелательные явления (НЯ) и серьезные НЯ в соответствии с классификацией MedDRA. Дополнительно оценивались локальные реакции на месте аппликации трансдермальной системы (зуд, покраснение, раздражение, дерматит) по стандартизированной шкале;
- удовлетворенность терапией. Анализировалась с помощью структурированного опросника для пациенток и их родителей/опекунов;
- ультразвуковые параметры. По данным ультразвукового исследования (УЗИ) органов малого таза оценивались размеры яичников, количество антральных фолликулов, толщина эндометрия;
- приверженность лечению. Определялась на основании анализа дневников пациенток и данных клинического осмотра.
Сбор данных осуществлялся на каждом визите (исходно, через один, три и шесть месяцев наблюдения). Лабораторные исследования (гормональный профиль, общий и биохимический анализ крови) проводились натощак. УЗИ органов малого таза выполнялось на 3–5-й день менструального цикла (при его наличии).
Объем выборки рассчитывали с целью обеспечения 90%-ной статистической мощности для выявления клинически значимой разницы в регулярности менструального цикла между группами при уровне значимости (α) 0,05 (двусторонний критерий). Статистический анализ выполняли с использованием пакета программ SAS (v. 9.3) по принципу intention-to-treat (ITT). Все статистические тесты были двусторонними. Критическим считался уровень значимости (p) < 0,05.
Количественные переменные представлены в виде среднего значения и стандартного отклонения (M ± SD), при распределении, отличном от нормального, – в виде медианы и интерквартильного размаха. Нормальность распределения проверяли исходя из критерия Шапиро – Уилка. При сравнении групп по первичным и вторичным конечным точкам использовали t-критерий Стьюдента или U-критерий Манна – Уитни. Динамику показателей оценивали с помощью дисперсионного анализа для повторных измерений (ANOVA). При сравнении частоты возникновения НЯ и других категориальных переменных применяли критерий χ² или точный критерий Фишера.
Результаты
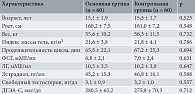
Демографические и исходные клинические характеристики пациенток обеих групп были сопоставимы, что подтверждает эффективность рандомизации (табл. 1). Средняя продолжительность менструального цикла до начала исследования в основной группе (ЕВРА) составила 65,5 ± 22,1 дня, в контрольной (циклическая витаминотерапия) – 67,2 ± 25,3 дня (p > 0,05). Уровни ФСГ, ЛГ, эстрадиола, свободного тестостерона и ДГЭА-С также не имели статистически значимых различий между группами до начала терапии.
К концу шестого месяца наблюдения в основной группе было зафиксировано статистически значимое улучшение регулярности цикла по сравнению с контрольной группой.
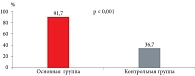
В основной группе регулярный менструальный цикл (21–45 дней) наблюдался у 55 (91,7%) пациенток, в то время как в контрольной – у 22 (36,7%) (p < 0,001) (рис. 1).
В основной группе средняя продолжительность цикла стабилизировалась и составила 28,4 ± 1,2 дня, тогда как в контрольной оставалась вариабельной – 44,5 ± 12,4 дня (p < 0,001).
Частота нормализации менструального цикла (21–35 дней) также была выше в основной группе – 60 против 25% (p < 0,001).
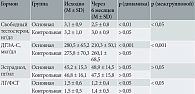
Через шесть месяцев терапии в основной группе отмечались значительные положительные изменения в гормональном профиле пациенток по сравнению с контрольной группой (табл. 2).
В основной группе зафиксировано достоверное снижение уровней свободного тестостерона – с 3,1 ± 0,9 до 2,5 ± 0,8 нг/дл (p < 0,01) и ДГЭА-С – с 280,5 ± 65,2 до 210,3 ± 50,1 мкг/дл (p < 0,001), а также нормализация ЛГ/ФСГ – с 1,5 ± 0,6 до 1,2 ± 0,4 (p < 0,05). В контрольной группе существенных изменений в отношении указанных гормональных параметров не зарегистрировано (p > 0,05). Уровень эстрадиола в обеих группах показал незначительную динамику (p > 0,05). Между группами не выявлено статистически значимых различий в изменении уровней эстрадиола (p > 0,05). Таким образом, терапия ЕВРА продемонстрировала эффективность в коррекции гиперандрогении и нормализации функционирования гипоталамо-гипофизарно-яичниковой оси, в то время как циклическая витаминотерапия не оказала статистически значимого влияния на гормональный статус пациенток.
Как уже отмечалось, количественную оценку динамики степени тяжести акне осуществляли по GAGS [1]. Сравнительный анализ продемонстрировал статистически значимое и более выраженное снижение показателей в основной группе (ЕВРА): средний балл GAGS достоверно снизился с 15,6 ± 3,2 до 6,3 ± 2,1 (на 59,6% от исходного; p < 0,001). В контрольной группе (циклическая витаминотерапия) также было зафиксировано статистически значимое снижение среднего балла с 14,9 ± 2,8 до 10,5 ± 2,4 (на 29,5% от исходного; p < 0,05). Межгрупповой анализ показал, что эффективность трансдермальной системы ЕВРА в купировании проявлений акне достоверно выше: абсолютное снижение составило 9,3 балла против 4,4 балла в контрольной группе (p < 0,01 между группами), что соответствует двукратному увеличению терапевтического эффекта (рис. 2).
Анализ динамики гирсутизма по шкале Ферримана – Голлвея выявил статистически значимое преимущество трансдермальной системы ЕВРА перед циклической витаминотерапией. В основной группе клинически значимое улучшение (снижение балла ≥ 1) зафиксировано у 18 (30%) пациенток, тогда как в контрольной – лишь у 6 (10%) (p < 0,01). Среди ответивших на терапию в основной группе средний балл достоверно снизился с 8,2 ± 2,5 до 6,5 ± 2,0 (p < 0,01), что соответствует редукции на 28% от исходного уровня. Среди ответивших на лечение пациенток контрольной группы (n = 6) наблюдалось незначительное снижение – с 8,0 ± 2,3 до 7,5 ± 2,1, не достигшее статистической значимости (p > 0,05). Таким образом, применение системы ЕВРА не только в три раза чаще приводит к улучшению показателей, но и обеспечивает более выраженный регресс симптомов у ответивших на лечение пациенток.
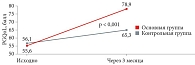
Согласно результатам опросника PGQoL, через шесть месяцев терапии в основной группе наблюдалось статистически значимое улучшение показателей качества жизни по сравнению с исходным уровнем (увеличение общего балла с 55,6 ± 8,2 до 78,9 ± 10,1; p < 0,001). В контрольной группе улучшение было менее выраженным (увеличение общего балла с 56,1 ± 7,9 до 65,3 ± 9,5; p < 0,05). При сравнении между группами показатели качества жизни были статистически значимо выше в основной группе (p < 0,01) (рис. 3).
Серьезных НЯ в исследовании не зарегистрировано. В основной группе наиболее частыми НЯ были кожные реакции в месте аппликации трансдермальной системы – 9 (15%) случаев. Местные кожные реакции были легкой степени выраженности (зуд, покраснение) и не требовали прекращения терапии. Общие системные НЯ, такие как головная боль и тошнота, отмечались у 3 (5%) и 1 (1,7%) пациентки соответственно.
В контрольной группе НЯ, связанные с приемом витаминных комплексов, отмечались редко и имели легкую степень. В частности, дискомфорт в желудочно-кишечном тракте отмечался у 2 (3,3%) пациенток (табл. 3).
Уровень удовлетворенности терапией был значительно выше в основной группе. 85% пациенток и их родителей/опекунов выразили высокую удовлетворенность лечением в силу улучшения параметров менструального цикла, положительной динамики кожных проявлений гиперандрогении и удобства применения. В контрольной группе этот показатель составил 55% (p < 0,001).
Через шесть месяцев терапии были зафиксированы следующие изменения.
Объем яичников. У пациенток основной группы средний объем яичников уменьшился с 8,5 ± 2,1 до 7,8 ± 1,9 см³. Несмотря на наметившуюся тенденцию к снижению, разница 0,7 см³ не достигла статистической значимости (p > 0,05). В контрольной группе средний объем яичников также продемонстрировал незначительное снижение – с 8,4 ± 2,0 до 8,2 ± 2,1 см³ без статистически значимых изменений (p > 0,05). Межгрупповое сравнение не выявило статистически значимых различий (p > 0,05).
Количество антральных фолликулов. В основной группе среднее количество антральных фолликулов увеличилось с 6,1 ± 1,5 до 7,2 ± 1,8, однако данная положительная динамика не достигла статистической значимости (p > 0,05). В контрольной группе прирост (с 6,2 ± 1,6 до 6,5 ± 1,7) также оказался статистически незначимым (p > 0,05). Межгрупповое сравнение не выявило достоверных различий по данному показателю (p > 0,05).
Толщина эндометрия. Анализ толщины эндометрия не показал статистически значимых различий между группами на всех этапах наблюдения, что говорит об отсутствии существенного влияния терапии на данный показатель.
Приверженность лечению. В обеих группах приверженность терапии была высокой. Несоблюдение режима (пропуск смены пластыря) зафиксировано у 3% пациенток основной группы. В контрольной группе график приема витаминов нарушили 5% пациенток. Различия статистически незначимы (p > 0,05).
Обсуждение
Данное проспективное рандомизированное контролируемое исследование демонстрирует существенное преимущество трансдермальной системы ЕВРА перед циклической витаминотерапией в коррекции клинических и лабораторных проявлений ДЯ у девочек-подростков. Ключевым результатом является значительное улучшение регулярности менструального цикла: в группе ЕВРА регулярный цикл (21–45 дней) достигнут у 91,7% пациенток, что в разы превышает показатель контрольной группы (36,7%). Это подтверждается стабилизацией средней продолжительности цикла и более высокой частотой нормальных (21–35 дней) циклов. Кроме того, применение трансдермальной системы ЕВРА ассоциируется с эффективным снижением уровней андрогенов (свободного тестостерона и ДГЭА-С) и нормализацией соотношения ЛГ и ФСГ, что клинически проявляется в купировании симптомов гиперандрогении, таких как акне и гирсутизм.
Улучшение клинических симптомов ДЯ прямо коррелирует с повышением качества жизни пациенток. Зафиксировано статистически значимое увеличение общего балла по опроснику PGQoL в группе ЕВРА (с 55,6 до 78,9; p < 0,001), что в 1,5 раза выше аналогичного показателя контрольной группы (с 56,1 до 65,3; p < 0,05). Межгрупповое сравнение показало статистически значимо более выраженное улучшение качества жизни пациенток основной группы (p < 0,01). Это подчеркивает важность комплексного подхода, при котором не только физиологические, но и психоэмоциональные аспекты состояния играют ключевую роль.
Вероятно, более высокая удовлетворенность терапией среди пациенток основной группы обусловлена удобством применения трансдермальной системы ЕВРА (еженедельная смена пластыря) по сравнению с ежедневным приемом витаминов. Высокую степень удовлетворенности отметили 85% пациенток группы ЕВРА, что значимо выше показателя контрольной группы (55%; p < 0,001). При этом высокая приверженность лечению (> 95%) в обеих группах не нивелирует преимущества ЕВРА с точки зрения субъективного восприятия терапии.
Полученные данные свидетельствуют о целесообразности включения трансдермальной системы ЕВРА в алгоритмы лечения ДЯ у подростков, а также обосновывают необходимость проведения дальнейших исследований, в том числе сравнительных.
Заключение
Трансдермальная система ЕВРА продемонстрировала высокую клиническую эффективность и преимущество перед циклической витаминотерапией у девочек-подростков с ДЯ. Применение препарата обеспечивает значимое улучшение не только менструальной функции и гормонального статуса, но также качества жизни пациенток, что позволяет рассматривать его как перспективный метод выбора в детской гинекологии.
E.V. Sibirskaya, PhD, Prof., P.O. Nikiforova
Russian University of Medicine
Russian Children’s Clinical Hospital – a Branch of N.I. Pirogov Russian National Research Medical University
N.I. Pirogov Russian National Research Medical University
Contact person: Polina O. Nikiforova, pol_nikiforova@mail.ru
The aim is to compare the effectiveness of the EVRA transdermal system and standard therapy in correcting the symptoms of ovarian dysfunction (OD) in adolescent girls and assess their impact on quality of life.
Material and methods. A prospective randomized controlled trial conducted in the Gynecology department of the Russian Children´s Clinical Hospital (March – August 2025) involved 120 girls aged 12 to 17 years, 11 months, and 29 days with clinically and laboratory-confirmed OD (menstrual disorders, hyperandrogenism, changes in the ratio of luteinizing (LH) and follicle-stimulating (FSH) hormones, increased androgen levels). Patients in a 1:1 ratio were randomly assigned to the EVRA group (EVRA transdermal patch, weekly change) and the control group (standardized cyclic vitamin therapy).
Results. The initial characteristics of the patients in both groups were comparable in age and duration of the menstrual cycle: in the control group – 15.3 ± 1.7 years and 67.2 ± 25.3 days, in the EVRA group – 15.1 ± 1.9 years and 65.5 ± 22.1 days, respectively. After six months, a regular cycle (21–45 days) was observed in 91.7% of patients in the EVRA group and 36.7% of patients in the control group (p < 0.001). The average cycle duration returned to 28.4 ± 1.2 days in the EVRA group and 44.5 ± 12.4 days in the control group (p < 0.001). In contrast to the control group, hormonal improvements were noted in the EVRA group: a decrease in the level of free testosterone (from 3.1 ± 0.9 to 2.5 ± 0.8 ng/dl; p < 0.01) and dehydroepiandrosterone sulfate (from 280.5 ± 65.2 to 210.3 ± 50.1 mcg/dl; p < 0.001), normalization of LH/FSH (from 1.5 ± 0.6 to 1.2 ± 0.4; p < 0.05). The symptoms of hyperandrogenism improved in the EVRA group: the severity of acne decreased by 28% (from 8.2 ± 2.5 to 6.5 ± 2.0; p < 0.01).
Minimal changes were recorded in the control group. The PGQoL scores increased from 55.6 ± 8.2 to 78.9 ± 10.1 in the EVRA group (p < 0.001) and from 56.1 ± 7.9 to 65.3 ± 9.5 in the control group (intergroup p < 0.01). No serious adverse events have been reported. Mild local skin reactions (itching, redness) in 9 (15%) patients of the EVRA group did not require discontinuation of therapy. Common systemic adverse events (headache in 3 (5%) patients and nausea in 1 (1.7%) patient) also did not result in discontinuation of therapy. In the control group, general adverse events were observed in 5 (8.3%) cases, while there were no local reactions.
Conclusions. The EVRA transdermal system is superior to cyclic vitamin therapy in the treatment of OD in adolescent girls, significantly improving cycle regularity, hormonal balance, symptoms of hyperandrogenism, and quality of life with a favorable safety profile and high satisfaction. The ease of use (weekly) makes the EVRA transdermal patch an effective alternative to cyclic vitamin therapy in pediatric gynecology.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.