количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Проблема комплаентности при проведении антибактериальной терапии у больных бактериальным риносинуситом
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Пульмонология и оториноларингология" №2
- Аннотация
- Статья
- Ссылки
В статье приведены результаты сравнительной оценки эффективности левофлоксацина (Таваник) и амоксициллина/клавуланата у больных, страдающих острым риносинуситом или имеющих клинические проявления обострения хронического риносинусита. Одним из важных условий достижения итоговой достоверно лучшей эффективности лечения является комплаенс, который был выше в группе пациентов, принимающих левофлоксацин.
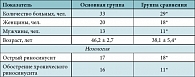
Таблица 1. Клиническая характеристика исследуемых групп
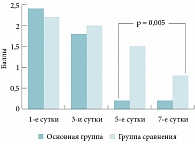
Рис. 1. Сравнительная динамика выраженности заложенности носа на фоне лечения у пациентов основной группы и группы сравнения
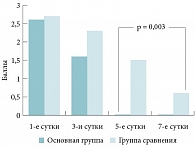
Рис. 2. Сравнительная динамика выраженности выделений из носа на фоне лечения у пациентов основной группы и группы сравнения
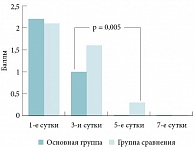
Рис. 3. Сравнительная динамика выраженности головной боли на фоне лечения у пациентов основной группы и группы сравнения
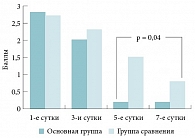
Рис. 4. Сравнительная динамика выраженности отека слизистой оболочки носа на фоне лечения у пациентов основной группы и группы сравнения
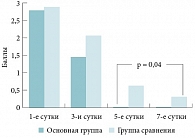
Рис. 5. Сравнительная динамика выраженности гнойного отделяемого в средних носовых ходах и/или полости носа на фоне лечения у пациентов основной группы и группы сравнения
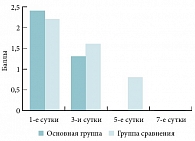
Рис. 6. Сравнительная динамика выраженности гиперемии слизистой оболочки носа на фоне лечения у пациентов основной группы и группы сравнения
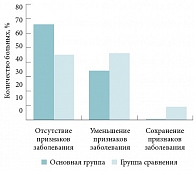
Рис. 7. Сравнительная динамика рентгенологических признаков риносинусита на фоне лечения у пациентов основной группы и группы сравнения
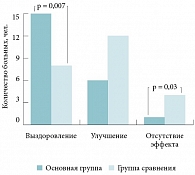
Рис. 8. Сравнительная частота исходов лечения пациентов, страдающих риносинуситом, в основной группе и группе сравнения
Весьма широко используется и термин «приверженность к терапии» (англ. adherence to therapy), который означает «соблюдение указаний врача». Несмотря на незначительные различия, термин близок по своему содержанию к термину «комплаентность» и в клинической практике часто его заменяет [3]. Приверженность к терапии – это характеристика поведения пациента, связанная с лечением (например, прием препарата, соблюдение диеты, изменение образа жизни, посещение клиники) и ее соответствие рекомендациям врача [4]. Лучшая приверженность к терапии достигается при сокращении как кратности приема препарата, так и длительности лечения пациента. По данным J. Peshere и соавт., пациенты нарушали режим при необходимости однократного в течение суток приема лекарственного препарата лишь в 14,9% случаев, при 3-кратном и более частом приеме в течение суток – в 27% случаев [23]. Аналогичные результаты приводит P. Kardas, обследовавший амбулаторных пациентов с обострением хронического бронхита [5, 6]. При одно- или двукратном суточном применении препарата рекомендованную длительность приема антибактериального средства соблюдали 80,3% против 68,6% больных, а междозовый интервал – 74,4% против 56,4% пациентов. Подобная тенденция подтверждена в метаанализе 76 исследований (комплаентность – 79% против 69%) [7].
Что же считать достаточной комплаентностью и как ее оценить? Степень комплаентности значительно варьирует и зависит от отношения пациента к рекомендации врача. Одни из них строго выполняют все рекомендации врача, другие никогда им не следуют [1]. Как правило, врачу сложно четко определиться со степенью комплаентности у пациента. Несмотря на довольно противоречивые мнения, большинство исследователей сходятся в том, что комплаентным считается пациент, который действительно регулярно принимает препарат в дозе, составляющей 80–120% от назначенной врачом [8].
Существует множество методов оценки комплаентности, от непосредственного измерения концентрации препарата в крови до подсчета использованных или оставшихся таблеток, специальных приспособлений, которые позволяют считать принятые таблетки, анкетирования пациентов. Однако необходимость использования перечисленных методов при коротких курсах антибактериальной терапии, проводимых в оториноларингологической практике, сомнительна. В этой связи при выборе антибактериального препарата разумным представляется, помимо основных требований, каковыми являются необходимый спектр антибактериальной активности и безопасность средства, особое внимание уделять факторам, способствующим улучшению комплаентности (режим и способ приема препарата). В конце 1990-х гг. в клинике появились препараты группы новых фторхинолонов, принципиально отличающихся по антимикробным свойствам от ранних фторхинолонов. Новые фторхинолоны имеют, прежде всего, значительно более высокую природную активность против грамположительных бактерий (пневмококков, стафилококков, энтерококков) и атипичных микроорганизмов (хламидий, микоплазм) [9].
Благодаря высокой активности новых фторхинолонов в отношении грамположительных микробов, включая S. pneumoniae, резистентных к другим антибиотикам, их в основном использовали для лечения внебольничных инфекций дыхательных путей, в связи с этим теперь их называют «респираторными фторхинолонами». Нужно иметь в виду, что наряду с повышенной активностью против грамположительных бактерий все новые фторхинолоны сохраняют, а в ряде случаев превосходят, высокую активность ранних фторхинолонов против грамотрицательных бактерий. В связи с этим в последние годы появляется все больше обоснований для применения этих препаратов при лечении не только респираторных инфекций, но также инфекций кожи и мягких тканей, урогенитальных инфекций. Именно поэтому термин «респираторные фторхинолоны» в настоящее время не совсем точно отражает клинический спектр активности этих препаратов, но обозначает их наиболее важную роль в практической медицине [9].
Первым из респираторных фторхинолонов был синтезирован левофлоксацин (Таваник), который и в настоящее время демонстрирует наиболее широкий спектр действия, в том числе против актуальных на сегодня возбудителей бактериального риносинусита: клинически значимых грамположительных, грамотрицательных и атипичных микроорганизмов [10, 11]. В отношении S. pneumoniae, грамотрицательных Enterobacter cloacae и Proteus mirabilis, а также Chlamydophila pneumoniae, Legionella pneumophila и Mycoplasma pneumoniae МПК90 не превышает 2 мкг/мл. Препарат активен против S. pyogenes (МПК 99,9% штаммов = 1 мкг/мл) [12], бета-гемолитических стрептококков (МПК 99% штаммов = 0,5–1 мкг/мл) [13]. Среди клинических штаммов H. influenzae (за исключением казуистичных случаев [14, 15]), M. catarrhalis (МПК90 ≤ 0,06 мкг/мл) устойчивость практически не встречается [15, 16, 17, 18]. Активность против Staphylococcus aureus (МПК90 ≤ 4 мкг/мл) находится в пределах верхней границы чувствительности или даже в зоне умеренной устойчивости; в разных странах доля чувствительных штаммов составляет 88–96%, в России – 91% [4]. Помимо перечисленных свойств левофлоксацин, так же как и другие фторхинолоны, способен оказывать бактерицидное действие на неактивные формы бактерий, формирующих биопленки. Подобный эффект продемонстрирован, в частности, в отношении P. aeruginosa [19], Stenotrophomonas maltophilia [20] и H. influenzae [21] – возбудителей тяжелых инфекций дыхательных путей.
При выборе антибактериального препарата для пациентов с бактериальным риносинуситом должны быть учтены следующие характеристики: активность воспаления, степень тяжести болезни, этиологическая значимость бактериальных возбудителей инфекции и их чувствительность к антибиотикам, побочные эффекты препарата, возраст пациента и его аллергологический анамнез. В качестве антибиотиков первого выбора при остром или обострении хронического риносинусита рекомендуется применение аминопенициллинов [22, 23]. Препаратом выбора в данном случае является амоксициллин. Альтернативными стартовыми антибиотиками являются пероральные цефалоспорины 2–3-го поколений. При отсутствии эффекта в течение первых 2–3 суток или у пациентов, которые в течение последних 3 месяцев получали антибиотикотерапию цефалоспоринами, выбор антибиотика проводится между защищенными аминопенициллинами, макролидами и респираторными фторхинолонами [3, 24, 25]. Учитывая вышеизложенное, нами проведено исследование, целью которого явилась оптимизация антибиотикотерапии у больных, страдающих бактериальным риносинуситом.
Материалы и методы исследования
Под наблюдением находилось 62 пациента (38 женщин, 24 мужчин) в возрасте от 22 до 69 лет (средний возраст 46,5 ± 7,3 года) с диагнозом «бактериальный риносинусит», как острый, так и обострение хронического, подтвержденный клинико-анамнестическими данными и результатами лабораторно-инструментальных методов исследования (табл. 1). Все пациенты в анамнезе до настоящего исследования уже получали антибиотикотерапию в течение 7–10 дней, которая по тем или иным причинам была прервана или оказалась неэффективной. В исследование не включались пациенты, имеющие в анамнезе аллергические реакции на фторхинолоны, а также нуждающиеся в одновременном назначении других системных антимикробных препаратов, с тяжелым течением заболевания, нуждающиеся в парентеральном введении антимикробных препаратов, госпитализации по любому поводу в предшествующие 14 дней.
Диагноз заболевания верифицирован на основании типичных для риносинусита клинических симптомов и данных рентгенографии. Учитывая анамнестические данные, для продолжения антибиотикотерапии были выбраны аминозащищенные пенициллины. В зависимости от тактики лечения больные были рандомизированы на 2 группы. В основной группе схема лечения предусматривала назначение левофлоксацина (Таваник) в дозировке 500 мг в сутки в течение 5 суток перорально. В группе сравнения назначался амоксициллина клавуланат в дозировке 500/125 мг 3 раза в сутки в течение 7 суток перорально. Помимо антибактериальных препаратов в схему комплексного лечения пациентов обеих групп входили по показаниям: топические деконгестанты, интраназальные глюкокортикостероиды, секретолитики, антигистаминные препараты. Метод пункции верхнечелюстных пазух в настоящем исследовании использовался при наличии экссудата в пазухе, сопровождающегося появлением распирающей болезненности в области ее проекции. Различия по частоте применения данного метода лечения между группами были статистически недостоверными (р > 0,05). Длительность наблюдения пациентов составила 7 дней.
Эффективность проводимой терапии оценивалась на 3, 5 и 7-е сутки и определялась по степени уменьшения выраженности субъективных и объективных симптомов риносинусита при оценке по 3-балльной системе до и после лечения:
- 3 балла: исходная выраженность симптома, сохранение субъективного признака риносинусита в той же степени;
- 2 балла: некоторое уменьшение выраженности симптома;
- 1 балл: существенное уменьшение выраженности симптома;
- 0 баллов: отсутствие патологического симптома.
- отсутствие эффекта: сохранение субъективных и объективных признаков риносинусита после проведения лечения;
- улучшение: существенное уменьшение субъективных и/или объективных признаков риносинусита после лечения;
- выздоровление: полное исчезновение субъективных и объективных симптомов риносинусита после завершения лечения.
Результаты исследования и их обсуждение
Согласно полученным результатам, у пациентов основной группы выраженность субъективных ощущений и объективных симптомов риносинусита, представленная в баллах, достоверно уменьшалась к 3-м суткам проведения лечения. К 5-м суткам у большинства больных воспалительные явления были полностью купированы. У пациентов группы сравнения динамика выраженности субъективных ощущений риносинусита, представленная в баллах, достоверно уменьшалась к 3-м суткам терапии, положительная динамика клинических проявлений прогрессировала к 5-м суткам, а полное купирование воспалительных симптомов у большинства больных произошло лишь к 7-му дню лечения, при этом те или иные симптомы заболевания по-разному изменялись в процессе лечения.
Не получено различий в уменьшении выраженности головной боли на фоне лечения у пациентов основной группы и группы сравнения. А выраженность заложенности носа и выделений из носа в группе сравнения к 7-м суткам была достоверно более значима, чем таковая в основной группе к 5-м суткам (р < 0,05) (рис. 1, 2, 3). Сходная тенденция отмечена при оценке динамики ряда субъективных симптомов, когда обе схемы лечения в отношении гиперемии слизистой оболочки были сравнимы по эффективности. В то же время средние баллы в отношении отека слизистой оболочки и наличия гнойных выделений в полости носа в контрольной группе к 7-м суткам были достоверно выше, чем таковые в основной группе к 5-м суткам (р < 0,05) (рис. 4, 5, 6).
Наличие значительного количества пациентов с «уменьшением» признаков заболевания как в основной группе, так и в группе сравнения было обусловлено включением в исследование пациентов с обострением хронического синусита, у которых в периоде ремиссии сохраняются те или иные рентгенологические критерии синусита (рис. 7). Тем не менее в основной группе при контрольном рентгенологическом исследовании ни у одного из пациентов не отмечалось сохранение признаков заболевания, в то время как в группе сравнения такие пациенты составили 9%. Полученные результаты не противоречили ожидаемому эффекту от назначения выбранных групп антибактериальных средств для лечения исследуемых больных. Однако имели место случаи неэффективности лечения. При этом обращала на себя внимание хорошая переносимость левофлоксацина (Таваник). У пациентов основной группы побочные эффекты практически отсутствовали. Лишь у 1 больного кратковременно отмечалась сыпь, которая после применения антигистаминного препарата лоратадина полностью исчезла на 2-е сутки. В то же время в контрольной группе почти у каждого 3-го больного (34,4%) отмечались случаи досрочного прекращения лечения (средний срок – 5,1 ± 0,3 сутки) не столько в связи с появлением побочных эффектов применения защищенных аминопенициллинов (макуло-папулезная сыпь, диспепсические расстройства), сколько из-за неудобного, по мнению пациентов, 3-кратного режима приема препарата. В основной группе случаев нарушения режима антибактериальной терапии зарегистрировано не было.
В результате проведенного исследования определена итоговая эффективность лечения. Среди пациентов, вошедших в основную группу, случаев выздоровления зарегистрировано достоверно больше, чем в группе сравнения. В основной группе не было выявлено ни одного случая отсутствия эффекта от проводимой терапии, чего нельзя сказать о группе сравнения. Мы считаем, что такие результаты связаны не столько с различием в противомикробной активности препаратов, сколько с нарушением комплаентности лечения (рис. 8). Это предположение косвенно подтверждается данными об отсутствии статистически достоверных различий между выраженностью симптомов заболевания на 3-и сутки лечения в обеих группах. В то же время по достижении среднего срока нарушения комплаентности лечения (~5-е сутки) указанные различия в основной группе и группе сравнения приобретали статистически значимый характер.
Выводы
К основным преимуществам левофлоксацина (Таваник) следует отнести оптимальный спектр действия в отношении актуальных возбудителей риносинусита, высокую безопасность и удобный режим дозирования. Результаты проведенного исследования подтверждают высокую эффективность и безопасность левофлоксацина (Таваник) при лечении больных с острым и обострением хронического риносинусита, что достигается большей комплаентностью за счет удобного режима приема препарата и меньшего количества побочных эффектов со стороны желудочно-кишечного тракта.
1. Leppik I.E. Compliance during treatment of epilepsy // Epilepsia. 1988. Vol. 29. Suppl. 2. P. 79–84.
2. Pechere J.C., Hughes D., Kardas P., Cornaglia G. Non-compliance with antibiotic therapy for acute community infections: a global survey // Int. J. Antimicrob. Agents. 2007. Vol. 29. № 3. P. 245–253.
3. Чучалин А.Г., Синопальников А.И., Козлов Р.С. и др. Внебольничная пневмония у взрослых. Практические рекомендации по диагностике, лечению и профилактике. М., 2010. 82 с.
4. Дехнич А.В., Эйдельштейн И.А., Нарезкина А.Д. Эпидемиология антибиотикорезистентности нозокомиальных штаммов Staphylococcus aureus в России: результаты многоцентрового исследования // Клиническая микробиология и антимикробная химиотерапия. 2002. № 4. С. 325–336.
5. Kardas P. Comparison of patient compliance with once-daily and twice-daily antibiotic regimens in respiratory tract infections: results of a randomized trial // J. Antimicrob. Chemother. 2007. Vol. 59. № 3. P. 531–536.
6. Kardas P. Patient compliance with antibiotic treatment for respiratory tract infections // J. Antimicrob. Chemother. 2002. Vol. 49. № 6. P. 897–903.
7. Claxton A.J., Cramer J., Pierce C. A systematic review of the associations between dose regimens and medication compliance // Clin. Ther. 2001. Vol. 23. № 8. Р. 1296–1310.
8. Paschal A.M., Hawley S.R., Romain T.S., Ablah E. Measures of adherence to epilepsy treatment: review of present practices and recommendations for future directions // Epilepsia. 2008. Vol. 49. № 7. P. 1115–1122.
9. Гучев И.А., Мелехина Е.В. Левофлоксацин (Таваник). Возможности и перспективы применения при внебольничных инфекциях нижних дыхательных путей // Русский медицинский журнал. 2009. Т. 11. № 19. С. 1277–1282.
10. Alou L., Aguilar L., Sevillano D. et al. Levofloxacin vs. azithromycin pharmacodynamic activity against S. pneumoniae and H. influenzae with decreased susceptibility to amoxicillin/clavulanic acid // J. Chemother. 2007. Vol. 19. № 6. P. 670–672.
11. Seral C., Suarez L., Rubio-Calvo C. et al. In vitro activity of cefditoren and other antimicrobial agents against 288 Streptococcus pneumoniae and 220 Haemophilus influenzae clinical strains isolated in Zaragoza, Spain // Diagn. Microbiol. Infect. Dis. 2008. Vol. 62. № 2. P. 210–215.
12. Jones R.N., Fritsche T.R., Sader H.S., Stilwell M.G. Activity of garenoxacin, an investigational des-F(6)-quinolone, tested against pathogens from community-acquired respiratory tract infections, including those with elevated or resistant-level fluoroquinolone MIC values // Diagn. Microbiol. Infect. Dis. 2007. Vol. 58. № 1. P. 9–17.
13. Biedenbach D.J., Toleman M.A., Walsh T.R., Jones R.N. Characterization of fluoroquinolone-resistant beta-hemolytic Streptococcus spp. isolated in North America and Europe including the first report of fluoroquinolone–resistant Streptococcus dysgalactiae subspecies equisimilis: report from the SENTRY Antimicrobial Surveillance Program (1997–2004) // Diagn. Microbiol. Infect. Dis. 2006. Vol. 55. № 2. P. 119–127.
14. Bastida T., Perez-Vazquez M., Campos J. et al. Levofloxacin treatment failure in Haemophilus influenzae pneumonia // Emerg. Infect. Dis. 2003. Vol. 9. № 11. P. 1475–1478.
15. Perez-Vazquez M., Roman F., Aracil B. Laboratory detection of Haemophilus influenzae with decreased susceptibility to nalidixic acid, ciprofloxacin, levofloxacin, and moxifloxacin due to GyrA and ParC mutations // J. Clin. Microbiol. 2004. Vol. 42. № 3. P. 1185–1191.
16. Gracia M., Diaz C., Coronel P. et al. Antimicrobial susceptibility of Streptococcus pyogenes in Central, Eastern, and Baltic European Countries, 2005 to 2006: the cefditoren surveillance program // Diagn. Microbiol. Infect. Dis. 2009. Vol. 64. № 1. Р. 52–56.
17. Jones R.N., Sader H.S., Fritsche T.R., Pottumarthy S. Comparisons of parenteral broad-spectrum cephalosporins tested against bacterial isolates from pediatric patients: report from the SENTRY Antimicrobial Surveillance Program (1998–2004) // Diagn. Microbiol. Infect. Dis. 2007. Vol. 57. № 1. Р. 109–116.
18. Sahm D.F., Brown N.P., Thornsberry C., Jones M.E. Antimicrobial susceptibility profiles among common respiratory tract pathogens: a GLOBAL perspective // Postgrad. Med. 2008. Vol. 120. № 3. Suppl. 1. Р. 16–24.
19. Ishida H., Ishida Y., Kurosaka Y. et al. In vitro and in vivo activities of levofloxacin against biofilm-producing Pseudomonas aeruginosa // Antimicrob. Agents Chemother. 1998. Vol. 42. № 7. P. 1641–1645.
20. Passerini de Rossi B., Garcia C., Calenda M. et al. Activity of levofloxacin and ciprofloxacin on biofilms and planktonic cells of Stenotrophomonas maltophilia isolates from patients with device-associated infections // Int. J. Antimicrob. Agents. 2009. Vol. 34. № 3. P. 260–264.
21. Kaji C., Watanabe K., Apicella M.A., Watanabe H. Antimicrobial effect of fluoroquinolones for the eradication of nontypeable Haemophilus influenzae isolates within biofilms // Tohoku J. Exp. Med. 2008. Vol. 214. № 2. P. 121–128.
22. Страчунский Л.С., Белоусов Ю.Б., Козлов С.Н. Антибактериальная терапия. М.: Фарммединфо, 2000. 191 с.
23. Страчунский Л.С., Каманин Е.И., Тарасов А.А. Влияние антибиотикорезистентности на выбор антимикробных препаратов в оториноларингологии // Consilium medicum. 2002. Т. 3. № 8. С. 352–357.
24. Яковлев С.В., Яковлев В.П. Современная антимикробная терапия в таблицах // Сonsilium mediсum. 2001. № 1. С. 12–14.
25. Alvarez F., Bouza E., Garcia-Rodriguez J.A. et al. Second consensus report on the use of antimicrobial agents in exacerbations of chronic obstructive pulmonary disease // Arch. Bronconeumol. 2003. Vol. 39. № 6. 274–282.
Новости на тему
29.04.2022 13:00:00
24.03.2022 16:00:00
05.07.2021
04.03.2021
06.11.2019
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.