Результаты оценки влияния растительного препарата с антиоксидантными свойствами на биохимические показатели крови и мочи при мочекаменной болезни
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. 60 пациентов с мочекаменной болезнью были распределены на две группы по 30 человек. Все пациенты получили общие рекомендации и рекомендации по диетотерапии, а пациентам основной группы помимо этого был назначен комплекс НефраДоз. Курс лечения составил 28–30 дней.
Результаты и их обсуждение. Под действием НефраДоза усилилась почечная экскреция камнеобразующего вещества – мочевой кислоты, оставаясь в диапазоне нормальных значений. Кроме того, обнаружена тенденция к увеличению почечной суточной экскреции натрия, магния и цитратов. Согласно данным общего клинического анализа мочи, у пациентов, принимавших НефраДоз, относительная плотность мочи была ниже, чем у больных, не получавших биодобавку. В основной группе также отмечено более высокое значение рН мочи по сравнению с контрольной. Уровень гематурии на фоне использования НефраДоза оказался почти в два раза ниже, чем в группе контроля. Содержание уробилиногена в моче больных основной группы было выше, чем в контрольной, но в пределах нормы.
Выводы. Применение комплекса НефраДоз при мочекаменной болезни может быть рекомендовано пациентам в качестве противорецидивного средства.
Материал и методы. 60 пациентов с мочекаменной болезнью были распределены на две группы по 30 человек. Все пациенты получили общие рекомендации и рекомендации по диетотерапии, а пациентам основной группы помимо этого был назначен комплекс НефраДоз. Курс лечения составил 28–30 дней.
Результаты и их обсуждение. Под действием НефраДоза усилилась почечная экскреция камнеобразующего вещества – мочевой кислоты, оставаясь в диапазоне нормальных значений. Кроме того, обнаружена тенденция к увеличению почечной суточной экскреции натрия, магния и цитратов. Согласно данным общего клинического анализа мочи, у пациентов, принимавших НефраДоз, относительная плотность мочи была ниже, чем у больных, не получавших биодобавку. В основной группе также отмечено более высокое значение рН мочи по сравнению с контрольной. Уровень гематурии на фоне использования НефраДоза оказался почти в два раза ниже, чем в группе контроля. Содержание уробилиногена в моче больных основной группы было выше, чем в контрольной, но в пределах нормы.
Выводы. Применение комплекса НефраДоз при мочекаменной болезни может быть рекомендовано пациентам в качестве противорецидивного средства.
Введение
Несмотря на очевидный прогресс в изучении мочекаменной болезни (МКБ), заболеваемость уролитиазом неуклонно растет как в мире в целом, так и в Российской Федерации в частности [1, 2]. В 2005 г. в России среди взрослого населения было зарегистрировано 646 532 случая МКБ, или 5,3% от всех болезней мочеполовой системы, а в 2016 г. – 866 742 случаев, или 5,7% соответственно. С 2005 по 2016 г. заболеваемость МКБ увеличилась на 34,1%, и ее рост был достаточно равномерным [1]. По данным литературы, рецидив камнеобразования происходит в 50% случаев в течение пяти лет [2]. В этой связи предупреждение рецидивов МКБ – одно из важных направлений снижения общей заболеваемости уролитиазом.
Причины уролитиаза до конца не изучены. Тем не менее известно, что к камнеобразованию могут приводить сопутствующие заболевания: первичный гиперпаратиреоз, почечный канальцевый ацидоз, подагра, метаболический синдром и др. [3–7], мутации определенных генов [8], регулярный прием кальцийсодержащих препаратов, витамина D [9, 10], инфекция мочевых путей [11]. Вместе с тем продолжаются исследования влияния макромолекул мочи на процессы литогенеза [12–16], анализируются физико-химические свойства мочи у пациентов с уролитиазом [17], изучается метаболизм камнеобразующих веществ в организме человека [18–21], проводится поиск генов, полиморфизмы которых являются факторами риска МКБ [22, 23]. Одновременно совершенствуется оборудование для хирургического лечения, появляются новые подходы к оперативному удалению конкрементов из верхних мочевых путей.
Отдельного внимания заслуживает метафилактика уролитиаза (комплекс мер, направленных на снижение риска повторного возникновения камней в мочевыводящей системе). Одна из главных составляющих метафилактики – индивидуальная специфическая диетотерапия [24–26].
При составлении рекомендаций необходимо оценить химический состав конкремента, концентрацию камнеобразующих веществ в крови и суточной моче, стереотип питания пациента. Если диетотерапия неэффективна, назначают медикаментозное лечение в зависимости от выявленных метаболических литогенных нарушений [24, 27]. При МКБ используются тиазидные диуретики, цитратные смеси, аллопуринол, метионин, магнийсодержащие препараты. В то же время многие исследователи обращают внимание на фитопрепараты и биологически активные добавки (БАД) растительного происхождения, которые давно и с успехом применяются в клинической практике [28] и эффективность которых доказана и проверена многими специалистами [28–30]. Одним из таких растительных средств является биодобавка к пище НефраДоз. В состав комплекса входят экстракты корней марены красильной, листьев ортосифона тычиночного, травы эпимедиума, корней родиолы розовой, корней солодки голой, листьев гинкго билоба, а также соединение органической природы, получаемое из растений, – ресвератрол.
Цель исследования
Изучить влияние БАД НефраДоз на метаболические показатели пациентов, страдающих МКБ, и определить возможности его использования в таких случаях.
Материал и методы
В исследовании приняли участие 60 больных МКБ – 35 мужчин и 25 женщин, средний возраст пациентов – 47,8 года. Основную группу составили 30 (50%) пациентов – 19 мужчин и 11 женщин, средний возраст – 43,2 года. В контрольную группу вошли 30 (50%) пациентов – 16 мужчин и 14 женщин, средний возраст – 49,1 года. Все пациенты получили общие рекомендации, им была назначена диетотерапия. В основной группе больные также принимали БАД НефраДоз. Курс лечения – 28–30 дней.
Проводился сбор анамнестических данных, оценивался стереотип питания с помощью компьютерной версии анализатора стереотипа питания, выполнялся биохимический анализ крови и суточной мочи на предмет функционального состояния почек, состояния обмена веществ, в том числе камнеобразующих.
Биохимические исследования осуществляли на автоматическом анализаторе ADVIA-1200 (Bayer Diagnostics). Кроме того, с помощью портативного анализатора мочи ЭТТА АМП-01 выполняли общий клинический анализ мочи, в частности определяли плотность и кислотно-щелочное состояние (рН) мочи, наличие или отсутствие воспалительного процесса в мочевыводящей системе.
НефраДоз принимали по одной капсуле (150 мг) два раза в день во время еды. Влияние комплекса на состояние пациентов с МКБ и одним или несколькими нарушениями обмена камнеобразующих веществ оценивали по объему выделенной мочи (диурезу), семи биохимическим показателям крови и мочи, отражающим функциональное состояние почек, обмена камнеобразующих веществ и ингибиторов камнеобразования, а также по десяти показателям общего клинического анализа мочи.
Статистическую достоверность полученных данных оценивали с помощью методов статистического анализа: критерия Манна – Уитни и t-критерия Стьюдента посредством компьютерной программы Statistica 10.0 (StatSoft USA).
Результаты и их обсуждение
На момент включения в исследование, по данным биохимического анализа крови, функциональное состояние почек в пределах нормы было у 26 (86,7%) пациентов. У четырех (13,3%) больных была повышена сывороточная концентрация креатинина.
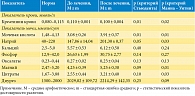
На фоне приема БАД диурез не изменялся, функциональное состояние почек у пациентов с нормальными показателями их очистительной функции также оставалось на прежнем уровне в пределах нормы. У четырех пациентов со сниженным клиренсом эндогенного креатинина отмечалась тенденция к улучшению функционального состояния почек: средняя сывороточная концентрация креатинина снизилась с 0,153 до 0,140 ммоль/л. Анализ данных, отражающих состояние обмена камнеобразующих веществ, показал, что под действием НефраДоза усилилась почечная экскреция мочевой кислоты. Однако уровень мочевой кислоты оставался в диапазоне нормальных значений. Обнаружена тенденция к увеличению почечной суточной экскреции натрия, магния и цитратов. Повышение натрия – вещества, влияющего на камнеобразование, также было в пределах нормы. Не исключено, что при увеличении выборки исследования повышение содержания в моче таких важных ингибиторов камнеобразования, как магний и цитрат, было бы подтверждено обоими статистическими критериями. Влияния НефраДоза на почечную суточную экскрецию камнеобразующих веществ: общего кальция, оксалатов и неорганических фосфатов – не отмечено.
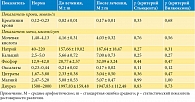
Проведен сравнительный анализ результатов в основной и контрольной группах (табл. 1 и 2). Оказалось, что статус пациентов с МКБ, получивших рекомендации общие и по диетотерапии, не изменился, в отличие от больных, дополнительно принимавших НефраДоз. Отсутствие эффекта от диетотерапии по результатам биохимических анализов можно объяснить тем, что уже имеющийся рацион питания у пациентов во многом совпадал с рекомендуемым.
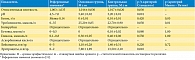
Результаты обследования больных уролитиазом на предмет возможного влияния НефраДоза на показатели общего клинического анализа мочи при его ежедневном мониторинге представлены в табл. 3 [31]. При сопоставлении данных общего клинического анализа мочи больных основной и контрольной групп оказалось, что у пациентов, принимавших НефраДоз, относительная плотность мочи была ниже, чем у больных, не получавших биодобавку, что обусловлено положительным влиянием БАД. Кроме того, в основной группе по сравнению с контрольной наблюдалось более высокое значение рН мочи, что является важным положительным фактором для больных уролитиазом. Уровень гематурии на фоне применения НефраДоза был почти в два раза ниже, чем у пациентов, не принимавших биодобавку. Содержание уробилиногена в моче больных основной группы было выше, чем в контрольной, но находилось в пределах нормы. Влияния БАД на другие показатели общего клинического анализа мочи (содержание белка, билирубина, кетонов, глюкозы, аскорбиновой кислоты и уровень лейкоцитов) не выявлено. Указанные показатели оставались в пределах нормы без изменений у пациентов и основной, и контрольной групп. Полученные результаты свидетельствуют о том, что НефраДоз не оказывает токсического действия на печень, почки и углеводный обмен. На фоне использования НефраДоза ремиссия воспалительного процесса в мочевой системе больных уролитиазом сохранялась. Побочных действий при приеме НефраДоза не отмечено.
Выводы
Результаты проведенного исследования показали, что применение БАД НефраДоз может улучшать очистительную функцию почек при ее снижении у пациентов с МКБ, что выражается в тенденции к уменьшению сывороточной концентрации креатинина. Соответственно НефраДоз можно рекомендовать пациентам с МКБ и сочетанной хронической болезнью почек.
Необходимо отметить, что на фоне приема НефраДоза увеличилась экскреция мочевой кислоты, оставаясь в пределах нормальных значений. Достаточно важным фактором влияния НефраДоза на метаболизм пациентов с уролитиазом нужно считать обнаруженную тенденцию к повышению почечной экскреции основных низкомолекулярных ингибиторов камнеобразования – магния и цитратов.
При использовании БАД НефраДоз существенно уменьшилась степень гематурии, а удельный вес и pH снизились незначительно, несмотря на статистическую достоверность. При уратном уролитиазе, а также выявленной гиперурикемии и/или гиперурикурии НефраДоз должен назначаться под контролем уровня мочевой кислоты в крови и моче.
Обнаруженные эффекты комплекса НефраДоз свидетельствуют о возможности его использования при МКБ для коррекции гипоцитратурии, гипомагниурии, гематурии, в том числе после установки дренажей в верхние мочевые пути. Кроме того, повышение почечной экскреции основных ингибиторов камнеобразования – цитрата и магния на фоне приема БАД Нефрадоз позволяет применять его для профилактики рецидива камнеобразования при любом типе уролитиаза.
M.Yu. Prosiannikov, PhD, O.V. Konstantinova, MD, PhD, S.A. Golovanov, MD, PhD, N.V. Anokhin, D.A. Voytko, PhD
N.A. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation, Moscow
Contact person: Mikhail Yu. Prosiannikov, prosyannikov@gmail.com
Purpose: to study the influence of biologically active additives NefraDoz on the metabolic parameters of patients suffering from urolithiasis, and to determine its application in patients with urolithiasis.
Material and methods. 60 patients with urolithiasis were divided into two groups of 30 patients. All patients received general recommendations and recommendations for diet therapy, and the patients of the main group, in addition, was assigned to the complex NefraDoz. The course of treatment was 28–30 days.
Results and discussion. Under the action of NefraDoz renal excretion stone-forming substances uric acid increased, within the range of normal values. In addition, there was a tendency to increase renal daily excretion of sodium, magnesium and citrates. According to the data of the general clinical analysis of urine, in patients taking NefraDoz, the relative density of urine was lower than in patients who did not receive supplements. In the main group it was also noted the higher pH of urine compared to the control. The level of hematuria on the background of NefraDoz use was almost two times lower than in patients of control group. The content of urobilinogen in the urine of the main group patients was higher than in the control group, but within normal limits.
Summary. The use of NefraDoz complex for kidney stones can be recommended to patients as a relapse prevention medicine.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.