Опыт применения растительного комплекса Уриклар в метафилактике нефролитиаза
- Аннотация
- Статья
- Ссылки
- English
Методом капиллярного электрофореза установлено, что прием растительного комплекса уже в первый месяц лечения способствовал снижению содержания фосфата в плазме крови на фоне повышения уровня сульфата, а также камнеобразующих ионов в моче, что позволило снизить риск развития рецидива заболевания.
Методом капиллярного электрофореза установлено, что прием растительного комплекса уже в первый месяц лечения способствовал снижению содержания фосфата в плазме крови на фоне повышения уровня сульфата, а также камнеобразующих ионов в моче, что позволило снизить риск развития рецидива заболевания.
Введение
Мочекаменной болезнью, по данным авторов из различных стран, страдает от 4 до 20% мирового населения и чаще всего лица трудоспособного возраста [1, 2]. Количество пациентов с мочекаменной болезнью в Российской Федерации за последние десять лет увеличилось более чем в 1,5 раза. Рецидивное образование конкрементов в органах мочевыделительной системы обусловлено наследственной предрасположенностью, образом жизни, пищевыми привычками [3], а также может быть спровоцировано сопутствующей патологией [4].
Современные методы лечения уролитиаза, как правило, позволяют избавить пациента от конкремента. Однако значительное количество резидуальных камней/фрагментов после дистанционной литотрипсии, хронический воспалительный процесс, метаболические изменения в организме требуют соответствующей коррекции во избежание повторного камнеобразования [1, 4, 5]. По данным различных отечественных и зарубежных литературных источников, в отсутствие метафилактических (противорецидивных) мероприятий рецидивы мочекаменной болезни возникают в 50–70% случаев. В связи с этим важно выявить тип метаболических нарушений и определить компонентный состав мочевых камней. Комплексное обследование пациентов, включающее методы лучевой и лабораторной диагностики, позволяет не только выбрать оптимальную тактику лечения, но и разработать индивидуальную программу профилактики рецидивного камнеобразования.
Моча содержит органические вещества и ионы, частично малорастворимые, а также буферный компонент. Согласно одной из основных теорий камнеобразования, ведущим механизмом считается пересыщение ионами, экскретируемыми с мочой, с последующим образованием ядра камня и его ростом. Определение компонентного состава камня и биохимических данных крови и мочи позволяет выявить тип камнеобразования и затем оценить значимость факторов формирования камней у каждого конкретного пациента. Однако анализ результатов комплексного исследования мочи недостаточно информативен из-за сложности учета многочисленных данных. По нашему мнению, перспективным методом является капиллярный электрофорез – метод многокомпонентного разделения неорганических и органических ионогенных соединений, который успешно используется при анализе различных объектов [6, 7].
Для определения состава мочевых конкрементов применяют инфракрасную спектроскопию [8], рентгенофлуоресцентный и рентгенофазовый анализы [9], поляризационную и сканирующую электронную микроскопии [10] и др. По рекомендациям европейских и российских ассоциаций урологов, предпочтительнее использовать инфракрасную спектрофотометрию и рентгеновскую дифрактометрию. Однако рентгенофазовый анализ не позволяет выявить аморфные фазы, а инфракрасная спектроскопия – кристаллические фазы. Все эти методики применимы только к извлеченному конкременту. В последнее время активно разрабатывается и внедряется в урологическую практику двухэнергетическая компьютерная томография [4, 7, 11]. Этот метод обладает важным преимуществом: помимо выявления анатомических особенностей он дает возможность с высокой точностью определять многокомпонентность мочевых камней как in vivo, так и in vitro.
На текущий момент известно более 40 составляющих элементов, участвующих в формировании мочевых камней. Они систематизированы, классифицированы и подразделены на четыре группы: оксалаты (из солей щавелевой кислоты), фосфаты (из солей ортофосфорной кислоты), ураты (из мочевой кислоты и ее солей) и другие камни (органические и неорганические соединения). По данным отечественных и зарубежных авторов, на территории Российской Федерации наиболее распространены уролиты смешанного типа, в частности оксалатно-уратные и оксалатно-фосфатные, а монокомпонентные конкременты встречаются редко. В настоящее время основную минеральную фазу, обнаруживаемую в уролитах почти 75% пациентов с мочекаменной болезнью, представляет оксалат кальция.
Сегодня в практике отсутствуют методики, позволяющие оценивать активность камнеобразования как при наличии конкремента, так и после его извлечения или самостоятельного отхождения по мочевым путям. Информация о составе конкремента, метаболических нарушениях и активности камнеобразования позволит контролировать этот процесс.
Цель исследования
Провести оценку анионного состава крови и мочи пациентов с мочекаменной болезнью методом капиллярного электрофореза, а также химического состава мочевых камней. Сравнить данные по компонентному составу уролитов, полученные с помощью рентгеновской дифрактометрии и инфракрасной спектрофотометрии. Изучить эффективность применения растительного комплекса Уриклар в метафилактике мочекаменной болезни.
Материал и методы
Известно, что мочекаменная болезнь характеризуется эндемичным распространением. В частности, в Красноярском крае присутствуют факторы, служащие пусковым механизмом развития мочекаменной болезни у населения, проживающего на этой территории. Согласно данным отчета урологической службы Красноярского края, за 2018 г. зарегистрирован 335 451 случай различных заболеваний органов мочевыделительной системы, из них 17 585 случаев – мочекаменной болезнью.
Ввиду недостаточной осведомленности пациентов об особенностях течения мочекаменной болезни и необходимости проведения литокинетической и литолитической терапии было принято решение организовать школы для пациентов с уролитиазом, чтобы в доступной форме объяснить им причины образования мочевых камней, возможности терапии и основные принципы метафилактики. В период с 2017 по 2018 г. были организованы и проведены школы для пациентов с мочекаменной болезнью на базе Краевой клинической больницы и Красноярской межрайонной клинической больницы скорой медицинской помощи им. Н.С. Карповича. Главными задачами были сформировать у пациентов ответственное отношение к своему здоровью, детально их дообследовать, а также своевременно скорректировать противорецидивную и литокинетическую терапию. Слушателями этих мероприятий стали пациенты урологических отделений и пациенты, направленные амбулаторными урологами.
В исследуемой когорте пациентов было 57 (52,4%) мужчин и 63 (47,6%) женщины (соотношение 1,1:1). Возраст пациентов составил от 22 до 80 лет (в среднем 49,7 ± 3,5 года, медиана – 50 лет, интерквартильный размах – от 45 до 56 лет). Большая часть (60,1%) пациентов были трудоспособного возраста (от 18 до 60 лет), что свидетельствует о социально-экономической значимости проблемы. Рецидивное течение уролитиаза отмечалось у всех пациентов. Коралловидный нефролитиаз выявлен у восьми человек. Размер уролитов варьировался от 10 до 42 мм. В 55 (46%) случаях камни локализовались справа, в 54 (45%) – слева. Двусторонний нефролитиаз имел место у 11 (9%) пациентов. Среди сопутствующих урологических заболеваний преобладали воспалительные процессы – 23 (19,4%) случая, среди соматических заболеваний – гастрит, хронический холецистит и желчнокаменная болезнь – 8 (6,9%) случаев.
С целью изучения влияния комплекса медико-социальных факторов на частоту рецидивов мочекаменной болезни было проведено анкетирование (30 вопросов):
по социально-гигиеническим факторам (возраст, пол, профессия, характер питания, физическая нагрузка, вредные привычки, питьевой режим и т.д.);
медико-биологическим факторам (характер предыдущего лечения, сроки госпитализаций, сопутствующие урологические заболевания, наследственность и т.д.);
клиническим факторам (анамнез, результаты анализов крови и мочи, данные ультразвуковых и рентгеновских исследований, методы лечения, осложнения и т.д.).
У 95% больных были выявлены факторы риска: недостаточное потребление жидкости, употребление воды из централизованного водоснабжения, несбалансированное питание с преобладанием продуктов животного происхождения, низкая физическая активность, систематическое употребление лекарств и биологически активных добавок, содержащих минеральные вещества. Среди медико-биологических факторов преобладали хронический пиелонефрит, частые обострения хронического пиелонефрита, отягощенная наследственность. У 57% пациентов индекс массы тела был выше нормы, что увеличивает риск формирования мочевых камней. Установлено, что у женщин с кальциевым типом камнеобразования частота гиперкальциурии линейно связана с избыточной массой тела и ожирением [12]. Независимо от пола ожирение ведет к гиперэкскреции мочевой кислоты и неорганических фосфатов [13].
Анкетирование 45 пациентов показало, что большая часть респондентов ведет малоподвижный образ жизни, а питание характеризует как однообразное и несбалансированное. Почти треть опрошенных употребляли менее 1,5 л воды в сутки, а 2 (4,4%) человека – и вовсе не более 500 мл. Лишь 7 (15,6%) больных указали на употребление более 2 л жидкости в сутки. Большинство респондентов, даже зная основные рекомендации по питанию, их не придерживались. На преобладание пищи животного происхождения в рационе указали 3 (6,7%) больных. Анализ анкетирования показал важность разъяснения пациентам роли адекватного водного баланса, диетотерапии, лекарственных веществ в комплексе лечебных мероприятий, направленных на коррекцию нарушений обмена камнеобразующих веществ в организме.
На догоспитальном этапе 89 больным было проведено определение компонентного состава мочевых камней с помощью двухэнергетической компьютерной томографии на 64-срезовом компьютерном томографе Discovery 750 HD (GE Healthcare). Это технология двухэнергетического сканирования, реализованная с помощью рентгеновской трубки, способной сверхбыстро переключать напряжение между 80 и 140 кВ, и детектора Gemstone, обеспечивающего сверхбыстрый отклик на импульсы рентгеновского излучения. Исследование проводилось без внутривенного контрастного усиления в положении пациента на спине. В зависимости от конституционных особенностей пациентов лучевая нагрузка колебалась от 4 до 7 мЗв [11, 14].
Всем пациентам выполнена дезинтеграция и извлечение камней почек методом перкутанной нефролитолапаксии. Удаленные камни подвергались дальнейшему исследованию методами инфракрасной спектроскопии с преобразованием Фурье и капиллярного электрофореза. С помощью капиллярного электрофореза определялись наличие и уровень оксалат-, фосфат-, сульфат-ионов в плазме крови и моче.
В период госпитализации всем пациентам проведено комплексное лабораторное и рентгенологическое обследование. Лабораторные методы обследования включали клинические анализы крови и мочи, бактериологическое исследование мочи, определение суточного объема и средних значений относительной плотности мочи и биохимический анализ суточной мочи. Биохимическое исследование суточной мочи проводилось с целью определения концентрации и экскреции камнеобразующих веществ, ингибиторов литогенеза, а также комплексообразователей. Изучалась экскреция оксалата, цитрата, кальция, магния, калия, мочевой кислоты, фосфора, натрия, хлорида аммония, сульфата, а также креатинина. Кроме того, определялись кислотность и суточный диурез. Исследование проводилось при соблюдении стандартных условий для каждой из перечисленных методик.
Пациентам были даны рекомендации по метафилактике:
- увеличение суточного диуреза до 2–2,5 л;
- поддержание относительной плотности мочи ниже 1010 г/л;
- равномерное распределение жидкости в течение дня, целесообразность приема жидкости в ночное время;
- сбалансированное питание с большим количеством балластного составляющего (пищевых волокон), растительных продуктов с целью уменьшения поступления и всасывания камнеобразующих веществ;
- ликвидация гиподинамии;
- устранение стрессовых ситуаций;
- адекватное лечение сопутствующих заболеваний и их осложнений.
Диетотерапия зависела в первую очередь от состава удаленных камней и выявленных нарушений в обмене веществ. В целом рекомендации по питанию заключались в уменьшении общего объема пищи при повышении ее разнообразия, ограничении употребления пищи, богатой камнеобразующими веществами, употреблении больше пищи, богатой веществами, ингибирующими литогенез, и достаточного количества жидкости, позволяющего поддерживать суточный диурез более 2 л.
В комплексное лечение 30 пациентов был включен растительный комплекс Уриклар.
Контрольная группа включала 50 человек, которые не получали метафилактического лечения, у них не определялся состав камня и тип камнеобразования.
Описательная статистика представлена абсолютными значениями, экстенсивными коэффициентами и стандартной ошибкой доли, качественные нормально распределенные учетные признаки – средними величинами и среднеквадратичным отклонением. Значимость различий между группами количественных признаков определялась с помощью критерия Стьюдента, а качественных признаков – критерия хи-квадрат при р < 0,05. Степень связи признаков определялась по критерию корреляции Пирсона.
Результаты
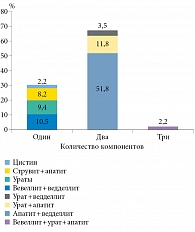
При анализе данных компонентного состава мочевых камней, полученных методом инфракрасной спектрометрии, установлено, что в большинстве случаев (67,1%) конкременты состояли из двух компонентов (рис. 1). Реже (30,5%) встречались однокомпонентные камни. Трехкомпонентные уролиты выявлены только у 2,2% пациентов. Следует отметить, что более чем у половины пациентов (51,8%) наблюдались двухкомпонентные конкременты, состоящие из апатита и ведделлита. Преобладание многокомпонентного состава связано с нарушением сразу нескольких звеньев обмена веществ или присоединением инфекции. При помощи инфракрасной спектроскопии определен минералогический состав удаленных конкрементов. Метаболические нарушения обнаружены у 41 больного: гиперкальциемия или гиперкальциурия – у 24, гиперурикемия и гиперурикурия – у 17.
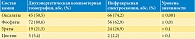
Следующим этапом исследования было сопоставление информации о минералогическом составе мочевых камней, полученной с помощью двухэнергетической компьютерной томографии и инфракрасной спектроскопии (табл. 1). При этом учитывались все элементы, формирующие уролит, и частота их встречаемости. По частоте выявления уратов и цистина между методами двухэнергетической компьютерной томографии и инфракрасной спектроскопии достоверных различий не было (высокий уровень значимости результатов, р > 0,1). Поскольку выборка с цистиновыми уролитами была слишком маленькой, нельзя говорить о надежности результатов. В идентификации уратных конкрементов данные, полученные при помощи двухэнергетической компьютерной томографии, соответствовали данным инфракрасной спектроскопии в 83% случаев (р < 0,05).
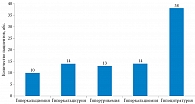
На рисунке 2 представлены варианты нарушений состава суточной мочи больных мочекаменной болезнью.
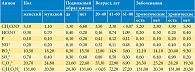
В таблице 2 отражены средние значения содержания анионов камней почек в зависимости от таких характеристик, как пол, возраст, образ жизни, сопутствующие заболевания. У мужчин среднее содержание оксалатов в исследуемых конкрементах было выше, чем у женщин. Кроме того, у пациентов, ведущих малоподвижный образ жизни, показатели оксалатов были немного выше, чем у людей, ведущих активный образ жизни. Эта тенденция прослеживается практически для всех анионов. Наибольшее содержание оксалат-ионов в исследуемых камнях почек наблюдалось в возрастной группе 20–40 лет и наименьшее – в группе 61–80 лет. У пациентов пожилого возраста в исследуемых образцах преобладали ацетат-, фторид- и сульфат-ионы. При хронических сопутствующих заболеваниях показатели оксалатов в исследуемых уролитах были значительно выше. Аналогичную зависимость отмечали и при сочетании мочекаменной болезни с другими урологическими заболеваниями. Присутствие хронических заболеваний значительно повышало содержание сульфатов, нитратов, фосфатов и уратов.
Высокие значения содержания различных анионов в исследуемых образцах камней могут быть связаны с качеством употребляемой питьевой воды, приемом медикаментов, сопутствующими заболеваниями. Например, наличие зубных протезов и использование зубных паст с высоким содержанием фтора могут повлиять на содержание фторидов в организме.
Высокое содержание нитритов в образцах мочи пациентов с мочекаменной болезнью может быть связано с бактериурией, присутствием в моче микроорганизмов, которые в процессе своей жизнедеятельности преобразуют нитраты в нитриты.
По данным корреляционного анализа, в уролитах установлена зависимость между содержанием различных анионов. В частности, обнаружена очень слабая корреляционная зависимость между следующими парами анионов: фторидом и нитритом, фторидом и ацетатом, фторидом и уратом, оксалатом и нитратом, оксалатом и ацетатом. Слабая корреляция наблюдалась между концентрациями оксалатов и фосфатов, сульфатов и уратов (r = -0,22; 0,27; 0,27; -0,42 соответственно).
При анализе образцов плазмы крови определяли такие ионы, как фториды, бромиды, нитриты, нитраты, сульфаты и оксалаты. Были обнаружены фосфаты (80%), ураты (75%), ацетаты (20%) и формиаты (40%). Все исследования проводили в пяти параллельных измерениях, причем относительное стандартное отклонение определения анионов всех образцов мочи и плазмы крови не превышало 6%.
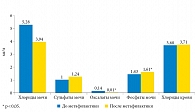
На рисунке 3 представлены результаты метафилактического лечения растительным комплексом Уриклар. Уже после первого курса лечения снижалось содержание оксалатов и увеличивался уровень фосфатов в моче. В биохимических анализах суточной мочи наблюдалось увеличение цитрата уже после первого месяца применения растительного комплекса Уриклар (р < 0,05). Прием растительного комплекса Уриклар уменьшал риск рецидива мочекаменной болезни в сравнении с контрольной группой на 22% (95%-ный доверительный интервал 0,89–37,7%).
Таким образом, сведения об анионном составе камней почек дают возможность лучше понять и оценить факторы, способствующие камнеобразованию. Это позволяет выбрать оптимальную тактику лечения и разработать систему мероприятий, направленных на предотвращение повторного камнеобразования. Анализ биологических жидкостей может быть полезен при оценке предрасположенности пациента к камнеобразованию, выявлении нарушения в обмене веществ, составлении профилактической диеты, оценке активности камнеобразования. Однако полученные выводы требуют дальнейшего изучения на больших выборках с привлечением мониторинга содержания анионов в организме человека.
Заключение
Двухэнергетическая компьютерная томография может быть использована для идентификации уратных камней in vivo, поскольку этот метод сопоставим с общепринятым методом инфракрасной спектроскопии (результаты были идентичны в 83% случаев).
По данным инфракрасной спектроскопии, в Красноярском крае чаще всего встречаются двухкомпонентные камни (67,1%), среди которых преобладают уролиты, состоящие из апатита и ведделлита (51,8%).
Использование капиллярного электрофореза позволяет с высокой специфичностью и чувствительностью определять при динамическом наблюдении изменение содержания ионов в моче в ответ на метафилактическое лечение.
Методом капиллярного электрофореза было установлено, что прием растительного комплекса Уриклар уже в первый месяц лечения способствовал снижению содержания фосфата в плазме крови на фоне повышения уровня сульфата, а также камнеобразующих ионов в моче.
Метафилактика, включавшая прием растительного комплекса Уриклар, уменьшала риск рецидива мочекаменной болезни в сравнении с контрольной группой на 22%. Следовательно, растительный комплекс Уриклар может применяться у пациентов с различными по составу конкрементами.
F.P. Kapsargin, MD, PhD, Prof., L.F. Zuyeva, V.N. Kozlyakova
Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University
Contact person: Lyubov F. Zuyeva, kapsargina0705@mail.ru
The article presents the results of a clinical study of the plant complex Uriklar effectiveness in the complex metaphylaxis of urolithiasis. The capillary electrophoresis method found that the reception of the plant complex in the first month of treatment contributed to the reduction of phosphate in the blood plasma, on the background of the increase in the level of sulfate, as well as stone-forming ions in the urine, which allowed reducing the risk of relapse.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.