Роль глюкозотолерантного теста и оценки гликированного гемоглобина в выявлении нарушений углеводного обмена у лиц с высоким риском развития сахарного диабета 2 типа
- Аннотация
- Статья
- Ссылки
- English
Цель – сравнить диагностическую значимость оценки уровня HbA1c и ПГТТ для выявления ранних нарушений углеводного обмена у лиц с двумя или более факторами риска развития сахарного диабета (СД) 2 типа.
Материал и методы. В исследовании приняли участие 238 пациентов с двумя и более факторами риска развития СД 2 типа. Всем пациентам был проведен ПГТТ с использованием 75 г безводной глюкозы и определен уровень HbA1c. Статистический анализ данных, полученных в ходе исследования, проводился с использованием современных методов прикладной статистики (R Foundation for Statistical Computing 4.2.1, Вена, Австрия). Описательные статистики представлены в виде абсолютной и относительной частот для качественных переменных и медианы (первого и третьего квартилей) для количественных переменных. Для сравнения количественных переменных применяли критерий Краскела – Уоллиса. Прогностическую ценность отрицательного и положительного результатов оценивали с помощью построения матрицы сопряженности (таблица 2 × 2).
Результаты. Согласно данным ПГТТ, нарушения углеводного обмена имели место у 58% (138) участников исследования, при этом у 18% (43) впервые был диагностирован СД 2 типа, у 40% (95) – предиабет. Диагноз впервые выявленного СД 2 типа на основании результатов определения уровня HbA1c (6,7 ± 0,9%) был установлен только у 6,5% (9) пациентов. У лиц с нарушенной гликемией натощак среднее значение HbA1c по данным ПГТТ составило 5,6 (5,3–5,9)%, у лиц с нарушением толерантности к глюкозе – 6,3 (6,0–6,3)%. При этом у 17% (7) пациентов с СД 2 типа, подтвержденным результатами ПГТТ, уровень HbA1c находился в диапазоне от 5,7 до 6,4%. Прогностическая ценность отрицательного результата (negative predictive value) использования HbA1c для диагностики предиабета и СД 2 типа оказалась низкой – 17% при 95%-ном доверительном интервале 6–33.
Выводы. Низкая прогностическая ценность отрицательного результата применения HbA1c для выявления ранних нарушений углеводного обмена указывает на важность проведения ПГТТ.
Цель – сравнить диагностическую значимость оценки уровня HbA1c и ПГТТ для выявления ранних нарушений углеводного обмена у лиц с двумя или более факторами риска развития сахарного диабета (СД) 2 типа.
Материал и методы. В исследовании приняли участие 238 пациентов с двумя и более факторами риска развития СД 2 типа. Всем пациентам был проведен ПГТТ с использованием 75 г безводной глюкозы и определен уровень HbA1c. Статистический анализ данных, полученных в ходе исследования, проводился с использованием современных методов прикладной статистики (R Foundation for Statistical Computing 4.2.1, Вена, Австрия). Описательные статистики представлены в виде абсолютной и относительной частот для качественных переменных и медианы (первого и третьего квартилей) для количественных переменных. Для сравнения количественных переменных применяли критерий Краскела – Уоллиса. Прогностическую ценность отрицательного и положительного результатов оценивали с помощью построения матрицы сопряженности (таблица 2 × 2).
Результаты. Согласно данным ПГТТ, нарушения углеводного обмена имели место у 58% (138) участников исследования, при этом у 18% (43) впервые был диагностирован СД 2 типа, у 40% (95) – предиабет. Диагноз впервые выявленного СД 2 типа на основании результатов определения уровня HbA1c (6,7 ± 0,9%) был установлен только у 6,5% (9) пациентов. У лиц с нарушенной гликемией натощак среднее значение HbA1c по данным ПГТТ составило 5,6 (5,3–5,9)%, у лиц с нарушением толерантности к глюкозе – 6,3 (6,0–6,3)%. При этом у 17% (7) пациентов с СД 2 типа, подтвержденным результатами ПГТТ, уровень HbA1c находился в диапазоне от 5,7 до 6,4%. Прогностическая ценность отрицательного результата (negative predictive value) использования HbA1c для диагностики предиабета и СД 2 типа оказалась низкой – 17% при 95%-ном доверительном интервале 6–33.
Выводы. Низкая прогностическая ценность отрицательного результата применения HbA1c для выявления ранних нарушений углеводного обмена указывает на важность проведения ПГТТ.


Значимость своевременного выявления ранних нарушений углеводного обмена обусловлена тем, что при сахарном диабете (СД) 2 типа риск возникновения сердечно-сосудистых заболеваний повышается на всех этапах кардиоваскулярного континуума – от эндотелиальной дисфункции до хронической сердечной недостаточности [1]. Согласно данным Всемирной организации здравоохранения (World Health Organization, WHO), в 2017 г. ежегодно регистрировалось около 500 тыс. случаев хронической почечной недостаточности, требующей заместительной терапии, 600 тыс. случаев потери зрения и порядка 1 млн случаев ампутации нижних конечностей [2].
В основе развития осложнений СД лежит хроническая гипергликемия, приводящая к прогрессирующему нарастанию неферментативного гликозилирования белков и накоплению продуктов гликирования [3]. Данные процессы начинаются задолго до манифестации СД 2 типа – уже на ранних этапах нарушений углеводного обмена, когда пациент либо не знает об их наличии, либо не придает должного внимания незначительному повышению гликемии [4]. Активный скрининг и выявление лиц с нарушениями углеводного обмена, в идеале на самых ранних этапах, обеспечит профилактику развития не только СД 2 типа, но и его осложнений [4].
В течение 25 лет золотым стандартом диагностики нарушений углеводного обмена считался пероральный глюкозотолерантный тест (ПГТТ) с 75 г глюкозы [5]. Его применение для диагностики СД началось в 20-е гг. XX в. [6]. Однако методика проведения ПГТТ и диагностические критерии нарушений углеводного обмена различались на разных этапах становления диабетологии как науки. Так, в 1954 г. S.S. Fajans и J.W. Conn проводили ПГТТ из расчета 1,75 г глюкозы на 1 кг массы тела и определяли гликемию через 1 час, 1 час 30 минут и через 2 часа (оценка гликемии натощак в то время не проводилась) [6, 7]. В разное время медицинские сообщества разных стран предлагали использовать для проведения ПГТТ 50- или 100-граммовые растворы глюкозы [6, 7]. В 1979 г. эксперты Национальной группы по сбору данных о диабете (National Diabetes Data Group, NDDG) признали недостаточным применение 50 г глюкозы для выявления нарушения толерантности к глюкозе (НТГ) у некоторых групп пациентов, подчеркнув при этом, что использование 100 г глюкозы часто плохо переносится и вызывает тошноту [8]. Поскольку углеводная нагрузка при приеме 75 и 100 г глюкозы у небеременных взрослых оказалась сопоставимой, первая доза была рекомендована для проведения ПГТТ.
Экспертами NDDG были предложены критерии нарушений углеводного обмена, представленные в табл. 1 [8].
В 1980–1985 гг. был принят консенсус по критериям диагностики нарушений углеводного обмена и утвержден ПГТТ с 75 г глюкозы [9]. Уровень глюкозы плазмы натощак (ГПН) ≥ 7,8 ммоль/л и через 2 часа после теста или в любое время суток ≥ 11,1 ммоль/л стал маркером сахарного диабета. Значения ГПН < 6,1 ммоль/л в сочетании с показателями через 2 часа после ПГТТ > 7,8 и < 11,1 ммоль/л служили доказательством наличия нарушения толерантности к глюкозе [9].
Методики проведения ПГТТ и критерии диагностики СД исторически также претерпевали изменения (табл. 2) [10]. В 1997 г. эксперты Американской диабетической ассоциации (American Diabetes Association, ADA) предложили снизить пороговое значение ГПН для выявления сахарного диабета с ≥ 7,8 до ≥ 7,0 ммоль/л [10].
В соответствии с рекомендациями ADA и WHO были утверждены новые критерии нарушений углеводного обмена. Так, уровень ГПН ≥ 7,0 ммоль/л через 2 часа после ПГТТ или в любое время суток ≥ 11,1 ммоль/л был признан критерием СД, уровень ГПН < 7,0 ммоль/л и через 2 часа после ПГТТ ≥ 7,8 и < 11,1 ммоль/л – критерием НТГ. Нарушенная гликемия натощак определялась по уровню ГПН от 6,1 до 6,9 ммоль/л, однако в 2003 г. ADA снизила диагностический порог до 5,6 ммоль/л [11].
На сегодняшний день перед проведением ПГТТ необходимо оценить наличие факторов риска развития СД 2 типа [12]. В настоящее время определить десятилетний риск развития СД 2 типа можно с помощью опросника Finnish Diabetes Risk Score (FINDRISС) [13]. Данный риск устанавливается исходя из антропометрических данных, пищевого поведения и физической активности, а также исходя из наследственной предрасположенности к развитию данного заболевания. Если суммарное количество баллов соответствует умеренному или высокому риску развития сахарного диабета 2 типа, проведение ПГТТ показано [12].
При проведении ПГТТ возможно возникновение краткосрочных побочных явлений, таких как тошнота, рвота, диарея, ощущение жара или озноба, головная боль, головокружение [14]. Именно поэтому пить приготовленный раствор глюкозы рекомендуется медленно. В него можно добавить сок лимона или лимонную кислоту. Однако важно помнить, что, даже если симптоматика присутствует, она не является жизнеугрожающей.
Единственным побочным эффектом, требующим повышенного внимания, считается реактивная гипогликемия, возникающая при проведении ПГТТ после родов у женщин с гестационным сахарным диабетом в анамнезе [15]. Реактивная гипогликемия может рассматриваться в качестве благоприятного прогностического фактора, так как ассоциирована с хорошим метаболическим профилем, включая повышенную чувствительность к инсулину и более высокую секреторную способность β-клеток [15, 16].
При назначении ПГТТ может возникнуть ряд проблем. Во-первых, это страх, связанный с мифом, что глюкоза может разрушить поджелудочную железу и привести к развитию сахарного диабета [17]. Во-вторых, длительность исследования. Часто пациенты не хотят проводить 2,0–2,5 часа в лаборатории [18]. В связи с этим альтернативным методом исследования становится определение гликированного гемоглобина (HbA1c). Уровень HbA1c ≥ 6,5% свидетельствует о развитии сахарного диабета, от 6,0 до 6,4% – о наличии нарушений углеводного обмена. Однако уровень HbA1c < 6,0% не исключает наличия нарушений углеводного обмена, а значит, не может служить маркером ранних нарушений углеводного обмена. Следовательно, оценка уровня HbA1c не является альтернативой ПГТТ [19].
С целью сравнения диагностической значимости определения уровня HbA1c с диагностической значимостью ПГТТ для выявления ранних нарушений углеводного обмена у лиц с высоким риском развития СД 2 типа нами было проведено собственное скрининговое исследование.
Материал и методы
В исследование вошли 238 пациентов, у которых имели место факторы риска развития СД 2 типа.
Критерии включения в исследование:
- избыточная масса тела или ожирение (индекс массы тела ≥ 25 кг/м2);
- наличие как минимум одного из следующих факторов риска развития СД 2 типа: возраст ≥ 45 лет, отягощенная наследственность по СД 2 типа, гестационный сахарный диабет или рождение плода > 4 кг в анамнезе, артериальная гипертензия, наличие сердечно-сосудистых заболеваний.
В исследование не включали пациентов, получавших сахароснижающую терапию или диетотерапию.
Критерии невключения:
- СД 1 типа и другие специфические типы СД;
- клиническая картина острой декомпенсации углеводного обмена;
- острое нарушение мозгового кровообращения, инфаркт миокарда в течение последнего месяца;
- беременность и период лактации.
Всем включенным в исследование пациентам был проведен ПГТТ, согласно положениям, приведенным в алгоритмах специализированной медицинской помощи больным СД 2025 г. Взятие венозной крови на 0-й и 120-й минутах проводилось в пробирки с ЭДТА. Кровь была центрифугирована на центрифуге СМ-6М (ELMI, Латвия) не позднее 15 минут после забора при 3500 об/мин в течение 10 минут. Определение уровня глюкозы проводилось в день забора крови на биохимическом анализаторе ARCHITECT c4000 (Abbott Diagnostics, США) стандартными наборами реактивов производителя. Уровень HbA1c определяли с помощью экспресс-метода (анализатор Abbott NycoCard Reader II, США).
Исследование было одобрено локальным этическим комитетом ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России (выписка из протокола заседания № 10 от 22.12.2015).
Для хранения и обсчета результатов исследования была создана матрица данных в виде электронных таблиц Microsoft Office Excel 2010. Статистический анализ и визуализация полученных данных проводились с использованием среды для статистических вычислений R 4.2.1 (R Foundation for Statistical Computing, Вена, Австрия). Описательные статистики представлены в виде абсолютной и относительной частот для качественных переменных, в виде медианы, а также первого и третьего квартилей (Q1–Q3) – для количественных переменных. Для сравнения количественных переменных использовали тест Краскела – Уоллиса. Различия показателей считали статистически значимыми при p < 0,05. Для оценки прогностической ценности отрицательного и положительного результатов использовали метод построения матрицы сопряженности (таблица 2 × 2).
Результаты
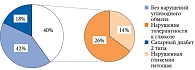
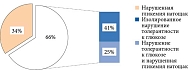
Согласно результатам ПГТТ, нарушения углеводного обмена имели место у 58% (138) обследованных. При этом впервые выявленный СД 2 типа обнаружен у 18% (43) пациентов, предиабет – у 40% (95). Необходимо отметить, что нарушение толерантности к глюкозе встречалось в два раза чаще, чем нарушенная гликемия натощак (рис. 1). При более детальном анализе этой группы были выделены пациенты с изолированным нарушением толерантности к глюкозе. Таковых насчитывался 41% (39) (рис. 2).
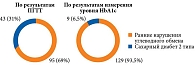
Согласно результатам оценки уровня HbA1c, СД 2 типа впервые был диагностирован у 6,5% (9) обследованных (рис. 3). Это число было меньше количества, полученного по результатам ПГТТ. Среднее значение HbA1c различалось у лиц с разными нарушениями углеводного обмена (р < 0,0001). Так, уровень HbA1c у лиц с нарушенной гликемией натощак в среднем составлял 5,6 (5,3–5,9)%, у лиц с нарушением толерантности к глюкозе – 6,3 (6,0–6,3)%, у лиц без нарушений углеводного обмена – 5,7 (5,5–6,0)%, у лиц с впервые выявленным СД 2 типа – 6,7 (6,5–6,9)%. Более того, у 17% (7) пациентов с СД 2 типа, подтвержденным результатами ПГТТ, уровень HbA1c находился в диапазоне от 5,7 до 6,4%.
Прогностическая ценность отрицательного результата (negative predictive value, NPV) использования HbA1c для диагностики предиабета и впервые выявленного СД 2 типа оказалась низкой – 17% (95%-ный доверительный интервал (ДИ) 6–33).
Обсуждение
Полученные нами данные согласуются с данными, представленными Национальным медицинским исследовательским центром эндокринологии [20]. Нами установлено, что ранние нарушения углеводного обмена в 1,2 раза чаще выявляются в виде изолированного нарушения толерантности к глюкозе, чем в виде нарушенной гликемии натощак. Это подтверждает общую закономерность. Результаты многочисленных исследований свидетельствуют о том, что центральную роль в развитии нарушений углеводного обмена играет именно нарушение толерантности к глюкозе [21]. Так, в исследовании DECODE, в ходе которого были проанализированы данные 13 европейских когортных исследований, включавших более чем 22 тыс. пациентов, регистрировалась повышенная смертность пациентов с НТГ, выявленным с помощью ПГТТ, тогда как корреляция между изменением уровня ГПН и смертностью отсутствовала [22]. Результаты данного исследования коррелируют с показателями научных работ немецких и японских ученых, согласно которым нарушение толерантности к глюкозе является значимым фактором риска развития сердечно-сосудистых заболеваний по сравнению с нарушенной гликемией натощак [23, 24].
Ряд характеристик HbA1c обусловливают преимущество его оценки перед проведением ПГТТ при диагностике сахарного диабета 2 типа [25]. Именно поэтому мы проанализировали соответствие результатов ПГТТ и определения уровня HbA1c в отношении выявления нарушений углеводного обмена [17].
Эксперты WHO и ADA отмечают, что рекомендуемый уровень HbA1c 6,5% обладает низкой чувствительностью для диагностики СД 2 типа. Вместе с тем уровень HbA1c < 6,5% не позволяет исключить наличие СД 2 типа у всех пациентов. Значение HbA1c 6,1% характеризуется большей чувствительностью и специфичностью в отношении диагностики данной патологии [26].
В нашей работе применение HbA1c не позволило выявить ранние нарушения углеводного обмена у значительной части пациентов с факторами риска развития диабета.
Прогностическая значимость NPV заключается в оценке вероятности отсутствия заболевания при получении отрицательного (нормального) результата теста. Этот показатель определяется как соотношение истинно отрицательных результатов к общему числу отрицательных результатов и выражается в процентах или в виде десятичной доли [27]. Согласно полученным нами данным, NPV использования HbA1c для диагностики предиабета и впервые выявленного СД 2 типа оказался низким и составил 17% (95% ДИ 6–33). На конгрессе Эндокринологического общества США (Endocrine Society, ENDO) 2019 г. также были представлены результаты исследования, свидетельствующие, что использование HbA1c для диагностики СД 2 типа связано с занижением распространенности заболевания [28].
Таким образом, из представленных нами результатов следует, что пациенты с уровнем HbA1c от 5,7 до 6,4% должны проходить ПГТТ для выявления ранних нарушений углеводного обмена. Кроме того, значение НbА1с, используемое для диагностики впервые выявленного СД 2 типа, должно быть меньше 6,5%. Это согласуется с выводами других авторов [29–31]. Так, группа ученых из Японии для скрининга СД 2 типа предложила использовать значение НbА1с, равное 6,0% [32], в то время как китайские ученые – 6,3% [33], а австралийская исследовательская группа – 5,5% [34]. Тем не менее необходимы дальнейшие проспективные исследования для уточнения роли HbA1c в качестве инструмента скрининга ранних нарушений углеводного обмена [31–33].
Исследование Е.А. Шестаковой, посвященное сопоставлению использования ПГТТ и оценки уровня HbA1c для диагностики нарушений углеводного обмена в Российской Федерации, показало несоответствие результатов этих методов [35]. При уровне HbA1c > 7% частота выявления СД 2 типа была идентична таковой при использовании ПГТТ [35]. Однако при уровне HbA1c < 7% результаты различались. Данная работа также продемонстрировала, что для верификации диагноза требуется именно ПГТТ.
Выводы
Прогностическая ценность отрицательного результата применения HbA1c для выявления ранних нарушений углеводного обмена составила 17%. Это обосновывает необходимость проведения ПГТТ.
F.V. Valeeva, PhD, Prof., T.S. Yilmaz, PhD, Yu.U. Sharipova, PhD, Zh.A. Rodygina, K.B. Khasanova, PhD, Z.R. Alimetova, PhD
Kazan State Medical University
Contact person: Zulfiya R. Alimetova, alzurg@mail.ru
With the invention of glycated hemoglobin (HbA1c) as a diagnostic test, the oral glucose tolerance test has become less frequently used in endocrinological practice, but still remains relevant. The use of the oral glucose tolerance test allows diagnosing early carbohydrate metabolism disorders and is much more significant than determining the HbA1c level.
Aim – assess the diagnostic value of determining the level of HbA1c in comparison with oral glucose tolerance test for the detection of early carbohydrate metabolism disorders among individuals with two or more risk factors for the development of type 2 diabetes mellitus.
Material and methods. The study involved 238 patients with two or more risk factors for type 2 diabetes. All patients underwent an oral glucose tolerance test using 75 g of anhydrous glucose and the level of HbA1c was determined. The statistical analysis of the data obtained during the study was carried out using modern methods of applied statistics (R Foundation for Statistical Computing 4.2.1, Vienna, Austria). Descriptive statistics are presented in the form of absolute and relative frequencies for qualitative variables and medians (1st and 3rd quartiles) for quantitative ones. The Kruskal – Wallis test was used to compare quantitative variables. To assess the predictive value of negative and positive results, the conjugacy matrix construction method was used (table 2 × 2).
Results. According to the results of the oral glucose tolerance test, carbohydrate metabolism disorders were detected in 58% (138) of the study participants, where 18% (43) of patients were diagnosed with diabetes mellitus type 2 for the first time, prediabetes – in 40% (95) people. The diagnosis of newly diagnosed diabetes mellitus type 2 based on the results of the HbA1c level (6.7 ± 0.9%) was established only in 6,5% (9) subjects. In patients with impaired fasting glycemia, according to oral glucose tolerance test, the average HbA1c value was 5.6 (5.3–5.9)%, in those with impaired glucose tolerance – 6.3 (6.0–6.3)%. However, in 17% (7) of patients with type 2 diabetes confirmed by the oral glucose tolerance test, the HbA1c level was in the range from 5.7 to 6.4%. The prognostic value of the negative predictive value of using HbA1c for the diagnosis of prediabetes and newly diagnosed type 2 diabetes turned out to be low – 17% with a 95% confidence interval of 6–33.
Conclusions. The low negative predictive value of HbA1c for detecting early carbohydrate metabolism disorders highlights the importance of performing an oral glucose tolerance test.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.