Биомаркеры когнитивной дисфункции у пациентов с цереброваскулярными заболеваниями и сахарным диабетом 2 типа
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить характер и связь клинико-нейровизуализационных изменений и биомаркеров, отражающих комплекс метаболических и гормональных нарушений у пациентов с хроническими ЦВЗ и СД 2 типа.
Материал и методы. Обследованы 102 человека. Первую группу составили 72 пациента с ЦВЗ: 35 – с СД 2 типа, 37 – без СД 2 типа. Возраст больных с СД 2 типа составил 65 [58; 70] лет, без СД 2 типа – 62 [58; 66] года. Во вторую группу вошли 30 человек в возрасте 63 [58; 64] лет без ЦВЗ. Проводили клинико-неврологический осмотр, нейропсихологическое тестирование, биохимическое исследование крови и магнитно-резонансную томографию головного мозга.
Результаты. Сахарный диабет 2 типа ассоциировался с большей частотой встречаемости когнитивных нарушений (КН) (57 vs 27%), а также с худшими результатами нейропсихологического тестирования. Наличие СД 2 типа у лиц с ЦВЗ было связано с более высокими значениями индекса триглицериды/глюкоза (ИТГ) и содержанием конечных продуктов гликирования (КПГ), а также с более низкими уровнями адипонектина и ирисина в крови. Выраженность гиперинтенсивности белого вещества (ГИБВ) головного мозга была больше у пациентов с СД 2 типа. Кроме того, выраженность ГИБВ и КН коррелировала с большими значениями ИТГ и циркулирующих КПГ и меньшими значениями адипонектина и ирисина. Содержание адипонектина в крови влияло на выраженность изменений головного мозга. Так, вероятность выявления ГИБВ (2-я и 3-я стадии по шкале Fazekas) и КН возрастала при уровне адипонектина менее 11,2 и 13,0 мкг/мл соответственно.
Выводы. Сочетание сосудистой патологии с СД 2 типа обусловливает более выраженные структурные изменения головного мозга и КН. Тяжесть когнитивных расстройств и выраженность ГИБВ коррелируют с уровнем КПГ, значением ИТГ, а также с содержанием адипонектина и ирисина в крови.
Цель – оценить характер и связь клинико-нейровизуализационных изменений и биомаркеров, отражающих комплекс метаболических и гормональных нарушений у пациентов с хроническими ЦВЗ и СД 2 типа.
Материал и методы. Обследованы 102 человека. Первую группу составили 72 пациента с ЦВЗ: 35 – с СД 2 типа, 37 – без СД 2 типа. Возраст больных с СД 2 типа составил 65 [58; 70] лет, без СД 2 типа – 62 [58; 66] года. Во вторую группу вошли 30 человек в возрасте 63 [58; 64] лет без ЦВЗ. Проводили клинико-неврологический осмотр, нейропсихологическое тестирование, биохимическое исследование крови и магнитно-резонансную томографию головного мозга.
Результаты. Сахарный диабет 2 типа ассоциировался с большей частотой встречаемости когнитивных нарушений (КН) (57 vs 27%), а также с худшими результатами нейропсихологического тестирования. Наличие СД 2 типа у лиц с ЦВЗ было связано с более высокими значениями индекса триглицериды/глюкоза (ИТГ) и содержанием конечных продуктов гликирования (КПГ), а также с более низкими уровнями адипонектина и ирисина в крови. Выраженность гиперинтенсивности белого вещества (ГИБВ) головного мозга была больше у пациентов с СД 2 типа. Кроме того, выраженность ГИБВ и КН коррелировала с большими значениями ИТГ и циркулирующих КПГ и меньшими значениями адипонектина и ирисина. Содержание адипонектина в крови влияло на выраженность изменений головного мозга. Так, вероятность выявления ГИБВ (2-я и 3-я стадии по шкале Fazekas) и КН возрастала при уровне адипонектина менее 11,2 и 13,0 мкг/мл соответственно.
Выводы. Сочетание сосудистой патологии с СД 2 типа обусловливает более выраженные структурные изменения головного мозга и КН. Тяжесть когнитивных расстройств и выраженность ГИБВ коррелируют с уровнем КПГ, значением ИТГ, а также с содержанием адипонектина и ирисина в крови.

![Таблица 3. Уровень метаболических и гуморальных биомаркеров в зависимости от степени гиперинтенсивности белого вещества головного мозга, оцениваемой по шкале Fazekas (Me [Q1; Q3])](/upload/resize_cache/iblock/3d1/mw4f3m0qdy9yykyg0r96rfgdl7muz3x9/195_350_1/Tanashyan5.jpg)
Введение
Сосудистые заболевания головного мозга – одна из важнейших медицинских и социально-экономических проблем современности в силу неуменьшающегося роста их развития, а также в силу связанных с ними показателей смертности и инвалидизации. Свой вклад вносит пандемия сахарного диабета (СД), в первую очередь СД 2 типа, поскольку данная патология влечет серьезные последствия для здоровья населения, являясь мощным независимым фактором риска развития как острых, так и хронических форм цереброваскулярных заболеваний (ЦВЗ). В последние годы доказан вклад СД 2 типа и в возникновение когнитивных нарушений (КН).
Имеющиеся на сегодняшний день данные свидетельствуют об общности факторов риска и предполагаемых патофизиологических механизмов формирования СД, когнитивных расстройств и деменции [1–3]. Определение связи между СД и ассоциированными с ним факторами риска развития КН может способствовать выявлению лиц наибольшего риска и разработке профилактических стратегий.
Известно, что при СД относительный риск возникновения КН, которые могут варьироваться от легких форм до деменции, достигает 1,91 при 95%-ном доверительном интервале (ДИ) 1,54–2,36 [4]. Развившиеся КН способны ухудшать приверженность лечению, нарушая самоконтроль СД и тем самым способствуя дальнейшему прогрессированию сосудистой патологии головного мозга. У пациентов с ЦВЗ отмечается особенно низкая приверженность к соблюдению рекомендаций по модификации образа жизни [5]. Дефицит физической активности может приводить не только к ухудшению гликемического контроля, накоплению жировой массы, но и к недостаточному высвобождению экзеркинов, в первую очередь ирисина, что способно негативно влиять на течение ЦВЗ и когнитивные функции.
При СД к модифицируемым факторам риска относят контроль гликемии, физическую активность, диету, курение и артериальную гипертензию (АГ), к немодифицируемым – возраст, генетическую предрасположенность, пол и длительность заболевания [6]. Для паттерна хронических ЦВЗ при СД 2 типа характерны одновременное нарушение углеводного обмена и нейрокогнитивных функций в виде нарушения памяти и внимания, значительное ухудшение управляющих функций мозга, инертность психических процессов, расстройство эмоционально-волевой сферы, сопровождающиеся нейрофизиологическими и нейровизуализационными изменениями [7–9]. Генез подобной когнитивной дисфункции сложный и включает нейровоспаление, церебральные микрососудистые нарушения, изменение церебрального клиренса, накопление патологических белков [6, 10].
Информативными в отношении состояния вещества головного мозга в современных условиях являются нейровизуализационные характеристики, получаемые при проведении магнитно-резонансной томографии (МРТ). К маркерам повреждения церебрального микрососудистого русла, ассоциированным с КН, относятся гиперинтенсивность белого вещества (ГИБВ), лакуны, церебральные микрокровоизлияния и расширенные периваскулярные пространства (ПВП). Показано, что СД 2 типа связан с общим снижением объема вещества головного мозга, большим количеством инфарктов и большим объемом гиперинтенсивности белого вещества [11, 12]. Отмечается, что у пациентов с плохо контролируемым СД 2 типа выраженность ГИБВ может быть ассоциирована с более низкой скоростью обработки информации [13]. Условия и маркеры клинической манифестации ГИБВ в виде когнитивной дисфункции не определены.
С учетом стремительного роста ассоциированных с сахарным диабетом КН необходим поиск новых общих биомаркеров с целью разработки подходов к диагностике и лечению указанных состояний. В последние годы особое внимание уделяется роли специфических биомаркеров, которые позволяют стратифицировать риск и раскрывают новые патогенетические звенья хронических ЦВЗ. Такие маркеры служат отражением не только метаболических нарушений (конечные продукты гликирования (КПГ) и другие индикаторы инсулинорезистентности, углеводного и липидного обмена), но и изменений образования адипо- и миокинов при СД 2 типа. Накопление КПГ может оказывать повреждающее воздействие на вещество головного мозга, вызывая прогрессирование сосудистых заболеваний [14, 15]. Комплексный индикатор инсулинорезистентности и глюкозолипотоксичности – индекс триглицериды/глюкоза (ИТГ) – продемонстрировал предикторные возможности в отношении наличия цереброметаболических нарушений. Показано, что повышенный ИТГ свидетельствует об увеличении риска развития метаболического синдрома, нарушений мозгового кровообращения и каротидного атеросклероза [16–18]. Получены данные и о связи повышенных значений ИТГ с КН [19, 20].
Среди агентов гуморальной регуляции в аспекте сосудистой патологии мозга могут быть выделены такие потенциально протективные гормоны, как адипонектин и ирисин. Адипонектин – важный фактор в метаболизме глюкозы и чувствительности клеток к инсулину, обладающий противовоспалительными, антиоксидантными и вазопротективными свойствами [21]. В пилотных исследованиях показан его эффект в отношении предотвращения поражения белого вещества головного мозга и снижения когнитивных функций [22]. Ирисин – гормон мышечной ткани, миокин, который играет роль в улучшении метаболизма глюкозы и свободных жирных кислот, стимулировании липолиза в адипоцитах. Более низкое содержание ирисина отмечено у пациентов с СД 2 типа [23]. Установлено также, что ирисин может оказывать положительное влияние на когнитивные функции [24].
Таким образом, несмотря на очевидную связь между СД 2 типа и ЦВЗ, гуморальные маркеры реализации структурных изменений вещества головного мозга и клинически значимые когнитивные расстройства при этой сочетанной патологии на сегодняшний день недостаточно изучены.
Цель исследования
Целью настоящего исследования стала оценка характера, а также взаимосвязи клинико-нейровизуализационных изменений и биомаркеров, отражающих комплекс метаболических и гормональных нарушений у пациентов с хроническими ЦВЗ, с учетом влияния СД 2 типа.
Материал и методы
В исследование были включены 102 человека. Их разделили на две группы – основную и контрольную. Первую, основную группу составили 72 пациента с хронической цереброваскулярной патологией, которые в свою очередь были разделены на две подгруппы. В первую подгруппу вошли 35 пациентов с ЦВЗ и СД 2 типа. Их возраст составил 65 [58; 70] лет. Вторая подгруппа была сформирована из 37 лиц с ЦВЗ, но без СД. Возраст пациентов данной подгруппы составил 62 [58; 66] года. Во вторую, контрольную группу вошли 30 человек в возрасте 63 [58; 64] лет без клинических и МРТ-признаков патологии головного мозга.
Критерии включения в исследование:
- наличие хронических ЦВЗ: подостро нарастающая хроническая ишемия головного мозга (по типу дисциркуляторной энцефалопатии);
- возраст 50–70 лет;
- наличие СД 2 типа (для первой подгруппы).
Критерии невключения в исследование:
- нарушения мозгового кровообращения в анамнезе;
- тяжелая соматическая или психическая патология;
- острые инфекционные заболевания в последние шесть месяцев;
- выраженные КН (≤ 15 баллов по Монреальской шкале оценки когнитивных функций (Montreal Cognitive Assessment, МоСА));
- СД 1 типа и другие специфические типы диабета.
Критерии исключения из исследования:
- отказ пациента от продолжения исследования;
- выявление клинических и визуализационных признаков нейродегенеративного процесса, в том числе болезни Альцгеймера;
- противопоказания к проведению МРТ.
Всем пациентам проводилось общеклиническое и неврологическое обследование.
Все обследованные пациенты подписали информированное согласие на участие в исследовании.
Диагноз хронических ЦВЗ устанавливался по результатам клинического осмотра и изучения анамнеза и подтверждался результатами инструментального обследования, в том числе ультразвукового и нейровизуализационного.
Когнитивный статус оценивался по шкале МоCA и Адденбрукской шкале оценки когнитивных функций III (Addenbrooke's Cognitive Examination III, ACE-III). Результат менее 26 баллов по шкале МоСА трактовался как наличие КН.
Проводился также клинический и биохимический анализ крови. Уровень гликированного гемоглобина (HbA1c) определяли с использованием гематологического импедансного анализатора Nihon Kohden MEK-7300K (Япония), автоматического биохимического анализатора Konelab 30i (Финляндия) с помощью наборов реагентов Randox (Великобритания), «Вектор-Бест» (Россия), Agappe (Швейцария) и экспресс-анализатора Wondfo Finecare FIA FS-113 (Китай).
Определение специфических биомаркеров, таких как КПГ, адипонектин и ирисин, в сыворотке/плазме крови проводили твердофазным иммуноферментным методом сэндвич-типа. Индекс триглицериды/глюкоза рассчитывали по формуле: ln [(триглицериды натощак (ммоль/л) × 88,495575) × (глюкоза плазмы натощак (ммоль/л) × 18,018018)] / 2.
Антропометрические показатели (рост, вес, индекс массы тела (ИМТ)) оценивали при нахождении пациента в легкой одежде, без обуви. Индекс массы тела рассчитывали по формуле: масса (кг) / рост, возведенный в квадрат (м2).
Оценку состояния серого и белого вещества головного мозга проводили на магнитно-резонансном томографе Siemens Magnetom Prisma (Германия) с величиной магнитной индукции 3 Тл с использованием 64-канальной радиочастотной катушки.
Для статистического анализа полученных результатов использовали программный пакет StatTech v. 4.11.2 (Россия). Количественные показатели оценивали на предмет соответствия нормальному распределению с помощью критерия Колмогорова – Смирнова. Количественные показатели, выборочное распределение которых соответствовало нормальному, описывали с помощью средней арифметической величины (M) и стандартного отклонения (SD). В отсутствие нормального распределения количественные данные представляли в виде медианы (Me), а также нижнего и верхнего квартилей (Q1; Q3). Для категориальных данных указывали абсолютные значения и процентные доли.
При анализе данных для несвязанных совокупностей применяли параметрический метод – Т-тест, для количественных переменных с ненормальным распределением и для сравнения по ранговой переменной – тест Манна – Уитни. Для сравнения по категориальным переменным использовали χ2 Пирсона или критерий Фишера. При анализе всех участников для оценки связи между количественными переменными применяли параметрический метод – корреляционный анализ Пирсона.
Для сравнения лабораторных показателей применяли критерий Краскела – Уоллиса с последующим попарным внутригрупповым анализом по U-критерию Манна – Уитни. Для построения прогностической модели вероятности определенного исхода использовали метод логистической регрессии. Мерой определенности, указывающей на ту часть дисперсии, которая может быть объяснена с помощью логистической регрессии, служил коэффициент R2 Найджелкерка.
Дискриминационную способность количественных признаков в прогнозировании определенного исхода оценивали с помощью ROC-анализа. Разделяющее значение количественного признака в точке cut-off устанавливали по наивысшему значению индекса Юдена.
Различия считали статистически значимыми при p < 0,05.
Результаты
Характеристика лиц, включенных в исследование, представлена в табл. 1.
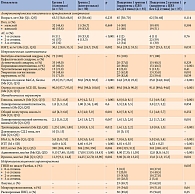
В основной группе по сравнению с контрольной группой имела место отягощенность по факторам риска (АГ, СД 2 типа) и уровню метаболических маркеров (ИТГ, циркулирующие КПГ). Различия также касались содержания гормонов жировой и мышечной ткани – адипонектина и ирисина.
Сосудистая патология головного мозга у включенных в исследование пациентов проявлялась вестибуло-атактическим, цефалгическим и астеническим синдромами, а также пирамидной симптоматикой и чувствительными нарушениями. При этом частота встречаемости вестибуло-атактического и цефалгического синдромов, пирамидной симптоматики оказалась сопоставимой у больных ЦВЗ с и без СД 2 типа. Астенические и чувствительные нарушения чаще фиксировались у лиц с ЦВЗ и СД 2 типа, чем у лиц с ЦВЗ, но без СД 2 типа, – 80,0 против 40,5% (p < 0,001) и 62,8 против 35,0% (p = 0,001). Анализ результатов оценки когнитивных функций показал, что наличие СД 2 типа сопровождалось повышением частоты встречаемости КН (57 против 27%), статистически значимо худшими результатами по шкале MoCA (24 [23; 25] против 25 [24; 26] баллов) и по шкале ACE-III (89 [84; 90] против 91 [89; 94] балла) (см. табл. 1).
Сопоставление клинико-метаболических параметров пациентов с ЦВЗ в зависимости от наличия или отсутствия СД 2 типа не выявило статистически значимых различий по степени АГ, значениям липидограммы (общий холестерин, триглицериды, липопротеины высокой плотности). У пациентов с СД 2 типа имели место большие значения ИМТ – 30,4 [28,2; 33,3] против 28,7 [25,3; 32,3] кг/м2. Метаболические нарушения у больных первой подгруппы первой группы сопровождались более высоким уровнем инсулинорезистентности (ИТГ) и КПГ, а также более низкими значениями потенциально протективных гормонов – адипонектина и ирисина (см. табл. 1 и рис. 1).
В ходе нейровизуализационного исследования изменения головного мозга в виде ГИБВ чаще обнаруживали у пациентов с ЦВЗ и СД 2 типа (p = 0,005), причем наиболее выраженные (2-я и 3-я степени по шкале Fazekas, или Fazekas 2–3) также имели место в данной подгруппе – 71,5 против 32,4% случаев. В то же время частота выявления лакун, микрокровоизлияний и расширенных ПВП в обеих подгруппах была сопоставимой. Нейровизуализационные характеристики обследованных пациентов представлены в табл. 1.
Для оценки клинико-метаболических ассоциаций был проведен корреляционный анализ когнитивного статуса и уровней исследуемых биомаркеров. Результаты по шкалам МоСА и ACE-III находились в прямой зависимости от содержания адипонектина и ирисина в сыворотке крови и в обратной зависимости от значений КПГ и ИТГ (табл. 2).
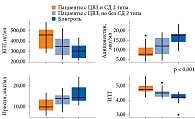
Проведенный анализ уровней исследуемых биомаркеров выявил различия у обследованных пациентов в зависимости от степени тяжести поражения белого вещества головного мозга (по шкале Fazekas) (рис. 2 и табл. 3).
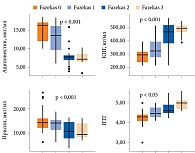
Исходя из гипотезы о потенциально нейропротективном воздействии адипонектина на состояние вещества головного мозга, был проведен ROC-анализ результатов нейровизуализации у пациентов с Fazekas 2–3 (рис. 3А).
Установлено, что уровень адипонектина в крови является статистически значимым предиктором выявления Fazekas 2–3 (площадь под кривой – 0,856 (95% ДИ 0,784–0,928; p < 0,001)). Пороговое значение адипонектина в точке cut-off, которой соответствовало наивысшее значение индекса Юдена, составило 11,2 мкг/мл. Чувствительность и специфичность полученной прогностической модели – 74,3 и 89,3% соответственно. Была проанализирована также зависимость наличия КН от уровня адипонектина (рис. 3Б). Установлено, что уровень адипонектина в крови является статистически значимым предиктором выявления КН (площадь под кривой – 0,867 (95% ДИ 0,763–0,972; p < 0,001)). Пороговое значение содержания адипонектина в точке cut-off, которой соответствовало наивысшее значение индекса Юдена, составило 13,0 мкг/мл. Отсутствие КН прогнозировалось при уровне адипонектина выше данной величины или равном ей. Чувствительность и специфичность полученной прогностической модели составили 81,0 и 90,2% соответственно.
Обсуждение
Синдемическое взаимодействие церебральных и метаболических расстройств отражается в концепции цереброметаболического здоровья. Наличие СД 2 типа связано со снижением когнитивных функций, механизм которого многокомпонентен [25]. При цереброметаболических расстройствах развитие и прогрессирование поражений головного мозга обусловлено вовлечением сосудов различного диаметра, изменениями системы гемореологии и гемостаза, мета- и нейровоспалением, нейродегенерацией, которые ассоциированы с избыточным адипогенезом, дислипидемией, дисгликемией и нарушением проницаемости гематоэнцефалического барьера, что приводит к формированию ЦВЗ, церебральной микроангиопатии и КН [25].
Полученные нами результаты подтверждают большую выраженность структурных и функциональных изменений головного мозга у больных ЦВЗ с СД 2 типа.
Результаты нейропсихологического тестирования статистически значимо находились в обратной связи с параметрами, отражающими инсулинорезистентность, глюкозолипотоксичность и накопление продуктов гликирования. Определены такие гуморальные факторы, как гормон жировой ткани адипонектин и миокин ирисин, напрямую ассоциированные с сохранностью когнитивных функций. Это подтверждается и в ряде других наблюдений [26–28].
Общеизвестна зависимость КН от степени структурного поражения вещества мозга при различных неврологических заболеваниях [29–31]. В ходе нашего исследования подтверждена связь между уровнями исследуемых биомаркеров и выраженностью изменений вещества головного мозга. Наиболее тяжелые повреждения по шкале Fazekas сопровождались более высокими значениями ИТГ и КПГ, что подтверждает роль гипергликемии, особенно хронической, а также гиперлипидемии и инсулинорезистентности в генезе нейрокогнитивных расстройств. Интегральным маркером инсулинорезистентности, которая является центральным звеном патогенеза СД 2 типа, является ИТГ, отражающий эффекты повышенного содержания глюкозы и триглицеридов на сосудистую стенку [17, 18].
При рассмотрении роли таких факторов жировой и мышечной ткани, как адипонектин и ирисин, в развитии структурных изменений головного мозга при СД 2 типа было выявлено, что повышенные значения КПГ и ИТГ, а также низкие значения ирисина и адипонектина связаны с более тяжелым поражением вещества головного мозга (Fazekas 2–3) и более выраженными когнитивными нарушениями (< 26 баллов по шкале MoCA). Полученные данные могут объясняться потенциальными церебропротективными свойствами этих гормонов [24, 32].
Важным аспектом в подтверждении биомаркерной роли адипонектина у больных ЦВЗ являются полученные пороговые уровни гормона. Более выраженным структурным изменениям головного мозга (Fazekas 2–3) соответствуют значения ниже 11,2 мкг/мл, а наличию КН – значения ниже 13,0 мкг/мл.
Заключение
Сочетание сосудистой патологии головного мозга с СД 2 типа характеризуется более выраженными структурными церебральными изменениями и когнитивными нарушениями, которые в свою очередь ассоциированы с уровнем метаболических и гормональных биомаркеров. Тяжесть когнитивных расстройств и поражения белого вещества головного мозга связана со значениями КПГ и ИТГ. Меньшее содержание адипонектина и ирисина в крови обусловливает большую выраженность поражения вещества головного мозга и когнитивной дисфункции. Гормоны жировой и мышечной ткани могут вносить вклад в формирование клинической картины ЦВЗ при СД 2 типа. В связи с этим возможно рекомендовать их оценку для выявления когнитивных нарушений у пациентов с ЦВЗ и СД 2 типа.
M.M. Tanashyan, Academician of the RAS, PhD, Prof., A.А. Panina, K.V. Antonova, PhD, N.E. Spryshkov, A.A. Shabalina, PhD, O.V. Lagoda, PhD, A.N. Sergeeva, PhD, G.I. Khvastochenko
Russian Сenter of Neurology and Neurosciences
Contact person: Anastasiya A. Panina, panina.a.a@neurology.ru
Type 2 diabetes mellitus (DM2) can affect the course of cerebrovascular diseases (CVD). However, the significance of complex metabolic markers, adipokines, and excerkins, in the clinic of CVD in DM2 has not been determined.
Aim – to estimate the nature and relationship of clinical and neuroimaging changes and biomarkers reflecting a complex of metabolic and hormonal disorders in patients with chronic CVD and DM2.
Material and methods. 102 people were explored. The first group consisted of 72 patients with CVD: 35 with DM2, 37 without DM2. The age of patients with type 2 diabetes was 65 [58; 70] years, and 62 [58; 66] years without type 2 diabetes. The second group included 30 individuals aged 63 [58; 64] years without CVD. Clinical and neurological research, neuropsychological testing, biochemical blood test and magnetic resonance imaging (MRI) of the brain were performed.
Results. The presence of type 2 diabetes was associated with a higher incidence of cognitive impairment (CI) (57 vs 27%), as well as with worse neuropsychological testing results. The presence of DM2 in patients with CVD was accompanied by higher levels of the triglycerides/glucose index (TGI) and advanced glycation end-products (AGEs) and lower values of adiponectin and irisin. The severity of white matter hyperintensivity (WMH) was greater in patients with DM2. The severity of WMH and CI are associated with high values of TGI and circulating AGEs and lower values of adiponectin and irisin. The concentration of adiponectin in the blood is associated with the severity of brain changes. Thus, the probability of detecting WMH (the second and third stages on the Fazekas scale) and CI increased with an adiponectin level of less than 11.2 and 13.0 mcg/ml, respectively.
Conclusions. The combination of vascular pathology and DM2 is characterized by more pronounced structural changes in the brain and CI. The severity of cognitive disorders and the severity of WMH are associated with the levels of AGEs, TGI, adiponectin and irisin in the blood.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.