Синдром беспокойных ног
- Аннотация
- Статья
- Ссылки
Современные критерии диагностики СБН, предложенные Международной исследовательской группой по СБН, включают четыре облигатных симптома, а также подтверждающие и сопутствующие клинические признаки (табл. 1).
Эпидемиология
Распространенность СБН, по данным различных авторов, составляет от 2 до 15%, он встречается чаще у лиц среднего и пожилого возраста, причем у мужчин реже, чем у женщин [1, 2]. В США в ходе телефонного опроса 1800 человек было выявлено, что в течение 5 и более ночей в месяц симптомы, характерные для СБН, испытывали 3% опрошенных в возрасте 18–29 лет, 10% – в возрасте 30–79 лет и 19% – в возрасте 80 лет и старше [3]. Наиболее крупное эпидемиологическое исследование, также проведенное посредством телефонного анкетирования более 23 000 жителей Германии, Франции, Великобритании, Испании и США, выявило распространенность симптомов СБН у 11,1% респондентов. При этом еженедельные симптомы отмечались в 9,6% случаев, а у 2,4% больных они оказывали существенное негативное влияние на качество жизни. Поскольку пациенты преимущественно обращались с жалобами на нарушения сна и не всегда акцентировали внимание врача на неприятных ощущениях в ногах и потребности в совершении движений ногами, только в 12% случаев им был поставлен правильный диагноз [1]. Хотя частота СБН увеличивается с возрастом, он наблюдается и у детей. Эпидемиологическое исследование более 10 тыс. семей выявило признаки СБН, отвечающие международным критериям, у 2% детей в возрасте от 8 до 17 лет [4]. Некоторые исследователи считают, что СБН у детей может быть связан с синдромом дефицита внимания и гиперактивности. В настоящее время нет единого мнения, являются ли эти два состояния коморбидными или они имеют общий патогенез [5, 6].
Этиология
В тех случаях, когда СБН возникает в отсутствие какого-либо другого неврологического или соматического заболевания, диагностируют первичный, или идиопатический, СБН. Если же СБН развивается на фоне другого заболевания, речь идет о вторичном (симптоматическом) синдроме. Обе эти формы встречаются с приблизительно равной частотой. Идиопатический СБН, как правило, дебютирует в молодом возрасте – 20–40 лет. По данным различных авторов, в более чем половине случаев первичного СБН выявляется положительный семейный анамнез, что указывает на роль генетического фактора. Анализ семейных случаев свидетельствует об аутосомно-доминантном типе наследования с высокой пенетрантностью гена. В настоящее время выявлена связь СБН с 8 генетическими локусами на разных хромосомах, однако говорить об определенном генетическим дефекте, ответственном за развитие заболевания, пока нельзя [6]. У пациентов с идиопатическим СБН отмечается более медленный темп прогрессирования. Симптоматический СБН развивается обычно после 50 лет, его причины могут быть самыми разными. По клиническим проявлениям он мало чем отличается от идиопатического СБН, а закономерности его развития и течения определяются первичным заболеванием. Наиболее частыми этиологическими факторами являются железодефицитная анемия, беременность, почечная недостаточность и полиневропатии.
СБН при железодефицитной анемии. Во многих исследованиях было показано, что недостаток железа (снижение уровня ферритина ниже 40 мкг/л) может стать причиной вторичного СБН. Важно иметь в виду, что недостаток железа не всегда сопровождается клинически выраженной анемией. Кроме того, о дефиците железа в организме более надежно свидетельствует уровень ферритина, а не сывороточного железа. Дефицит железа можно с высокой вероятностью заподозрить у пациентов с уровнем ферритина < 50 нг/мл и достоверно диагностировать, если этот показатель снижается до уровня < 20 нг/мл [3, 7, 8].
СБН при беременности. Во время беременности, чаще всего во втором и третьем триместре, у 10–40% женщин может возникать СБН, который проходит после родоразрешения. В большинстве случаев отмечается сравнительно легкая симптоматика, не требующая проведения лечебных мероприятий. Причины ассоциации между СБН и беременностью точно не известны. Наиболее вероятны гипотезы, связывающие СБН с метаболическими нарушениями, в частности дефицитом железа и фолатов, а также с гормональными изменениями в виде увеличения пролактина, прогестерона и эстрогенов [12, 17, 20].
СБН при почечной недостаточности. СБН отмечается у 15–40% пациентов в терминальной стадии почечной недостаточности, особенно у больных, находящихся на гемодиализе, которые вынуждены во время процедуры проводить несколько часов в состоянии покоя [3, 6]. Диагностика СБН при уремии осложняется наличием коморбидных нарушений, в особенности наличием у этих больных периферической полиневропатии.
СБН при полиневропатиях. Частыми причинами симптоматического СБН являются полиневропатии, как приобретенные (алкогольная, диабетическая, амилоидная, порфирийная и др.), так и наследственные, в том числе наследственная сенсомоторная невропатия 2 типа [7]. СБН встречается при полиневропатиях с преимущественным поражением аксонов и вовлечением в процесс тонких сенсорных волокон. Согласно данным различных авторов, распространенность СБН при полиневропатиях имеет чрезвычайно широкий диапазон – от 5 до 54% [5, 6, 14].
Случаи вторичного СБН также описаны при сахарном диабете, амилоидозе, резекции желудка, недостаточности витамина В12, фолиевой кислоты, тиамина, магния, при алкоголизме, хронических обструктивных заболеваниях легких, гипотиреозе и тиреотоксикозе, ревматоидном артрите, болезни Шегрена, порфирии, тяжелой сердечной недостаточности, рассеянном склерозе, поражениях спинного мозга и других заболеваниях [15, 16]. СБН нередко наблюдается у пациентов с болезнью Паркинсона, однако единого мнения о частоте встречаемости до настоящего времени у исследователей нет. Обсуждается вопрос о возможных общих патогенетических механизмах этих заболеваний [17, 18, 19]. Иногда проявления СБН отмечаются у здоровых лиц в период стресса, после интенсивной физической нагрузки, при избыточном потреблении кофеинсодержащих напитков и алкоголя. Вызывать или усиливать СБН могут различные лекарственные препараты, в первую очередь нейролептики, трициклические антидепрессанты, селективные ингибиторы обратного захвата серотонина, препараты лития, нифедипин и другие антагонисты кальция [16].
Патогенез СБН
Патогенез синдрома до конца не изучен. Большинство исследователей сходятся во мнении, что патофизиология СБН тесно связана с дофаминергической дисфункцией, нарушением гомеостаза железа и генетической предрасположенностью. На важную роль дофаминергических систем в развитии СБН указывает усиление симптоматики под влиянием нейролептиков, блокирующих дофаминовые рецепторы, а также средств, блокирующих высвобождение дофамина (резерпиноподобные препараты). В то же время показана высокая эффективность дофаминергических средств (препаратов леводопы и агонистов дофаминовых рецепторов) в лечении СБН. Вероятно, в патогенезе СБН ключевая роль принадлежит дисфункции нисходящих диэнцефально-спинальных дофаминергических путей. Эта система регулирует прохождение сенсорной импульсации через спинной мозг и сегментарные механизмы регуляции движений [3, 16]. Во многих работах выявлена обратная зависимость между уровнем ферритина и выраженностью СБН [8]. Недостаток железа может непосредственно влиять на дисфункцию дофаминергической системы. С одной стороны, железо является кофактором для фермента, участвующего в синтезе дофамина, с другой – входит в состав белка D2‑рецептора. Следовательно, дефицит этого микроэлемента может приводить к нарушению продукции дофамина и чувствительности D2‑рецепторов. Положительный эффект наркотических анальгетиков, стимулирующих опиоидные рецепторы (кодеин, морфин), доказывает роль эндогенных опиоидов в развитии СБН. Терапевтический эффект бензодиазепинов и препаратов вальпроевой кислоты при СБН может свидетельствовать о роли ГАМК-ергических систем в патогенезе заболевания [16]. Несомненно, что дисфункция периферической нервной системы также играет важную роль в развитии симптомов СБН, о чем свидетельствует большая распространенность этого синдрома у больных с полиневропатией. Возможно, что патология периферической нервной системы, а также изменения в спинном мозге из-за патологической афферентации могут вызывать изменения в структурах ЦНС, вовлеченных в развитие СБН [6, 13, 20].
Клиническая картина
Клиническая картина представлена сенсорными и моторными нарушениями, которые имеют определенный суточный ритм. Сенсорные нарушения проявляются в виде патологических ощущений, которые описываются пациентами как зуд, «мурашки», покалывание, жжение, чувство сдавления или распирания и др. Чаще эти ощущения не носят болезненного характера, однако часть пациентов характеризуют их как болевые различной интенсивности. Неприятные ощущения обычно возникают в глубине голеней обеих ног, однако могут быть асимметричными и даже односторонними; иногда при прогрессировании заболевания они распространяются вверх, захватывая бедра, руки и реже туловище. Сенсорные жалобы возникают или усиливаются в покое (в положении лежа, реже сидя). Так как неприятные ощущения уменьшаются при активных движениях, то больные вынуждены либо ходить, либо просто двигать ногами в постели. В некоторых, более легких случаях помогает растирание и массирование ног, принятие горячих или холодных ванн, одевание теплых носков. Симптомы СБН имеют четкий суточный ритм, возникая или усиливаясь в вечерние и ночные часы. В типичных случаях симптомы достигают максимальной выраженности в период с 0 до 4 часов утра, минимальной выраженности – с 6 до 12 часов утра. Некоторые пациенты испытывают легкие проявления СБН и в дневные часы в случае длительного физического покоя. В тяжелых случаях и при длительном течении заболевания характерный суточный ритм исчезает, и симптомы становятся постоянными. В подобных случаях больные испытывают трудности при посещении кино, театра, длительных перелетах и поездках на автомобиле. В связи с неприятными ощущениями в конечностях и необходимостью постоянно совершать движения больные долгое время не могут заснуть. Более 90% пациентов жалуются на трудности засыпания или тревожный сон с постоянными пробуждениями. СБН является четвертой по частоте причиной развития бессонницы [7, 8]. Трудности засыпания и пробуждения, дневная сонливость ведут к раздражительности, снижению концентрации внимания, общей слабости и утомляемости. На фоне вышеуказанных нарушений у многих пациентов вторично развиваются тревога и депрессия [1, 14, 21]. Взаимоотношения между СБН и этими эмоциональными расстройствами достаточно сложны и широко обсуждаются в литературе. С одной стороны, СБН может способствовать развитию депрессии благодаря своему негативному влиянию на сон. С другой стороны, лечение антидепрессантами пациентов с легкими проявлениями СБН может усилить проявления последнего.
Фрагментация сна может быть обусловлена не только неприятными ощущениями и связанной с ними двигательной активностью, но и с периодическими движениями конечностей во сне (ПДК), возникающими у большинства пациентов с СБН. ПДК представляют собой ритмичные движения, которые продолжаются от 0,5 до 5 секунд и повторяются с равномерными интервалами каждые 20–40 секунд. Эти стерео-типные движения в типичных случаях проявляются тыльным сгибанием стопы и разгибанием большого пальца, что может напоминать рефлекс Бабинского. Иногда сгибание наблюдается также в коленном и тазобедренном суставах, в отдельных случаях – в локтевом. Как правило, ПДК преобладают в первой половине ночи. В тяжелых случаях движения не прекращаются всю ночь и даже могут наблюдаться в состоянии бодрствования. ПДК не являются облигатным признаком СБН, тем не менее они наблюдаются приблизительно у 80% пациентов. В тех случаях, когда двигательная активность не является причиной ночных пробуждений, больные могут даже не подозревать о наличии у них ПДК и узнают о них от родственников, либо они выявляются при полисомнографическом исследовании. Полисомнография является надежным диагностическим тестом для выявления подобных нарушений, при этом для количественной оценки был предложен индекс ПДК, который равен количеству движений за один час сна. Индекс ПДК используется для диагностики и оценки тяжести СБН, а также для контроля эффективности лечения. Синдром периодических движений в конечностях диагностируется в том случае, когда при полисомнографии регистрируется более 5 типичных движений в час. Количество ПДК соответствует тяжести СБН [22, 23]. ПДК могут наблюдаться при синдроме апноэ во сне, нарколепсии, беременности, железодефицитной анемии, уремии, диабете, других соматических и неврологических заболеваниях. Кроме того, ПДК могут представлять собой самостоятельный вариант парасомнии.
Таким образом, нарушения сна при СБН связаны не только с типичными проявлениями самого синдрома, но и с наличием ПДК. В некоторых случаях у пациента не возникает проблем при отходе ко сну, но, просыпаясь ночью из-за ПДК, он может испытывать трудности с повторным засыпанием из-за проявлений СБН.
Дифференциальный диагноз
Проводя дифференциальную диагностику, в первую очередь необходимо определить, страдает пациент СБН или другим заболеванием с подобными симптомами (акатизией, ночными крампи, полиневропатией, сосудистой патологией нижних конечностей, гипнической миоклонией, синдромом «болезненные ноги – движущиеся пальцы»). При акатизии отсутствуют сенсорные нарушения, а моторная активность связана с чувством внутренней потребности двигаться или менять позу. Для акатизии нетипична приуроченность к ночному времени, она обычно встречается у больных, длительно получавших нейролептики. Ночные крампи характеризуются внезапными, болезненными сокращениями мышц голени, обычно односторонними. При этом пальпаторно определяется уплотненная мышца. При сосудистой патологии нижних конечностей часто наблюдаются кожные изменения, изменение температуры конечности и ослабленный периферический пульс. Кроме того, симптомы ослабевают при отдыхе и усиливаются во время двигательной активности. Синдром «болезненные ноги – движущиеся пальцы» характеризуется интенсивной, жгучей болью с медленными атетоидными движениями в пальцах стопы [16]. При нем также отсутствует суточный ритм, и боли не облегчаются движением.
Наиболее часто приходится проводить дифференциальную диагностику СБН и полиневропатии. Это нередко вызывает трудности, так как на фоне текущей невропатии может наблюдаться развитие вторичного СБН. Сенсорные проявления невропатии иногда схожи с таковыми при СБН, но они не вызывают вынужденной двигательной активности, не облегчаются при движениях и не имеют суточного ритма. Для исключения вторичных причин СБН необходимо провести полное неврологическое и соматическое обследование. Для выявления железодефицитных состояний нужно определить уровень ферритина в сыворотке крови. Ввиду значительной частоты у пациентов с СБН полиневропатий различного генеза в целях диагностики следует выполнить электронейромиографию и установить скорость проведения по двигательным и чувствительным волокнам. Если установлен диагноз полиневропатии, следующий шаг – поиск ее причины, проведение биохимического анализа крови для исключения диабета и почечной недостаточности. Полисомнография с оценкой сна и подсчетом индекса PLMS используется в основном при дифференциальной диагностике с другими парасомниями, в научных исследованиях и для объективной оценки эффективности лечения. Для рутинной диагностики СБН полисомнография не является обязательной.
Лечение
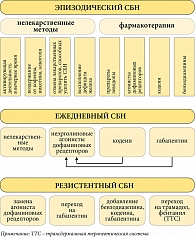
Несмотря на достаточно высокую распространенность СБН, у большинства пациентов проявления эпизодические и умеренные, не требующие врачебной помощи. Тем не менее от 15 до 20% пациентов испытывают частые и выраженные симптомы, приводящие к ухудшению качества жизни [24]. Именно для этой категории больных важную роль играет раннее установление диагноза и подбор адекватной терапии. При выборе терапии необходимо учитывать возраст пациентов (например, нежелательно применение бензодиазепинов у пожилых больных в связи с риском ухудшения когнитивных функций); частоту и регулярность симптомов (эпизодическое применение препаратов или постоянная терапия); выраженность симптомов и наличие болей (при тяжелом течении СБН, сопровождающемся болевыми проявлениями, могут потребоваться опиоиды) (рис. 1). В случае диагностики вторичных форм СБН необходимо проводить лечение основного заболевания (полиневропатии, уремии, дефицита железа и т. д.), приводящего к его развитию.
Немедикаментозная терапия достаточно эффективна при СБН и включает следующие рекомендации:
- умеренная физическая нагрузка в течение дня;
- соблюдение гигиены сна;
- ограничение приема пищи на ночь;
- исключение крепкого чая, кофе и других кофеинсодержащих продуктов (кока-кола, шоколад), алкоголя перед сном;
- отказ от курения;
- принятие горячих (реже холодных) ванн для ног;
- интенсивное растирание ног перед сном;
- умственная активность, требующая значительного внимания (видеоигры, рисование, дискуссии, работа за компьютером и т. д.);
- физиотерапевтические процедуры (магнитотерапия, лимфопресс, массаж, грязи и т. д.), однако их эффективность индивидуальна.
При необходимости медикаментозного лечения СБН дозы лекарственных препаратов повышают постепенно до достижения эффекта (метод титрования дозы). В случае необходимости могут комбинироваться препараты с различным механизмом действия. Как правило, терапевтические дозировки для лечения СБН значительно меньше, чем при использовании препарата по стандартным показаниям. Дофаминергическая терапия наиболее эффективна, она приводит к улучшению состояния более чем у 90% больных. В 80‑х годах прошлого столетия были проведены исследования, показавшие эффективность препаратов леводопы при СБН у 85% пациентов. Препараты леводопы достаточно быстро способствуют регрессу симптомов, однако короткий период полувыведения стандартных препаратов леводопы не обеспечивает длительного облегчения. Нередко отмечается рикошетное усиление симптомов во второй половине ночи и в утренние часы [1]. При длительном использовании лекарств данной группы необходимо помнить о феномене аугментации – усилении признаков СБН в процессе терапии, что проявляется более ранним возникновением, усилением и распространением симптомов на проксимальные отделы ног и даже рук. Данный побочный эффект может возникнуть вскоре после начала лечения препаратами леводопы, спустя несколько месяцев до 80% пациентов ощущают усиление симптоматики [25]. В настоящее время препаратами выбора при СБН являются агонисты дофаминовых рецепторов (АДР), которые по эффективности не уступают препаратам леводопы, но гораздо реже могут вызвать развитие аугментации. Наиболее изученным препаратом этой группы является неэрголиновый АДР – прамипексол. Преимуществом этого лекарственного средства является прежде всего эффективность в минимальных дозах (0,125–0,5 мг вечером). Согласно данным нескольких крупных рандомизированных исследований, прамипексол хорошо переносится, его эффективность не падает на протяжении длительного времени, улучшаются не только субъективные сенсорные проявления, но и объективные параметры сна, в том числе значительно уменьшается индекс ПДК при полисомнографическом исследовании [20]. Как было указано выше, у пациентов с СБН нередко развивается депрессия. В связи с тем, что прамипексол обладает антидепрессивными свойствами, его применение у данных пациентов особенно оправдано [20, 21]. Бензодиазепины могут применяться при наличии толерантности к другим группам препаратов, а также при выраженных нарушениях сна. Наиболее часто применяемые бензодиазепины – клоназепам, алпразолам. Из побочных эффектов отмечаются дневная сонливость и риск возникновения когнитивных нарушений, особенно у пожилых пациентов. Эффективность антиконвульсантов (карбамазепин, габапентин, ламотриджин) в целом умеренна, их назначение возможно в случае неэффективности дофаминергической терапии. Они могут быть полезны при сочетании СБН и периферической нейропатии, а также если пациенты описывают свои ощущения как боль. Из побочных эффектов отмечается тошнота, головокружение, избыточная седация. В тяжелых, трудноизлечимых случаях возможно применение опиатов (кодеин, трамадол). В число побочных эффектов, связанных с приемом опиатов, входят головокружение, тошнота и рвота, запоры, задержка мочи и изредка – кардиальные проблемы (ортостатическая гипотензия, аритмии, тахи- и брадикардии). Привыкание, лекарственная зависимость и синдром отмены отмечаются реже, чем при использовании высоких доз, однако необходимо учитывать возможность развития данных серьезных осложнений. Пациентам со сниженным уровнем ферритина (менее 45 мкг/л) необходимо назначать сульфат железа по 325 мг внутрь 3 раза в день (около 100 мг элементарного железа). В течение нескольких месяцев эта терапия позволяет восстановить запасы железа (следует поддерживать уровень ферритина более 50 мкг/л) и уменьшить или устранить проявления СБН. При дефиците фолиевой кислоты также требуется соответствующая заместительная терапия.
Заключение
СБН – широко распространенное неврологическое заболевание, которое достаточно редко диагностируется. Диагностика не требует сложных и трудоемких исследований и базируется на клиническом анализе симптомов, выявляемых у пациента. Практикующему врачу необходимо помнить о существовании данного заболевания и тщательно анализировать жалобы больного на нарушения сна, необычные сенсорные ощущения в ногах и т. д. СБН является излечимым заболеванием, следовательно, ранняя диагностика и рационально подобранная терапия могут значительно улучшить качество жизни большинства пациентов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.