Состояние минеральной плотности костной ткани у пациентов с малотравматичными переломами в пожилом возрасте: как повысить приверженность лечению
- Аннотация
- Статья
- Ссылки
Остеопороз (ОП) является хроническим заболеванием скелета. Для ОП характерно повышение риска малотравматичных переломов (МП) вследствие снижения прочности костной ткани. Прочность кости характеризуется двумя основными параметрами – минеральной плотностью костной ткани (МПК) и качеством кости. Необходимо понимать: выявленное при денситометрическом обследовании снижение МПК не является единственным признаком, указывающим на ОП. Качество кости, которое в настоящее время не может быть определено в рутинной медицинской практике, имеет важное значение, когда речь идет о прочностных характеристиках костной ткани. В этой связи можно предположить, что в реальной клинической практике имеет место гиподиагностика ОП, так как перенесшим МП пациентам этот диагноз не ставится без денситометрического подтверждения снижения МПК.
В настоящее время МП рассматривают как один из основных независимых факторов риска возникновения последующих переломов. Так, например, известно, что наличие перелома позвонка в анамнезе повышает риск последующего перелома этой же локализации в 4 раза, а МП любой локализации увеличивает риск возникновения следующего перелома в 2,2 раза [1, 2]. На риск возникновения МП влияет также низкая МПК. В исследовании M.R. McClung и соавт. продемонстрировано, что у пациенток с низкой МПК и переломом позвонка в анамнезе риск перелома шейки бедра увеличивается в 2 раза в возрасте после 70 лет [3].
Предупреждение возникновения малотравматичных переломов является основной целью медикаментозной терапии ОП. Процесс лечения всегда длительный, а полноценный эффект противоостеопоротических препаратов зависит от тщательности соблюдения рекомендаций по их приему. К сожалению, ОП входит в число тех хронических заболеваний, при которых недостаточное выполнение рекомендаций по лечению или преждевременное его прерывание имеет тяжелые последствия, названные экспертами ВОЗ «мировой проблемой огромной значимости». В отчете ВОЗ, посвященном лечению хронических заболеваний, указано, что пациенты тщательно выполняют врачебные рекомендации в течение длительного времени не более чем в 50% случаев [4]. Низкая приверженность лечению, уменьшающая эффективность противоостеопоротических препаратов, сводит к минимуму все усилия, направленные на профилактику возникновения МП. Например, в исследовании, проведенном J.R. Curtis и соавт., было продемонстрировано, что у больных с комплаентностью менее 50% по сравнению с пациентами, приверженность лечению которых достигала 90%, риск переломов возрастал на 40% [5].
МП являются не только серьезным осложнением ОП, требующим длительного дорогостоящего лечения, но и в значительной мере снижают качество жизни (КЖ) пациентов. Понятие КЖ в настоящее время рассматривается в медицине как отражение воздействия патологического процесса на человека. Кроме того, динамика КЖ служит для оценки эффективности лечения. ОП, как и другие хронические заболевания, ухудшает качество жизни, особенно в случае возникновения МП. Так, по данным KOFOR – шведского исследования качества жизни пациентов с остеопоротическими переломами трех локализаций (позвонков, проксимального отдела бедра и дистального отдела предплечья), КЖ резко снизилось после МП любого типа, а через 12 месяцев восстановление КЖ до «допереломного» уровня произошло только при наиболее легком варианте МП – переломе дистального отдела предплечья. При переломах проксимального отдела бедра и позвонков КЖ оставалось значительно сниженным, причем хуже всего оно восстанавливалось при переломах позвонков [6].
Целью нашего исследования являлось изучение приверженности лечению женщин постменопаузального возраста, перенесших малотравматичные переломы, частоты остеопороза с учетом определения минеральной плотности костной ткани в различных отделах скелета.
Материал и методы исследования
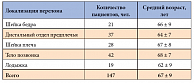
В исследование включены 172 женщины, перенесшие МП в возрасте 50 лет и старше (средний возраст 66 ± 8 лет). Распределение пациенток в зависимости от локализации перелома представлено в таблице 1. Cреди женщин всех групп достоверной разницы в возрасте выявлено не было.
Все пациентки были проанкетированы сразу после перенесенного перелома и через 4 и 12 месяцев с помощью унифицированного вопросника, в котором отмечалась получаемая терапия, сроки ее назначения и длительность приема. Для оценки КЖ использовался вопросник состояния здоровья EQ-5D. Денситометрическое обследование проведено у 147 человек (средний возраст 67 ± 9 лет) на аппарате Discovery A (Hologic) в трех областях: в поясничном отделе позвоночника, проксимальном отделе бедренной кости и дистальном отделе предплечья недоминантной руки.
Статистическая обработка полученных данных проводилась с использованием пакета прикладных программ Statistica 6,0 StatSoft.
Результаты и обсуждение
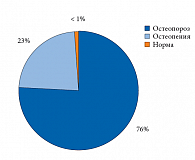
Проведенное денситометрическое обследование женщин с МП различной локализации показало, что ОП хотя бы в одной из областей измерения был выявлен у 76% больных, а остеопения – у 23% обследованных. Нормальные показатели МПК во всех трех отделах были зафиксированы менее чем в 1% случаев – у одной пациентки в возрасте 51 года с продолжительностью постменопаузы 1,5 года (рис. 1).
Среди обследованных ОП чаще выявлялся в поясничном отделе позвоночника и дистальном отделе предплечья (у 53% и 61% пациентов соответственно), а остеопения – в 34% и 33% соответственно. В проксимальном отделе бедра в большем количестве случаев была зафиксирована остеопения – 56%, а ОП – только у 30% больных.
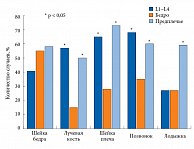
Нами была проанализирована частота ОП в различных областях измерения в зависимости от локализации перелома (рис. 2). Так, при переломах проксимального отдела бедра ОП чаще выявлялся в костях предплечья и бедра (у 56% и 58% женщин), а в позвоночнике ОП был зафиксирован несколько реже – у 41% обследованных лиц с данным видом перелома.
Интересно, что при переломах лучевой кости, шейки плечевой кости и позвонков остеопороз выявлялся примерно с одинаковой частотой как в позвоночнике, так и в предплечье и встречался достоверно чаще, чем в проксимальном отделе бедра. Наиболее часто ОП был отмечен у женщин, перенесших перелом шейки плечевой кости: его частота в дистальном отделе предплечья составила 75%, в позвоночнике – 64%. Аналогичные показатели при переломах позвонков зафиксированы на уровне 67% и 60% соответственно, а при переломах дистального отдела предплечья – 56% и 50% соответственно.
При переломах лодыжки снижение МПК более чем на 2,5 стандартных отклонения (СО) Т-критерия выявлено в 2 раза чаще в области предплечья, чем в поясничном отделе позвоночника и проксимальном отделе бедра (59%, 26% и 26% соответственно). Следует отметить, что при этом типе переломов средний возраст пациентов был наименьшим (61 ± 9 лет). Таким образом, у большинства пациентов с МП была снижена МПК, что требовало назначения противоостеопоротической терапии.
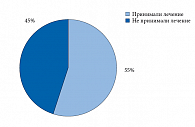
Анализ приема противоостеопоротических препаратов всеми пациентами, перенесшими МП, проводился на основе данных анкетирования, полученных через 12 месяцев после перенесенных МП. В течение этого года начали прием различных препаратов 95 (55%) больных. Среди них только 40 человек (42%) принимали противоостеопоротические препараты в течение всего года наблюдения. 17 (18%) пациентов начали и прервали лечение в течение первых четырех месяцев после перелома, а 38 (40%) начали лечение через 4 месяца и позже (в среднем через 5,8 мес.). Подавляющее большинство лечившихся – 69 (73%) человек – принимали только препараты кальция и витамина D, 8 пациентов (8%) получали кальцитонин, 13 человек (14%) лечились бисфосфонатами (БФ) и 5 женщин (5%) – стронция ранелатом. В то же время 77 (45%) человек не получали никаких противоостеопоротических препаратов в течение всего этого срока после перелома (рис. 3). Среди лиц, не прошедших денситометрическое обследование, терапию получали лишь 32%, в то время как пациенты с исследованной МПК получали терапию в 78% случаев (p < 0,0001). Лечение чаще проводилось у лиц с диагностированным по критериям ВОЗ (Т-критерий < -2,5 СО) ОП в любой из областей измерения. Это может быть связано с тем, что, с одной стороны, врач может обоснованно выписывать препарат по льготному рецепту, а с другой стороны, пациенты получают доказательство необходимости лечения.
В нашем исследовании установлено, что пациенты, принимая препараты патогенетического действия, такие как БФ или стронция ранелат, не всегда дополнительно принимали кальций с витамином D, что может влиять на эффективность терапии. Известно, что у женщин постменопаузального возраста суточное потребление кальция должно составлять 1500 мг [7]. Однако в реальности в средних и старших возрастных группах населения ежедневное употребление кальция с пищей редко превышает 600 мг. Так, по данным исследования, проведенного в ГУ МОНИКИ им. М.Ф. Владимирского, среднее суточное потребление кальция у пациентов пожилого возраста составило 554 ± 285 мг [8]. Результаты ранее проведенного в НИИР РАМН исследования свидетельствуют: женщины в постменопаузе получали с продуктами питания несколько больше кальция (705 ± 208 мг/сутки), однако этот показатель зависел от времени года (летом больше, чем зимой), а также от религиозного календаря (во время православных постов потребление кальция с молочными продуктами у части пациентов снижалось до нуля) [9]. Только 5% лиц ежедневно употребляли достаточное количество кальция. Около 75% получали менее 800 мг в сутки, при этом 22% из них – менее одной трети от рекомендованной нормы. 60% пациентов последовали рекомендациям врачей увеличить поступление кальция с пищей, тем не менее этот показатель увеличился в среднем лишь на 134 мг/сут, чего было явно недостаточно, то есть свыше 60% женщин продолжали получать кальций в количестве менее 800 мг/сутки. Кроме того, кишечная абсорбция кальция у лиц после 60 лет, как правило, снижена по причине недостаточной продукции почками активного метаболита витамина D, а также из-за сопутствующих заболеваний желудочно-кишечного тракта. В то же время во многих исследованиях было патогенетически обосновано и доказано, что оптимальным вариантом для восполнения дефицита кальция и витамина D являются комбинированные препараты, так как каждый из компонентов необходим для полноценного проявления эффекта другого [10]. В этой связи в настоящее время предложено следующее решение данной проблемы – объединить в одной упаковке два вида лекарственных веществ, что может повысить как приверженность пациентов лечению, так и его эффективность. Так, представленный на отечественном фармацевтическом рынке препарат Осталон® Кальций-Д («Гедеон Рихтер», Венгрия) выпускается в виде набора и содержит базисный препарат для лечения ОП – 4 таблетки алендроната по 70 мг для приема 1 раз в неделю, а также 28 таблеток, в состав которых входит по 600 мг кальция и 400 МЕ витамина D, для ежедневного приема. Таким образом, пациент, приобретая одну упаковку, сразу получает комплекс лекарств, необходимых для адекватной терапии ОП.
Одна из наиболее частых локализаций остеопоротических переломов – тело позвонка. Пациенты часто жалуются на острые боли в спине, а отсутствие вовремя начатого лечения может приводить к хронизации боли, вследствие чего КЖ пациентов значительно ухудшается.
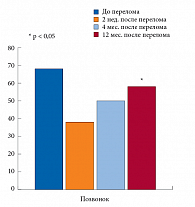
В нашем исследовании мы оценили КЖ пациентов с переломами позвонков в течение двух недель после перелома. Пациентов также просили отметить показатели КЖ до перелома, затем больные повторно опрашивались через 4 и 12 месяцев.
Как видно из данных рисунка 4, резкое ухудшение качества жизни отмечалось сразу после перелома, оно не возвращалось к первоначальному уровню даже через 12 месяцев после МП.
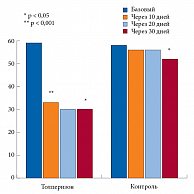
Основной вклад в ухудшение КЖ пациента вносит болевой синдром (БС). По этой причине при переломе позвонка и наличии у больного острой или хронической боли необходимо ее быстрое купирование, что невозможно без применения симптоматических средств, к которым относятся нестероидные противовоспалительные препараты (НПВП) и миорелаксанты. Использование НПВП у пожилых больных часто ограничено в связи с возможными нежелательными явлениями. Многих побочных эффектов, характерных для НПВС, лишены миорелаксанты, применение которых патогенетически обосновано в комплексной терапии БС различного генеза. Представителем этой группы лекарственных средств является Мидокалм – миорелаксант центрального действия, воздействующий на несколько звеньев патогенеза боли [11–15]. Препарат продемонстрировал высокую эффективность в снижении болевого синдрома у больных с ОП (рис. 5). Наш опыт показал, что Мидокалм хорошо переносится – нежелательные явления зафиксированы не были, вследствие чего отмены препарата не потребовалось ни у одного из участников наблюдения [16].
Заключение
В настоящее время пациенты в пожилом возрасте, перенесшие МП, в реальной клинической практике часто остаются без противоостеопоротической терапии, что в большей мере связано с тем, что врачи не назначают лечение лицам, не прошедшим денситометрическое обследование (главный критерий диагноза ОП). В то же время в нашей стране медицинские учреждения не обеспечены необходимым количеством денситометров для обследования всех нуждающихся в этом пациентов. Результаты нашей работы показали: у всех пациентов с МП была снижена МПК, причем в 76% случаев это снижение составляло 2,5 и более стандартных отклонения, что соответствует диагнозу ОП по критериям ВОЗ. Таким образом, врачам в их повседневной практике следует придерживаться клинических рекомендаций, изданных Российской ассоциацией по остеопорозу, в которых на основании зарубежного и отечественного опыта предлагается назначать противоостеопоротическую терапию всем пациентам после перенесенного МП без обязательного измерения МПК. Необходимо помнить, что патогенетическая терапия проводится на фоне адекватного поступления кальция и витамина D с продуктами питания. Кроме того, рекомендуется симптоматическая терапия для снижения болевого синдрома, что позволит улучшить КЖ пациентов после МП.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.