Современная тактика лечения гепатоцеллюлярного рака
- Аннотация
- Статья
- Ссылки

Ежегодно в мире регистрируется до 1000000 новых случаев ГЦР, и погибает от этой болезни ежегодно в мире около 600000 человек (3; 7). Заболеваемость очень высока в странах Восточной Азии. Например, в Монголии – 99 случаев на 100000 населения, в Корее 49 случаев на 100000 населения, в Китае 39 случаев на 100000 населения, в Японии 29 случаев на 100000 населения. В странах Африканского региона, включающего в себя Гамбию, Гвинею, Мали, Республику Мозамбик, заболеваемость колеблется от 11 до 20 случаев на 100000 населения, такая же заболеваемость ГЦР в Италии, Испании, латиноамериканских странах. Заболеваемость колеблется от 5 до 10 случаев на 100000 населения во Франции, Германии и Великобритании. Заболеваемость меньше, чем 5 случаев на 100000 населения в России, США, Канаде, в Скандинавских странах (4; 8; 9). Отмечаются также различия в заболеваемости у лиц разных этнических групп, проживающих в одной стране. Например, афроамериканцы заболевают ГЦР чаще, чем другие жители этой страны. Возможно, это связано с миграцией населения из эндемичных по вирусным гепатитам стран (10; 11).
Заболеваемость ГЦР увеличивается с возрастом, и пик заболеваемости приходится на 65 лет (12; 13). В Северной Америке и Восточной Европе (14) за последние 2 десятилетия пик заболеваемости сместился к 50 годам. В западных странах 90% ГЦР развивается на фоне цирроза печени, а в странах Азии и Африки ГЦР возникает в равной степени как у больных с циррозом печени, так и без него (в литературе ГЦР – «De Novo») (4; 15).
По данным отчетов ВОЗ заболеваемость ГЦР в мире ежегодно растет (2) (таблица 1).
Как очевидно из представленной таблицы, заболевают в основном мужчины, например, из 714600 заболевших в 2002 году ГЦР, 71% заболевших оказались мужского пола. Рост заболеваемости ГЦР, возможно, связан со степенью распространенности вирусных гепатитов В и С. По данным центра контроля заболеваемости в Атланте, заболеваемость гепатитом С на будущее десятилетие составит 8 случаев на 10000 населения (10), следовательно, ожидается дальнейший повсеместный рост заболеваемости ГЦР.
Стадирование
На данный момент в литературе имеется множество различных классификаций ГЦР. Самыми распространенными из них являются: Итальянская (CLIP), Японская (Okuda) и Барселонская (BCLC) классификации.
Барселонская клиническая классификация рака печени (Barcelona Clinic Liver Cancer) была создана на основе результатов, полученных в нескольких рандомизированных когортных исследованиях барселонской группой исследователей, и рекомендована Европейским (EASL) и Американским (AASLD) обществами по изучению болезней печени как стандарт для проведения научных исследований и ведения пациентов ГЦР (16; 17).
В этой классификации стадирование основано на трех основных моментах:
- статус опухоли (размер и количество опухолевых узлов в печени, наличие или отсутствие макроскопически определяемой инвазии сосудов и наличие внепеченочных метастазов);
- функция печени (оценивается по шкале Child-Pugh и портальному давлению);
- соматический статус пациента (оценивается по шкале Eastern Cooperative Oncology Group (ECOG)).
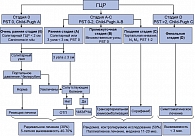
Этиологический фактор в этой классификации не является столь значимым. В Барселонской классификации для каждой из 5 стадий болезни предусмотрены определенные варианты лечения (рисунок 1).
Пациенты солитарным опухолевым узлом менее 2 см и нормальным портальным давлением (стадия 0) являются оптимальными кандидатами на резекцию печени. Следуя этому алгоритму, радикальное лечение можно провести около 30% пациентов со стадиями 0-А. При наличии макроскопически определяемой сосудистой инвазии опухолью метастазов в лимфатические узлы, метастазов в другие органы либо при неудовлетворительном соматическом статусе пациенты определяются в стадию С. Наилучший в настоящее время результат лечения достигается при назначении препарата Нексавар® (сорафениб) – первого и пока единственного препарата, увеличивающего общую и беспрогрессивную выживаемость у данных пациентов.
Лечебная тактика может изменяться при миграции стадии в пределах данной классификации или возникновении противопоказаний к продолжению проводимого лечения.
Лечение ГЦР. Резекция печени
На данный момент основным методом лечения первичного рака печени остается хирургическое. В литературе продолжает обсуждаться вопрос о возможности проведения резекции печени при наличии в ней сопутствующих патологических процессов, выполнения повторных оперативных вмешательств при выявлении рецидивов и метастазов в оставшейся части печени. При невозможности оперативного вмешательства в связи с выраженными сопутствующими заболеваниями или распространенностью опухолевого процесса используется радиочастотная термоаблация, чрескожная инъекция этанола в опухоль, криодеструкция, трансартериальная химиоэмболизация опухоли и системная химиотерапия.
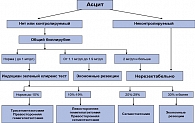
Учитывая, что ГЦР зачастую развивается на фоне цирроза печени, интересным является взгляд японских ученых на проблему хирургического лечения. Выбор оптимальных кандидатов для хирургического лечения основывается на распространенности болезни и функциональных резервов печени, что позволяет сократить количество послеоперационных осложнений и смертность (35, 36). При отборе пациентов ГЦР с сопутствующим циррозом печени для оперативного лечения в Японии придерживаются критериев Makuuchi (37) (рисунок 2). Основными критериями, определяющими возможный объем резекции печени, являются: характеристики асцита, уровень сывороточного билирубина и результаты клиренс-теста индоциан зеленым (ICG R15).
Тест ICG R15 заключается в динамике очищения крови от индоциана зеленого у пациента через 15 мин. после в/в ведения стандартного количества вещества. Клиническое значение этого теста было представлено в результатах исследования Lau с соавт. (38). При проспективном сравнительном анализе, проведенном для выявления лучшего теста, определяющего функциональный резерв печени у пациентов ГЦР, было установлено, что лучшим является тест с индоцианом зеленым. При оценке функции печени перед выполнением резекции печени восточные исследователи ориентировались на классификацию Чайлд и индоциановый тест, западные центры – на биохимические показатели и классификацию Чайлд. При анализе послеоперационных результатов установлено, что п/о осложнения возникали одинаково часто, однако п/о смертность была больше у западных врачей, а 5-летняя выживаемость лучше у восточных (39; 43).
Тромбоз ветвей портальной вены
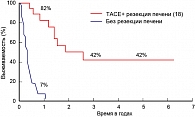
Тромбоз ветвей портальной вены является одним из самых плохих прогностических признаков (44; 47). Медиана выживаемости этих больных составляет 2,7 мес., в то время как без портального тромбоза медиана составляет 24,7 мес. (34). Minagawa с соавт. сообщает, что предоперационная трансартериальная химиоэмболизация у больных ГЦР с тромбозом воротной вены приводит к увеличению сроков выживаемости пациентов, если в печени не более 2 узлов, ствол воротной вены не оклюзирован опухолевым тромбом и темп снижения индоциана зеленого за 15 мин. более 20%. Цель химиоэмболизации – прервать быстрый рост опухолевого тромба. При таком подходе к лечению этого контингента однолетняя выживаемость составила 82%, 3- и 5-летняя – 42%, тогда как без операции однолетняя выживаемость составила 7% (48) (рисунок 3).
Повторные резекции печени
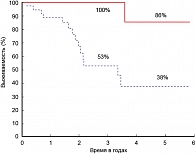
Частота рецидивов в течение 5 лет наблюдения после резекции печени по поводу ГЦР, по данным разных авторов, колеблется от 77 до 100% случаев. Рецидив заболевания в сочетании с вирусными гепатитами становится основной причиной смерти больных. Оптимальным методом лечения рецидивов опухоли является повторная резекция печени (49; 50). Исследователи из Японии рекомендуют выполнять повторные резекции печени пациентам, у которых первичная резекция печени выполнялась по поводу солитарного узла, рецидив развился не ранее, чем через 1 год после первой операции и опухоль не затрагивает воротную вену. При соблюдении вышеуказанных условий 5-летняя выживаемость после повторной резекций составила более 80%. При определении показаний к повторным резекциям печени, аналогичным с показаниями к первичной резекции, 5-летняя выживаемость составила менее 40% (51) (рисунок 4).
Анатомические резекции
В 1985 году Makuuchi предложил собственную методику анатомических резекций печени «УЗИ-контролируемые сегментэктомии» (58). Эта техника проста и широко распространена в мире (59; 65). Методика: под контролем интраоперационного УЗИ выполняется пункция необходимой ветви воротной вены, вводится красящее вещество, и по границе прокрашивания паренхимы намечается линия резекции печени. Такие резекции печени при ГЦР теоретически исключают внутрипеченочные гематогенные метастазы и позволяют надеяться на наилучшую безрецидивную выживаемость больных.
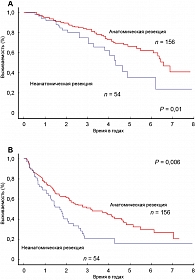
Makuuchi и соавт. проанализировали результаты разных вариантов лечения (рисунок 5). В группе пациентов ГЦР после «анатомических» резекций общая 5-летняя выживаемость составила 66%, после «неанатомических» резекций – 35%, безрецидивная выживаемость также достоверно возросла у пациентов из I группы. При этом автор отмечает, что послеоперационная летальность в этих группах сопоставима. Аналогичные результаты получены при других ретроспективных исследованиях (64; 66).
Эмболизация воротной вены
Предоперационная эмболизация воротной вены (ЭВВ) преследует цель гипертрофии печени и уменьшения кровопотери (67). Японский исследователь для того, чтобы показать значимость методики проанализировал 51 случай эмболизации правой ветви воротной вены перед резекцией печени (68). Через 20 дней после эмболизации значение индоцианового теста улучшилось на 4,3%, а левая доля печени увеличилась на 8% (68). Все пациенты перенесли процедуру удовлетворительно. Функция печени восстановилась в течение 1 недели. Послеоперационные осложнения и летальность в этой группе оказались такими же, как и у пациентов без эмболизации. Общая 5-летняя выживаемость группы составила 44%.
Для некоторых пациентов ГЦР, нуждающихся в обширной резекции печени, ЭВВ является необходимой предоперационной процедурой. Также ЭВВ позволяет сократить операционную кровопотерю и отказаться от трансфузии препаратов крови, что, по мнению ряда авторов, увеличивает сроки безрецидивной выживаемости (55, 57).
Трансплантация
В настоящее время трансплантация печени рассматривается как стандарт лечения у пациентов с ранними стадиями ГЦР и сопутствующим циррозом или другими запущенными болезнями печени (52, 53). Трансплантация печени уменьшает риск внутрипеченочного прогрессирования болезни, улучшает функцию органа, позволяет провести максимально полное морфологическое исследование всей печени, позволяет надеяться на увеличение сроков выживания без прогрессирования болезни. Самым большим недостатком трансплантации печени является дефицит донорских органов. Оптимальные кандидаты на трансплантацию определены в 90-х годах – единичный узел менее 5 см или 3 узла, но не более 3 см каждый, без выхода опухоли за пределы печени и сосудистой инвазии (54). Общая 5-летняя выживаемость больных ГЦР с сопутствующим циррозом составляет около 26% после резекции печени и около 65% после трансплантации (34). 5-летняя выживаемость при соблюдении Миланских критериев отбора больных ГЦР на трансплантацию печени, по данным многих центров, составляет более 70% (69; 70). На данный момент рядом исследователей сообщается об аналогичных результатах общей выживаемости у пациентов после трансплантации печени по критериям Университета штата в Сан-Франциско (SFSU) (солитарный узел до 6,5 см, или не более 3 узлов максимальным размером узла 4,5 см и общим размером до 8 см при отсутствии макроскопически определяемой сосудистой инвазии и метастазов опухоли в лимфатические узлы), однолетняя выживаемость составляет более 90%, а 5-летняя – 72% (71). Критерии отбора больных ГЦР на трансплантацию печени продолжают активно изучаться. В своих последних публикациях Мазаферро и соавт. предлагают новую прогностическую модель («до семи» – где семерка либо максимальный размер единичного узла, либо общее количество узлов) в отборе пациентов, чья выживаемость может быть улучшена за счет проведения трансплантации печени (74). 5-летняя выживаемость у данной группы пациентов при отсутствии микроваскулярной инвазии, по данным Мазаферро, составляет 71%, что сопоставимо с результатами трансплантаций при соблюдении Миланских критериев (74). В период ожидания донорского органа для контроля опухолевого процесса может применяться неоадъювантное лечение (ЧЭИ, РЧА, ХЭПА). При сроке ожидания донорского органа более 1 года около 50% больных ГЦР перестают соответствовать критериям для трансплантации органа. При анализе «стоимость-эффективность» метода установлено, что наибольшая эффективность трансплантации достигается при ожидании органа не более 7 мес. (72, 75).
Послеоперационное адъювантное лечение
Резекция печени является основным методом лечения при ГЦР, но частое развитие рецидивов и метастазов опухоли значительно ухудшают результаты такого лечения. Для снижения частоты внутриорганных метастазов необходимо проведение эффективного адъювантного лечения. В настоящее время, анализируя доступную нам литературу, мы не нашли сообщений о статистически доказанной эффективной адъювантной терапии ГЦР. Адъювантное лечение, проводимое после резекции печени и рекомендуемое в литературе, – это трансартериальная химиоэмболизация, ретиноидная терапия, иммуно- и интерферонотерапия. В восьми исследованиях авторы отмечают положительные результаты данных методов лечения (69; 78).
Muto и соавт. докладывают, что прием ретиноидов увеличивает время до прогрессирования. Пероральное лечение полипреноевой кислотой (polyprenoic acid) после резекции печени значительно сокращает случаи рецидивов ГЦР (69).
Lau и соавт. сообщают, что адъювантное внутриартериальное введение iodine-131-lipiodol (131I-lipiodol) сокращает количество локальных рецидивов и увеличивает время безрецидивной и общей выживаемости больных ГЦР после радикальной резекции печени (70). Больные ГЦР после резекции печени, которым проводилась данная адъювантная терапия, выздоравливали в течение 6 недель. Медиана безрецидивного периода у леченых 131I-lipiodol составила 57,2 мес., а в контрольной группе 13,6 мес. Общая 3-летняя выживаемость была соответственно 86,4% и 46,3%. 131I-lipiodol не обладает значимым токсическим эффектом, и его применение у больных ГЦР после резекции печени увеличивает общую и безрецидивную выживаемость больных ГЦР.
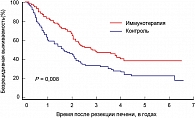
S.Yamazaki и соавт. применяли адаптивную иммунотерапию. Забиралась периферическая кровь пациента, и лимфоциты культивировались в присутствии интерлейкина-2 в течение 2 недель, затем ранее активированные Т-лимфоциты возвращались тому же пациенту (71). Таким образом, было пролечено 143 пациента ГЦР. Результаты представлены в рисунке 6. Иммунотерапия аутологичными лимфоцитами, активированными in vitro с рекомбинантным интерлейкином-2, введенная пятикратно в течение первого месяца после резекции печени, увеличивает сроки до прогрессирования.
Локорегионарное лечение и химиотерапия. Чрескожная абляция
Больным ГЦР, которым не показано выполнение резекции или трансплантации печени альтернативным методом лечения, является чрескожное аблативное воздействие на опухоль. Принцип абляции базируется на деструкции опухолевых клеток путем химического (этанол) или физического (радиоволны, лазер) воздействия, которое может изменять температуру в опухоли и вызывать девитализацию.
Из всех локорегионарных методик наиболее распространена чрескожная этаноловая инъекция (ЧЭИ) (20). При прецизионном отборе больных эффективность ЧИЭ может быть сравнима с хирургическим лечением, 5-летняя выживаемость может достигать 72% (21, 22). Малая частота осложнений и низкая стоимость этой процедуры являются дополнительными преимуществами данного метода. Основными недостатками ЧИЭ являются: необходимость многократных инъекций в разные области опухоли и невозможность достигнуть полного некроза при больших размерах опухоли.
Радиочастотная аблация (РЧА) более эффективна по сравнению с ЧИЭ и позволяет добиться полного некроза опухоли в узлах более 2 см при более редких лечебных вмешательствах (23). РЧА – при помощи энергии радиочастотных волн приводит к термическому повреждению и коагуляционному некрозу опухоли. Исследование показало, что РЧА эффективнее ЧИЭ в отношении достижения полного некроза опухоли (90% против 80%) даже при более редких лечебных манипуляциях (1,2 против 4,8) (24). Осложнения после РЧА (плевральный выпот, кровотечение) возникают чаще, чем после ЧИЭ (24, 25). Эффективность РЧА снижается при размерах опухоли более 3 см (1).
Химиоэмболизация
Химиоэмболизация опухоли применяется перед хирургическим лечением для повышения резектабельности, в период ожидания донорского органа при трансплантации печени или как паллиативное лечение больных ГЦР с сохранной функцией печени только при отсутствии асцита (26). В отличие от опухоли паренхима печени на 85% кровоснабжается из бассейна воротной вены, поэтому эмболизация печеночной артерии (ЭПА) вызывает ишемический некроз опухоли. Введение химиотерапевтических препаратов в печеночную артерию (цисплатин, доксорубицин, адриамицин, митомицин С) вместе с эмболизацией печеночной артерии (ХЭПА) позволяет максимально повысить концентрацию этих веществ в печени, избежать системной токсичности этих препаратов. При сравнении ЭПА и ХЭПА в группе пациентов с ХЭПА опухоль уменьшилась на 61% против 16%. Одногодичная выживаемость пациентов ГЦР при ХЭПА, по данным некоторых авторов, достигает 82% (27, 30).
Системное лечение
Системной химиотерапии ГЦР посвящено много клинических исследований. К сожалению, до недавнего времени ни один препарат или комбинация препаратов не позволяли статистически достоверно увеличивать сроки выживания больных (31). В рандомизированных, контролируемых клинических исследованиях тамоксифен, октреотид, интерферон, интерлейкин-2 не показали достоверной эффективности при ГЦР (32). Углубленное изучение молекулярной биологии ГЦР позволило создавать таргетные препараты, которые дают новые надежды в лечении этой болезни (33). Таргетная терапия нацелена на факторы роста, их рецепторы и внутриклеточные сигнальные преобразования, при помощи которых контролируется клеточный цикл. Полученные положительные результаты при изучении ингибитора рецепторов тирозинкиназ – сорафениба (Нексавар®), позволили рекомендовать его для лечения ГЦР (79). Нексавар® проявляет ингибиторную активность в отношении нескольких киназ (VEGF, PDGF, c-kit receptor, Raf), затрудняя тем самым пролиферацию опухолевых клеток (т.е. рост опухоли), а также нарушает ангиогенез (т.е. кровоснабжение опухоли) и т.д.
Заключение
Хирургическое лечение гепатоцеллюлярного рака требует точной предоперационной оценки функционального резерва печени. У пациентов с сопутствующим циррозом печени возможно использование алгоритма Макуучи. Общая 5-летняя выживаемость после резекции печени по поводу ГЦР в крупномасштабных исследованиях составляет около 50%, однако результаты безрецидивной выживаемости остаются неудовлетворительными. В настоящее время, анализируя доступную нам литературу, мы не нашли сообщений о статистически доказанной эффективной адъювантной терапии ГЦР. В лечении рецидивов болезни наиболее часто применяются повторные резекции печени, трансартериальная химиоэмболизация, методы локальной аблации.
Трансплантация печени имеет два преимущества: удаляются первичная опухоль и измененная печень, как возможное место для рецидива. Трансплантация становится методом выбора в лечении пациентов ГЦР и запущенной стадией сопутствующего заболевания печени.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.