количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Современные стратегии терапии атипичных лицевых болей
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Неврология и Психиатрия" №3 (32)
- Аннотация
- Статья
- Ссылки
- English
В статье приведены результаты исследования эффективности комбинированной обезболивающей и противотревожной терапии у пациентов с атипичными лицевыми болями.
Показано, что комплексное применение нестероидных противовоспалительных препаратов в сочетании с анксиолитиками (Тенотен) способствовало более выраженному снижению болевого синдрома за счет стабилизации эмоционального фона и позволяло быстрее улучшить состояние больных и повысить их качество жизни.
В статье приведены результаты исследования эффективности комбинированной обезболивающей и противотревожной терапии у пациентов с атипичными лицевыми болями.
Показано, что комплексное применение нестероидных противовоспалительных препаратов в сочетании с анксиолитиками (Тенотен) способствовало более выраженному снижению болевого синдрома за счет стабилизации эмоционального фона и позволяло быстрее улучшить состояние больных и повысить их качество жизни.

Рис. 1. Динамика уровня боли по ВАШ в основной группе (НПВП + Тенотен) и группе сравнения (НПВП) через 10 дней от начала терапии (средний балл по группам)

Рис. 2. Динамика уровня тревоги по шкале Гамильтона по группам (средний балл по группам)
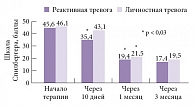
Рис. 3. Динамика уровня реактивной и личностной тревоги по шкале Спилбергера в основной группе
Актуальность проблемы
Атипичные лицевые боли в структуре всех болевых синдромов занимают обособленное место ввиду их специфичности. Прозопалгии ассоциируются с высокой частотой рецидивов, риском формирования хронической боли. Результаты эпидемиологических исследований свидетельствуют о том, что наряду с болевыми синдромами различной локализации и головными болями атипичные лицевые боли являются одной из причин утраты трудоспособности. Следует отметить, что в основном прозопалгиями страдают женщины трудоспособного возраста (от 27 до 50 лет). Кроме того, диагностика и лечение атипичных болевых синдромов характеризуются значительными материальными затратами как на амбулаторную, так и на стационарную помощь. Это связано с тем, что традиционное обследование не позволяет выявить причину боли и диагностика прозопалгии представляет определенные затруднения на догоспитальном этапе.
Кроме того, атипичные лицевые боли имеют тенденцию к хронизации и протекают на фоне психологического дискомфорта, социальной дезадаптации, длительных эмоциональных переживаний, стрессов (а порой являются причиной возникновения болевого синдрома), что повышает расходы на проводимое лечение. При этом, как свидетельствуют результаты фармакоэкономических исследований, объемы этих затрат постоянно возрастают. Анализируя долю прозопалгий среди всех болевых синдромов в популяции и связанные с ними материальные затраты, следует учитывать, что часть больных по ряду обстоятельств не обращаются за медицинской помощью, предпочитая советоваться с родственниками, близкими людьми, ищут помощь на интернет-форумах. Это искажает представление о реальных затратах на лечение данного контингента больных в популяции [1–2].
Патогенез дисфункциональных болей
Из всех прозопалгий 75% составляют болевые синдромы, вызванные мышечно-тоническим и дисфункциональным компонентами [3]. При этом сам термин «дисфункциональная боль» является дискутабельным, поскольку граница между «функциональным» и «органическим» становится все призрачнее.
Понимание патогенеза дисфункционального болевого синдрома лица имеет чрезвычайно важное значение для проведения адекватной терапии. Главное отличие дисфункционального типа боли от ноцицептивной и нейропатической заключается в том, что традиционное обследование не позволяет выявить причину боли или органические заболевания, которые могли бы ее вызвать. Решающее значение в патогенезе дисфункциональной боли имеют не органические заболевания или повреждения, а психологические, социальные факторы и эмоциональный стресс. Именно они играют ключевую роль в нарушении адекватной работы нисходящих норадренергической и серотонинергической систем, в результате чего обычные неболевые стимулы начинают восприниматься как болевые. Кроме того, в специальных исследованиях продемонстрировано, что дисфункциональный компонент боли может развиться у части больных при длительно персистирующих периферических болевых синдромах.
Причинно-следственные соотношения хронической дисфункциональной боли и психогенных факторов различны. Длительно существующий болевой синдром вызывает отрицательные эмоции, нарушает сон, ограничивает возможности больного, снижает качество его жизни и, соответственно, может стать причиной формирования тревоги, а впоследствии и депрессивных расстройств. Развитие тревоги при хронической боли чаще происходит у пациентов, преувеличивающих значимость своего заболевания. Присоединяющаяся к боли тревога ухудшает переносимость боли, усиливает ее и способствует ее хронизации. Появление тревоги и депрессии при болевых синдромах может быть спровоцировано лекарственной терапией. Так, длительный прием препаратов с анальгетическим эффектом, в частности нестероидных противовоспалительных препаратов (НПВП), может приводить к формированию тревожно-депрессивной симптоматики.
В настоящее время пересмотрены взгляды на роль психогенных факторов в развитии атипичных прозопалгий [4]. Наиболее характерным клиническим проявлением атипичной прозопалгии дисфункционального генеза является наличие болевого синдрома, не соответствующего расположению ветвей тройничного нерва, отсутствие пароксизмальности и четкой зависимости от провоцирующих факторов (по сравнению с тригеминальной невралгией), отсутствие ответа на стандартную терапию.
Критерии диагностики прозопалгии
При наблюдении пациента с дисфункциональным болевым синдромом, локализующимся в орофациальной области, необходимо исключать наличие тригеминальной невралгии, герпетическое поражение черепных нервов, новообразования лицевого скелета, последствия стоматологических вмешательств челюстно-лицевой зоны, а также демиелинизирующий процесс в головном мозге.
Главное в диагностике атипичных лицевых болей – тщательный сбор анамнеза. К сожалению, параклинические методы диагностики не являются основными и в большинстве случаев не выявляют органического поражения мозга. Однако методы нейровизуализации могут быть рекомендованы в случае усиления болевого синдрома, изменения характера прозопалгии, отсутствия положительного эффекта от терапии.
Наибольшие затруднения испытывает врач, сталкиваясь с хроническим затяжным характером соматизированных депрессий, которые выделяются под названием дистимий. Дистимией называют хроническую невротическую неглубокую депрессию с повышенным тревожным фоном настроения, длящуюся не менее двух лет. Именно при дистимии на первый план в клинической картине часто выходят хронические болевые синдромы различной локализации.
Хроническая боль часто становится самостоятельным заболеванием, являясь единственным симптомом, длительно беспокоящим пациента, и зачастую причину этой боли определить так и не удается, то есть для хронического болевого синдрома свойственно отсутствие прямой связи с органической патологией. Хронической болью страдают в среднем 15–20% общей популяции населения. Известно, что большинство пациентов с тревогой страдают хроническими болевыми синдромами, часто диффузного характера. И наоборот, боль часто ведет к появлению тревожности и напряженности, которые сами по себе способствуют усилению восприятия боли. Любое хроническое заболевание, сопровождающееся болью, влияет на эмоции и поведение человека. Хроническая боль, при которой тревога и депрессия являются основными симптомообразующими факторами, имеет свои особенности [5].
Терапия атипичных лицевых болей
Вероятность развития болевого синдрома, длительность течения и степень его выраженности в значительной степени определяются эмоциональным состоянием больных, о чем было сказано выше, в частности наличием тревожных, депрессивных нарушений, рядом психосоциальных факторов. Некоторые личностные особенности пациента: повышенная тревожность, избыточное чувство ответственности, сниженный эмоциональный фон – играют не последнюю роль в формировании и становлении миофасциального болевого синдрома лица и атипичных лицевых болей дисфункционального генеза. Своевременное распознание этих индивидуальных особенностей, определение их роли в запуске болевого синдрома позволяют выбрать оптимальную рентабельную терапию, сократить сроки лечения, снизить вероятность хронизации боли.
Еще одной характеристикой дисфункционального болевого синдрома является его интенсивность. Выделяют слабые, умеренные и сильные боли. Эта характеристика также учитывается при выборе анальгетической терапии. Для усиления обезболивающего эффекта часто приходится прибегать к комбинированной терапии препаратов различных классов. Принимая во внимание тот факт, что психогенная составляющая в развитии дисфункционального болевого синдрома играет ведущую роль, необходимо воздействие в первую очередь на негативную установку больного на течение заболевания.
Возможности препаратов, регулирующих активность белка S100
Существует взаимосвязь между развитием тревожных, депрессивных и других невротических расстройств и мозгоспецифическим белком S100, который экспрессируется и секретируется клетками микроглии и астроцитами. Белок S100 играет важную роль в реализации основных функций нейронных систем головного мозга, таких как генерация и проведение нервного импульса, регуляция синаптических и метаболических процессов, пролиферация и дифференцировка нейронов и клеток глии. В этой связи перспективным направлением в терапии невротических расстройств является применение препаратов, регулирующих активность белка S100.
Принципиально новым способом регуляторного воздействия представляется использование антител к белку S100. Так, препарат Тенотен содержит релиз-активные антитела к S100. Тенотен модифицирует функциональную активность белка S100, что обеспечивает нейротрофическое действие препарата, способствует восстановлению процессов нейрональной пластичности, препятствует развитию невротических и неврозоподобных состояний. Отсутствие седативного и миорелаксирующего эффекта, сочетаемость с другими препаратами обусловливают перспективность применения препарата для купирования невротических симптомов, сопровождающих различные соматические заболевания. Фармакологические эффекты Тенотена включают также стрессопротективное действие, регуляцию энергетического метаболизма нейронов, влияние на пролиферацию и дифференцировку клеток головного мозга. Кроме того, Тенотен обладает широким спектром психотропной, нейротропной, вегетомодулирующей активности. Взаимодействуя с ГАМК-А-бензодиазепиновым рецепторным комплексом, Тенотен оказывает ГАМК-миметический эффект. Препарат не вызывает заторможенности, дневной сонливости, мышечной расслабленности, зависимости и связанного с ней синдрома отмены даже при длительной терапии, поэтому может быть использован у людей, ведущих активный образ жизни, у людей, в профессии которых требуется особая концентрация внимания, например водителей, работников с точными механизмами и др.
Цель, материал и методы исследования
Целью проведенного исследования было изучение уровня тревожности пациентов с хроническими дисфункциональными болевыми синдромами на примере пациентов с лицевыми болями. В исследовании приняли участие 149 пациентов (43 мужчин и 106 женщин) с хроническими атипичными лицевыми болями в возрасте от 40 до 68 лет. Критерием отбора было наличие атипичной лицевой боли по МКБ-10 (G50.1. Атипичная лицевая боль), определяющейся как персистирующая боль в области лица, не имеющая признаков невралгий черепных нервов и не ассоциированная с объективными симптомами или органическими заболеваниями.
Пациенты были протестированы на наличие признаков тревоги при сборе жалоб и данных анамнеза, а также с помощью специализированных шкал. Всем пациентам проводилась оценка уровня боли и уровня тревожности для определения взаимодействия двух этих параметров. Для оценки уровня болевого синдрома использовалась визуально-аналоговая шкала (ВАШ). Выраженность болевого синдрома в среднем составила 4,6 ± 0,9 балла по ВАШ. Для определения уровня тревоги использовались шкалы Гамильтона и Спилбергера (для уточнения уровня личностной тревожности и реактивной тревоги на момент обследования).
В исследование не включались пациенты с декомпенсированной соматической патологией, острыми респираторными вирусными инфекциями, ранним реконвалесцентным периодом после перенесенных вирусных инфекций, гемодинамически значимыми сосудистыми мальформациями брахиоцефальных сосудов, очаговыми поражениями нервной системы и наличием травматических костных дефектов черепа и шейного отдела позвоночника.
В последующем все пациенты были разделены на две группы: пациенты основной группы (n = 103) получали НПВП (Ксефокам по 8 мг 2 р/сут) в сочетании с анксиолитической терапией (препарат Тенотен по 2 таблетки 3 р/сут), пациенты контрольной группы (n = 46) получали только НПВП. Продолжительность терапии в обеих группах составила 10 дней. При выписке всем пациентам основной группы был рекомендован прием препарата Тенотен в течение 3 месяцев.
Оценка эффективности комбинации обезболивающей терапии и анксиолитиков проводилась в стационаре на 10-й день терапии. Через 1 и 3 месяца после начала приема препарата Тенотен было проведено контрольное тестирование пациентов для оценки уровня тревожности и оценки рецидива болевого синдрома.
Результаты исследования
Анализ возрастных характеристик пациентов, вошедших в исследование, позволяет утверждать, что атипичные лицевые боли встречаются чаще среди лиц трудоспособного возраста (34% в возрасте 40–50 лет, 42% в возрасте 50–60 лет, 24% старше 60 лет). У подавляющего числа лиц (86,7%) с хроническими дисфункциональными болевыми синдромами клинически были выявлены признаки вегетативной дисфункции, проявляющиеся колебаниями артериального давления (67,5%), наличием склонности к тахикардии (64,9%), ярко-красным стойким дермографизмом (52,9%), наличием сосудистого «ожерелья» (17,8%), гипергидрозом ладоней и стоп (53,6%), дискинезией желудочно-кишечного тракта (20,2%), гипервентиляционным синдромом (33,5%), диссомническими расстройствами (19,2%).
При первичном обследовании пациентов с хроническими прозопалгиями с применением шкалы Гамильтона для оценки тревоги был выявлен высокий уровень тревожности. Важно отметить: чем больше была продолжительность заболевания, тем выше был уровень тревожности. Выраженность уровня тревоги по шкале Гамильтона у пациентов составила в среднем 20,75 ± 8,3 балла. Психологическое исследование (с использованием шкалы тревоги Спилбергера) показало наличие выраженных тревожных расстройств у всех пациентов: реактивная и личностная тревога в среднем составили соответственно 45,6 ± 3,4 и 46,1 ± 4,2 балла.
При оценке уровня боли по шкале ВАШ на 10-й день терапии отмечалось снижение боли в обеих группах, но более выраженное уменьшение болевого синдрома отмечалось среди пациентов основной группы (снижение показателей ВАШ до 1,1 ± 1,0 баллов, р < 0,005) в сравнении с контрольной группой (снижение показателей ВАШ до 2,5 ± 1,1 балла, р < 0,03) (рис. 1).
По данным психологического исследования по шкале Гамильтона в основной группе отмечено снижение уровня тревоги с 20,75 ± 8,3 до 18,5 ± 5,6 балла, что составило -11% (р < 0,03), в контрольной группе сохранился практически исходный уровень тревоги – 20,3 ± 5,4 балла. Следовательно, стабилизация эмоционального фона влияет на динамику показателей болевого синдрома (рис. 2).
Данные оценки по шкале Спилбергера на 10-й день терапии в группе пациентов, принимающих препарат Тенотен, свидетельствуют о положительной динамике по шкале реактивной тревоги (35,4 ± 4,3 балла, р < 0,01) и незначительной положительной тенденции по шкале личностной тревоги (43,1 ± 4,5 балла). В группе пациентов контрольной группы показатели реактивной и личностной тревоги остались без изменения.
В дальнейшем через 1 и 3 месяца от начала терапии было проведено дополнительное тестирование данной группы пациентов по шкале тревоги Гамильтона и по шкале реактивной и личностной тревоги Спилбергера.
Через 1 месяц после начала терапии показатели уровня тревоги по шкале Гамильтона в основной группе составили 14,5 ± 5,5 балла, что было меньше на 30% от исходного уровня тревоги (р < 0,03); в контрольной группе уровень тревоги по данной шкале существенно не изменился и составил 19,6 ± 4,6 балла (р < 0,05).
По данным шкалы реактивной и личностной тревоги Спилбергера через месяц была также отмечена выраженная положительная динамика в основной группе (19,4 ± 2,7 и 21,5 ± 3,1 балла соответственно, р < 0,01) и незначительные изменения в контрольной группе (39,4 ± 2,4 и 39,8 ± 3,4 балла соответственно).
Оценка уровня тревоги была проведена и через 3 месяца от начала терапии. Наблюдалась значимая положительная динамика у пациентов, принимающих Тенотен: 13,4 ± 4,2 балла по шкале Гамильтона и 17,4 ± 2,9 и 19,5 ± 3,5 балла по шкале реактивной и личностной тревоги Спилбергера соответственно (рис. 3). В контрольной группе динамика не наблюдалась и показатели остались на уровне предыдущих.
Следует подчеркнуть, что в течение 3 месяцев после проведенной терапии в стационаре у 7 пациентов контрольной группы (16,2%) отмечены рецидивы заболевания, проявляющиеся усилением болевого синдрома, повышением тревожности. В основной группе усиление болевого синдрома не отмечалось.
Выводы
Атипичные лицевые боли в структуре всех болевых синдромов занимают обособленное место ввиду их специфичности. Прозопалгии ассоциируются с высокой частотой рецидивов, риском формирования хронической боли. Результаты эпидемиологических исследований свидетельствуют о том, что наряду с болевыми синдромами различной локализации и головными болями атипичные лицевые боли являются одной из причин утраты трудоспособности. Следует отметить, что в основном прозопалгиями страдают женщины трудоспособного возраста (от 27 до 50 лет). Кроме того, диагностика и лечение атипичных болевых синдромов характеризуются значительными материальными затратами как на амбулаторную, так и на стационарную помощь. Это связано с тем, что традиционное обследование не позволяет выявить причину боли и диагностика прозопалгии представляет определенные затруднения на догоспитальном этапе.
Кроме того, атипичные лицевые боли имеют тенденцию к хронизации и протекают на фоне психологического дискомфорта, социальной дезадаптации, длительных эмоциональных переживаний, стрессов (а порой являются причиной возникновения болевого синдрома), что повышает расходы на проводимое лечение. При этом, как свидетельствуют результаты фармакоэкономических исследований, объемы этих затрат постоянно возрастают. Анализируя долю прозопалгий среди всех болевых синдромов в популяции и связанные с ними материальные затраты, следует учитывать, что часть больных по ряду обстоятельств не обращаются за медицинской помощью, предпочитая советоваться с родственниками, близкими людьми, ищут помощь на интернет-форумах. Это искажает представление о реальных затратах на лечение данного контингента больных в популяции [1–2].
Патогенез дисфункциональных болей
Из всех прозопалгий 75% составляют болевые синдромы, вызванные мышечно-тоническим и дисфункциональным компонентами [3]. При этом сам термин «дисфункциональная боль» является дискутабельным, поскольку граница между «функциональным» и «органическим» становится все призрачнее.
Понимание патогенеза дисфункционального болевого синдрома лица имеет чрезвычайно важное значение для проведения адекватной терапии. Главное отличие дисфункционального типа боли от ноцицептивной и нейропатической заключается в том, что традиционное обследование не позволяет выявить причину боли или органические заболевания, которые могли бы ее вызвать. Решающее значение в патогенезе дисфункциональной боли имеют не органические заболевания или повреждения, а психологические, социальные факторы и эмоциональный стресс. Именно они играют ключевую роль в нарушении адекватной работы нисходящих норадренергической и серотонинергической систем, в результате чего обычные неболевые стимулы начинают восприниматься как болевые. Кроме того, в специальных исследованиях продемонстрировано, что дисфункциональный компонент боли может развиться у части больных при длительно персистирующих периферических болевых синдромах.
Причинно-следственные соотношения хронической дисфункциональной боли и психогенных факторов различны. Длительно существующий болевой синдром вызывает отрицательные эмоции, нарушает сон, ограничивает возможности больного, снижает качество его жизни и, соответственно, может стать причиной формирования тревоги, а впоследствии и депрессивных расстройств. Развитие тревоги при хронической боли чаще происходит у пациентов, преувеличивающих значимость своего заболевания. Присоединяющаяся к боли тревога ухудшает переносимость боли, усиливает ее и способствует ее хронизации. Появление тревоги и депрессии при болевых синдромах может быть спровоцировано лекарственной терапией. Так, длительный прием препаратов с анальгетическим эффектом, в частности нестероидных противовоспалительных препаратов (НПВП), может приводить к формированию тревожно-депрессивной симптоматики.
В настоящее время пересмотрены взгляды на роль психогенных факторов в развитии атипичных прозопалгий [4]. Наиболее характерным клиническим проявлением атипичной прозопалгии дисфункционального генеза является наличие болевого синдрома, не соответствующего расположению ветвей тройничного нерва, отсутствие пароксизмальности и четкой зависимости от провоцирующих факторов (по сравнению с тригеминальной невралгией), отсутствие ответа на стандартную терапию.
Критерии диагностики прозопалгии
При наблюдении пациента с дисфункциональным болевым синдромом, локализующимся в орофациальной области, необходимо исключать наличие тригеминальной невралгии, герпетическое поражение черепных нервов, новообразования лицевого скелета, последствия стоматологических вмешательств челюстно-лицевой зоны, а также демиелинизирующий процесс в головном мозге.
Главное в диагностике атипичных лицевых болей – тщательный сбор анамнеза. К сожалению, параклинические методы диагностики не являются основными и в большинстве случаев не выявляют органического поражения мозга. Однако методы нейровизуализации могут быть рекомендованы в случае усиления болевого синдрома, изменения характера прозопалгии, отсутствия положительного эффекта от терапии.
Наибольшие затруднения испытывает врач, сталкиваясь с хроническим затяжным характером соматизированных депрессий, которые выделяются под названием дистимий. Дистимией называют хроническую невротическую неглубокую депрессию с повышенным тревожным фоном настроения, длящуюся не менее двух лет. Именно при дистимии на первый план в клинической картине часто выходят хронические болевые синдромы различной локализации.
Хроническая боль часто становится самостоятельным заболеванием, являясь единственным симптомом, длительно беспокоящим пациента, и зачастую причину этой боли определить так и не удается, то есть для хронического болевого синдрома свойственно отсутствие прямой связи с органической патологией. Хронической болью страдают в среднем 15–20% общей популяции населения. Известно, что большинство пациентов с тревогой страдают хроническими болевыми синдромами, часто диффузного характера. И наоборот, боль часто ведет к появлению тревожности и напряженности, которые сами по себе способствуют усилению восприятия боли. Любое хроническое заболевание, сопровождающееся болью, влияет на эмоции и поведение человека. Хроническая боль, при которой тревога и депрессия являются основными симптомообразующими факторами, имеет свои особенности [5].
- Клиническая феноменология болевого синдрома не отвечает критериям ни одного из известных соматических или неврологических заболеваний. Многочисленные диагностические исследования не выявляют текущего органического заболевания, которое могло бы объяснить болевой синдром.
- Важной характеристикой боли является ее длительность. Международная ассоциация боли предлагает считать хронической болью ту боль, которая продолжается сверх нормального периода заживления и длится не менее трех месяцев. В соответствии с критериями DSM-IV предлагается увеличить срок болевого синдрома до шести месяцев. Вопрос об отнесении болевого синдрома к хроническому решается индивидуально, исходя из предшествующей клинической картины и клинической феноменологии собственно болевого синдрома.
- Хроническая боль может носить или постоянный, или рецидивирующий характер. Боль возможно отнести к хронической, даже если она непостоянна и возникает лишь эпизодически, но не реже 15 дней в месяц.
- Для хронических болей тревожно-депрессивного генеза характерна сенестопатическая окраска боли – жжение, мурашки, чувство холода, «ползание и шевеление под кожей».
- Хронические болевые синдромы обычно имеют не одну локализацию. Так, у больного с хроническими головными болями могут выявляться и предменструальные боли, и периодические боли в пояснице и т.д.
- Поведение больных с психогенной болью имеет свою специфику, которая определяется прежде всего внутренней картиной болезни с убежденностью больного в наличии у него органического соматического или неврологического заболевания. У пациентов с психогенной болью выявляется так называемый болевой анамнез – эпизоды болей в разных частях тела в прошлом. Нередко у этих пациентов в анамнезе имелись близкие родственники, длительно страдавшие болями. После выявления особенностей хронического болевого синдрома, которые позволяют заподозрить психогенный характер боли, следует проанализировать психическое состояние больного.
Терапия атипичных лицевых болей
Вероятность развития болевого синдрома, длительность течения и степень его выраженности в значительной степени определяются эмоциональным состоянием больных, о чем было сказано выше, в частности наличием тревожных, депрессивных нарушений, рядом психосоциальных факторов. Некоторые личностные особенности пациента: повышенная тревожность, избыточное чувство ответственности, сниженный эмоциональный фон – играют не последнюю роль в формировании и становлении миофасциального болевого синдрома лица и атипичных лицевых болей дисфункционального генеза. Своевременное распознание этих индивидуальных особенностей, определение их роли в запуске болевого синдрома позволяют выбрать оптимальную рентабельную терапию, сократить сроки лечения, снизить вероятность хронизации боли.
Еще одной характеристикой дисфункционального болевого синдрома является его интенсивность. Выделяют слабые, умеренные и сильные боли. Эта характеристика также учитывается при выборе анальгетической терапии. Для усиления обезболивающего эффекта часто приходится прибегать к комбинированной терапии препаратов различных классов. Принимая во внимание тот факт, что психогенная составляющая в развитии дисфункционального болевого синдрома играет ведущую роль, необходимо воздействие в первую очередь на негативную установку больного на течение заболевания.
Возможности препаратов, регулирующих активность белка S100
Существует взаимосвязь между развитием тревожных, депрессивных и других невротических расстройств и мозгоспецифическим белком S100, который экспрессируется и секретируется клетками микроглии и астроцитами. Белок S100 играет важную роль в реализации основных функций нейронных систем головного мозга, таких как генерация и проведение нервного импульса, регуляция синаптических и метаболических процессов, пролиферация и дифференцировка нейронов и клеток глии. В этой связи перспективным направлением в терапии невротических расстройств является применение препаратов, регулирующих активность белка S100.
Принципиально новым способом регуляторного воздействия представляется использование антител к белку S100. Так, препарат Тенотен содержит релиз-активные антитела к S100. Тенотен модифицирует функциональную активность белка S100, что обеспечивает нейротрофическое действие препарата, способствует восстановлению процессов нейрональной пластичности, препятствует развитию невротических и неврозоподобных состояний. Отсутствие седативного и миорелаксирующего эффекта, сочетаемость с другими препаратами обусловливают перспективность применения препарата для купирования невротических симптомов, сопровождающих различные соматические заболевания. Фармакологические эффекты Тенотена включают также стрессопротективное действие, регуляцию энергетического метаболизма нейронов, влияние на пролиферацию и дифференцировку клеток головного мозга. Кроме того, Тенотен обладает широким спектром психотропной, нейротропной, вегетомодулирующей активности. Взаимодействуя с ГАМК-А-бензодиазепиновым рецепторным комплексом, Тенотен оказывает ГАМК-миметический эффект. Препарат не вызывает заторможенности, дневной сонливости, мышечной расслабленности, зависимости и связанного с ней синдрома отмены даже при длительной терапии, поэтому может быть использован у людей, ведущих активный образ жизни, у людей, в профессии которых требуется особая концентрация внимания, например водителей, работников с точными механизмами и др.
Цель, материал и методы исследования
Целью проведенного исследования было изучение уровня тревожности пациентов с хроническими дисфункциональными болевыми синдромами на примере пациентов с лицевыми болями. В исследовании приняли участие 149 пациентов (43 мужчин и 106 женщин) с хроническими атипичными лицевыми болями в возрасте от 40 до 68 лет. Критерием отбора было наличие атипичной лицевой боли по МКБ-10 (G50.1. Атипичная лицевая боль), определяющейся как персистирующая боль в области лица, не имеющая признаков невралгий черепных нервов и не ассоциированная с объективными симптомами или органическими заболеваниями.
Пациенты были протестированы на наличие признаков тревоги при сборе жалоб и данных анамнеза, а также с помощью специализированных шкал. Всем пациентам проводилась оценка уровня боли и уровня тревожности для определения взаимодействия двух этих параметров. Для оценки уровня болевого синдрома использовалась визуально-аналоговая шкала (ВАШ). Выраженность болевого синдрома в среднем составила 4,6 ± 0,9 балла по ВАШ. Для определения уровня тревоги использовались шкалы Гамильтона и Спилбергера (для уточнения уровня личностной тревожности и реактивной тревоги на момент обследования).
В исследование не включались пациенты с декомпенсированной соматической патологией, острыми респираторными вирусными инфекциями, ранним реконвалесцентным периодом после перенесенных вирусных инфекций, гемодинамически значимыми сосудистыми мальформациями брахиоцефальных сосудов, очаговыми поражениями нервной системы и наличием травматических костных дефектов черепа и шейного отдела позвоночника.
В последующем все пациенты были разделены на две группы: пациенты основной группы (n = 103) получали НПВП (Ксефокам по 8 мг 2 р/сут) в сочетании с анксиолитической терапией (препарат Тенотен по 2 таблетки 3 р/сут), пациенты контрольной группы (n = 46) получали только НПВП. Продолжительность терапии в обеих группах составила 10 дней. При выписке всем пациентам основной группы был рекомендован прием препарата Тенотен в течение 3 месяцев.
Оценка эффективности комбинации обезболивающей терапии и анксиолитиков проводилась в стационаре на 10-й день терапии. Через 1 и 3 месяца после начала приема препарата Тенотен было проведено контрольное тестирование пациентов для оценки уровня тревожности и оценки рецидива болевого синдрома.
Результаты исследования
Анализ возрастных характеристик пациентов, вошедших в исследование, позволяет утверждать, что атипичные лицевые боли встречаются чаще среди лиц трудоспособного возраста (34% в возрасте 40–50 лет, 42% в возрасте 50–60 лет, 24% старше 60 лет). У подавляющего числа лиц (86,7%) с хроническими дисфункциональными болевыми синдромами клинически были выявлены признаки вегетативной дисфункции, проявляющиеся колебаниями артериального давления (67,5%), наличием склонности к тахикардии (64,9%), ярко-красным стойким дермографизмом (52,9%), наличием сосудистого «ожерелья» (17,8%), гипергидрозом ладоней и стоп (53,6%), дискинезией желудочно-кишечного тракта (20,2%), гипервентиляционным синдромом (33,5%), диссомническими расстройствами (19,2%).
При первичном обследовании пациентов с хроническими прозопалгиями с применением шкалы Гамильтона для оценки тревоги был выявлен высокий уровень тревожности. Важно отметить: чем больше была продолжительность заболевания, тем выше был уровень тревожности. Выраженность уровня тревоги по шкале Гамильтона у пациентов составила в среднем 20,75 ± 8,3 балла. Психологическое исследование (с использованием шкалы тревоги Спилбергера) показало наличие выраженных тревожных расстройств у всех пациентов: реактивная и личностная тревога в среднем составили соответственно 45,6 ± 3,4 и 46,1 ± 4,2 балла.
При оценке уровня боли по шкале ВАШ на 10-й день терапии отмечалось снижение боли в обеих группах, но более выраженное уменьшение болевого синдрома отмечалось среди пациентов основной группы (снижение показателей ВАШ до 1,1 ± 1,0 баллов, р < 0,005) в сравнении с контрольной группой (снижение показателей ВАШ до 2,5 ± 1,1 балла, р < 0,03) (рис. 1).
По данным психологического исследования по шкале Гамильтона в основной группе отмечено снижение уровня тревоги с 20,75 ± 8,3 до 18,5 ± 5,6 балла, что составило -11% (р < 0,03), в контрольной группе сохранился практически исходный уровень тревоги – 20,3 ± 5,4 балла. Следовательно, стабилизация эмоционального фона влияет на динамику показателей болевого синдрома (рис. 2).
Данные оценки по шкале Спилбергера на 10-й день терапии в группе пациентов, принимающих препарат Тенотен, свидетельствуют о положительной динамике по шкале реактивной тревоги (35,4 ± 4,3 балла, р < 0,01) и незначительной положительной тенденции по шкале личностной тревоги (43,1 ± 4,5 балла). В группе пациентов контрольной группы показатели реактивной и личностной тревоги остались без изменения.
В дальнейшем через 1 и 3 месяца от начала терапии было проведено дополнительное тестирование данной группы пациентов по шкале тревоги Гамильтона и по шкале реактивной и личностной тревоги Спилбергера.
Через 1 месяц после начала терапии показатели уровня тревоги по шкале Гамильтона в основной группе составили 14,5 ± 5,5 балла, что было меньше на 30% от исходного уровня тревоги (р < 0,03); в контрольной группе уровень тревоги по данной шкале существенно не изменился и составил 19,6 ± 4,6 балла (р < 0,05).
По данным шкалы реактивной и личностной тревоги Спилбергера через месяц была также отмечена выраженная положительная динамика в основной группе (19,4 ± 2,7 и 21,5 ± 3,1 балла соответственно, р < 0,01) и незначительные изменения в контрольной группе (39,4 ± 2,4 и 39,8 ± 3,4 балла соответственно).
Оценка уровня тревоги была проведена и через 3 месяца от начала терапии. Наблюдалась значимая положительная динамика у пациентов, принимающих Тенотен: 13,4 ± 4,2 балла по шкале Гамильтона и 17,4 ± 2,9 и 19,5 ± 3,5 балла по шкале реактивной и личностной тревоги Спилбергера соответственно (рис. 3). В контрольной группе динамика не наблюдалась и показатели остались на уровне предыдущих.
Следует подчеркнуть, что в течение 3 месяцев после проведенной терапии в стационаре у 7 пациентов контрольной группы (16,2%) отмечены рецидивы заболевания, проявляющиеся усилением болевого синдрома, повышением тревожности. В основной группе усиление болевого синдрома не отмечалось.
Выводы
- Хронический дисфункциональный болевой синдром, как правило, сопровождается повышением уровня тревожности. Комплексное применение НПВП в сочетании с анксиолитиками (Тенотен) в терапии пациентов с хроническим дисфункциональным болевым синдромом способствует более выраженному снижению болевого синдрома за счет стабилизации эмоционального фона и позволяет быстрее улучшить состояние пациентов и восстановить их качество жизни.
- В ходе проведенного исследования зафиксировано достоверное снижение уровня тревоги в группе пациентов, принимавших препарат Тенотен. На 10-й день в этой группе уровень тревоги по шкале Гамильтона уменьшился на 11% (р < 0,01), а уровень боли – на 76% (р < 0,01), в то время как у пациентов, не принимающих Тенотен, на фоне базовой терапии НПВП уровень тревоги снизился только на 2% и соответственно уровень боли – на 46% (р < 0,01).
- Продолжительное (более 1 месяца) применение анксиолитического препарата Тенотен способствует стабилизиции эмоционального фона, снижению реагирования на психотравмирующие факторы, что уменьшает опасность возникновения рецидивов и в целом предотвращает хронизацию процесса. Это подтверждается результатами контрольного тестирования через 1 и 3 месяца, которые свидетельствуют о выраженном снижении тревоги (р < 0,01) и отсутствии рецидивов в контрольной группе.
- В ходе исследования отмечено, что Тенотен не вызывает побочных эффектов и хорошо переносится пациентами.
1. Breivik H., Collett B., Ventafridda V. et al. Survey of chronic pain in Europe // Eur. J. Pain. 2006. Vol. 10. № 4. P. 287–333.
2. Neville A., Peleg R., Singer Y. et al. Chronic pain a population-based study // Isr. Med. Assoc. J. 2008. Vol. 10. № 10. P. 676–680.
3. Стояновский Д.Н. Боль в области спины и шеи. К.: Здоров’я, 2002. 392 с.
4. Ярошевский А.А. Интенсивность болевых ощущений и личностная тревожность у пациентов с цервикогенной цефалгией мышечного напряжения // Медицинская психология. 2008. № 4. С. 89–92.4. Ярошевский А.А. Интенсивность болевых ощущений и личностная тревожность у пациентов с цервикогенной цефалгией мышечного напряжения // Медицинская психология. 2008. № 4. С. 89–92.
5. Вейн А.М., Воробьева О.В. Болезненный мышечный спазм: алгоритм диагностики и терапии // Русский медицинский журнал. 2003. Т. 11. № 8. С. 438–440.
Current treatment strategies for atypical facial pain
M.N. Sharov, O.N. Fischenko
Moscow State University of Medicine and Dentistry named after A.I. Evdokimov, Neurology Department of the Dentistry Faculty
Contact person: Olga Nikolayevna Fischenko, of177@bk.ru
Efficacy of analgesic and anxiolytic combination therapy was studied in patients with atypical facial pain. Treatment with combinations of nonsteroidal anti-inflammatory drugs and anxiolytic (Tenoten) produced better pain control due to effects on emotional status and resulted in faster patients’ quality of life improvement.
Key words: prosopalgia, dysfunctional pain syndrome, nonsteroidal anti-inflammatory drugs, anxiolytic
M.N. Sharov, O.N. Fischenko
Moscow State University of Medicine and Dentistry named after A.I. Evdokimov, Neurology Department of the Dentistry Faculty
Contact person: Olga Nikolayevna Fischenko, of177@bk.ru
Efficacy of analgesic and anxiolytic combination therapy was studied in patients with atypical facial pain. Treatment with combinations of nonsteroidal anti-inflammatory drugs and anxiolytic (Tenoten) produced better pain control due to effects on emotional status and resulted in faster patients’ quality of life improvement.
Key words: prosopalgia, dysfunctional pain syndrome, nonsteroidal anti-inflammatory drugs, anxiolytic
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье приведены результаты исследования эффективности комбинированной обезболивающей и противотревожной терапии у пациентов с атипичными лицевыми болями.
Показано, что комплексное применение нестероидных противовоспалительных препаратов в сочетании с анксиолитиками (Тенотен) способствовало более выраженному снижению болевого синдрома за счет стабилизации эмоционального фона и позволяло быстрее улучшить состояние больных и повысить их качество жизни.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
