Современные технологии диагностики и лечения хронических цереброваскулярных заболеваний. XVIII Российский национальный конгресс «Человек и лекарство». Образовательный семинар компании «Валента Фарма»
- Аннотация
- Статья
- Ссылки





Одно из главных достижений отечественной фармакологии последнего десятилетия – создание нейромодуляторов, препаратов нового класса, которые «…соразмерно влияют на функциональное состояние центральной нервной системы в целом». По словам автора нейромодуляторной концепции и разработчика препарата Фенотропил® Валентины Ивановны АХАПКИНОЙ, «…избирательная активность таких веществ проявляется уже в самом организме в зависимости от наличия болезней, расстройств или предпосылок к ним». Нейромодуляторы регулируют уровень функциональной активности ЦНС, приводя его к норме, поэтому эффекты этих препаратов проявляются у больных людей, когда есть нарушение функций, или в ситуациях острого напряжения и утомления у здоровых. Очень важно, что нейромодуляторы не метаболизируются, а полностью выводятся из организма в неизменном виде. Основные показания к применению: хроническая цереброваскулярная недостаточность, черепно-мозговые травмы, астенические и невротические состояния, депрессии средней и легкой тяжести, психоорганические синдромы, судорожные состояния, профилактика гипоксии, повышение устойчивости к стрессу, к воздействию низких температур. Нейромодуляторы можно с успехом использовать для лечения лекарственной зависимости, наркомании, хронического алкоголизма и ожирения алиментарно-конституционального генеза. Фенотропил® – не просто препарат ноотропного действия, он обладает нейромодуляторной активностью. Фенотропил® показан не только для повышения функциональной активности мозга в стрессовых ситуациях у здоровых людей, но и при заболеваниях ЦНС, невротических состояниях, нарушении процессов обучения, депрессии, психорганических синдромах, судорожных состояниях, ожирении. Однако назначение данного лекарственного средства, как и любого другого, должно быть обоснованным, поэтому практикующие специалисты должны как можно больше знать о его возможностях, свойствах и особенностях применения. Именно такую задачу поставили перед собой организаторы образовательного семинара. Врачей, пришедших на это мероприятие, познакомили с результатами последних клинических исследований препарата. Кроме того, приглашенные эксперты проинформировали слушателей о том, какие изменения произошли в представлениях ученых о патогенезе хронических цереброваскулярных заболеваний, рассказали о молекулярных и биохимических аспектах развития этих патологий, о новых диагностических технологиях, механизмах действия нейрометаболических препаратов. Особое внимание было уделено внедрению новых технологий медикаментозного лечения хронической ишемии мозга.
Современные представления о патогенезе хронических цереброваскулярных заболеваний
Известно, что уровень регионального мозгового кровотока составляет 55–80 мл на 100 г вещества мозга (мозговой кровоток в целом составляет примерно 15% от минутного выброса сердца). При этом из крови экстрагируются 50% кислорода и 10% глюкозы. Значительный объем вырабатываемой энергии направляется на поддержание энергетического обмена, а остальная часть расходуется на высвобождение нейромедиаторов и функционирование клеточных структур мозга. Очевидно, что мозг чрезвычайно чувствителен к недостаточности кровообращения, которое приводит к снижению кислородного обеспечения и энергетическому дефициту. Даже небольшие изменения в обеспечении кислородом мозга – на 10–15 мл – проявляются начальными признаками недостаточности мозгового кровообращения. При снижении этого уровня на 20–30 мл на 100 г вещества мозга появляются клинические симптомы энцефалопатии. Дальнейшее снижение уровня регионального церебрального кровотока (при условии его неадекватной компенсации) может привести к развитию инфаркта мозга. Независимо от того, что лежит в основе нарушений – атеросклероз, гипертоническая болезнь и т.д., – запускается ряд патогенетических механизмов, приводящих к прогрессированию недостаточности мозгового кровообращения.
Ишемическое повреждение развивается не линейно, а каскадно. Ишемический каскад особенно стремительно развивается в условиях острого нарушения мозгового кровообращения, но те же механизмы задействованы и при хронической недостаточности мозгового кровообращения: нарушения поступления кислорода и глюкозы ведут к деполяризации клеточных мембран, высвобождению глутамата, активации NMDA-рецепторов, кальциевых каналов. Затем происходят увеличение внутриклеточного кальция, активация ферментов, синтез окиси азота и образование свободных радикалов, а как результат (при выраженных нарушениях) – гибель нейронов.
Выделяются несколько степеней критического уровня реакции тканей головного мозга на снижение кровотока. При первом уровне (менее 50 мл/100 г ткани мозга/мин) снижаются синтез белков и экспрессия генов. Затем активируется анаэробный гликолиз, увеличивается экстракция из крови лактата, развивается лактацидоз. В результате повреждения клеточной мембраны и внутриклеточного накопления ионов натрия, хлора и ацидоза возникает ишемический отек мозга. При глубокой ишемии мозга (до 30 мл/100 г ткани мозга/мин) отмечаются дестабилизация клеточных мембран, нарушения каналов ионного транспорта, высвобождение возбуждающих нейротрансмиттеров. Большое значение в развитии патологии имеет оксидантный стресс, характеризующийся избыточным накоплением свободных радикалов и активацией процессов перекисного окисления липидов. Взаимодействие оксидантного стресса с ишемическим каскадом дает эффект взаимного усиления и, по общему мнению всех экспертов, единственно адекватным направлением лечения может быть разрыв звеньев этого процесса.
Механизмы действия нейрометаболических препаратов для лечения хронических цереброваскулярных заболеваний
Однако класс ноотропных препаратов чрезвычайно обширен и разнообразен. Они обладают разными механизмами действия, отличаются мишенью воздействия и вызываемыми эффектами. Только группа пирролидоновых ноотропных препаратов (рацетамы) включает более 10 оригинальных препаратов. В классификации «истинных» ноотропов (их основной, а иногда и единственный эффект – улучшение мнестических функций) появились и другие семейства, включающие холин-, ГАМК-, пептидергические и другие вещества. Существуют ноотропные препараты смешанного действия, у которых положительные когнитивные эффекты дополняются, а нередко и перекрываются другими, не менее значимыми эффектами. Поэтому лечащий врач должен хорошо ориентироваться в многообразии препаратов, знать, через какие молекулярные мишени и синаптические механизмы ноотропы осуществляют модулирующее действие на когнитивные процессы, какие звенья в нейрохимическом механизме действия являются общими для всех ноотропов, а какие – специфическими.
Известно, что многие когнитивные функции зависят от функционирования основных нейромедиаторных систем мозга – холинергической, адренергической, дофамнергической, ГАМК-ергической и глутаматергической. Однако до последнего времени не было известно, какая связь между ноотропами и рецепторами, являются ли именно они молекулярными мишенями для ноотропов, и если «да», то какие синаптические механизмы участвуют в реализации их действия. Например, многие считают, что у ноотропа пирацетама и Фенотропила есть общие элементы в структуре. Однако и с точки зрения химии, и с точки зрения фармакологии это не так. Многочисленные клинические исследования показали, что эти препараты обеспечивают разное фармакологическое действие и разный клинический эффект. В спектре фармакологических эффектов этих двух препаратов совпадений лишь два: они оба усиливают когнитивные функции и улучшают мозговое кровообращение. На этом действие пирацетама заканчивается, а Фенотропил® имеет еще ряд эффектов: противогипоксический, вегетостабилизирующий, антиастенический, психоактивирующий, анксиолитический, антидепрессивный, противосудорожный, антиагрессивный, анальгетический, анорексигенный. Фенотропил® также повышает физическую работоспособность и устойчивость к экстремальным воздействиям. К этому следует добавить: длительность курса приема Фенотропила составляет 2–8 недель против 8–24 недель курса пирацетама. И это немаловажно для пациента. Очевидно, что в отличие от своих предшественников Фенотропил характеризуется чрезвычайно широким спектром фармакологических и терапевтических эффектов.
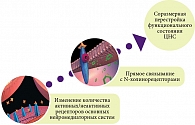
Представленные в экспериментах, проведенных на лабораторных животных, данные о рецепторном механизме действия Фенотропила «…не только согласуются с современными взглядами об основных нейрохимических мишенях ноотропных средств (прямое или опосредованное вовлечение дофаминовых рецепторов в механизмы когнитивной деятельности и эффекты ноотропных препаратов; роль в этих процессах серотониновых рецепторов 5-HT2 типа), но и привносят абсолютно новые элементы. Исследования показали, что Фенотропил® активен в первую очередь в отношении холинергических рецепторов никотинового типа и NMDA-глутаматных рецепторов (рис. 1). Причем в отношении первых он обнаруживает прямое действие, а увеличение концентрации вторых ученые объясняют механизмом нейромодуляции», – подчеркнул профессор Г.И. Ковалев.
Алгоритм лечения хронической ишемии мозга
Для квалифицированного невролога, хорошо знакомого с особенностями каждой нейромедиаторной системы мозга и нейрохимическими механизмами действия ноотропов, это выполнимо. Такой врач выберет для своего пациента эффективный препарат. Кроме того, учитывая, что хроническая ишемия мозга имеет мультифакторный патогенез, а значительная часть пациентов – люди пожилого и старческого возраста, как правило, имеющие сочетанную патологию, специалист назначит лекарство, которое имеет сразу несколько фармакологических эффектов. В этом заключается суть мультимодальной терапии и относительно нового перспективного класса лекарственных препаратов – нейромодуляторов, которые оказывают неспецифическое воздействие на различные нейромедиаторные системы. В физиологических условиях часть рецепторов находится в неактивном состоянии. При патологии количество неактивных рецепторов увеличено. После введения нейромодулятора происходит активация рецепторов. Медиатор начинает взаимодействовать с большим количеством рецепторов. У каждого такого модулятора есть мономодальное действие, т.е. воздействие на какой-то один симптом, а также мультимодальное и нейромодулирующее. Нейромодулирующий эффект заключается в антидепрессивном и анксиолитическом действии и в непрямом противосудорожном действии. Примером такого лекарственного средства является отечественный препарат Фенотропил®, который уже сегодня назначается не только при хронической ишемии мозга, но и при лечении когнитивных нарушений, депрессивных расстройств, эпилепсии как добавление к базисным препаратам. Фенотропил повышает устойчивость тканей мозга к гипоксии, оказывает положительное влияние на обменные процессы и кровообращение головного мозга, стимулирует окислительно-восстановительные процессы, повышает энергетический потенциал организма за счет утилизации глюкозы, улучшает регионарный кровоток в ишемизированных участках головного мозга.
Таким образом, перспективным направлением лечения хронической ишемии мозга является применение нейромодулирующей фармакотерапии. Курсовое назначение нейромодулятора (2 курса по 4 недели в год) особенно показано для коррекции фармакорезистентных клинических синдромов.
Коморбидность депрессии, тревоги и астении при гипертонической энцефалопатии
Очевидно, что развивающиеся расстройства настроения, связанные с нарушениями в эмоциональной сфере (которые часто диагностируются с трудом), являются независимым прогностически ухудшающим фактором риска для лечения любых заболеваний. При этом видоизменяется ответ организма на любую лекарственную терапию. Больным с гипертензией назначаются немало лекарственных средств: антиагреганты, антиоксиданты, вазоактивные препараты и др., в том числе средства, которые корректируют эмоциональный фон. Существует опасность возникновения полипрагмазии (либо вынужденной, либо необоснованной). Полипрагмазия всегда увеличивает риск лекарственных взаимодействий, а соответственно и риск возникновения лекарственной ятрогении. Осложнения лекарственной терапии занимают 4–6-е место среди причин смертности, 5% госпитализаций связаны с лекарственными осложнениями. Для преодоления необоснованной полипрагмазии необходимо исключить применение одновременно нескольких препаратов однонаправленного действия. Наиболее рациональный подход к лечению – многоцелевая терапия, то есть назначение такого лекарственного средства, «…которое будет охватывать максимальное число клинических эффектов, которые мы хотим получить».
Для лечения и профилактики гипертонической энцефалопатии могут быть использованы антиагреганты, антиоксиданты, вазоактивные препараты, ноотропы и в первую очередь нейромодуляторы. Если говорить о коморбидности депрессии и астении при гипертонической энцефалопатии, то для лечения таких пациентов можно порекомендовать препарат Фенотропил®. Если врач диагностирует коморбидную тревогу, то в таком случае необходимо к терапии добавлять Тералиджен®, который оказывает вегетостабилизирующий, анксиолитический (противотревожный), умеренно гипотензивный эффекты. Кроме того, за счет влияния на гистаминовые рецепторы он обладает успокаивающим, снотворным и противоаллергическим действием. Препарат хорошо переносится пожилыми пациентами и детьми, поэтому Тералиджен разрешен к применению с 7 лет. Комплексный механизм действия препарата Тералиджен позволяет снять тревожную симптоматику у такого рода пациентов, облегчить их страдания и внутреннее напряжение, что позволяет врачу добиться отличных результатов в лечении.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.