Терапия надежды: биологическая терапия и тяжелая эозинофильная бронхиальная астма. Результаты реальной клинической практики. XXVIII Национальный конгресс по болезням органов дыхания
- Аннотация
- Статья
- Ссылки








Тяжелая эозинофильная астма: кому может быть назначена анти-ИЛ-5-терапия
Доклад заведующего кафедрой пульмонологии Северо-Западного государственного медицинского университета им. И.И. Мечникова, д.м.н., профессора Александра Викторовича ЕМЕЛЬЯНОВА был посвящен диагностике и таргетной терапии тяжелой эозинофильной астмы с использованием моноклональных антител к интерлейкину (ИЛ) 5.
Фенотип астмы – это описательные характеристики, не связанные с механизмами болезни, включающие физиологию, триггеры, маркеры воспаления дыхательных путей. Эндотипы – характеристики астмы, учитывающие механизмы, которые могут быть представлены в различных фенотипах. Эти определения приведены в статье J. Lötvall и соавт., опубликованной в 2011 г.1
Разные типы воспаления дыхательных путей у больных БА были выявлены еще раньше. Так, J. Simpson и соавт. в 2006 г. при изучении индуцированной мокроты у больных БА в 40% случаев обнаружили эозинофильное воспаление с уровнем эозинофилов ≥ 3%, в 20% – нейтрофильное воспаление с уровнем нейтрофилов ≥ 61%, в 8% – смешанное гранулоцитарное, то есть эозинофильно-нейтрофильное, воспаление с уровнем эозинофилов ≥ 3% и нейтрофилов ≥ 61%, в 31% случаев – малогранулоцитарное воспаление с уровнем эозинофилов < 3% и нейтрофилов < 61%2.
Эозинофильная астма считается распространенным фенотипом БА. Согласно данным зарубежных авторов, эозинофильное воспаление имеет место у 56–62% больных тяжелой астмой3. Эти данные соответствуют результатам отечественного исследования, проведенного в условиях реальной клинической практики. Из 103 пациентов с тяжелой астмой у 63% выявлено преимущественно эозинофильное воспаление дыхательных путей4.
Тяжелая БА подразделяется на два эндотипа: БА, обусловленная воспалением 2-го типа (Т2-астма), и БА, не связанная с воспалением 2-го типа (не Т2-астма). Эозинофильный тип воспаления дыхательных путей, как правило, проявление Т2-эндотипа, который реализуется за счет доминирования Th2-лимфоцитарного ответа (атопическая эозинофильная БА) и/или высокой активности врожденных лимфоидных клеток 2-го типа – ILC2 (неатопическая эозинофильная астма). Как Th2-клетки, так и ILC2-клетки увеличивают уровни ИЛ-5, необходимого для продукции, созревания, накопления и активации эозинофилов5. ИЛ-5 играет важную роль в формировании неконтролируемого эозинофильного воспаления в бронхолегочном отделе при атопическом и неатопическом Т2-эндотипе тяжелой БА.
В ряде исследований оценивали влияние уровня эозинофилов в периферической крови как маркера эозинофильного воспаления дыхательных путей на исходы тяжелой астмы. Например, в одном из проспективных исследований у пациентов с тяжелой неконтролируемой БА, уровнем эозинофилов крови ≥ 400 кл/мкл с двумя и более обострениями в год частота обращений за неотложной помощью и госпитализаций превышала таковую у пациентов с уровнем эозинофилов крови < 400 кл/мкл6. По мнению профессора А.В. Емельянова, именно эту категорию больных следует считать целевой группой для таргетной терапии препаратами моноклональных антител к ИЛ-5, в частности реслизумабом.
Возможными диагностическими критериями тяжелой эозинофильной БА являются:
- подтвержденный диагноз тяжелой БА;
- персистирующая эозинофилия крови и/или мокроты, выявленная два раза и более;
- частые обострения БА (свыше двух раз за 12 месяцев);
- зависимость от системных глюкокортикостероидов (ГКС), применяемых для достижения контроля БА.
В качестве малых критериев рассматриваются:
- позднее начало БА;
- патология верхних дыхательных путей (хронические риносинуситы, нередко сочетающиеся с назальными полипами);
- повышенный уровень других биомаркеров эозинофильного воспаления;
- фиксированная бронхиальная обструкция;
- воздушные ловушки и наличие слизистых пробок, обтурирующих мелкие бронхи7.
ИЛ-5 участвует в реализации эозинофильного воспаления, поэтому терапия тяжелой эозинофильной БА направлена, в частности, на блокирование его действия. С этой целью используются непосредственно антитела к ИЛ-5 либо антитела к его рецептору. За рубежом для клинического применения одобрено моноклональное антитело к субъединице рецептора ИЛ-5 бенрализумаб. Зарегистрированные за рубежом и в России моноклональные антитела собственно к молекуле ИЛ-5 представлены меполизумабом и реслизумабом.
Реслизумаб (Синкейро) – препарат гуманизированных моноклональных антител (IgG4к), высоко аффинных к ИЛ-5. Он показан для лечения тяжелой эозинофильной астмы с повышенным уровнем эозинофилов в периферической крови (≥ 400 кл/мкл). В марте 2016 г. FDA (Food and Drug Administration – Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобрило лекарственную форму реслизумаба для внутривенного введения. В сентябре 2016 г. было получено одобрение EMA (European Medicines Agency – Европейское медицинское агентство), и в апреле 2017 г. препарат был зарегистрирован в России. В 2018 г. эксперты GINA (Global Initiative for Asthma – Глобальная инициатива по лечению астмы) рекомендовали реслизумаб в качестве дополнительной терапии 5-й ступени при неконтролируемой тяжелой эозинофильной астме.
Реслизумаб специфически связывается с молекулой ИЛ-5. Он занимает критический участок или эпитоп на поверхности ИЛ-5, блокируя его биоактивность и препятствуя взаимодействию ИЛ-5 с его рецептором. В итоге нарушается процесс, лежащий в основе патофизиологии бронхиального воспаления при астме.
Программа BREATH включала четыре рандомизированных плацебоконтролируемых клинических исследования III фазы и одно открытое исследование открытой фазы. В исследованиях оценивали эффективность и безопасность реслизумаба при неконтролируемой БА на фоне повышенного содержания эозинофилов в крови8–11. Дальнейший post-hoc-анализ включал исследования эффективности и безопасности реслизумаба у пожилых пациентов с БА, пациентов с поздней астмой, назальным полипозом и т.д.
В двух идентичных 52-недельных исследованиях сравнивали эффективность реслизумаба 3 мг/кг и плацебо у 953 пациентов с тяжелой БА на фоне повышенного содержания эозинофилов в периферической крови (≥ 400 кл/мкл) с более чем одним обострением на фоне приема системных ГКС в течение 12 месяцев. Большинство пациентов принимали умеренные и высокие дозы ингаляционных ГКС в комбинации с бета-2-адреномиметиками длительного действия8.
Результаты двух исследований показали, что реслизумаб достоверно (р < 0,0001) более значимо снижал частоту обострений по сравнению с плацебо (рис. 1).
На фоне применения реслизумаба частота обострений в первом исследовании снизилась на 50%, во втором – на 59%.
В обоих исследованиях реслизумаб продемонстрировал преимущество перед плацебо в улучшении функции легких. Подобное улучшение наблюдалось в начале и сохранялось до 52-й недели (рис. 2).
Реслизумаб достоверно (р < 0,0001) более выраженно улучшал объем форсированного выдоха за первую секунду (ОФВ1) по сравнению с плацебо: в первом исследовании в группе реслизумаба прирост ОФВ1 от исходного уровня составил 235 мл, в группе плацебо – 109 мл, во втором исследовании – 201 и 111 мл соответственно. В обоих исследованиях реслизумаб продемонстрировал эффективность в улучшении качества жизни пациентов с БА, согласно опроснику AQLQ (Asthma Quality of Life Question naire).
Таким образом, применение реслизумаба у пациентов с тяжелой эозинофильной БА, не контролируемой ингаляционными ГКС (ИГКС), способствовало раннему (спустя два-три дня от введения первой дозы) и стабильному снижению уровня эозинофилов в крови (на 92%), а также эозинофилов в мокроте (на 95,4%). На фоне терапии реслизумабом частота обострений в среднем снижалась на 54% (50–59%), что приводило к раннему (на четвертой неделе) и долгосрочному улучшению функции легких, контролю БА, повышению качества жизни пациентов при сопоставимой с группами плацебо переносимости. Причем данный эффект был долгосрочным и сохранялся до конца исследования12.
По словам профессора А.В. Емельянова, важно, что эффективность реслизумаба в отношении показателей ОФВ1 зависела от уровня эозинофилов в крови (≥ 400 кл/мкл). У пациентов с исходным уровнем эозинофилов ≥ 400 кл/мл терапия реслизумабом обеспечила более значимое улучшение показателей ОФВ1, форсированной жизненной емкости легких и частоты использования бета-2-агонистов короткого действия по сравнению с плацебо. Исследователи пришли к выводу, что количество эозинофилов в крови ≥ 400 кл/мкл позволяет идентифицировать пациентов, отвечающих на лечение реслизумабом13. Это и служит критерием, на основании которого назначается данный лекарственный препарат, рекомендованный к использованию в клинической практике.
Профессор А.В. Емельянов проанализировал результаты исследования эффективности реслизумаба у пациентов с поздней астмой. Как правило, это пациенты обоего пола с началом астмы во взрослом возрасте, отсутствием или незначительной гиперчувствительностью к ингаляционным аллергенам, риском тяжелых обострений, хроническим риносинуситом/полипозом носа, повышенной чувствительностью к аспирину, повышенным уровнем эозинофилов, невысоким или нормальным уровнем IgE, низким ОФВ1, наличием воздушных ловушек и динамической гиперинфляцией. Пациенты с поздней астмой обычно отвечают на лечение системными ГКС и демонстрируют хороший ответ на терапию моноклональными антителами к ИЛ-514.
Применение реслизумаба у пациентов с поздней астмой снижало частоту обострений на 75% по сравнению с плацебо. Кроме того, реслизумаб характеризовался более выраженным эффектом у пациентов с поздней БА, дебютом в возрасте старше 40 лет по сравнению с пациентами с ранней БА, дебютом в возрасте младше 40 лет: 75 против 42%.
Аналогичная тенденция наблюдалась и в отношении функции легких: реслизумаб улучшал ОФВ1 на 167 мл у пациентов с поздней астмой по сравнению с плацебо. У пациентов с ранней астмой этот показатель на фоне приема реслизумаба составил 68 мл15.
Эффективность терапии реслизумабом оценивали у пожилых больных тяжелой эозинофильной БА. Реслизумаб снижал частоту обострений на 67% у пожилых пациентов (≥ 65 лет) по сравнению с плацебо. Эффективность реслизумаба была менее выраженной у пациентов более молодого возраста (18–64 года): снижение частоты обострений на 53% по сравнению с плацебо. Реслизумаб продемонстрировал преимущество перед плацебо и в улучшении функции легких. Улучшение было более выраженным в группе пожилых больных астмой: ОФВ1 увеличился на 150 мл по сравнению с плацебо.
Резюмируя сказанное, профессор А.В. Емельянов подчеркнул, что:
- эозинофильная астма – наиболее частый фенотип тяжелой астмы;
- реслизумаб снижает частоту обострений, улучшает легочную функцию, качество жизни и контроль БА при назначении в течение года при уровне эозинофилов в крови ≥ 400 кл/ мкл;
- максимальный эффект наблюдается при лечении поздней астмы (с дебютом в возрасте ≥ 40 лет) и астмы у пожилых (≥ 65 лет);
- переносимость препарата обычно хорошая. Риск развития анафилаксии всего 0,19%.
Реслизумаб в лечении больных тяжелой аллергической астмой с повышенным уровнем эозинофилов. Клинический разбор
Профессор кафедры клинической аллергологии и иммунологии Российской медицинской академии непрерывного профессионального образования, д.м.н. Наталья Михайловна НЕНАШЕВА акцентировала внимание участников симпозиума на эффективности и перспективах использования анти-ИЛ-5-моноклональных антител при тяжелых формах аллергической астмы с высоким уровнем эозинофилов в крови.
Установлено, что атопия является причиной тяжелой формы БА только в том случае, если доказана четкая связь между воздействием аллергена и клиническими проявлениями и обострениями астмы. У пациентов с анамнезом атопии развитие БА не всегда обусловлено аллергическим характером воспаления. В связи с этим в случае подтвержденной сенсибилизации к аллергенам и отсутствия контроля над заболеванием на фоне адекватного лечения проводят дифференциальную диагностику тяжелой аллергической и тяжелой эозинофильной БА. Цель подобного диагностирования – выявить высокий уровень эозинофилии крови или мокроты, уточнить возраст манифестации заболевания, оценить взаимосвязь между аллергенами и клиническими проявлениями и обострениями БА7.
Как известно, астма – гетерогенное заболевание. Тяжелая эозинофильная БА может иметь атопический и неатопический генез. Неатопический генез может характеризоваться Т2-иммунным ответом, реализуемым врожденными лимфоидными клетками 2-го типа (ILC2-клетки). Как правило, неатопическая эозинофильная БА – это тяжелая астма с момента дебюта, атопическая – тяжелая БА с детства или с утяжелением во взрослом возрасте. Для тяжелой эозинофильной астмы характерно наличие коморбидной патологии в виде аллергического ринита, назального полипоза, синуситов, инфекции16.
Фенотипы, связанные с воспалением 2-го типа, могут не только отличаться, но и частично совпадать. По оценкам, перекрест эозинофильного и аллергического фенотипов БА, ассоциированных с тяжелой эозинофильной астмой, встречается у 25–55% пациентов с БА17–19. Следовательно, достаточно большое число больных имеют признаки аллергической БА и выраженное эозинофильное воспаление.
Какой препарат биологической терапии наиболее оптимален для такой категории больных?
В исследовании IDEAL, проведенном в условиях реальной клинической практики (с участием центров из Австралии, Канады, США, стран Евросоюза), из когорты больных тяжелой БА были отобраны пациенты, которым можно было назначить один или несколько моноклональных антител – омализумаб, меполизумаб и реслизумаб в соответствии с инструкциями. В итоге отмечалось некоторое совпадение групп пациентов, подходящих для лечения и анти-ИЛ-5-моноклональными антителами, и анти-IgE-препаратами20.
Можно ли аллергию считать дифференцирующим маркером для анти-IgE- или анти-ИЛ-5-терапии? Доказано, что эффективность анти-ИЛ-5-препаратов не зависит от наличия или отсутствия атопии у больных астмой с повышенным уровнем эозинофилов в крови.
На эффективность реслизумаба у больных БА не влияет наличие или отсутствие аллергенспецифических IgE. Это продемонстрировал ретроспективный анализ данных 52-недельного исследования III фазы реслизумаба, который назначали пациентам с эозинофильной астмой, атопией и без атопии21. Атопический статус определяли по уровням аллергенспецифических IgE для десяти наиболее распространенных аэроаллергенов.
Критерии включения в исследование:
- взрослые и подростки в возрасте 12–75 лет;
- наличие неконтролируемой умеренной и тяжелой астмы (≥ 1,5 балла по ACQ (Asthma Control Questionnaire – Опросник по контролю над астмой));
- терапия ИГКС (≥ 440 мкг флутиказона или эквивалент) + другим препаратом базисной терапии;
- обратимость бронхиальной обструкции (≥ 12% после ингаляции бета-2-агонистом);
- более одного обострения БА за 12 месяцев, предшествовавших включению в исследование;
- при стероидзависимой БА – применение пероральных ГКС;
- уровень эозинофилов в крови ≥ 400 кл/мкл.
Большинство пациентов (63%) имели положительный атопический статус. У IgE-положительных пациентов (n = 303) количество положительных специфических IgE-тестов в среднем составило 3,8. 77% имели положительные тесты с двумя и более аллергенами. Наиболее распространенными были три аллергена – клещ домашней пыли, шерсть собаки, пыльца тимофеевки. Из 303 атопически позитивных участников исследования 162 получали плацебо, 141 – реслизумаб.
Атопически негативные пациенты (37%) были старше, имели более высокий уровень эозинофилов в крови, характеризовались склонностью к приему пероральных ГКС, чаще страдали хроническим риносинуситом, назальными полипами, перенесли операции на назальных пазухах. Из 177 атопически негативных пациентов 80 получали плацебо, 97 – реслизумаб.
Ретроспективный анализ результатов исследования показал преимущество реслизумаба перед плацебо в снижении уровня обострений БА и улучшении функции легких у пациентов как с атопией, так и без нее (рис. 3).
Согласно полученным данным, у всех пациентов с положительным атопическим статусом и без такового значимо снижалась частота клинических обострений БА на фоне терапии реслизумабом по сравнению с плацебо: реслизумаб способствовал снижению числа обострений БА у специфически IgE-позитивных пациентов на 40%, у специфически IgE-негативных – на 66%.
Аналогичная тенденция наблюдалась и в отношении улучшения легочной функции. При использовании реслизумаба статистически значимое увеличение ОФВ1 наблюдалось у всех пациентов с положительным атопическим статусом и без такового: по сравнению с плацебо прирост ОФВ1 у специфически IgE-позитивных пациентов составил 138 мл, у специфически IgE-негативных – 178 мл.
Оценка контроля БА (ACQ) и качества жизни (AQLQ) у пациентов в зависимости от атопического статуса подтвердила преимущество реслизумаба перед плацебо. У пациентов с атопией и без таковой зафиксированы аналогичные улучшения контроля БА и качества жизни после 52 недель лечения реслизумабом относительно плацебо.
Итак, почти 2/3 пациентов с эозинофильной астмой имели атопический статус, выявленный с помощью специфического IgE-теста на общие аллергены. Реслизумаб 3 мг/кг (внутривенно каждые четыре недели) продемонстрировал эффективность в снижении обострений астмы, улучшении функции легких у пациентов с атопической и неатопической эозинофильной БА. Показатели контроля над астмой улучшились у всех пациентов независимо от атопического статуса. Приведенные данные свидетельствуют о том, что анти-ИЛ-5-терапия приносит ощутимую пользу.
Интерес представляют и данные ретроспективного анализа M. Humbert и соавт.22 Ученые сравнивали эффективность реслизумаба и плацебо у пациентов, подходивших для лечения омализумабом. На фоне применения реслизумаба частота обострений БА снижалась на 42%, ОФВ1 увеличивался на 173 мл, оценка по AQLQ улучшалась на 0,37 по сравнению с плацебо.
В заключение профессор Н.М. Ненашева пояснила, что в клинических рекомендациях Российского респираторного общества и Российской ассоциации аллергологов и иммунологов представлен алгоритм выбора иммунобиологического препарата при тяжелой астме. В частности, пациентам с тяжелой аллергической БА можно назначать как омализумаб, так и анти-ИЛ-5-препараты23.
Эозинофильная астма и полипозный риносинусит: преображая мир тусклых красок
Заведующая отделением бронхиальной астмы Института иммунологии ФМБА России, д.м.н., профессор Оксана Михайловна КУРБАЧЕВА рассмотрела актуальные аспекты использования биологических препаратов моноклональных антилел у больных эозинофильной астмой и полипозным риносинуситом.
Полипозный риносинусит (ПРС) – хроническое заболевание слизистой оболочки носа и околоносовых пазух, в основе патогенеза которого лежит воспалительная реакция. Заболевание характеризуется образованием и рецидивирующим ростом полипов и доминированием эозинофилов или нейтрофилов.
Любое воспаление – системный процесс. Характеризуя роль медиаторов в развитии эозинофильного воспаления при Т2-астме, профессор О.М. Курбачева отметила, что эозинофилы привлекаются в зону воспаления при участии ряда интерлейкинов. Каскад воспалительных событий, вызванный Th-2-цитокинами (ИЛ-4, ИЛ-5, ИЛ-13), в конечном итоге приводит к основным клиническим проявлениям БА. Ключевым регулятором активности эозинофилов в патофизиологии БА считается ИЛ-524. С учетом роли ИЛ-5 в реализации эозинофильного воспаления блокирование его эффектов становится важной составляющей терапии заболеваний, в том числе БА, в основе которых лежит данный тип воспаления. Главное – определить пациентов, у которых именно это звено является ведущим в формировании воспаления.
Как правило, выбор основывается преимущественно на клинических критериях, одним из которых считается наличие сопутствующих заболеваний. Если у пациента с тяжелой БА имеется аллергический ринит, логично предположить, что астма также имеет аллергическое происхождение. При наличии у больного астмой полипоза можно говорить о не-IgE-зависимом воспалении.
Полипозный риносинусит относится к распространенным заболеваниям. Согласно российским данным, показатель обращаемости больных ПРС составляет 4,9 на 10 тыс. населения, при этом ежегодно регистрируются 70 тыс. новых случаев ПРС. Следовательно, ПРС может наблюдаться у 1,5 млн россиян. Средний возраст пациентов с дебютом ПРС составляет 42 года. Мужчины страдают этим заболеванием примерно в 2,3 раза чаще женщин25.
По гистологическому строению полипы подразделяются на отечные эозинофильные, воспалительные фиброзные, полипы с гиперплазией серозно-слизистых желез, полипы с атопией стромальной ткани. Именно пациенты с отечными эозинофильными полипами, ткань которых на 77–78% представлена эозинофилами, относятся к наиболее распространенной категории больных26.
Следует отметить, что качество жизни пациентов с ПРС невысокое, поскольку их беспокоит не только заложенность носа, но также боль и ощущение давления в лицевой области, отсутствие обоняния. Нередко имеют место головокружение, боль или давление в ушах, зубная боль, кашель, неприятный запах изо рта. Не исключены дисфония, слабость, нарушение сна. На фоне такого симптомокомплекса жизнь пациентов с ПРС постепенно утрачивает яркие краски.
Существует ли связь между атопией и ПРС? Несмотря на ряд исследований, роль IgE-зависимой аллергической реакции в патогенезе ПРС достоверно не доказана. В то же время при аллергическом скрининговом обследовании позитивные кожные тесты отмечались у 50–84% пациентов с ПРС, 60% пациентов имели полисенсибилизацию. Вместе с тем в период цветения растений у этих пациентов не наблюдалось существенного ухудшения состояния, что ставит под сомнение причинно-следственную связь аллергии и ПРС.
У больных БА частота ПРС значительно выше, чем в популяции, – 7–15%. Между тем у пациентов с ПРС астма диагностируется в 29–70% случаев. Компьютерная томография позволяет установить изменения в околоносовых пазухах у 100% больных стероидозависимой БА. При сочетании ПРС и БА взаимное утяжеление заболеваний и увеличение выраженности симптомов снижают качество жизни пациентов и затрудняют проведение лечебных мероприятий.
Согласно EPOS (European Position Paper on Rhinosinusitis and Nasal Polyps – Европейский согласительный документ по риносинуситу) и клиническим рекомендациям, к лечению ПРС надо подходить с терапевтических позиций. В целом с учетом различного генеза носовых полипов лечение при разных формах и стадиях ПРС может быть только консервативным, комбинированным (хирургическое лечение + терапия) либо только хирургическим. Профессор О.М. Курбачева уточнила, что на текущий момент данных о негативном влиянии хирургических вмешательств в полости носа на течение БА нет.
Как известно, респираторные заболевания, ассоциированные с гиперчувствительностью к аспирину, были описаны еще в начале ХХ в., а в 1922 г. вышли в свет первые работы с описанием успешной гипосенсибилизации аспирином с целью контроля ПРС и БА. Результаты первого двойного слепого плацебоконтролируемого исследования, опубликованные в 1984 г., показали, что гипосенсибилизация аспирином улучшает состояние пациента с БА и контролирует полипозный процесс, но не имеет отсроченного эффекта27.
Заболевание манифестирует в возрасте 30–40 лет, чаще у женщин, и может прогрессировать даже при исключении из схемы терапии аспирина или нестероидных противовоспалительных препаратов (НПВП). Гиперчувствительностью к аспирину страдают около 20–40% больных хроническим риносинуситом и астмой.
При аллергическом рините доказана эффективность анти-IgE-терапии. Анти-ИЛ-5-моноклональные антитела успешно изучались при эозинофильных процессах, не связанных с IgE-воспалением (астматическая триада).
Оценке эффективности реслизумаба у больных БА с сопутствующим ПРС, а также лекарственной гиперчувствительностью к аспирину или без таковой был посвящен post-hoc-анализ данных двух ключевых 52-недельных исследований III фазы программы BREATH28. Пациенты с ПСР и БА (n = 150) характеризовались сопоставимыми демографическими показателями, но отличались от группы больных БА без проявлений ПРС (n = 800) более тяжелым течением астмы (более низкие показатели ОФВ1, более частое применение пероральных ГКС и бета-2-агонистов длительного действия, более низкий контроль БА). В отличие от пациентов без ПРС у пациентов с БА и ПРС уровень эозинофилов был достоверно выше, а показатель аллергической сенсибилизации значительно ниже.
Использование реслизумаба способствовало снижению частоты обострений в общей популяции – на 44%, в группе больных БА с ПРС – на 83% по сравнению с плацебо. Этот показатель оставался высоким и у больных БА и ПРС с чувствительностью к аспирину и без таковой – 79 и 84% соответственно.
Аналогичная тенденция наблюдалась и в отношении частоты обострений БА, потребовавших назначения системных ГКС на срок более трех дней. На фоне применения реслизумаба частота обострений в общей популяции снизилась на 47%, у больных БА и ПРС – на 84%, пациентов с БА и ПРС без чувствительности к аспирину – на 85%, больных БА и ПРС с чувствительностью к аспирину – на 83% по сравнению с плацебо.
Применение реслизумаба у больных тяжелой неконтролируемой астмой в сочетании с ПРС значимо улучшило функцию легких: прирост ОФВ1 у пациентов с БА и ПРС в среднем составил 320 мл. Такая же положительная динамика отмечалась в данной подгруппе в отношении улучшения контроля астмы и качества жизни29.
На основании полученных данных были сделаны следующие выводы:
- добавление реслизумаба к терапии больных БА и ПРС снижает частоту клинически значимых обострений БА на 83% по сравнению с плацебо (у больных с гиперчувствительностью к аспирину и без таковой на 79 и 84% соответственно);
- применение реслизумаба ассоциировано с улучшением легочной функции, показателей контроля БА и качества жизни;
- с учетом высокой эффективности реслизумаба у больных БА в сочетании с ПРС и гиперчувствительностью к аспирину (или без нее) целесообразно проведение специальных проспективных исследований терапии реслизумабом в отношении собственно ПРС.
Таким образом, наличие ПРС у больных тяжелой астмой служит основным клиническим критерием отбора пациентов для проведения анти-ИЛ-5-терапии. «Благодаря адекватной тактике лечения, в том числе улучшению носового дыхания, наши пациенты обретают новые краски жизни», – резюмировала профессор О.М. Курбачева.
Результаты использования реслизумаба в реальной клинической практике
Заведующая консультативно-диагностическим отделением городской клинической больницы (ГКБ) № 52 г. Москвы, главный внештатный аллерголог-иммунолог Северного и Северо-Западного административных округов г. Москвы Елена Николаевна БОБРИКОВА поделилась опытом успешного применения реслизумаба у пациентов с тяжелой БА, поступающих на лечение в Центр аллергологии и иммунологии, созданный на базе ГКБ № 52.
Центр аллергологии и иммунологии включает консультативно-диагностические отделение и дневной стационар с кабинетом биологической генно-инженерной терапии. Выбор кандидата на иммунобиологическую терапию основан на комплексном мультидисциплинарном подходе.
Основная цель первичного приема в кабинете биологической терапии заключается в рассмотрении возможности назначения терапии 5-й ступени по GINA, а также в необходимости подтверждения диагноза БА, оценки факторов, препятствующих контролю над заболеванием, определения атопического статуса, уровня эозинофильного воспаления, исключения глистной инвазии, проведения консультации смежных специалистов, оценки соотношения «польза – риск». При наличии показаний, благоприятном соотношении «риск – польза» осуществляется выбор моноклонального антитела, рассчитываются доза и кратность приема.
В Центре иммунологии накоплен опыт применения анти-IgE-препаратов (омализумаба) у 44 больных БА. С июля 2018 г. проводится биологическая терапия анти-ИЛ-5-препаратом реслизумабом (Синкейро). Ее получают пять пациентов с тяжелой астмой, еще трое больных проходят дообследование перед назначением данной терапии.
Кинический пример 1. Пациентка Б., 71 год, рост – 151 см, вес – 70 кг, индекс массы тела (ИМТ) – 30,7 кг/м2. В мае 2018 г. поступила в Центр иммунологии и аллергологии с жалобами на персистирующие симптомы (кашель с отделением мокроты, одышка при небольшой физической нагрузке) с эпизодами диспноэ до 4–6 раз в день, практически ежедневные ночные симптомы, высокую потребность в бета-2-агонистах короткого действия. Симптомы астмы возникают на холоде, при контакте с резкими запахами, уборке пыли дома, минимальной физической нагрузке. У пациентки отмечаются постоянное затрудненное носовое дыхание, сниженное обоняние, ринорея, ежедневная потребность в деконгестантах.
Анамнез. Явления риноконъюнктивита весной и летом с семи лет, в настоящее время симптомы аллергического ринита – круглый год. В 1996 г. в возрасте 50 лет появились первые приступы удушья, диагностирована БА, состояние прогрессивно ухудшалось. В 2016–2017 гг. отмечалось до четырех приступов удушья в год. За предшествующие 12 месяцев имели место два обострения, потребовавшие назначения дополнительных доз системных ГКС и ИГКС.
Аллергоанамнез и другие факторы. Круглогодичный аллергический ринит с детства, псориаз, полисенсибилизация (пыльцевые, бытовые аллергены). Семейный анамнез не отягощен. Не курит. Не подвергалась пассивному курению. Профессиональные вредные факторы отсутствуют.
Анамнез лечения. Аллергенспецифическую иммунотерапию не получала. С 2002 г. проводилась регулярная терапия беклометазона дипропионатом в низких дозах, в сезон пыления – короткие курсы системных ГКС. С 2010 г. по настоящее время – комбинированная терапия ИГКС в высокой дозе + бета-2-агонисты длительного действия. В 2011–2016 гг. дополнительно применяла триамцинолон 4 мг/сут, сейчас – салметерол + флутиказон 50/500 мкг два раза в сутки, тиотропия бромид 2,5 мкг два вдоха один раз в сутки, эпизоды курсового приема небулизированного будесонида.
Сопутствующая патология. Псориаз, распространенная форма. Хронический гастрит. Гипертоническая болезнь 2-й степени, риск 3.
Результаты обследования. Физикальные данные: ACQ – 5 баллов, на фоне утренней ингаляции салметеролом/флутиказоном дыхание жесткое, хрипы сухие, свистящие, рассеянно над всеми легочными полями. Лабораторные исследования (за 12 месяцев): общий IgE – крайне высокие значения за 12 месяцев, июль 2018 г. – 1638 МЕ/мл, персистирующая эозинофилия крови на протяжении нескольких лет (> 300 кл/мкл), в мае 2018 г.– 14% (980 кл/мкл), на момент подбора иммунобиологической терапии в июле 2018 г. – 12% (636 кл/мкл), положительный тест на специфический IgE (домашняя пыль, клещи домашней пыли, перо подушки, шерсть кошки, пыльца березы, ольхи, полыни).
Функция внешнего дыхания (ФВД) в динамике: ОФВ1 исходно 45–56%, обратимость обструкции при пробе с бронхолитиком, ОФВ1/ФЖЕЛ < 0,7.
Другие методы исследования: рентгенография органов грудной клетки (ОГК) не выявила очаговых и инфильтративных изменений, корни не расширены, структурные синусы свободные.
По мнению Е.Н. Бобриковой, при назначении биологической терапии данной пациентке прежде всего нужно учитывать пожилой возраст (71 год), сопутствующую патологию, астму поздней манифестации (50 лет), тяжелое персистирующее течение заболевания, не контролируемое на 4–5-й ступени терапии по GINA, поливалентную сенсибилизацию, круглогодичный аллергический ринит в сочетании с псориазом, высокий ИМТ, частые обострения астмы, персистирующую эозинофилию крови, высокий общий IgE, фиксированную бронхиальную обструкцию.
Поскольку у пациентки Б. тяжелая неконтролируемая аллергическая БА с эозинофильным воспалением, круглогодичным аллергическим ринитом, распространенной формой псориаза и ожирением 1-й степени, целесообразно в схему лечения в качестве иммунобиологического препарата включить омализумаб. Однако у ряда больных астмой с клинически значимой атопией и подтвержденной связью между экспозицией аллергенов и развитием симптомов/обострений расчет дозы омализумаба возможен только при определенных показателях, в частности при уровне общего IgE 30–1500 МЕ/мл. У пациентки Б. уровень общего IgE составлял 1638 МЕ/мл, что не соответствовало критериям назначения омализумаба.
Выраженная эозинофилия, частые обострения астмы, потребность в регулярном приеме системных ГКС, невозможность использования анти-IgE-терапии послужили основанием для назначения пациентке Б. анти-ИЛ-5-терапии реслизумабом (Синкейро). Доза препарата Синкейро и режим введения подбирались на основании инструкции: разовая доза составила 210 мг (3 мг/кг на 70 кг), 21 мл (два флакона и 1 мл).
Таким образом, с июля 2018 г. пациентка Б. получает 200 мг препарата Синкейро (два флакона) каждые четыре недели. Уже после приема первой дозы Синкейро отмечалось выраженное улучшение показателей ОФВ1 (+390 мл) и ОФВ1/ФЖЕЛ (> 0,7).
На фоне трехмесячной терапии препаратом Синкейро (реслизумабом) у пациентки Б. наблюдаются выраженное субъективное улучшение состояния, восстановление восприятия запахов (субъективная оценка), уменьшение выраженности симптомов БА по ACQ, улучшение функции легких (ОФВ1 – 110%), снижение уровня эозинофилов в периферической крови (2,4%, 78 кл/мкл) и суммарной дозы ИГКС, уменьшение потребности в назальных сосудосуживающих препаратах.
По словам Е.Н. Бобриковой, совершенно неожиданным результатом трехмесячной терапии препаратом Синкейро стало выраженное снижение активности псориатического поражения кожи.
Клинический пример 2. Пациентка К., 43 года, рост – 167 см, вес – 57 кг, ИМТ – 20,4 кг/м2, под наблюдением врача находится с февраля 2015 г. За медицинской помощью обратилась по поводу персистирующих симптомов (заложенность в груди по утрам, одышка при ускоренной ходьбе, кашель), эпизодов ночного апноэ один-два раза в неделю, постоянного затрудненного носового дыхания, постоянного слизистого отделяемого из носа, отсутствия восприятия запахов, искаженного восприятия вкуса пищи, ежедневной потребности в деконгестантах.
Анамнез. В 2012 г. в возрасте 37 лет диагностирована астма. Заболевание манифестировало с эпизода тяжелого обострения. Имеет место лекарственная гиперчувствительность к НПВП с развитием бронхоспазма. Страдает полипозным риносинуситом, перенесла две полипэктомии. В настоящий момент – полипозные вегетации. За предшествующие два месяца – два обострения астмы, повлекшие за собой увеличение суточной дозы ИГКС.
Аллергоанамнез и другие факторы. Клинических данных об атопии нет. Аллергоанамнез, равно как и семейный анамнез, не отягощен. Не курит. Пассивному курению никогда не подвергалась.
Анамнез лечения. Регулярно использует будесонид/формотерол 160/4,5 мкг по две дозы два раза в сутки. Интраназально применяет мометазона фуроат 50 мкг по две дозы два раза в сутки в каждый носовой ход.
Результаты обследования. Физикальные данные: ACQ – 15 баллов. На фоне утренней ингаляции будесонидом/формотеролом дыхание жесткое, хрипы сухие, единичные. Лабораторные исследования (за 12 месяцев): при аллергическом обследовании с использованием аллергочипа методом ImmunoCAP ISAC иммуноглобулинов класса Е к аллергокомпонентам не выявлено. Персистирующая эозинофилия крови (> 300 кл/мкл): февраль 2018 г. – 17% (595 кл/мкл), на момент подбора иммунобиологической терапии в августе 2018 г. – 17,4% (680 кл/мкл).
Другие методы исследования. Рентгенография ОГК: легочные поля прозрачные, очаговых и инфильтративных изменений не выявлено.
При подборе пациентке К. иммунобиологической терапии следует обратить внимание на позднее начало астмы, тяжелое течение с дебюта заболевания, частые обострения БА, хронический рецидивирующий ПРС, непереносимость НПВП, персистирующую эозинофилию (> 300 кл/мкл), отсутствие атопического анамнеза, отрицательные IgE-тесты.
Поскольку пациентка страдает эндогенной БА (эозинофильной, НПВП-ассоциированной) с тяжелым, неконтролируемым течением в сочетании с ПРС, было принято решение о добавлении к базисной терапии реслизумаба (Синкейро). Доза препарата Синкейро и режим введения рассчитывались на основании инструкции: необходимая разовая доза составила 171 мг (3 мг/кг на 57 кг), 17 мл (один флакон и 7 мл). Пациентка К. получает 170 мг реслизумаба (1,7 флакона Синкейро) каждые четыре недели.
Уже через месяц терапии препаратом Синкейро у пациентки улучшилась функция дыхания: прирост ОФВ1 составил 160 мл, ОФВ1/ФЖЕЛ > 0,7.
Оценка динамики симптомов риносинусита по опроснику SNOT-20 и результаты осмотра ЛОР-врачом подтвердили значительное купирование симптомов ПРС: носовое дыхание улучшилось, выделения из носа незначительные, водянистые, слизистая оболочка бледно-розовая. В среднем носовом ходе с двух сторон – полипозные вегетации, размер которых по сравнению с июлем 2018 г. не увеличен, отечность слизистой оболочки носовых раковин отсутствует.
Оценка динамики состояния пациентки К. после трех месяцев терапии реслизумабом показала уменьшение выраженности симптомов астмы – улучшение клинического контроля по ACQ, улучшение функции легких (несмотря на исходные показатели), значительное снижение уровня эозинофилов в периферической крови. Согласно субъективной оценке, терапия препаратом Синкейро способствовала значительному улучшению самочувствия, восстановлению восприятия запахов и вкусов, снижению потребности в назальных сосудосуживающих препаратах.
Преимущества индивидуального расчета дозы и внутривенной формы введения Синкейро
Как отметил заведующий кафедрой общей и клинической фармакологии Российского университета дружбы народов, д.м.н., профессор Сергей Кенсаринович ЗЫРЯНОВ, в настоящее время препарат Синкейро (реслизумаб), зарегистрированный в США, Канаде, странах Евросоюза, России, Израиле, Южной Корее, успешно внедряется в мировую клиническую практику для лечения больных тяжелой БА с эозинофильным типом воспаления дыхательных путей. Солидная доказательная база демонстрирует высокую эффективность препарата Синкейро, обусловленную его тройным действием в виде снижения частоты обострений, улучшения функции легких и повышения качества жизни.
Синкейро характеризуется оптимальной дозой, рассчитываемой в зависимости от веса. Инфузия проводится в индивидуально подобранных дозах из расчета 3 мг/кг каждые четыре недели, поставляется в виде раствора 100 мг/10 мл, готового для разбавления и внутривенного введения. По оценкам, инфузионная терапия препаратом Синкейро хорошо переносится пациентами. Около девяти из десяти пациентов отдают предпочтение дальнейшему лечению препаратом Синкейро8, 11, 29.
В чем заключаются преимущества препарата Синкейро перед другими иммунобиологическими препаратами, в частности омализумабом?
Во-первых, Синкейро (реслизумаб) в отличие от омализумаба эффективен и при аллергической, и при неаллергической форме БА с уровнем эозинофилов в крови ≥ 400 кл/мкл.
Во-вторых, кратность введения препарата Синкейро (реслизумаба) не зависит от рассчитанной дозы (один раз в четыре недели), что значительно сокращает частоту запланированных обращений в учреждения здравоохранения.
В-третьих, препарат Синкейро для внутривенного введения характеризуется 100-процентной биодоступностью (для сравнения: биодоступность омализумаба для подкожного введения – 62%, меполизумаба – 74–80%).
Абсолютная биодоступность Синкейро (реслизумаба) позволяет достигать максимальной терапевтической концентрации уже в конце инфузии препарата, в то время как максимальная терапевтическая концентрация омализумаба отмечается через семь-восемь дней после введения, а меполизумаба – через 6–8 дней. Более высокая доза и внутривенное введение обеспечивают и большее количество препарата там, где это необходимо.
Реслизумаб обладает более высокой аффинностью к ИЛ-5 по сравнению с меполизумабом и характеризуется более высокой эффективностью при ингибировании активности ИЛ-5. Важно, что реслизумаб обеспечивает скорректированный в зависимости от веса подход к выбору дозы с целью оптимальной эффективности у разных категорий пациентов30.
Поскольку разовая доза препарата Синкейро рассчитывается исходя из веса пациента, перед каждым введением препарата больного следует взвешивать. Необходимая доза препарата Синкейро (мл) рассчитывается по формуле:
требуемое количество = 0,3 мг × масса тела (кг).
Рекомендуемая доза составляет 3 мг/кг один раз в четыре недели.
Как часто возникают нежелательные реакции при внутривенном введении препарата Синкейро?
Анафилактические реакции во время введения препарата или через 20 минут после завершения инфузии уже на второй дозе имели место у 0,19% пациентов (три случая из 1611). Проявления включали одышку, хрипы, желудочно-кишечные симптомы, озноб, поражения кожи или слизистых оболочек. Выявленные реакции были полностью разрешены на стандартной терапии без остаточных явлений. Ни у кого из пациентов не зафиксирована иммунная реакция в виде образования антител на реслизумаб31.
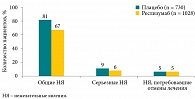
Объединенные данные, полученные в рамках программы BREATH, продемонстрировали сопоставимый с плацебо профиль безопасности реслизумаба (рис. 4).
Частота развития всех нежелательных явлений и серьезных нежелательных явлений в группе реслизумаба была даже несколько ниже, чем в группе плацебо (67 и 6% против 81 и 9% соответственно). Частота отмены лечения вследствие нежелательных явлений была равнозначной во всех группах – 5%.
Причинно-следственная связь между использованием реслизумаба и риском развития злокачественных новообразований не установлена.
В доклинических исследованиях реслизумаб не оказывал важного с точки зрения фармакологии мутагенного или канцерогенного воздействия.
Терапевтические лекарственные препараты могут оказывать непредвиденное токсическое воздействие на мышечные ткани32. Чтобы оценить, приводит ли терапия реслизумабом к повреждению мышц, миозиту или рабдомиолизу, были проанализированы нежелательные явления со стороны скелетной мускулатуры. Согласно анализу, в отличие от пациентов группы плацебо у большинства пациентов группы реслизумаба наблюдались нежелательные явления, связанные с миалгией и носившие временный характер. Однако данные, которые указывали бы на повреждение мышц, миозит или рабдомиолиз, отсутствовали.
Результаты программы BREATH в отношении профиля безопасности реслизумаба8, 10, 13 показали, что:
- частота развития нежелательных явлений в группе реслизумаба ниже, чем в группе плацебо;
- типы зарегистрированных нежелательных явлений вполне ожидаемые для исследуемой популяции (например, назофарингит, головная боль, синусит);
- все летальные исходы или усугубления БА не связаны с применением реслизумаба;
- достаточно редкие анафилактические реакции контролируемые и расценены как нежелательная лекарственная реакция на реслизумб.
В целом реслизумаб в виде внутривенной инфузии в дозе 3,0 мг/кг каждые четыре недели характеризуется приемлемым профилем безопасности.
«На сегодняшний день мы имеем высокоэффективный препарат в лекарственной форме с абсолютной биодоступностью. Наличие такой лекарственной формы позволяет достигать высоких результатов и достаточно безопасно лечить наших пациентов», – подчеркнул профессор С.К. Зырянов в заключение.
Заключение
Подводя итог, председатель симпозиума профессор А.В. Емельянов отметил, что появление в арсенале российских специалистов нового анти-ИЛ-5-иммунологического биопрепарата Синкейро (реслизумаба), зарегистрированного в России, расширяет возможности лечения больных тяжелой неконтролируемой БА с эозинофильным воспалением.
Результаты рандомизированных исследований и клинический опыт продемонстрировали хорошую переносимость и высокую эффективность препарата Синкейро в случае аллергической и неаллергической тяжелой БА, позднего дебюта заболевания, полипозного риносинусита, а также при наличии или отсутствии гиперчувствительности к аспирину.
Клинические эффекты препарата Синкейро (реслизумаба) проявляются снижением частоты обострений БА, улучшением функции легких и контроля заболевания.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.