Долгосрочная эффективность нетакимаба при лечении пациентов с псориазом
- Аннотация
- Статья
- Ссылки
- English





Введение
Псориаз – хроническое воспалительное и генетически детерминированное заболевание с распространенностью около 2–3% в мире [1]. Наличие коморбидных патологий, включая воспалительные заболевания кишечника, ангиопатии и ишемическую болезнь сердца, метаболический синдром, лимфому, депрессивные расстройства, влияет на физическое и эмоциональное состояние пациента, а также приверженность к лечению [2]. Негативное влияние псориаза на качество жизни пациентов сопоставимо с влиянием патологий сердечно-сосудистой системы и онкологических заболеваний [3]. С каждым годом данные о патогенезе псориаза расширяются. Теперь механизмы развития заболевания не ограничиваются расстройством пролиферации кератиноцитов. Его клинические проявления являются вторичными по отношению к сложному взаимодействию между иммунными клетками, клетками кожи и дермальным эндотелием, а также каскаду различных провоспалительных цитокинов и хемокинов [4, 5].
С учетом иммуноопосредованных механизмов развития и мультифакторной природы терапия псориаза кожи (ПсО) часто пожизненная и зависит от множества аспектов, таких как клинический фенотип, распространенность и тяжесть процесса, наличие псориатического артрита (ПсА), сопутствующих и коморбидных патологий. Стандартные системные базисные («традиционные») методы лечения не в полной мере отвечают потребностям пациентов и врачей из-за ограниченной эффективности, побочных эффектов и различных неудобств. Знание патогенетических механизмов, лежащих в основе развития ПсО, позволяет сегодня избирательно воздействовать генно-инженерными биологическими препаратами (ГИБП) на ключевые звенья иммунопатогенетического каскада, практически не влияя на защитные факторы иммунной системы пациента, в отличие от базисной противовоспалительной терапии. В настоящее время ГИБП все чаще используются при терапии псориаза и псориатического артрита ввиду хорошего профиля безопасности и эффективности [6, 7]. Несмотря на то что большинство данных об этих препаратах получены в результате относительно ограниченных краткосрочных наблюдений, в последнее время появляется все больше исследований о накопившемся опыте длительного применения ГИБП. Наиболее часто используемый параметр для оценки эффективности – это процент субъектов исследования, у которых наблюдается 75%-ное улучшение индекса площади и тяжести псориаза (дельта Psoriasis Area and Severity Index (PASI) 75), оцененное после 12 недель лечения [8]. Также при изучении эффективности терапии часто оценивается качество жизни пациентов согласно дерматологическому индексу качества жизни (ДИКЖ). Все чаще в литературе упоминают термин «выживаемость терапии». Он отражает время от начала терапии ГИБП до ее прекращения по каким-либо причинам. Это интегральная характеристика препарата, отражающая его эффективность, переносимость и общую приемлемость для пациента и врача [9]. Опыт показывает, что в то время как у многих пациентов, принимавших ГИБП, наблюдаются отличные долгосрочные результаты, у некоторых пациентов первоначальное улучшение не сохраняется. Таким образом, необходимо полное понимание эффективности этих препаратов при более длительных курсах терапии.
На сегодняшний день одними из наиболее перспективных достижений фармакотерапии для лечения псориаза, псориатического артрита среди иммуносупрессивных средств являются ГИБП из группы ингибиторов интерлейкина (ИЛ) 17А (анти-ИЛ-17А), так как считается, что данный цитокин является одной из ключевых молекул, участвующих в аутовоспалительных реакциях при ПсО и ПсА. В настоящее время накоплен опыт использования анти-ИЛ-17А для оценки не только краткосрочной эффективности, но и отдаленных результатов.
В исследовании U. Mrowietz и соавт. во время наблюдения в течение трех лет в когорте пациентов, получавших стандартную схему препарата анти-ИЛ-17А, устойчивый ответ на лечение в виде показателя PASI 90 отмечался у 63,8% больных, PASI 100 – у 42,6%. При использовании препарата анти-ИЛ-17А по мере требования PASI 90 и PASI 100 в группе лечения через три года составили 14,8 и 5,3% соответственно [10].
Практический и научный интерес представляют результаты проведенного клинического исследования SCULPTURE (n = 842 пациента), целью которого была оценка долгосрочной эффективности анти-ИЛ-17А у пациентов со среднетяжелым и тяжелым псориазом. В течение 156 недель пациенты получали терапию по стандартной схеме (непрерывно с фиксированными промежутками), либо прерывистым курсом с возобновлением лечения только в случае рецидива псориаза. Результаты исследования показали, что при непрерывном фиксированном режиме введения не наблюдалось снижение терапевтического эффекта: через 52 недели дельта PASI 90 отмечали у 88,9% пациентов, через три года – у 83%. ДИКЖ держался на уровне 0/1 у 72,7% исследуемых в течение года и у 65,5% через три года. Профиль безопасности анти-ИЛ-17А оставался благоприятным на протяжении всех трех лет исследования [11].
При оценке более 2000 пациентов в исследованиях ERASURE и FIXTURE (n = 2042) было показано более быстрое достижение показателей ДИКЖ 0/1 на фоне терапии препаратом анти-ИЛ-17А по сравнению с другими ГИБП из группы ингибиторов фактора некроза опухоли альфа (анти-ФНО-α) на 12-й и 24-й неделе соответственно [12]. Максимальный терапевтический результат в отношении тяжести и распространенности псориатических высыпаний был зарегистрирован на 16-й неделе лечения. В этот срок значения индекса PASI 75 достигли 86,1% (ERASURE) и 86,7% (FIXTURE) пациентов на фоне лечения анти-ИЛ-17А. Через год непрерывного лечения отмечалась высокая эффективность, где терапевтический ответ по PASI 75 сохранялся у 74,3% (ERASURE) и 86,7% (FIXTURE) пациентов на фоне терапии анти-ИЛ-17А.
Согласно метаанализу J. Ryoo и соавт. по результатам семи клинических исследований, посвященных оценке эффективности и безопасности анти-ИЛ-17А, большинство пациентов сохраняли ответ PASI 90 на 52-й неделе исследования [13].
В клиническом исследовании R. Ruiz-Villaverde и соавт. были ретроспективно проанализированы данные эффективности анти-ИЛ-17А у 171 пациента с бляшечным псориазом в течение 152 недель терапии. В общей сложности 171 пролеченный пациент был ретроспективно зарегистрирован и проанализирован в течение 152 недель (у 37,40% был диагностирован ПсА). Средняя выживаемость ГИБП у пациентов с ПсА составила 86% (расчетное среднее время выживаемости 130 недель) в сравнении с 88% (расчетное среднее время выживаемости 133 недели) у пациентов без ПсА [14].
S. Dastoli и соавт. также провели многоцентровое ретроспективное исследование с целью анализа долгосрочной эффективности анти-ИЛ-17А на протяжении 240 недель у пациентов с псориазом средней и тяжелой степени. Лечение анти-ИЛ-17А привело к значительному снижению среднего балла PASI у всех пациентов в группе, на 4-й и 12-й неделе во всех других оцениваемых показателях (p < 0,0001), а также с 24-й до 48-й, 96-й, 144-й, 192-й и 240-й недели (p ≤ 0,0001 для всех оценок, за исключением 192-й недели (p = 0,024), с 96-й по 192-ю неделю (p = 0,018) и с 144-й по 192-ю неделю (p = 0,007)). Отмечалось и снижение распространенности процесса согласно индексу BSA у всех пациентов от исходного уровня до 4-й, 12-й и 24-й недели (p < 0,0001) и с 48-й до 96-й, 144-й, 240-й недели (p = 0,001; p = 0,0001 и p = 0,008 соответственно). К 4-й неделе только 22,5% пациентов остались в группе с тяжелой BSA, а остальные – в группе со средней (62,7%) или легкой (14,8%) степенью. Улучшения по BSA продолжались с течением времени, и к 24-й неделе только у 1,5% пациентов отмечалась BSA > 10. Доля пациентов с BSA > 10 оставалась очень низкой при продолжении лечения анти-ИЛ-17А, и от 83,0 до 93,6% пациентов находились в группе BSA < 5 к 24-й неделе. Кроме того, отмечалось выраженное и устойчивое улучшение качества жизни пациентов согласно ДИКЖ [15].
Исследование GESTURE показало, что анти-ИЛ-17А обеспечивают выраженный и устойчивый ответ в течение 2,5 лет при трудно поддающемуся лечению ладонно-подошвенного псориаза. Первичная конечная точка, оценка ppIGA (Palmoplantar Investigator's Global Assessment) 0 или 1, была достигнута на 16-й неделе. Эффект сохранялся в течение 2,5 лет, при этом около 60% пациентов достигли чистой или почти чистой кожи ладоней и подошв (ppIGA 0 или 1). Через 2,5 года средний процент ладонно-подошвенного псориаза также снизился (-74,7%). В общей сложности около 18% пациентов не испытывали проблем с двигательными функциями рук и ног [16].
По данным ретроспективного исследования M. Burlando и соавт., также отмечалась эффективность и безопасность анти-ИЛ-17А в течение 156 недель терапии. Клинический ответ, который был достигнут уже к 12-й неделе, сохранялся в течение следующих трех лет у большинства пациентов. Не было обнаружено статистически значимой разницы между био-наивными и био-переключаемыми пациентами, а масса тела и продолжительность заболевания не влияли на эффективность препарата [17].
Кроме того, по данным других исследований и собственного опыта, была отмечена не только высокая эффективность анти-ИЛ-17А при псориазе кожи, но и при поражениях костно-суставной системы [18].
Согласно недавнему исследованию [20], к 52-й неделе 100% пациентов достигли уровня PASI 75, 90,5% – PASI 90 и 85,7% – PASI 100, NAPSI 100 (Nаil Psoriasis Severity Index, индекс тяжести псориатического поражения ногтевых пластинок) отмечалось у 71,4% пациентов на фоне терапии анти-ИЛ-17А. Все пациенты отмечали уменьшение интенсивности воспалительной боли на 12-й, 24-й и 52-й неделе со средним значением BASDAI (Bath Ankylosing Spondylitis Disease Activity Index – Батский индекс активности анкилозирующего спондилита) 5,9 (SD = 2,3); 4,1 (SD = 1,3) и 2,7 (SD = 0,9) соответственно. Установлено, что 90,5% пациентов достигли ACR20 (American College of Rheumatology – Консенсус Американской коллегии ревматологов) к концу исследования на 52-й неделе. При этом большинство пациентов (85,7%) достигли ремиссии или низкой активности заболевания по DAPSA (Disease Activity in Psoriatic Arthritis – Индекс активности псориатического артрита) через 24 недели терапии. Среднее значение ASDAS (Аnkylosing Spondylitis Disease Activity Score – Индекс активности анкилозирующего спондилита) на 12-й, 24-й, 52-й неделях составило 3,07 (0,9); 2,2 (1,0) и 2,3 (0,9) соответственно [19–21].
В исследовании Л.С. Кругловой и соавт. была проанализирована долгосрочная эффективность (52 недели) анти-ИЛ-17А у пациентов с небольшим сроком заболевания (менее одного года). К четвертой неделе 68,75% пациентов достигли уровня PASI 75, 37,5% – PASI 90 и 18,75% – PASI 100. К восьмой неделе дельта PASI 75 отмечена у 87,5% пациентов, у 68,75% – PASI 90 и у 50% – PASI 100. К 24-й неделе 100% пациентов достигли уровня PASI 75, 81,25% – PASI 90 и 68,75% – PASI 100. К 52-й неделе дельта PASI 75 отмечена у 100% пациентов, у 100% – PASI 90 и у 87,5% – PASI 100. Пациенты с меньшим стажем заболевания на фоне терапии анти-ИЛ-17А достигают PASI 75, PASI 90, PASI 100 в более короткие сроки (сравнение с данными клинических исследований) [22].
В международном многоцентровом двойном слепом плацебо-контролируемом клиническом исследовании PLANETA также показана долгосрочная эффективность анти-ИЛ-17А на протяжении 56 недель терапии. В общей сложности 77,7; 83,3 и 0% пациентов имели ответ PASI 75 на 12-й неделе при терапии анти-ИЛ-17А один раз в две недели, один раз в четыре недели и контрольной группе (плацебо) соответственно. Эффект сохранялся в течение всего однолетнего периода терапии [23].
Длительный устойчивый ответ на терапию анти-ИЛ-17А отмечался и при терапии псориаза у детей (средний возраст – 13,5 лет) в течение 108 недель. Достижение дельта PASI 75 отмечалось у 91,7% пациентов, PASI 90 – у 79,0%, PASI 100 – у 55,1%, sPGA (Static Physician Global Assessment, статическая глобальная оценка врача) 0 или 1 у 78,3% и sPGA 0 у 52,4%. Улучшения со стороны ногтевых пластин отмечались у 68,1% пациентов, со стороны поражений на ладонях и стопах – у 90,0%, волосистой части головы – у 76,2%, в паховой области – у 87,5% [24].
Последние исследования показывают, что ИЛ-17А также играет важную роль в патогенезе ожирения и метаболического синдрома, а применение препаратов анти-ИЛ-17А обосновано при наличии данных коморбидных состояний [25]. Согласно исследованиям при анализе выживаемости ГИБП было показано, что индекс массы тела (ИМТ) ≥ 30 кг/м2 отрицательно влиял на выживаемость терапии, однако в меньшей степени для анти-ИЛ-17А по сравнению с другими ГИБП [26]. Большинство исследований описывают положительную корреляцию терапии анти-ИЛ-17А и высокого ИМТ в виде отсутствия увеличения индекса (возрастания массы тела). Сравнительное исследование, проведенное Takamura и соавт., впервые показало, что лечение анти-ИЛ-17А не влияет на массу тела, сообщалось о постоянных уровнях ИМТ после семи месяцев терапии [27]. Их семилетнее ретроспективное исследование также показало, что по сравнению с инфликсимабом (где средний ИМТ увеличился с 24,7 до 25,7 кг/м2 после семи месяцев) лечение анти-ИЛ-17А поддерживало средние уровни ИМТ на постоянном уровне [26]. Аналогичным образом, результаты 12-недельного клинического исследования (UNCOVER-1, UNCOVER-2 и UNCOVER-3) показали, что анти-ИЛ-17А не оказали влияние как на показатели сердечно-сосудистой системы, так и на массу тела [28].
K. Reich и соавт. в своих работах указывают, что как профили эффективности, так и безопасности анти-ИЛ-17А были схожи независимо от веса тела пациентов. Кроме того, не наблюдалось существенных различий в показателях ответа PASI 75 между степенью ИМТ [29]. Эти данные подтверждаются и в других исследованиях [30, 31].
В ряде работ сообщается, что у пациентов, получавших лечение анти-ИЛ-17А в течение 52 недель, отмечалась не только выраженная положительная динамика от проведенной терапии в виде регресса высыпаний, но также стойко снижался индекс массы тела [25].
У пациентов с псориазом, которые находятся на терапии ГИБП, в т.ч. анти-ИЛ-17А, могут возникать обострения псориаза (вторичная неэффективность или ускользание эффекта). Тем не менее в ряде случаев обострения заболевания целесообразно не прерывать сразу терапию, а вместо этого использовать местные кортикостероиды, УФВ 311 нм, что позволяет вернуть контроль над псориазом.
Несмотря на то что к настоящему времени не опубликовано результатов прямых сравнительных исследований долгосрочной терапии анти-ИЛ-17А и другими биологическими препаратами, полученные данные по непрерывному лечению анти-ИЛ-17А больных псориазом выглядят весьма впечатляющими, так как позволяют добиться у подавляющего числа больных уменьшения значений PASI не только на 75%, но и на 90%, 100%, что в полной мере соответствует стратегии «лечение до достижения цели» (Т2Т). В этой связи именно значения индекса PASI 90, а не традиционный ответ на терапию PASI 75, могут быть рассмотрены в качестве новой глобальной цели по эффективности терапии больных псориазом, к которой следует стремиться в реальной клинической практике. Ранее недостижимое у большинства пациентов стойкое и долгосрочное уменьшение абсолютных значений индекса PASI 90 в настоящий момент несет определяющее значение для устойчивости терапии ГИБП при псориазе и повышения качества жизни пациентов с данным дерматозом.
Цель анализа обобщенных данных длительного применения отечественного препарата нетакимаб (Эфлейра) – исследование долгосрочной эффективности и влияния на качество жизни в целом в когорте пациентов, а также в зависимости от наличия избыточной массы тела у пациентов.
Материал и методы
В наблюдательное многоцентровое исследование были включены данные пациентов, которые ответили на терапию нетакимабом как минимум по PASI 75 в сроки 52 недели и продолжали лечение на протяжении 156 недель.
Критерии включения в исследование: возраст старше 18 (включительно) и младше 65 лет, пациенты с установленным диагнозом вульгарный псориаз, исходный индекс PASI более 10 баллов, достижение PASI 75 в контрольной точке 52 недели, соблюдение режима введения нетакимаба, высокая комплаентность, наблюдение в течение трех лет, подписание информированного согласия.
Критерии невключения в исследование: возраст младше 18 и старше 65 лет, отличные от вульгарного фенотипы псориаза, низкая комплаентность пациентов.
Для статистического анализа отдаленных результатов наблюдений применения ГИБП нетакимаб (анти-ИЛ-17А) отобрали 241 пациента с диагнозом бляшечный (вульгарный) псориаз, находившегося на терапии данным препаратом в течение трех лет. Среди них 132 (54,8%) женщины и 109 (45,2%) мужчин. Средний возраст – 43,6 ± 5,9 лет (минимальный возраст – 24 года, максимальный возраст – 60 лет). Длительность заболевания варьировала от 2 до 37 лет и в среднем составила 12,4 ± 3,7 лет. Все пациенты получали препарат нетакимаб 120 мг в виде 2 п/к инъекций на 0-й, 1-й, 2-й неделях и затем один раз в четыре недели.
В результате исследования был получен датасет с данными по показателям PASI и ДИКЖ с включением 241 пациента, находящегося под наблюдением на протяжении 156 недель. Контрольные точки оценки показателей: 0-я, 12-я, 24-я, 36-я, 52-я, 78-я, 104-я, 156-я недели. Также было проведено исследование данных по показателям PASI и ДИКЖ у пациентов в зависимости от наличия избыточной массы тела (ИМТ > 25).
Статистическая обработка выполнена в среде R v. 4.3.1. Рассчитан процент достижения пациентами PASI 75, 90, 100 и ДИКЖ 0–1, 2–5, 6–10, 11–20, 21–30 на точках оценки. Рассчитаны проценты достигших и доверительные интервалы (по методу Клоппера – Пирсона). С учетом наличия информации о тяжести псориаза (PASI на 0-й неделе более 20 баллов) дополнительно проведена оценка влияния тяжести процесса на достижение самого благоприятного исхода – PASI 100. Для этого была использована модель логистической регрессии с расчетом отношения шансов с 95% ДИ на каждой точке оценки. Сравнение среднего балла PASI на начало исследования у пациентов с избыточной и с нормальной массой тела проведено при помощи t-критерия Стьюдента – Уэлча, значение в группах представлены в виде среднего (стандартного отклонения). Сравнение долей пациентов, достигших того или иного PASI или степени качества жизни по ДИКЖ, проведено при помощи точного критерия Фишера.
Результаты
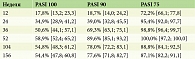
В группу наблюдения были включены пациенты, достигшие PASI 75 и более в контрольной точке 52 недели. Динамика индекса тяжести псориаза в сроки до 52 недель включительно была следующей: через 12 недель наблюдений количество пациентов, достигших PASI 75, PASI 90 и PASI 100, составило 72,2; 18,7 и 17,8% соответственно. Через год (контрольная точка 52 недели) терапии нетакимабом количество пациентов, достигших PASI 75, PASI 90 и PASI 100, составило 100,0; 89,6 и 58,9% соответственно. Через два года (контрольная точка 104 недели) терапии нетакимабом количество пациентов с сохраненным эффектом по PASI 75, PASI 90 и PASI 100 составило 88,8; 78,0 и 54,8% соответственно. Через три года (контрольная точка 156 недель) терапии нетакимабом количество пациентов с сохраненным эффектом по PASI 75, PASI 90 и PASI 100 составило 87,1; 77,6 и 54,4% соответственно (табл. 1). Таким образом, у пациентов, находившихся под наблюдением и продолжающих терапию в течение трех лет, по PASI 100 достоверно значимая отрицательная динамика отсутствовала, по PASI 90 и PASI 75 снизилось количество ответчиков на 10%.
В зависимости от массы тела (МТ) отмечалась следующая динамика: в контрольной точке 52 недели достижение PASI 75, PASI 90 и PASI 100 у пациентов с нормальной массой тела составило 100,0; 91,4 и 67,9% соответственно, у пациентов с избыточной массой тела – 100,0; 87,1 и 46,5%. Таким образом, только по показателю достижение чистой кожи (PASI 100) группы достоверно значимо отличались (р = 0,027). В контрольной точке 104 недели достижение PASI 75, PASI 90 и PASI 100 у пациентов с нормальной массой тела составило 92,9; 83,6 и 64,3% соответственно, у пациентов с избыточной массой тела – 83,2; 70,3 и 41,6%. Таким образом, через два года наблюдений статистически значимо группы отличались по показателям PASI 90 (р = 0,038) и PASI 100 (р = 0,041). В контрольной точке 156 недель достижение PASI 75, PASI 90 и PASI 100 у пациентов с нормальной массой тела составило 90,7; 82,1 и 63,6%, у пациентов с избыточной массой тела 82,2; 71,3 и 41,6% соответственно. Таким образом, через три года наблюдений статистически значимо группы отличались по показателям PASI 75 (р = 0,031), PASI 90 (р = 0,026) и PASI 100 (р = 0,019) (табл. 2).
Динамика показателя качества жизни (ДИКЖ) коррелировала с динамикой показателя клинических симптомов (PASI) (табл. 3). В контрольной точке 52 недели 93,8% пациентов отметили отсутствие отрицательного влияния или незначительное влияние на качество жизни (ДИКЖ ≤ 5 баллов). В контрольных точках 104 и 156 недель количество пациентов с ДИКЖ ≤ 5 баллов составило 92,5 и 84,6%.
Анализ динамики показателя ДИКЖ в группах пациентов в зависимости от массы тела показал, что в контрольной точке 52 недели достижение ДИКЖ 0–1, ДИКЖ 2–5 и ДИКЖ > 5 у пациентов с нормальной массой тела составило 66,4; 22,9 и 5,7%, у пациентов с избыточной массой тела – 45,5; 38,6 и 6,9% соответственно. Таким образом, по показателю ДИКЖ (отсутствие влияния или незначительное влияние на качество жизни) группы достоверно значимо отличались (р = 0,025 и р = 0,033). В то же время по совокупному показателю (ДИКЖ ≤ 5 баллам) группы достоверно значимо не отличались (р = 0,487) (табл. 4). В контрольной точке 104 недели достижение ДИКЖ 0–1, ДИКЖ 2–5 и ДИКЖ > 5 у пациентов с нормальной массой тела составило 69,3; 20,0 и 3,6%, у пациентов с избыточной массой тела – 49,5; 23,8 и 13,9% соответственно (табл. 4). Таким образом, по показателю ДИКЖ 0–1 (отсутствие отрицательного влияния на качество жизни) и ДИКЖ > 5 баллов группы достоверно значимо различались (р = 0,069 и р = 0,078). В контрольной точке 156 недель достижение ДИКЖ 0–1, ДИКЖ 2–5 и ДИКЖ > 5 баллов у пациентов с нормальной массой тела составило 64,3; 21,4 и 8,6% соответственно, у пациентов с избыточной массой тела – 47,5; 24,8 и 14,9% соответственно (табл. 4). Таким образом, по показателю ДИКЖ 0–1 (отсутствие отрицательного влияния на качество жизни) и ДИКЖ > 5 баллов группы достоверно значимо различались (р = 0,031 и р = 0,015).
Обсуждение
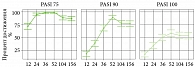
В результате анализа полученных данных при наблюдении в сроки 156 недель было показано, что 87,1% пациентов, ответивших на терапию нетакимабом в сроки до 52 недель, в дальнейшем удерживали ответ (рис. 1). Таким образом, вторичная неэффективность наблюдалась в 12,9% случаев. При этом количество пациентов с ответом по PASI 100 достоверно значимо не изменялось (58,9% на 52-й неделе и 54,4% на 156-й неделе), по PASI 90 количество пациентов снизилось на 12% (89,6% на 52-й неделе и 77,6% на 156-й неделе) (рис. 1). Полученные данные в реальной клинической практике показали хороший долгосрочный эффект применения нетакимаба, при этом пациенты, достигшие полного очищения кожи в сроки 52 недели, удерживали эффект на протяжении трех лет.
Изучение показателей качества жизни в контрольной точке 52 недели показало, что 93,8% пациентов отметили полное отсутствие отрицательного влияния или незначительное влияние на качество жизни (ДИКЖ ≤ 5 баллам). В контрольных точках 104 и 156 недель количество пациентов с ДИКЖ ≤ 5 баллам составило 92,1 и 88,8% (рис. 2). Таким образом, в целом по группе пациентов отсутствовала достоверно значимая отрицательная динамика по показателю ДИКЖ в сроки 104 (р = 0,208) и 156 недель (р = 0,422).
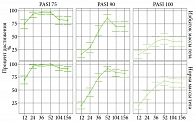
В зависимости от массы тела в контрольной точке 52 недели группы отличались по показателю достижение чистой кожи (PASI 100, р = 0,027). В контрольной точке 104 недели группы пациентов с нормальной или избыточной массой тела отличались по показателям PASI 90 (р = 0,038) и PASI 100 (р = 0,041). В контрольной точке 156 недель статистически значимо группы отличались по показателям PASI 75 (р = 0,031), PASI 90 (р = 0,026) и PASI 100 (р = 0,019) (рис. 3).
Анализ динамики показателя ДИКЖ в группах пациентов в зависимости от массы тела показал, что в контрольной точке 52 недели по показателю ДИКЖ (отсутствие влияния или незначительное влияние на качество жизни) группы достоверно значимо отличались (р = 0,025 и р = 0,033), в то же время по совокупному показателю (ДИКЖ ≤ 5 баллам) группы достоверно значимо не отличались (р = 0,487) (рис. 4). В контрольной точке 104 недели по показателю ДИКЖ 0–1 (отсутствие отрицательного влияния на качество жизни) и ДИКЖ > 5 баллов группы достоверно значимо различались (р = 0,019 и р = 0,028) (рис. 4). В контрольной точке 156 недель достижение по показателю ДИКЖ 0–1 (отсутствие отрицательного влияния на качество жизни) и ДИКЖ > 5 баллов группы достоверно значимо различались (р = 0,031 и р = 0,015) (рис. 4).
Выводы
- В данном многоцентровом наблюдательном исследовании была показана высокая эффективность отечественного препарата нетакимаб у пациентов с бляшечным псориазом в условиях реальной клинической практики в долгосрочном (156 недель) периоде наблюдений.
- Динамика индекса тяжести псориаза в сроки 104 недели терапии нетакимабом показала, что количество пациентов с сохраненным эффектом по PASI 75, PASI 90 и PASI 100 составило 88,8; 78,0 и 54,8% соответственно, в контрольной точке 156 недель – 87,1; 77,6 и 54,4% соответственно. Таким образом, у пациентов, находившихся под наблюдением и продолжающих терапию в течение трех лет, по PASI 100 достоверно значимая отрицательная динамика отсутствовала, по PASI 90 и PASI 75 снизилось количество ответчиков на 10%.
- В зависимости от массы тела в контрольной точке 52 недели различие наблюдалось только по показателю достижение чистой кожи (PASI 100, р = 0,027). В контрольной точке 104 недели группы достоверно значимо отличались по показателям PASI 90 (р = 0,038) и PASI 100 (р = 0,041). В контрольной точке 156 недель статистически значимо группы отличались по показателям PASI 75 (р = 0,031), PASI 90 (р = 0,026) и PASI 100 (р = 0,019).
- Данные динамики показателей PASI коррелировали с показателями качества жизни (ДИКЖ). В целом по группе в контрольной точке 52 недели 93,8% пациентов отметили отсутствие отрицательного влияния или незначительное влияние на качество жизни (ДИКЖ ≤ 5 баллам). В контрольных точках 104 и 156 недель количество пациентов с ДИКЖ ≤ 5 баллам составило 92,5 и 84,6% соответственно.
- Анализ динамики показателя ДИКЖ в группах пациентов в зависимости от массы тела показал следующее: в контрольной точке 52 недели по показателю ДИКЖ (отсутствие влияния или незначительное влияние на качество жизни) группы достоверно значимо отличались (р = 0,025 и р = 0,033). В то же время по совокупному показателю (ДИКЖ ≤ 5 баллам) группы достоверно значимо не отличались (р = 0,487). В контрольных точках 104 и 156 недель по показателю ДИКЖ 0–1 балл и ДИКЖ > 5 баллов группы достоверно значимо различались (р = 0,019 / р = 0,031 и р = 0,028 / р = 0,015).
L.S. Kruglova, PhD, Prof., N.S. Rudneva, PhD, O.R. Ziganshin, PhD, Prof., I.S. Vladimirova, PhD, E.A. Shatokhina, PhD, Prof., A.A. Khotko, PhD, E.M. Seredinina, PhD, E.P. Pavlikova, PhD, Prof., I.G. Egoshina, A.S. Bridan-Rostovskaya, N.O. Pereverzina, PhD
Central State Medical Academy of Department of Presidential Affairs, Moscow
Tula Regional Clinical Skin and Venereological Dispensary
Chelyabinsk Regional Clinical Skin and Venereological Dispensary
Skin and Venereological dispensary No. 10, Clinic of Dermatology and Venereology, St. Petersburg
Medical Scientific and Educational Institute of Lomonosov Moscow State University, Moscow
Clinical Skin and Venereological dispensary, Krasnodar
Kuzbass Clinical Skin and Venereological Dispensary, Novokuznetsk
National Medical Research Center of Otorhinolaryngology, Moscow
Contact person: Natalia S. Rudneva, natalya.rudneva@tularegion.ru
The study resulted in a dataset with data on Psoriasis Area and Severity Index (PASI) and quality of life indicators (DLQI) indices, including 241 patients observed for 156 weeks, including depending on the presence of excess weight. Study results. This multicenter observational study demonstrated the high efficacy of the domestic drug netakimab in patients with plaque psoriasis in real clinical practice in the long-term (156 weeks) observation period. The dynamics of the psoriasis severity index during 104 weeks of netakimab therapy showed that the number of patients with a preserved effect on PASI 75, PASI 90 and PASI 100 was 88.8; 78.0 and 54.8%, respectively, at the control point of 156 weeks – 87.1; 77.6 and 54.4%, respectively. Thus, in patients who were under observation and continued therapy for 3 years, there was no significant negative dynamics according to PASI 100, the number of responders decreased by 10% according to PASI 90 and PASI 75. Depending on body weight, at the control point of 52 weeks, only according to the PASI 100 indicator the groups differed significantly (p = 0.027). At the control point of 104 weeks, the groups differed significantly according to PASI 90 (p = 0.038) and PASI 100 (p = 0.041). At the control point of 156 weeks, the groups differed statistically significantly according to PASI 75 (p = 0.031), PASI 90 (p = 0.026) and PASI 100 (p = 0.019). These dynamics of PASI indicators correlated with DLQI. In the group as a whole, at the control point of week 52, 93.8% of patients reported no negative impact or minor impact on quality of life (DLQI ≤ 5 points). At the control points of weeks 104 and 156, the number of patients with DLQI ≤ 5 points was 92.5 and 84.6%. Analysis of the dynamics of the DLQI indicator in the patient groups depending on body weight showed the following: at the control point of week 52, the groups differed significantly in the DLQI indicator (no impact or minor impact on quality of life) (p = 0.025 and p = 0.033). At the same time, the groups did not differ significantly in the total indicator (DLQI ≤ 5 points) (p = 0.487). At the control point of 104 weeks and 156 weeks, the groups significantly differed in terms of the DLQI of 0-1 point and DLQI of more than 5 points (p = 0.019/p = 0.031 and p = 0.028/p = 0.015).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.