Влияние иммуномодулятора Галавит на качество жизни больных немелкоклеточным раком легкого II – III стадии
- Аннотация
- Статья
- Ссылки


Наиболее важной причиной рака легкого является курение. Показатели заболеваемости в различных странах хорошо отражают историю развития привычки к курению. Установлено, что в мире причиной этого заболевания в 86% случаев среди мужчин и в 49% случаев среди женщин стало курение (20).
Ежегодно в мире регистрируется 921 тыс. смертей от рака легкого. Абсолютное число умерших в России увеличилось за 20-летний период на 40% и достигло в 2000 г. 58,9 тыс. (4). В структуре умерших от злокачественных новообразований доля рака легкого составляла 30,8% у мужчин и 6,6% у женщин.
В ранжированном ряду 45 стран мира (21) смертность от рака легкого мужского населения России занимает 3 место (после Венгрии и Польши), женского – 27 место.
За период с 1970 по 1997 гг. отмечено снижение смертности от этой формы рака в большинстве стран мира среди мужского населения и рост показателей среди женского населения (21, 24).
Очень малое различие в среднем возрасте заболевших (64,7 г.) и умерших (65,1 г.) является следствием неблагоприятного прогноза при этой форме опухоли, характеризующейся высокой летальностью (4). По данным SEER, пятилетняя выживаемость больных в США составляет 14%, в Европе – всего 8%, такие же показатели в России (19, 22).
В молодом возрасте вероятность для больного злокачественным новообразованием легкого умереть от этого заболевания значительно выше, чем от другой причины, в 40-44 года эти различия достигают 37-кратных размеров, а в 70-74 года – сокращается до 13-кратных.
Основными критериями при выборе оптимального метода лечения больных раком легкого является распространенность опухолевого процесса (размеры первичной опухоли, степень метастатического поражения внутригрудных лимфатических узлов, прорастание соседних органов и структур, отсутствие или наличие отдаленных метастазов и их локализация), т.е. стадия заболевания в соответствии с классификацией по стадиям и Международной классификацией по системе TNM, локализация и форма роста опухоли, ее гистологическая структура и степень анаплазии (16).
В настоящее время единственным радикальным методом лечения немелкоклеточного рака легкого II-III стадии остается хирургический.
Немелкоклеточный рак легкого представляет собой морфологически неоднородную группу, включающую в основном плоскоклеточный рак (70-75%), аденокарциному (20-25%) различной дифференцировки и другие, редкие формы рака. Они объедены в одну группу немелкоклеточного рака по органному принципу и близким отдаленным результатам (3).
Так как злокачественный опухолевый процесс, оперативное вмешательство и развивающиеся в послеоперационном периоде осложнения приводят к значительной иммуносупрессии, одним из направлений, повышающих эффективность этиопатогенетической терапии в настоящее время является использование иммунотропных препаратов и разработка адекватных методов направленной иммунокоррекции в комплексной терапии.
Непосредственным влиянием на иммунную систему через макрофагальное звено посредством изменения функциональной активности макрофагов обладает иммуномодулятор Галавит.
Препарат был зарегистрирован в 1997 г. (8) как противовоспалительное средство с иммуномодулирующими свойствами (регистрационный номер 97/91/3; сертификат соответствия 31-042-224) под названием «Галавит».
Он разработан под руководством профессора А.П. Хохлова в ММА им. И.М. Сеченова (5, 11) и ЗАО ЦСМ «Медикор», представляет собой натриевую соль аминофталазина, которая воздействует на иммунную систему преимущественно через макрофагальное звено.
Препарат проявляет свою противовоспалительную активность вследствие способности обратимо (на 6-8 часов) ингибировать синтез макрофагами провоспалительных цитокинов ФНО и ИЛ-1 (1, 6, 7, 10). При этом Галавит способен восстанавливать угнетенную фагоцитарную функцию макрофагов и нейтрофилов и, следовательно, противоинфекционную защиту. Одновременно восстанавливается и антиген-представляющая функция макрофагов, активизируются процессы репарации поврежденных тканей, купируются клинические симптомы интоксикации (16), восстанавливается адекватное функционирование иммунной системы.
В исследование был включен 61 пациент, находившийся на лечении в хирургическом торакальном отделении НУЗ ЦКБ №2 им. Н.А. Семашко ОАО «РЖД» в период с 2000 по 2004 гг. Диагноз «плоскоклеточный рак легкого, стадия IА-IIIА, T1-3N0-2M0» был установлен до хирургического лечения и был подтвержден данными гистологических и цитологических исследований.
Работа проводилась на основе требований и стандартов международных клинических исследований лекарственных средств «Качественная Клиническая Практика – Good Clinical Practice/GCP», которая позволяет регулировать применение клинических испытаний, обеспечивая надежность полученных данных, а также защищая права, неприкосновенность и конфиденциальность испытуемых.
Исследование было спланировано и проведено методом рандомизированного двойного слепого контролируемого исследования, которое является «золотым стандартом» в области клинических испытаний, т.к. совместное применение технологии слепого исследования и рандомизации предотвращает воздействие на результаты испытания наиболее грубых погрешностей.
Все больные методом рандомизации были разделены на две группы. Рандомизация проводилась по году рождения: больные с четным годом рождения составляли первую группу и получали препарат серии №1, больные с нечетным годом рождения составляли вторую группу и получали препарат серии №2.
Препараты обеих серий поставлялись в виде белого кристаллического порошка во флаконах по 100 мг, которые разводили водой для инъекций непосредственно перед введением в количестве 3 мл, и вводили в виде внутримышечных инъекций. Первая инъекция производилась после завершения обследования, подтверждения возможности хирургического лечения, подписания информированного согласия включения в исследование. Препарат применяли в дозе 100 мг внутримышечно в течение 3-х дней до хирургического вмешательства, включая день операции, в течение 2-х дней после операции и далее каждые 3 дня до 51-х суток после операции.
Как подразумевает методика двойного слепого рандомизированного плацебо-контролируемого исследования, ни пациент, ни врачи не знали до окончания работы в какой из серий препарата находился Галавит, а в какой – плацебо.
По окончанию исследования конверты с данными были открыты и оказалось, что Галавит серии №1 – это истинный препарат, а Галавит серии №2 – это плацебо. Таким образом, названные нами по номерам группы больных – группа №1 и группа №2 в дальнейшем будут называться группа Галавита (основная) и группа плацебо (контрольная) соответственно.
Статистически значимых различий в группах по возрасту не отмечено. Средний возраст больных первой группы составил 61,3±2,7, а больных второй группы 59,8±3,1.
В зависимости от распространенности опухолевого процесса хирургическое лечение производилось в различных объемах, однако частота применения разных видов операций в сравниваемых группах практически не различалась, в основной группе была выполнена 21 пульмонэктомия и 10 лобэктомий, в контрольной группе – 18 пульмонэктомий и 12 лобэктомий.
Таким образом, представленные группы больных были примерно идентичны как по возрасту, так и по объему перенесенных хирургических вмешательств.
Уровень качества жизни считается одним из ключевых параметров при изучении результатов лечения (12). Изучение качества жизни больных проводилось с помощью специальных анкет, разработанных EORTC (European Organization of Treatment for Cancer – Европейская организация по лечению рака). Эти анкеты заполнялись больными перед началом лечения, на 3-е и 51-е сутки после операции. Также использовали шкалу Карновского, по которой оценивали общее состояние больных при поступлении и после проведения лечения.
Оперативное вмешательство по поводу рака легкого – тяжелая травма с повреждением жизненно важных органов и структур в грудной клетке. Опухолевый процесс и сопутствующие хронические заболевания значительно снижают адаптивные и функциональные возможности организма больного к травме. В литературе описано состояние хронического стресса у онкологических больных.
Как видно из таблицы 1, среднее значение индекса Карновского до лечения у больных немелкоклеточным раком легкого II-III стадии было примерно одинаковым и составляло в основной группе 65%, а в контрольной группе среднее значение данного показателя составило 61%. На 51-е сутки после операции качество жизни было оценено повторно, и оказалось, что в основной группе состояние больных улучшилось, среднее значение индекса составило 75%, тогда как у пациентов контрольной группы состояние практически не изменилось, и средняя величина индекса Карновского равнялась 62%.
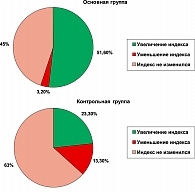
При рассмотрении общего состояния больных не по средним величинам, а внутри каждой группы индивидуально по больным, выяснилось, что в основной группе, получавших Галавит, клиническое улучшение общего состояния наблюдалось у 16 человек, ухудшение состояния отмечено у 1 больного (увеличение одышки при физической нагрузке), а у 14 пациентов индекс Карновского оставался неизменным, т.е. на том же уровне, что и до лечения.
В контрольной группе, получавших плацебо, наблюдалась иная картина. Улучшение общего состояния отмечено у 7 человек, что в 2,3 раза меньше, чем в первой группе. Ухудшение состояния зарегистрировано у 4 пациентов. Индекс Карновского остался неизменным у 19 пациентов. Данные представлены в таблице 2 и диаграммах 1 и 2.
Известно, что больные онкологическими заболеваниями не всегда адекватно оценивают свое состояние и уровень качества жизни. Для них характерны крайние оценки своего состояния – от эйфории, когда больные находятся в стадии отрицания, вытеснения негативной информации, до депрессии и суицидальных поступков (2).
Для изучения самооценки уровня качества жизни больных нами использовались специальные анкеты качества жизни, разработанные EORTC (European Organization of Treatment for Cancer – Европейская организация по лечению рака) и рекомендованные для применения в онкологической клинике Всемирной организации здравоохранения. Эти анкеты заполнялись больными и анализировались врачом перед началом лечения и в конце лечения. Опросный лист отражал три основные сферы человеческой жизнедеятельности и включал вопросы, касающиеся физической, психической и социальной сторон жизни.
При анализе анкет оказалось, что подавляющее большинство больных адекватно оценивали свое физическое состояние, испытывая боль, слабость и другие симптомы заболевания, т.е. оценивали состояние как тяжелое или средней степени тяжести. При этом больные испытывали подавленность, растерянность и другие симптомы психической дезадаптации разной степени выраженности. При анализе ответов, касающихся социальной стороны жизни нами было установлено относительное благополучие в этой сфере, что, по-видимому, следует трактовать, как то, что вопросы социальной адаптации в обществе не волнуют пациентов так же сильно, как симптомы физического или психического страдания.
При проведении сравнительной оценки по группам, выяснилось, что до лечения больные обеих групп примерно одинаково оценивали свое состояние как удовлетворительное или средней тяжести, при наличии симптомов психической дезадаптации и относительном благополучии в социальной сфере. Так 30,6% больных основной группы и 29,4% больных контрольной группы оценивали свое состояние как средней тяжести/тяжелое. Однако после лечения оказалось, что 90,3% больных основной группы считают свое состояние улучшившимся. Оценивая свое психическое состояние при помощи таких понятий, как наличие подавленности, растерянности, страха, 90,3% больных этой группы также отметили уменьшение этих симптомов. Отвечая на вопрос об изменении своего здоровья и качества жизни в процессе лечения, больные, получавшие Галавит, отмечали изменения в лучшую сторону – 32,3% больных считали свое здоровье улучшившимся и 42% больных считали улучшившимся качество своей жизни. В социальной сфере, по мнению больных, изменений не произошло.
Больные контрольной группы, оценивая свое состояние и уровень качества жизни после лечения, почти не отметили изменений в лучшую сторону, отмечая ухудшение физического (30,3% больных) и/или психического состояния (22,2%), или считали свое состояние не изменившимся – 47,5% больных не отмечали каких-либо изменений. В социальной сфере больные данной группы также не отметили изменений.
Таким образом, при проведении хирургического лечения у больных немелкоклеточным раком легкого II-III стадии на фоне применения Галавита нами отмечено клиническое улучшение состояния пациентов, что отражает их опросный лист, а также оценка качества жизни по шкале Карновского, которая увеличилась с 65% до 75%.
У пациентов контрольной группы, получавших плацебо, на фоне стандартной терапии состояние практически не менялось и соответствовало 61% и 62% по шкале Карновского.
Таким образом, анализируя эффективность хирургического лечения больных немелкоклеточным раком легкого II-III стадии на фоне применения Галавита и плацебо, было отмечено улучшение качества жизни больных, что считается одним из ключевых параметров при изучении результатов лечения.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.