Эффективность иммунотерапии при распространенном плоскоклеточном раке кожи: опыт Национального медицинского исследовательского центра онкологии им. Н.Н. Блохина
- Аннотация
- Статья
- Ссылки
- English
Цель. Оценить эффективность и переносимость анти-PD-1-терапии у пациентов с местно-распространенным и метастатическим ПКРК.
Материал и методы. Одноцентровое ретроспективное исследование проводилось на базе ФГБУ НМИЦ онкологии им. Н.Н. Блохина Минздрава РФ (декабрь 2019 г. – июль 2024 г.). В исследование были включены 45 пациентов, получавших пембролизумаб (n = 19), ниволумаб (n = 15), пролголимаб (n = 8) или цемиплимаб (n = 3) в разных линиях терапии. Эффективность оценивалась на основании частоты объективного ответа (ЧОО), данных выживаемости без прогрессирования (ВБП) и общей выживаемости (ОВ). Прогностические факторы анализировали с помощью регрессии Кокса.
Результаты. Медиана наблюдения составила 20,5 мес. ЧОО среди всех пациентов, получавших ингибиторы контрольных точек иммунного ответа, – 20,0%; уровень контроля заболевания – 42,2%; медиана ВБП – 4,1 мес. (95%-ный доверительный интервал (ДИ) 2,2–10,7); медиана ОВ – 19,9 мес. (95% ДИ 12,0–36,6). При назначении анти-PD-1-препаратов в первой линии (n = 35) ЧОО достигала 25,7%; медиана ВБП – 5,33 мес. (95% ДИ 2,7–15,1); медиана ОВ – 21,4 мес. (95% ДИ 12,03 – не достигнута). При многофакторном анализе отсутствие объективного ответа ухудшало ОВ (отношение рисков (ОР) = 11,96; 95% ДИ 1,55–92,26; p = 0,017) и ВБП (ОР = 10,85; 95% ДИ 2,42–48,70; p = 0,002). Метастатическая форма заболевания снижала показатели ОВ (ОР = 2,79; p = 0,051) и ВБП (ОР = 3,06; p = 0,024). Более высокие показатели ОВ были отмечены у женщин (ОР = 0,41; p = 0,041).
Нежелательные явления 3–4-й степени по CTCAE v5.0 составили 4,4% (2 из 45 пациентов), что привело к завершению терапии.
Заключение. Эффективность анти-PD-1-терапии в реальной клинической практике оказалась ниже, чем в регистрационных клинических исследованиях. Отсутствие ответа на фоне проводимой иммунотерапии и метастатическая форма заболевания – главные неблагоприятные прогностические факторы.
Цель. Оценить эффективность и переносимость анти-PD-1-терапии у пациентов с местно-распространенным и метастатическим ПКРК.
Материал и методы. Одноцентровое ретроспективное исследование проводилось на базе ФГБУ НМИЦ онкологии им. Н.Н. Блохина Минздрава РФ (декабрь 2019 г. – июль 2024 г.). В исследование были включены 45 пациентов, получавших пембролизумаб (n = 19), ниволумаб (n = 15), пролголимаб (n = 8) или цемиплимаб (n = 3) в разных линиях терапии. Эффективность оценивалась на основании частоты объективного ответа (ЧОО), данных выживаемости без прогрессирования (ВБП) и общей выживаемости (ОВ). Прогностические факторы анализировали с помощью регрессии Кокса.
Результаты. Медиана наблюдения составила 20,5 мес. ЧОО среди всех пациентов, получавших ингибиторы контрольных точек иммунного ответа, – 20,0%; уровень контроля заболевания – 42,2%; медиана ВБП – 4,1 мес. (95%-ный доверительный интервал (ДИ) 2,2–10,7); медиана ОВ – 19,9 мес. (95% ДИ 12,0–36,6). При назначении анти-PD-1-препаратов в первой линии (n = 35) ЧОО достигала 25,7%; медиана ВБП – 5,33 мес. (95% ДИ 2,7–15,1); медиана ОВ – 21,4 мес. (95% ДИ 12,03 – не достигнута). При многофакторном анализе отсутствие объективного ответа ухудшало ОВ (отношение рисков (ОР) = 11,96; 95% ДИ 1,55–92,26; p = 0,017) и ВБП (ОР = 10,85; 95% ДИ 2,42–48,70; p = 0,002). Метастатическая форма заболевания снижала показатели ОВ (ОР = 2,79; p = 0,051) и ВБП (ОР = 3,06; p = 0,024). Более высокие показатели ОВ были отмечены у женщин (ОР = 0,41; p = 0,041).
Нежелательные явления 3–4-й степени по CTCAE v5.0 составили 4,4% (2 из 45 пациентов), что привело к завершению терапии.
Заключение. Эффективность анти-PD-1-терапии в реальной клинической практике оказалась ниже, чем в регистрационных клинических исследованиях. Отсутствие ответа на фоне проводимой иммунотерапии и метастатическая форма заболевания – главные неблагоприятные прогностические факторы.







Введение
Плоскоклеточный рак кожи (ПКРК) занимает второе место среди немеланомных злокачественных опухолей кожи, уступая только базальноклеточному раку кожи. Заболеваемость ПКРК неуклонно растет во всем мире, что связывают с увеличением продолжительности жизни, накоплением ультрафиолетового облучения и совершенствованием регистрации [1, 2]. Большинство пациентов с локальными формами ПКРК могут быть излечены с помощью хирургического метода [3, 4]. Однако у части пациентов развиваются местные рецидивы, регионарные или отдаленные метастазы. Наиболее часто (до 85%) наблюдается поражение регионарных лимфатических узлов, реже – метастатическое поражение легких, печени, головного мозга, кожи и костей [5, 6].
Ключевыми факторами риска развития распространенных форм ПКРК служат толщина опухоли более 6 мм и глубина инвазии, периневральный и лимфоваскулярный рост, а также развитие на фоне хронических воспалительных и рубцовых изменений кожи [7]. Наличие негативных факторов прогноза заболевания обусловливает повышение 5-летнего риска локального рецидива или метастазирования на 20% [8, 9].
До недавнего времени стандартом лекарственной терапии при местно-распространенном или метастатическом ПКРК служили ингибиторы EGFR (цетуксимаб) и платиносодержащие режимы химиотерапии. Однако эффективность этих режимов ограничена: частота объективных ответов (ЧОО) не превышает 30%, а продолжительность ответа, как правило, невелика [10–12].
Переломным моментом стало внедрение ингибиторов контрольных точек иммунного ответа (анти-PD-1-препаратов). В 2018 г. были впервые опубликованы результаты клинического исследования EMPOWER-CSCC-1 по изучению эффективности и переносимости цемиплимаба при местно-распространенном и метастатическом ПКРК. Среди пациентов с метастатической (n = 75) и нерезектабельной местно-распространенной (n = 33) формами заболевания ЧОО составила 47% (95%-ный доверительный интервал (ДИ) 38–57) [13, 14]. В другом исследовании KEYNOTE-629, опубликованном в 2020 г., иммунотерапия пембролизумабом продемонстрировала ЧОО 34–50% в зависимости от линии лечения и PD-L1-статуса и медиану выживаемости без прогрессирования (ВБП) 6,9 мес. у пациентов с местно-распространенным или метастатическим ПКРК [15, 16]. На сегодняшний день оба препарата вошли в международные клинические рекомендации в качестве стандарта 1-й линии лекарственной терапии для данной категории пациентов [2, 17–19].
Тем не менее данные регистрационных исследований не всегда полностью экстраполируются на реальную клиническую практику. Пациенты в рутинной практике более гетерогенны: они старше, имеют больше сопутствующих заболеваний, нередко получают анти-PD-1 на более поздних линиях, а также могут иметь особенности течения опухоли – в частности, развитие ПКРК на фоне хронических повреждений кожи (рубцов, ожогов, длительно незаживающих ран). Подобные различия могут оказывать влияние как на клиническое течение заболевания, так и на результаты системной терапии, что требует дополнительного анализа.
В России систематические данные об эффективности и переносимости анти-PD-1-терапии при нерезектабельном или метастатическом ПКРК кожи в реальной практике до настоящего времени отсутствовали.
Цель исследования – оценить эффективность и переносимость анти-PD-1-терапии у пациентов с местно-распространенным и метастатическим ПКРК в условиях реальной клинической практики одного центра.
Материал и методы
Дизайн исследования и этические аспекты. Проведено одноцентровое ретроспективное когортное клиническое исследование на базе отделения опухолей кожи отдела лекарственного лечения ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Работа выполнена в соответствии с Хельсинкской декларацией (1964 г. с последующими дополнениями). В силу ретроспективного характера информированное согласие пациентов на участие в анализе не требовалось. Однако следует отметить, что при первичном обращении в НМИЦ онкологии им. Н.Н. Блохина все пациенты подписывают добровольное информированное согласие, которое включает, помимо согласия на медицинские вмешательства, разрешение на обработку персональных данных и использование обезличенной медицинской информации в научных, статистических и образовательных целях, в том числе для проведения ретроспективных исследований. В рамках настоящей работы все данные были деидентифицированы перед анализом, что исключает возможность их прямой связи с конкретным пациентом.
Пациенты и критерии. В анализ последовательно включены все пациенты, соответствовавшие следующим критериям: возраст – взрослые (≥ 18 лет); диагноз – гистологически подтвержденный ПКРК; стадия заболевания – нерезектабельный местно-распространенный (III стадия по AJCC 8-го пересмотра) или метастатический (IV стадия) ПКРК; лечение – не менее одного введения анти-PD-1-препарата в период с декабря 2019 по июль 2024 г.; наличие данных – доступность первичной медицинской документации для ретроспективного анализа. Критерии исключения: отсутствие данных наблюдения (менее одного контрольного визита).
Решение о нерезектабельности принималось мультидисциплинарной командой центра компетенции по опухолям кожи, в состав которой входили химиотерапевты, хирурги-онкологи и радиотерапевты. Критериями нерезектабельности считали: невозможность выполнения R0-резекции без риска потери функции органа, наличие множественных регионарных метастазов, не подлежащих полному хирургическому удалению, а также отказ пациента от хирургического лечения. Стадирование проводили в соответствии с 8-й редакцией классификации Американского объединенного комитета по раку (AJCC) на основании данных инструментальных методов исследования, выполненных не более чем за четыре недели до начала иммунотерапии.
Лекарственное лечение. Для лекарственного лечения (табл. 1) использовался один из следующих препаратов: пембролизумаб (200 мг каждые три недели в/в, кап., n = 19); ниволумаб (240 мг каждые две недели в/в, кап., n = 15); пролголимаб (1 мг/кг один раз в 14 дней в/в, кап., n = 8); цемиплимаб (350 мг каждые три недели в/в, кап., n = 3). Выбор определялся доступностью и решением лечащего врача.
Терапию продолжали до прогрессирования заболевания по критериям оценки ответа солидных опухолей на терапию (RECIST 1.1 – Response Evaluation Criteria in Solid Tumors), неприемлемой токсичности или отмены терапии по решению врача. Допускалось проведение паллиативной лучевой терапии на отдельные очаги поражения (например, костные метастазы) на фоне иммунотерапии по решению консилиума.
Оценка эффективности. Первичная конечная точка – ЧОО, определяемая как доля пациентов, достигших полного ответа (ПО) или частичного ответа (ЧО) согласно критериям RECIST 1.1. Вторичные конечные точки: контроль над заболеванием – сумма частоты ПО, частоты ЧО и стабилизации заболевания; ВБП – время от начала иммунотерапии до прогрессирования или смерти от любой причины; общая выживаемость (ОВ) – время от начала иммунотерапии до даты смерти от любой причины (пациенты, у которых не наступил летальный исход, цензурированы на дату последнего контакта). Ответ на лекарственное лечение оценивали на основании клинической картины и/или инструментальных методов исследования (компьютерной томографии, магнитно-резонансной томографии, позитронно-эмиссионной томографии с 18F-фтордезоксиглюкозой (18F-ФДГ) и внутривенным контрастированием) в рамках критериев RECIST 1.1. Радиологическая оценка проводилась исходно (за четыре недели до начала терапии) и далее каждые 12 ± 2 недели на протяжении всего периода лечения. Клиническая оценка включала сравнение размеров опухоли с помощью линейки по данным фотодокументации. Оценку ответа выполняли лечащие врачи-химиотерапевты, специализирующиеся на опухолях кожи; пересмотр радиологических данных одним врачом-рентгенологом не проводился.
Оценка безопасности. Нежелательные явления (НЯ) регистрировались на каждом визите, классифицировались в соответствии с Common Terminology Criteria for Adverse Events (CTCAE) версии 5.0. В анализ безопасности включены все зарегистрированные НЯ 3–4-й степени тяжести, а также НЯ 1–2-й степени, которые привели к задержке терапии (более трех недель), отмене препарата или госпитализации. НЯ 1–2-й степени без клинической значимости в работе не анализируются в силу ретроспективного дизайна и неполноты регистрации.
Статистический анализ. Размер выборки не рассчитывался ввиду описательного характера исследования – проанализирована вся доступная когорта пациентов за указанный период. Описательная статистика: категориальные переменные представлены как абсолютные значения (n) и проценты (%). Анализ выживаемости: кривые ВБП и ОВ построены по методу Каплана – Мейера. Медианы выживаемости приведены с 95%-ными доверительными интервалами (ДИ). Сравнение подгрупп выполнено с помощью логрангового (log-rank) теста. Регрессионный анализ: для выявления факторов прогноза проведен одно- и многофакторный анализ пропорциональных рисков Кокса (Cox regression). В однофакторную модель включены следующие переменные: пол (мужской vs женский); возраст на момент начала терапии (непрерывная переменная); стадия заболевания (метастатическая vs местно-распространенная); локализация первичной опухоли (голова/шея vs другие); наличие хронического поражения кожи (да vs нет); линия терапии (первая vs вторая и последующие); достижение объективного ответа (да vs нет; анализировался как зависящая от времени (time-dependent) ковариата). Переменные с p < 0,20 в однофакторном анализе включены в многофакторную модель (метод прямого пошагового включения, stepwise forward). Результаты представлены как отношение рисков (ОР) и 95% ДИ. Статистическая значимость: порог статистической значимости принят как p < 0,05. Все тесты двусторонние. Программное обеспечение: анализ выполнен в среде R версии 4.3.0 (R Foundation for Statistical Computing, Вена, Австрия).
Результаты
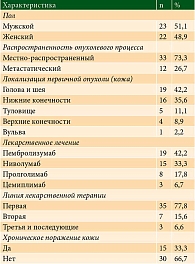
Характеристика когорты пациентов. С декабря 2019 по июль 2024 г. в исследование были включены 45 пациентов с нерезектабельным местно-распространенным или метастатическим ПКРК, получивших хотя бы один цикл анти-PD1-иммунотерапии. Медиана наблюдения составила 20,5 мес. (95% ДИ 1,6–62,2 мес.). Демографические и клинические характеристики пациентов представлены в табл. 2. Количество мужчин и женщин было сопоставимым: 23 (51,1%) и 22 (48,9%) соответственно. Средний возраст на момент начала иммунотерапии составил 60,3 года.
Местно-распространенный ПКРК диагностирован у 33 пациентов (73,3%), метастатический – у 12 (26,7%). Наиболее частой локализацией первичной опухоли были голова и шея – 19 пациентов (42,2%), нижние конечности – 16 (35,6%). У 15 пациентов (33,3%) ПКРК развился на фоне хронических поражений кожи (на фоне рубцов после ожогов и длительно незаживающих ран).
Иммунотерапия первой линией была проведена 35 пациентам (78%), второй – семи (16%), третьей и далее – трем (6%). Наиболее часто в лечении пациентов с местно-распространенным или метастатическим ПКРК использовались такие лекарственные препараты, как пембролизумаб (42%) или ниволумаб (33%), реже назначалась терапия пролголимабом (18%) или цемиплимабом (7%).
Противоопухолевый ответ. Оценка ответа на проводимое лечение была возможна у 39 из 45 пациентов (87%) (рис. 1), 6 пациентов выбыли из оценки до проведения контрольного обследования. ПО зарегистрирован у двух пациентов (4,4%), ЧО – у семи пациентов (15,6%), стабилизация заболевания была достигнута у десяти пациентов (22,2%), прогрессирование заболевания зарегистрировано у 20 пациентов (44,4%).
ЧОО в общей когорте составила 20,0%. Частота контроля заболевания (ЧКЗ) составила 42,2%.
В подгруппе пациентов, получивших анти-PD-1-терапию в первой линии (n = 35), ЧОО была выше и составила 25,7%, в том числе ПО – у 2 (5,7%), ЧО – у 7 (20,0%). ЧКЗ в первой линии достигла 42,9%.
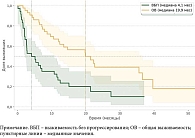
ВБП была оценена у 36 пациентов (у 9 пациентов отсутствовала документированная дата прогрессирования или достаточная длительность наблюдения). Медиана ВБП составила 4,1 мес. (95% ДИ 2,2–10,7). Показатели 12-, 24- и 36-месячной ВБП – 26,4%, 15,1% и 10,1% соответственно. В первой линии терапии медиана ВБП достигла 5,33 мес. (95% ДИ 2,7–15,1). ОВ была оценена у 44 пациентов. Медиана ОВ составила 19,9 мес. (95% ДИ 12,0–36,6). Показатели ОВ через 12, 24 и 36 мес. составили 67,1%, 39,2% и 33,6% соответственно. В первой линии терапии медиана ОВ составила 21,4 мес. (95% ДИ 12,0 мес. – не достигнута). Сводные данные приведены в табл. 3, кривые для ОВ и ВБП представлены на рис. 2.
Результаты регрессионного анализа Кокса суммированы в табл. 4 и представлены на рис. 3. Анализ ВБП был проведен у 36 пациентов. При многофакторном анализе отсутствие объективного ответа (ОР = 10,85; 95% ДИ 2,42–48,70; p = 0,002) и метастатическая форма болезни (ОР = 3,06; 95% ДИ 1,16–8,07; p = 0,024) были наиболее значимыми прогностическими факторами. Анализ ОВ был проведен среди 44 пациентов. В однофакторной модели отсутствие объективного ответа давало ОР 7,53 (95% ДИ 1,02–55,79; p = 0,048). При многофакторном анализе этот прогностический фактор был еще более выраженным – ОР 11,96 (95% ДИ 1,55–92,26; p = 0,017). Женский пол ассоциировался с более продолжительной выживаемостью независимо от других факторов (ОР = 0,41; 95% ДИ 0,17–0,96; p = 0,041). Метастатическая форма болезни ухудшала прогноз (ОР = 2,79; 95% ДИ 1,00–7,81; p = 0,051). Возраст на момент диагностики неоперабельной формы заболевания, локализация (голова и шея), а также хронические поражения кожи не оказали значимого влияния на выживаемость пациентов. Кривые выживаемости по ответу на терапию и стадии показаны на рис. 4 и 5.
Безопасность. При анализе были зафиксированы в медицинской документации только НЯ 3–4-й степени по CTCAE v5.0. У 2 (4,4%) из 45 пациентов были выявлены НЯ 3–4-й степени, что привело к завершению терапии.
Обсуждение
Представленное исследование – первый в Российской Федерации анализ эффективности и безопасности анти-PD-1-терапии у пациентов с нерезектабельным местно-распространенным и метастатическим ПКРК в реальной клинической практике.
В нашей когорте (n = 45) ЧОО составила 20,0%, медиана ВБП – 4,1 месяца, медиана ОВ – 19,9 месяца. В первой линии терапии ЧОО была несколько выше (25,7%), но все равно оставалась значительно ниже показателей регистрационных исследований. Частота тяжелых НЯ (3–4-й степени) оказалась низкой – 4,4%. Ключевыми независимыми прогностическими факторами неблагоприятного исхода явились отсутствие объективного ответа на иммунотерапию (ОР для
ОВ = 11,96; p = 0,017) и исходно метастатическая стадия заболевания (ОР для ВБП = 3,06; p = 0,024). Женский пол ассоциировался с более продолжительной ОВ (ОР = 0,41; p = 0,041), однако этот результат требует осторожной интерпретации.
Сравнение с регистрационными исследованиями. В клиническом исследовании EMPOWER-CSCC-1 (фаза II) ЧОО составила 44–50%, медиана длительности ответа – 41 мес. Расширенное наблюдение (медиана 77 мес.) подтвердило стойкость ответов: 5-летняя длительность ответа – 65%, 5-летняя ОВ – 60% [13, 14]. В клиническом исследовании KEYNOTE-629 (фаза II) ЧОО составила 50% при местно-распространенной и 35% при метастатической форме заболевания, медиана длительности ответа не достигнута. В 1-й линии ЧОО достигала 42%, причем ответ был значимо выше у PD-L1-позитивных пациентов (55% vs 17%, p = 0,02) [15, 16].
Более низкие показатели эффективности иммунотерапии в нашем исследовании связаны, возможно, с отсутствием строгих критериев отбора. Также важно отметить, что в нашей когорте 33% пациентов имели хронические поражения кожи (рубцы после ожогов, длительно незаживающие раны), что может быть ассоциировано с особыми биологическими характеристиками опухоли – иным микроокружением, более высокой частотой мутаций в генах-супрессорах и, возможно, первичной резистентностью к иммунотерапии. Кроме того, 22% пациентов получили анти-PD-1-препараты во второй и последующих линиях, тогда как в регистрационных исследованиях большинство больных не имели предшествующей системной терапии. Наконец, в нашем клиническом исследовании не проводился отбор пациентов по уровню экспрессии PD-L1, тогда как в исследовании KEYNOTE-629 ЧОО на фоне терапии пембролизумабом была значительно выше у PD-L1-позитивных пациентов.
Ключевой прогностический маркер – это отсутствие объективного ответа на лечение. Отсутствие противоопухолевого ответа повышало риск смерти в нашем исследовании практически в 12 раз. Это важно с практической точки зрения: у пациентов при первой клинической и инструментальной оценке эффективности проводимой иммунотерапии (как правило, через 10–12 недель) в случае прогрессирования заболевания целесообразно рассматривать смену терапии или эскалацию режима (добавление к иммунотерапии анти-EGFR- или химиотерапии).
Частота НЯ 3–4-й степени по CTCAE v5.0 составила 4,4% (у двух из 45 пациентов), что привело к прекращению терапии. Этот показатель сопоставим или даже ниже, чем в клинических регистрационных исследованиях, где частота тяжелых осложнений достигала 7–10%. Это может быть связано с ретроспективным дизайном и неполной регистрацией НЯ в медицинской документации. Тем не менее профиль безопасности анти-PD-1-терапии в реальной практике можно охарактеризовать как приемлемый.
Ограничения исследования: ретроспективный дизайн и небольшая выборка (n = 45). Особенно это касается подгруппового анализа (например, всего 12 пациентов с метастатической стадией, что объясняет широкие доверительные интервалы в регрессионном анализе). Гетерогенность терапии: четыре разных анти-PD1-препарата, разные линии лечения, отсутствие рандомизации. Сравнение эффективности между препаратами невозможно. Нет данных о PD-L1-статусе, мутационной нагрузке и других потенциальных биомаркерах. Отсутствие систематической оценки качества жизни и НЯ 1–2-й степени. Это ограничивает выводы о реальной переносимости терапии.
Заключение
Проведенное исследование – первый в Российской Федерации анализ эффективности и безопасности анти-PD-1-терапии при нерезектабельном местно-распространенном и метастатическом плоскоклеточном раке кожи в реальной клинической практике. Наши данные демонстрируют, что эффективность анти-PD-1-препаратов в условиях реальной практики скромнее, чем в регистрационных исследованиях: ЧОО составила 20,0% (в первой линии – 25,7%), медиана ВБП – 4,1 мес. (в первой линии – 5,3 мес.), медиана ОВ – 19,9 мес. (в первой линии – 21,4 мес.), ОВ 36 мес. – у 10% (в первой линии – у 33,6%), что подтверждает целесообразность назначения ингибиторов PD-1 на ранних этапах лечения. Тем не менее у части пациентов (около трети в первой линии) удается достичь длительного контроля заболевания. Профиль безопасности оказался приемлемым: частота тяжелых (3–4-й степени) НЯ составила 4,4%, что сопоставимо или ниже зарегистрированного в клинических исследованиях, хотя нельзя исключить неполноту регистрации НЯ в силу ретроспективного дизайна. Наиболее значимыми независимыми прогностическими факторами неблагоприятного исхода явились отсутствие объективного ответа на иммунотерапию (повышает риск смерти почти в 12 раз) и исходно метастатическая стадия заболевания. Женский пол показал ассоциацию с лучшей ОВ (ОР = 0,41; p = 0,041), однако этот результат следует рассматривать как предварительный и требующий подтверждения в более крупных когортах, поскольку он может объясняться неучтенными смешивающими факторами. Пациентов с хроническими поражениями кожи (рубцы, ожоги, длительно незаживающие раны) не следует исключать из терапии, хотя эффективность у них может быть ниже. Таким образом, анти-PD-1-терапия является клинически значимым, но не универсальным методом лечения нерезектабельного ПКРК в реальной российской практике. Для повышения эффективности лечения необходимы дальнейшие проспективные исследования с унифицированной оценкой биомаркеров и оптимизацией отбора пациентов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов при проведении исследования и подготовке рукописи.
K.V. Orlova, PhD, Z.R. Magomedova, V.V. Nazarova, PhD, A.E. Akhmetyanova, N.N. Petenko, PhD, K.Yu. Ivanilov, I.S. Romanov, PhD, I.V. Samoylenko, PhD, L.V. Demidov, PhD
N.N. Blokhin National Medical Research Center of Oncology, Moscow
Institute of Continuing Education and Professional Development of N.I. Pirogov Russian National Research Medical University, Moscow
Contact person: Kristina V. Orlova, krisman03@gmail.com
Cutaneous squamous cell carcinoma (cSCC) is the second most common non-melanoma skin cancer worldwide. Patients with unresectable locally advanced or metastatic disease have a poor prognosis. Although anti-PD-1 immune checkpoint inhibitors have been established as the standard of care based on results of pivotal clinical trials, real-world evidence on their effectiveness and safety in the Russian Federation remains limited.
Objective. To evaluate the efficacy and tolerability of anti-PD-1 therapy in patients with locally advanced and metastatic cSCC in routine clinical practice.
Materials and methods. This single-center retrospective study was conducted at the N.N. Blokhin National Medical Research Center of Oncology, Ministry of Health of Russia, between December 2019 and July 2024.
The analysis included 45 patients who received pembrolizumab (n = 19), nivolumab (n = 15), prolgolimab (n = 8), or cemiplimab (n = 3) across different lines of therapy. Efficacy endpoints included objective response rate (ORR), disease control rate (DCR), progression-free survival (PFS), and overall survival (OS). Prognostic factors were assessed using univariate and multivariate Cox proportional hazards regression models.
Results. At a median follow-up of 20.5 months, the ORR was 20.0% and the DCR was 42.2%. Median PFS was 4.1 months (95% CI: 2.2–10.7), and median OS was 19.9 months (95% CI: 12.0–36.6). In the first-line setting (n = 35), ORR increased to 25.7%, median PFS was 5.33 months (95% CI: 2.7–15.1), and median OS was 21.4 months (95% CI: 12.03 – not reached).
On multivariate analysis, lack of objective response was the strongest independent predictor of inferior OS (hazard ratio (HR) 11.96; 95% CI: 1.55–92.26; p = 0.017) and PFS (HR 10.85; 95% CI: 2.42–48.70; p = 0.002). Metastatic disease was independently associated with worse PFS (HR 3.06; p = 0.024) and showed a trend toward shorter OS (HR 2.79; p = 0.051). Female sex was associated with significantly better OS (HR 0.41; p = 0.041). Grade 3–4 adverse events (CTCAE v5.0) occurred in 4.4% of patients (2/45), resulting in treatment discontinuation.
Conclusion. In real-world clinical practice, the efficacy of anti-PD-1 therapy in locally advanced and metastatic cSCC was modest and lower than that observed in registrational clinical trials. Absence of objective response and the presence of distant metastases were the most significant negative prognostic factors.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.