количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Клинические случаи
Возможности комплексного лечения заболеваний желудочно-кишечного тракта
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Гастроэнтерология" №6
- Аннотация
- Статья
- Ссылки
Рассматривается возможность применения комбинированных растительных препаратов с доказанным механизмом действия, эффективностью и безопасностью при функциональных и психосоматических заболеваниях.
В статье приводятся данные о современных подходах к терапии заболеваний желудочно-кишечного тракта (ЖКТ), даются рекомендации по тактике лечения, исследуется возможность применения различных патогенетических средств, имеющих несколько механизмов действия или сложный состав, обсуждаются вопросы выбора препарата для лечения заболеваний ЖКТ.
Рассматривается возможность применения комбинированных растительных препаратов с доказанным механизмом действия, эффективностью и безопасностью при функциональных и психосоматических заболеваниях.
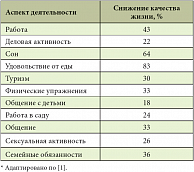
Таблица 1. Ухудшение различных аспектов качества жизни при изжоге

Таблица 2. Типы серотониновых рецепторов
Современные тенденции развития общества делают роль медицины все более значимой. Ускоряющийся ритм жизни создает дополнительные условия для роста распространенности функциональных заболеваний, в том числе функциональной диспепсии. Изменение структуры и режима питания, повышение уровня потребления пищи быстрого приготовления, содержащей большое количество жиров и легких углеводов, увеличение стрессовой нагрузки на работе, обилие информации, изменение ритма сна и бодрствования – все это служит фоном для появления и прогрессирования различных нарушений. До момента соматизации расстройств и присоединения органных изменений врачи сталкиваются с функциональными нарушениями. Очень часто такие нарушения связаны с пищеварительной системой. Вместе с тем пациенты становятся все более требовательными: считают необходимым корректировать любые, даже минимальные симптомы, нередко не являющиеся признаком заболевания. Все более актуальным становится понятие «качество жизни».
Качество жизни и приверженность больных лечению
Качество жизни является достаточно широким понятием, предполагающим не только наличие материальной обеспеченности или соответствующих определенному уровню условий жизни, но и напрямую зависящим от состояния здоровья и изменения самочувствия, влияния здоровья на коммуникации в социуме, психологический и социальный статус, от свободы выбора, действия стресса, избыточной озабоченности и обстоятельности. Таким образом, качество жизни включает в себя факторы, связанные и не связанные со здоровьем. К связанным со здоровьем факторам, по определению Всемирной организации здравоохранения (ВОЗ), относится физическое, психологическое и социальное благополучие.
Различные заболевания в разной степени снижают или ухудшают качество жизни пациентов. Весьма интересные результаты показало исследование H. Liker и соавт. (2005), включавшее более 130 тыс. пациентов. По итогам обследования было определено, что изжога, как один из симптомов гастроэзофагеальной рефлюксной болезни (ГЭРБ), значимо снижает качество жизни в сфере рабочей деятельности на 43%, ухудшает сон на 64%, уменьшает удовольствие от еды на 84%, ограничивает возможности занятия спортом на 33%, ухудшает контакт с детьми на 18%, нарушает сексуальную активность на 26% (табл. 1). Исследования, рассматривавшие изменение качества жизни при других симптомах со стороны ЖКТ, показывают сходные результаты. Особое ухудшение самочувствия вызывают нарушения дефекации (поносы, запоры), метеоризм, а также боли и дискомфорт в животе. Снижение качества жизни при заболеваниях органов пищеварения сопоставимо с таковым при заболеваниях сердечно-сосудистой системы [1, 2].
Одной из особенностей современного пациента является желание качественного или количественного изменения показателей состояния его здоровья. Пациенты становятся все более требовательны в этих вопросах, при этом встречные требования со стороны лечащего врача соблюдаются ими не всегда правильно и не в полном объеме. Учитывая сложившиеся особенности взаимодействия врача и пациента, во всех случаях выявления нарушения пациентом врачебных рекомендаций необходимо (хотя бы в одностороннем порядке) отражать это в медицинской документации. Современные рекомендации и данные множества международных исследований учитывают степень приверженности пациентов лечению (комплаентность). Большое значение в формировании приверженности лечению имеют разъяснения лечащим врачом сущности и принципов действия препаратов; эти разъяснения также отчасти ответственны за получение эффекта плацебо [1, 3]. Основные принципы увеличения приверженности лечению при медикаментозной терапии заключаются в следующих ключевых постулатах:
- Один препарат предпочтительнее нескольких препаратов.
- Один прием предпочтительнее нескольких приемов.
- Простая схема приема предпочтительнее.
- Разделение таблеток нежелательно.
- Готовая форма выпуска (таблетки, капсулы) предпочтительнее.
Эти принципы сформулированы в основном в клинических исследованиях, включавших пациентов с сохраненными когнитивными функциями и ориентированных на сотрудничество с лечащим врачом. Например, уменьшение количества препаратов способствует снижению риска эпизодов «забывания» о приеме лекарственного средства или ошибочного применения другого препарата; уменьшение кратности приема лекарственных средств позволяет избавиться от необходимости длительное время носить препараты с собой.
Терапия пациентов с сочетанной патологией
Следует помнить о пациентах, которые имеют сочетанную патологию, когнитивные нарушения, определенные черты личности, такие как обстоятельность, впечатлительность и другие. Поэтому в ряде ситуаций целесообразно назначение относительно сложной схемы лечения, сочетание нескольких препаратов с различным механизмом действия, режимом приема по истечении определенного количества дней или временного интервала после приема пищи. В ряде случаев подобные меры увеличивают приверженность лечению и повышают доверие к врачу. Например, назначение приема препаратов через определенное время после еды несколько раз в день способствует тому, что пациент акцентирует внимание на процессе лечения и, помня об этом постоянно, не забывает принять препарат согласно предписанию врача [1, 3, 4].
Учитывая стандарты лечения заболеваний, а также множество действующих на организм патогенных факторов, часто требуется многокомпонентная комплексная терапия заболеваний [2, 4]. Стандартизованный подход к решению такой проблемы наглядно иллюстрируется следующими примерами. Так, при лечении ишемической болезни сердца возникает необходимость одновременного приема нитратов, антиагрегантов, бета-блокаторов, ингибиторов ангиотензинпревращающего фермента (АПФ), статинов и других препаратов. При этом кардиологическое заболевание лишь в редких случаях бывает изолированным. Терапия метаболического синдрома должна включать коррекцию дислипидемии, артериальной гипертонии, нарушения толерантности к глюкозе и восстановление функции печени при неалкогольном стеатогепатите [3, 4].
В лечении язвенной болезни желудка также существует необходимость одновременного приема антацидных препаратов, ингибиторов протонной помпы (ИПП), гастропротекторов. При идентификации Helicobacter pylori требуется добавление двух антибактериальных препаратов и пробиотиков для профилактики развития побочных эффектов на фоне терапии [5, 6]. Результативность лечения холестатических заболеваний определяется правильным балансом процессов растворения билиарного сладжа или конкрементов и желчегонного действия. При этом важную роль играет регуляция обмена желчных кислот, нормализация состава желчи. Симптоматическая терапия (спазмолитики и пищеварительные ферменты) обеспечивает в процессе лечения повышение качества жизни [7, 8, 9].
При такой многокомпонентной терапии у врача могут возникать сложности с выбором препарата, анализом возможного лекарственного взаимодействия, риска развития побочных эффектов или изменения эффективности других компонентов терапии. Следствием политерапии явился поиск лекарственных средств, действующих одновременно на несколько звеньев патогенеза заболевания. Таким образом, используя один препарат, мы получаем два и более эффектов. Примером могут служить эссенциальные фосфолипиды, обладающие гепатопротекторным (цитопротекторным), мембраностабилизирующим, антифибротическим эффектами [2, 3, 5, 6, 7, 9].
Существует альтернативный вариант применения комбинированных препаратов, более распространенный в кардиологической практике, – использование лекарственных форм, содержащих, например, ингибиторы АПФ и диуретики, сартаны и диуретики, то есть одного препарата, имеющего в своем составе два и более действующих вещества. Примером из гастроэнтерологической практики могут служить препараты пищеварительных ферментов, содержащие панкреатин (липазу, амилазу и протеазу) и компоненты желчи.
Политерапия в гастроэнтерологии
В гастроэнтерологии часто возникает необходимость назначения нескольких лекарственных средств одновременно, например при функциональных или психосоматических заболеваниях в качестве симптоматической терапии [5, 7, 9]. Так, при функциональной диспепсии возникает комплекс симптомов, включающий изжогу, боли, чувство раннего насыщения, тяжести и переполненности в эпигастрии. При этом комплексное обследование не выявляет у больного органического заболевания, что объясняло бы наличие указанных симптомов. В связи с этим требуется только функциональная коррекция, затрагивающая одновременно несколько механизмов [6, 8, 10].
Существует множество теорий, объясняющих этиологию и патогенез функциональных заболеваний. Так, считается, что висцеральная гиперчувствительность является одним из основных механизмов при функциональных нарушениях. Установлено, что такие пациенты имеют повышенную чувствительность к растяжению желудка [10, 11]. Гиперчувствительность желудка провоцирует развитие симптомов вследствие активации рецепторов. У пациентов с гиперчувствительностью активация определенных зон коры головного мозга происходила при меньшем растяжении желудка, чем у пациентов без гиперчувствительности [12].
При этом исследования показывают, что зачастую нет взаимосвязи между выраженностью воспалительных изменений и жалоб у пациентов, а уменьшение активности гастрита редко приводит к уменьшению жалоб [11, 13]. Значимая часть пациентов с морфологическими признаками гастрита не предъявляют жалоб, так же как и пациенты с «немыми» язвами. Результаты исследований показывают, что изжога и боли в эпигастрии значительно чаще встречаются у пациентов с функциональными нарушениями на фоне вегетативной дисфункции [13, 14].
Психологические особенности и структура личности пациентов с функциональными нарушениями требуют специального подхода к терапии. Психосоциальные факторы, по мнению ряда авторов, определяют поведение больного, отношение к болезни и особенности клиники [15, 16]. Исследования подтвердили связь симптомов диспепсии с психосоциальными факторами, такими как соматизация, тревога и жизненные стрессовые события. Пациенты с функциональными симптомами подвержены ипохондрии, фобиям, тревожности и беспокойству по поводу состояния здоровья, что служит основной причиной их обращения к врачам [15, 16].
Пациентам с функциональными расстройствами, принимая в расчет их особенности – висцеральную гиперчувствительность, не зависящую от органических изменений, психологические характеристики, – в соответствии с современными рекомендациями назначают целый ряд лекарственных препаратов. В схему лечения включают антациды, ИПП, пищеварительные ферменты, пробиотические препараты, средства, влияющие на моторику ЖКТ, спазмолитики, прокинетики, анксиолитики и антидепрессанты [17, 18, 19].
Значительный интерес представляет комбинированный препарат STW 5 (Иберогаст), содержащий 9 различных растительных компонентов: иберийку горькую (Iberis amara), дягиль лекарственный (Angelica archangelica), ромашку аптечную (Matricaria chamomilla), тмин обыкновенный (Carum carvi), расторопшу пятнистую (Silybum marianum), мелиссу лекарственную (Melissa officinalis), мяту перечную (Mentha piperita), чистотел майский (Chelidonium majus), солодку голую (Glycyrrhiza glabra). Продолжительность курса лечения составляет от 2 до 6 недель.
Сочетание трав в данном препарате демонстрирует интересные практические результаты. Иберогаст обладает прокинетическим и одновременно спазмолитическим действием, легким противовоспалительным действием, в целом уменьшая симптоматику и диспептические проявления [20–24]. Таким образом, применение данного препарата, в том числе в качестве монотерапии функциональных заболеваний ЖКТ, соответствует постулатам повышения приверженности пациентов к терапии: один препарат – несколько эффектов. Для большинства растительных препаратов длительно не изученным остается механизм их действия. В случае Иберогаста проводился ряд исследований, в которых была установлена селективность компонентов препарата к интерстинальным серотониновым рецепторам 5-НТ3, 5-НТ4, мускариновым М3, опиоидным рецепторам [25, 26]. Типы серотониновых рецепторов указаны в таблице 2.
Эффективность и безопасность применения препарата Иберогаст при функциональных заболеваниях ЖКТ, в том числе при синдроме раздраженного кишечника (СРК), продемонстрированы в ряде клинических исследований [27, 28]. Механизм действия препарата при СРК заключается преимущественно в блокаде ряда рецепторов [29, 30]. Одно из крупных многоцентровых двойных слепых плацебоконтролируемых исследований, включающее 208 больных СРК, продемонстрировало значимое уменьшение общего индекса симптомов и абдоминальной боли при монотерапии Иберогастом. Выраженность абдоминальных симптомов, оцененных по визуальным аналоговым шкалам, по окончании курса лечения в группе Иберогаста составила 27,3 балла (в начале лечения – 59,1 балла) против 45,5 баллов в группе плацебо. Различия между группами были статистически достоверны [31, 32]. Важным является то, что положительный эффект терапии не зависит от преобладания симптомов. Причины подобного феномена требуют дальнейшего изучения.
Выводы
В современной гастроэнтерологии целесообразным представляется использование лекарственных средств, действующих на несколько патологических механизмов заболевания одновременно. При ряде заболеваний это позволит сократить количество назначаемых препаратов. С учетом психологических особенностей пациентов необходим правильный подбор схемы назначения препарата и режима его приема. При функциональных и психосоматических заболеваниях возможно применение комбинированных растительных препаратов с доказанным механизмом действия, отличающихся хорошей эффективностью и безопасностью.
1. Liker H., Hungin P., Wiklund I. Managing gastroesophageal reflux disease in primary care: the patient perspective // J. Am. Board. Fam. Pract. 2005. Vol. 18. № 5. P. 393–400.
2. Fischler B., Tack J., De Gucht V., Shkedy Z.I., Persoons P., Broekaert D., Molenberghs G., Janssens J. Heterogeneity of symptom pattern, psychosocial factors, and pathophysiological mechanisms in severe functional dyspepsia // Gastroenterology. 2003. Vol. 124. № 4. P. 903–910.
3. Вялов С.С., Степченко А.А., Дронова Т.А., Винницкая Е.В. Выбор препарата для лекарственной терапии с учетом особенностей субстанции // Архивъ внутренней медицины. 2012. № 4 (6). С. 34–38.
4. Вялов С.С. Комбинированная терапия НАЖБП: суммация гепатопротективного эффекта // РЖГГК. 2011. Т. 21. № 5. С. 83.
5. Tack J., Bisschops R., Sarnelli G. Pathophysiology and treatment of functional dyspepsia // Gastroenterology. 2004. Vol. 127. № 4. P. 1239–1255.
6. Маев И.В., Самсонов А.А., Трухманов А.С., Голубев Н.Н., Иванченко Е.А. Эффективность использования нового прокинетика с двойным механизмом действия итоприда гидрохлорида у больных функциональной диспепсией // Сonsilium Medicum. Гастроэнтерология. 2007. № 2. С. 33–38.
7. Tack J., Talley N.J., Camilleri M., Holtmann G., Hu P., Malagelada J.R., Stanghellini V. Functional gastroduodenal disorders // Gastroenterology. 2006. Vol. 130. № 5. P. 1466–1479.
8. Вялов С.С. Сравнительная оценка эффективности антацидных препаратов в лечении патологии желудочно-кишечного тракта у лиц молодого возраста // РМЖ. 2010. Т. 18. № 22. С. 1–5.
9. Stanghellini V., De Ponti F., De Giorgio R., Barbara G., Tosetti C., Corinaldesi R. New developments in the treatment of functional dyspepsia // Drugs. 2003. Vol. 63. № 9. P. 869–892.
10. Keohane J., Quigley E.M. Functional dyspepsia and nonerosive reflux disease: clinical interactions and their implications // MedGenMed. 2007. Vol. 9. № 3. P. 31.
11. Вялов С.С., Кузнецов В.И., Чорбинская С.А., Ходорович А.М. Основные принципы диагностики и лечения гастроэзофагорефлюксной болезни (ГЭРБ) в поликлинических условиях. М.: РУДН, 2010. 21 с.
12. Kindt S., Tack J. Impaired gastric accommodation and its role in dyspepsia // Gut. 2006. Vol. 55. № 12. P. 1685–1691.
13. Вялов С.С. Клинико-патофизиологические особенности хронического гастрита, сочетанного с ГЭРБ, у лиц молодого возраста из разных климато-географических регионов // РЖГГК. 2011. № 5. С. 132.
14. Lopez Gaston A., Andrusch A., Catuogno P. Functional dyspepsia and infection by Helicobacter pylori: a causal relation does not exist // Acta Gastroenterol. Latinoam. 2003. Vol. 33. № 1. P. 13–21.
15. Сидоров П.И., Соловьев А.Г., Новикова И.А. Психосоматическая медицина. Руководство для врачей. М.: Медпресс-информ, 2006. 568 с.
16. Tominaga K., Higuchi K., Iketani T., Ochi M., Kadouchi K., Tanigawa T., Shiba M., Watanabe T., Fujiwara Y., Oshitani N., Nagata T., Kiriike N., Arakawa T. Comparison of gastrointestinal symptoms and psychological factors of functional dyspepsia to peptic ulcer or panic disorder patients // Inflammopharmacology. 2007. Vol. 15. № 2. P. 84–89.
17. Яковенко Э.П., Агафонова Н.А., Яковенко А.В., Иванов А.Н., Прянишникова А.С., Краснолобова Л.П., Попова Е.В. Роль моторных нарушений в механизмах формирования клинических проявлений синдрома раздраженного кишечника (СРК) и СРК-подобных нарушений. Вопросы терапии // Consilium Medicum. Гастроэнтерология. 2011. № 1. С. 69–73.
18. Агафонова Н.А., Яковенко Э.П., Прянишникова А.С., Яковенко А.В., Иванов А.Н. Патогенетические подходы в лечении синдрома раздраженного кишечника // Лечащий врач. 2011. № 7. С. 10–14.
19. Ардатская М.Д. Синдром раздраженного кишечника. Клиническая лекция // Consilium Medicum. 2010. Т. 12. № 8. С. 48–54.
20. Roesch W., Liebregts T., Gundermann K.J., Vinson B., Holtmann G. Phytotherapy for functional dyspepsia: a review of the clinical evidence for the herbal preparation STW 5 // Phytomedicine. 2006. Vol. 13. Suppl. 5. P. 114–121.
21. Nikolay K. Funktionelle Gastroenteropathien im therapeutischen Blindvergleich von Metoclopramid mit dem Phytopharmakon Iberogast // Gastro. Entero. Hepatologie. 1984. Vol. 2. № 4. P. 24–28.
22. Pilichiewicz A.N., Horowitz M., Russo A., Maddox A.F., Jones K.L., Schemann M., Holtmann G., Feinle-Bisset C. Effects of Iberogast on proximal gastric volume, antropyloroduodenal (APD) motility and gastric emptying in healthy men // Am. J. Gastroenterol. 2007. Vol. 102. № 6. P. 1276–1283.
23. Schemann M., Michel K., Zeller F., Hohenester B., Ruhl A. Region-specific effects of STW 5 (Iberogast) and its components in gastric fundus, corpus and antrum // Phytomedicine. 2006. Vol. 13. Suppl. 5. P. 90–99.
24. Khayyal M.T., Seif-El-Nasr M., El-Ghazaly M.A., Okpanyi S.N., Kelber O., Weiser D. Mechanisms involved in the gastro-protective effect of STW 5 (Iberogast) and its components against ulcers and rebound acidity // Phytomedicine. 2006. Vol. 13. Suppl. 5. P. 56–66.
25. Houghton L.A., Rogers J., Whorwell P.J., Campbell F.C., Williams N.S., Goka J. Zamifenacin (UK-76, 654) a potent gut M3 selective muscarinic antagonist, reduces colonic motor activity in patients with irritable bowel syndrome // Aliment. Pharmacol. Ther. 1997. Vol. 11. № 3. P. 561–568.
26. Berman S.M., Chang L., Suyenobu B., Derbyshire S.W., Stains J., Fitzgerald L., Mandelkern M., Hamm L., Vogt B., Naliboff B.D., Mayer E.A. Condition-specific deactivation of brain regions by 5-HT3 receptor antagonist Alosetron // Gastroenterology. 2002. Vol. 123. № 4. P. 969–977.
27. Saller R., Pfister-Hotz G., Iten F., Melzer J., Reichling J. Iberogast: a modern phytotherapeutic combined herbal drug for the treatment of functional disorders of the gastrointestinal tract (dyspepsia, irritable bowel syndrome) – from phytomedicine to “evidence based phytotherapy”. A systematic review // Forsch Komlementarmed Klass Naturheilk. 2002. Vol. 9. Suppl. 1. P. 1–20.
28. Madisch A., Holtmann G., Plein K., Hotz J. Treatment of irritable bowel syndrome with herbal preparations: results of а double-blind, randomized, placebo-controlled, multi-centre trial // Aliment. Pharmacol. Ther. 2004. Vol. 19. № 3. P. 271–279.
29. Simmen U., Kelber O., Okpanyi S.N., Jaeggi R., Bueter B., Weiser D. Binding of STW 5 (Iberogast) and its components to intestinal 5-HT, muscarinic M3, and opioid receptors // Phytomedicine. 2006. Vol. 13. Suppl. 5. P. 51–55.
30. Simmen U., Kelber O., Jaggi R., Buter B., Okpanyi S.N.,Weiser D. Relevance of the herbal combination of STW 5 for its binding affinity to the muscarinic M3 receptor // Naunyn Schmiedebergs Arch. Pharmacol. 2003. Vol. 367. Suppl. 1. P. R22.
31. Von Arnim U., Peitz U., Vinson B., Gundermann K.J., Malfertheiner P. STW 5, a phytopharmacon for patients with functional dyspepsia: results of a multicenter, placebo-controlled double-blind study // Am. J. Gastroenterol. 2007. Vol. 102. № 6. P. 1268–1275.
32. Michael S., Kelber O., Vinson B., Nieber K. Herbal preparations STW 5 and STW 6 inhibit ileal inflammation-mediated motility disorders // Gut Supplement V. 2006. Vol. 55. P. A1–A352.
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.