Диагностика и лечение синдрома обструктивного апноэ сна у взрослых. Рекомендации Российского общества сомнологов
- Аннотация
- Статья
- Ссылки
- English

Введение
Синдром обструктивного апноэ сна (СОАС) является одним из наиболее распространенных патологических состояний, непосредственно связанных со сном, и количество страдающих им пациентов в экономически развитых странах продолжает прогрессивно увеличиваться. В отсутствие адекватной и своевременной медицинской помощи СОАС приводит не только к значительному ухудшению качества жизни больного, но и к большому числу негативных медико-социальных последствий, включая высокий риск тяжелой сердечно-сосудистой патологии и возрастающую вероятность дорожно-транспортных происшествий. Вместе с тем на сегодняшний день разработаны инструменты для точной диагностики и методы эффективного лечения СОАС [1–4].
Настоящие рекомендации по диагностике и лечению СОАС у взрослых пациентов – первое в Российской Федерации практическое руководство, разработанное на уровне всероссийской профессиональной организации врачей-сомнологов и направленное на стандартизацию деятельности отечественных специалистов, занимающихся респираторной медициной сна. Рекомендации были предложены членами научного совета Российского общества сомнологов, прошли обсуждение с участием всех членов общества, были рассмотрены и утверждены на IV Российской научно-практической конференции с международным участием «Клиническая сомнология» (2018).
Авторы рекомендаций выполнили систематический обзор литературы, представленной в базе данных PubMed и российской научной электронной библиотеке Elibrary.ru, а также проанализировали текущие рекомендации Американской академии медицины сна, Американского торакального общества, Американской академии стоматологической медицины сна, Канадского торакального общества, Европейского респираторного общества и ряда других врачебных организаций и ассоциаций [5–30]. Некоторые рекомендации, содержащиеся в этих документах, были перенесены в настоящее руководство с небольшими изменениями или без таковых. На основании собственного практического опыта авторы постарались максимально актуализировать и адаптировать существующую мировую практику к реальным условиям работы российских специалистов в области медицины сна. Выводы, полученные в результате этой работы, представляют собой согласительный документ и оформлены в виде настоящих рекомендаций.
Для обозначения уровня значимости приведенных рекомендаций была использована следующая доказательная база.
Стандарт. Основывается на результатах целого ряда рандомизированных контролируемых исследований и крупных метаанализов. В большинстве случаев совпадает со стандартами, принятыми в странах Западной Европы и Северной Америки.
Рекомендация. Основывается на результатах отдельных рандомизированных контролируемых, большом числе нерандомизированных неконтролируемых или наблюдательных исследований и прошло проверку многолетней клинической практикой.
Мнение. Основывается на отдельных нерандомизированных неконтролируемых или наблюдательных исследованиях, описании случаев и личном практическом опыте авторов данных рекомендаций.
Ключевые понятия, определения и классификация
СОАС – нарушение дыхания во сне, характеризующееся повторяющимися эпизодами прекращения дыхания или существенного уменьшения дыхательного потока при сохранении дыхательных усилий в результате обструкции верхних дыхательных путей, что обычно вызывает снижение насыщения крови кислородом и фрагментацию сна, сопровождается храпом и избыточной дневной сонливостью [15].
Согласно существующему определению, обструктивное апноэ – дыхательная пауза во время сна с отсутствием или значительным, более чем на 90% от исходного, уменьшением носоротового воздушного потока длительностью 10 секунд и более на фоне сохраняющихся дыхательных усилий [8]. Обструктивное апноэ завершается реакцией активации – микропробуждением головного мозга. Смешанное апноэ, начинающееся как центральное с исчезновения носоротового воздушного потока и дыхательных усилий, но в дальнейшем характеризующееся возобновлением дыхательных усилий, исходя из существующих на сегодняшний день представлений о физиологии нарушений дыхания во время сна, следует приравнивать по клиническому значению к обструктивному. Необходимо иметь в виду, что часть эпизодов апноэ, которые не сопровождаются визуально различимыми при записи полисомнографии или респираторной полиграфии дыхательными движениями грудной клетки и брюшной стенки и поэтому классифицируются как центральные, в некоторых случаях также могут носить обструктивный характер. Это объясняется тем, что у некоторых пациентов рефлекторно происходит прекращение дыхательных усилий в ответ на обструкцию верхних дыхательных путей или для регистрации сигнала дыхательных движений просто не хватает чувствительности соответствующих датчиков. В связи с этим, если полиграфическая картина центральных апноэ регистрируется преимущественно в положении пациента на спине, а возобновление дыхания сопровождается храпом, есть вероятность, что они также исходно носят обструктивный характер (рекомендация).
Обструктивное гипопноэ характеризуется уменьшением носоротового воздушного потока на 30% и более по сравнению с исходным в течение не менее 10 секунд в сочетании со снижением сатурации кислородом на 3% и более и/или реакцией активации. Типичные признаки обструктивного гипопноэ: храп, уплощение кривой воздушного потока на вдохе и торакоабдоминальный парадокс (противофазные движения грудной клетки и брюшной стенки) во время события. При отсутствии пищеводного датчика давления дифференцировка обструктивного и центрального гипопноэ может быть затруднена и не является обязательной (стандарт) [7].
Респираторные эпизоды, включающие визуально различимое изменение воздушного потока и увеличение дыхательных усилий в сочетании с реакцией активации и при этом не достигающие критериев гипопноэ, называют микропробуждениями, связанными с дыхательными усилиями. Регистрация этих дыхательных событий при полисомнографии не является обязательной [7].
Ниже представлены диагностические критерии СОАС [15].
А. Присутствует хотя бы один симптом из перечисленных ниже.
- Неосвежающий сон, дневная сонливость, чувство усталости и разбитости в течение дня или бессонница.
- Пробуждение с ощущением задержки дыхания, нехватки воздуха или удушья.
- Постоянный храп и/или остановки дыхания во время сна, со слов окружающих.
При полисомнографии или респираторной полиграфии выявляются следующие обструктивные события.
Б. Пять и более любых обструктивных респираторных событий за час сна (при полисомнографии) или за час исследования (при респираторной полиграфии) в сочетании с критериями пункта А, или
В. 15 и более любых обструктивных респираторных событий за час сна (при полисомнографии) или за час исследования (при респираторной полиграфии) независимо от наличия критериев пункта А.
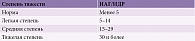
Степень тяжести СОАС оценивают на основании индекса апноэ – гипопноэ (ИАГ) или индекса дыхательных расстройств (ИДР) [11]. ИАГ – среднее суммарное количество апноэ и гипопноэ за час сна (при полисомнографии) или за час исследования (при респираторной полиграфии). ИДР – среднее суммарное количество всех дыхательных событий (апноэ, гипопноэ и микропробуждений, связанных с дыхательными усилиями) за час сна (при полисомнографии). Из текста должно быть понятно, с помощью какого диагностического метода (полисомнографии или респираторной полиграфии) рассчитан тот или иной индекс (стандарт) [15]. Следует принимать во внимание, что частота респираторных событий по результатам респираторной полиграфии может недооцениваться. Это связано с тем, что не учитывается время бодрствования во время исследования и не регистрируются дыхательные события (гипопноэ и микропробуждения, связанные с дыхательными усилиями), сопровождающиеся реакциями активации при отсутствии значимых десатураций (стандарт) [31, 32].
В таблице 1 представлена классификация СОАС по степени тяжести (стандарт), которая не просто отражает мнение ряда экспертов, но имеет клиническое обоснование. Полученные в нескольких масштабных эпидемиологических исследованиях данные свидетельствуют о том, что именно после пяти патологических респираторных событий за час сна обычно появляется и постепенно прогрессирует характерная для СОАС клиническая симптоматика. При ИАГ ≥ 15 начинает увеличиваться связанный с апноэ сна риск сердечно-сосудистых и обменных нарушений. При ИАГ ≥ 30 значительно возрастает вероятность возникновения тяжелых сердечно-сосудистых осложнений, в том числе приводящих к смертельному исходу.
Следует подчеркнуть, что между величиной ИАГ и выраженностью субъективной симптоматики существует достаточно слабая корреляционная связь. В ряде случаев пациенты с весьма умеренными расстройствами дыхания во время сна могут описывать характерную клиническую картину СОАС, в то время как некоторые больные со значительно большим числом эпизодов апноэ, напротив, предъявляют минимум жалоб. Кроме того, все данные о связи между СОАС и разнообразными сердечно-сосудистыми осложнениями получены на основании оценки величины ИАГ, а связь между субъективной симптоматикой, сердечно-сосудистой заболеваемостью и смертностью не установлена. Необходимо также иметь в виду, что характерные для СОАС жалобы, и в первую очередь дневная сонливость, неспецифичны и широко распространены в популяции. Поэтому при оценке тяжести СОАС надо прежде всего ориентироваться на величину ИАГ или ИДР и только потом – на клинические проявления заболевания (стандарт) [11, 12, 23].
Диагностика
Большое число заболеваний может сопровождаться жалобами на нарушения сна и разнообразными сопутствующими дневными симптомами, включая дневную сонливость. Изолированная оценка внешних проявлений болезни в ходе непосредственного опроса больного или опосредованно с помощью разработанных для первичного выявления пациентов с обструктивным апноэ сна специальных опросников не может быть основанием для окончательной постановки диагноза СОАС (стандарт) [9, 33]. Несмотря на то что в типичных случаях можно с достаточно высокой вероятностью заподозрить это заболевание на основании имеющихся у пациента симптомов и признаков, на данный момент нет достоверного способа чисто клинической диагностики СОАС, и диагноз обязательно должен быть подтвержден инструментальными методами исследования (стандарт) [11]. Решение о необходимости специализированного обследования и его объеме может основываться на первичном анализе клинической картины заболевания в целом и результатах некоторых инструментальных методов обследования, например суточного мониторирования электрокардиограммы или артериального давления (стандарт) [9].
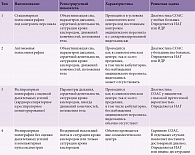
Существует целый ряд значительно отличающихся друг от друга по техническим характеристикам диагностических устройств, позволяющих объективно измерять различные параметры дыхания во время сна и с той или иной точностью выявлять имеющиеся респираторные нарушения. Чаще всего это оборудование подразделяют на четыре типа (табл. 2) [10, 34, 35].
Наиболее точным методом диагностики СОАС является стационарная полисомнография под контролем персонала (стандарт) [10], которая проводится в условиях сомнологического центра. Полисомнография в автономном режиме с использованием портативных устройств и без наблюдения персонала во время исследования может выполняться как в сомнологическом центре, так и за его пределами, в том числе амбулаторно. Полисомнография включает в себя одновременную регистрацию таких параметров, как электроэнцефалограмма, электроокулограмма, подбородочная электромиограмма, назальный (при помощи носовых канюль) и ороназальный (при помощи термистора) воздушный поток, торакоабдоминальные дыхательные усилия, электрокардиограмма, сатурация крови кислородом, положение тела, электромиограмма нижних конечностей. Это единственная на сегодняшний день методика, позволяющая не просто выявить патологические респираторные события, но и соотнести их с истинной продолжительностью и структурой сна. В результате такого исследования можно получить величину ИАГ или при регистрации микропробуждений, связанных с дыхательными усилиями, ИДР [8].
Респираторная полиграфия (кардиореспираторное и респираторное мониторирование), проводимая как в стационаре, так и амбулаторно, в первую очередь предназначена для подтверждения диагноза СОАС у пациентов с высокой претестовой вероятностью выраженного (средней или тяжелой степени) СОАС (стандарт) [10, 31, 34]. Основным недостатком метода является невозможность объективизировать процесс сна. Полученный в итоге ИАГ потенциально может оказаться меньше, чем ИАГ, выявленный при полисомнографии. У пациентов с очень тяжелой обструкцией это не приводит к недооценке степени тяжести СОАС и изменению тактики лечения, но по мере уменьшения выраженности нарушений дыхания вероятность недооценки степени тяжести или даже ложноотрицательного результата возрастает.
Под высокой претестовой вероятностью следует понимать сочетание избыточной дневной сонливости с как минимум двумя из трех критериев:
- постоянный громкий храп;
- остановки дыхания во сне, которые замечают окружающие, и/или пробуждения с одышкой или удушьем;
- артериальная гипертензия (рекомендация).
Кроме того, портативные кардиореспираторные системы также могут достоверно выявлять клинически значимый СОАС и при исходно низкой претестовой вероятности (рекомендация), но при этом не позволяют исключить наличие СОАС, в том числе средней и тяжелой степени (стандарт) [10, 36].
В нашей стране под кардиореспираторным мониторированием традиционно понимают такой вариант респираторной полиграфии, при котором в числе прочего регистрируется электрокардиограмма. Если оценивается только частота пульса на основании пульсоксиметрии, то говорят о респираторном мониторировании. Применительно к диагностике СОАС эта разница несущественна, а использование такой классификации не обязательно (мнение).
На сегодняшний день представлено множество моделей кардиореспираторных и респираторных мониторов от разных производителей, которые по формальным критериям могут быть отнесены к устройствам третьего типа. Минимально достаточный набор регистрируемых параметров предполагает оценку назального воздушного потока с помощью носовой канюли, регистрацию дыхательных усилий посредством индуктивной плетизмографии и сатурации крови кислородом (стандарт) [14, 31]. Предпочтительно использовать два торакоабдоминальных ремня, позволяющих по отдельности оценить дыхательные усилия в области груди и живота, однако наличие только одного ремня также приемлемо (рекомендация).
Основным препятствием для использования респираторной полиграфии при диагностике СОАС следует считать жалобы пациента на выраженные нарушения инициирования и поддержания сна. Из-за того, что нельзя оценить реальное время сна при сочетании вероятного СОАС и инсомнии, может существенно недооцениваться тяжесть нарушений дыхания во сне и изначально снижаться ценность результатов исследования у этой категории больных (стандарт). Кроме того, на результат кардиореспираторного или респираторного мониторирования может повлиять наличие у пациента коморбидных патологических состояний, сопровождающихся необструктивными нарушениями дыхания во время сна: центральными апноэ, гиповентиляцией и гипоксемией (стандарт) [10].
Респираторные мониторы с двумя каналами регистрации данных (воздушный поток и сатурация) уступают по информативности устройствам третьего типа. Однако на практике нередко складывается ситуация, когда другие инструментальные методы диагностики СОАС недоступны. В тех случаях, когда претестовая вероятность выраженного СОАС высока и отсутствуют тяжелые коморбидные состояния, респираторное мониторирование без оценки дыхательных усилий можно рассматривать в качестве приемлемой и достоверной диагностической методики наравне с устройствами третьего типа (мнение).
Компьютерная мониторинговая пульсоксиметрия позволяет выявлять связанные с СОАС повторяющиеся десатурации, но не обладает достаточной чувствительностью для диагностики СОАС, не фиксирует дыхательные события как основной клинический признак СОАС и не дает определять степень тяжести СОАС (за исключением тяжелых случаев). Этот метод может быть использован для инструментального скрининга, но не рекомендуется для рутинной диагностики СОАС (стандарт) [27, 36].
Анализ результатов, полученных с помощью любого из существующих диагностических методов, должен в обязательном порядке проводить специалист, имеющий достаточную квалификацию в области респираторной медицины сна (стандарт). Использование медицинских заключений, основывающихся только на автоматической компьютерной расшифровке результатов исследования, неприемлемо (стандарт) [8, 10, 27].
Широкая распространенность в популяции обструктивных нарушений дыхания во время сна и отсутствие реальной возможности провести углубленное обследование всем потенциально нуждающимся в этом больным обусловливают необходимость разработки оптимальных принципов диагностики СОАС. Одним из них может быть широкое использование более простых и доступных диагностических методов. На практике этот подход обозначается как поэтапное выявление СОАС. Данная концепция ступенчатой диагностики предполагает, что на первом этапе лечащий врач оценивает клиническую картину заболевания и имеющийся риск СОАС при помощи стандартного осмотра, сбора анамнеза и опросников. Дополнительным скрининговым методом может быть компьютерная мониторинговая пульсоксиметрия. Затем пациентам с высокой претестовой вероятностью выраженного СОАС и минимальным числом факторов, способствующих как ложноположительным, так и ложноотрицательным результатам, проводится кардиореспираторное или респираторное мониторирование. Если выявляется выраженная степень СОАС и предполагается неинвазивная вентиляция постоянным положительным давлением воздушного потока во время сна (Constant Positive Airway Pressure, СиПАП-терапия), на этом диагностика может быть закончена. При отсутствии высокой претестовой вероятности, наличии факторов, препятствующих проведению кардиореспираторного и респираторного мониторирования, а также в тех случаях, когда необходимо уточнить степень тяжести СОАС и рассматриваются варианты лечения, отличные от СиПАП-терапии, пациента следует направить на полисомнографию (рекомендация). Это не означает, что полисомнографию нельзя использовать в качестве диагностической процедуры первой линии для диагностики СОАС у всех пациентов в тех случаях, когда это возможно.
Лечение
Целью лечения СОАС являются нормализация ИАГ, устранение храпа, избыточной дневной сонливости, гипоксемии во сне и восстановление нормальной структуры сна (стандарт) [21, 23].
Перед началом лечения пациент должен пройти адекватное обследование для подтверждения диагноза и уточнения степени тяжести СОАС, так как тяжесть заболевания в значительной степени определяет выбор дальнейшей тактики. Начало любого лечения только на основании клинических признаков недопустимо (стандарт). В обязательном и интенсивном лечении нуждаются пациенты с тяжелой степенью СОАС (стандарт), при легкой и средней степени тяжести СОАС решение о необходимости активной терапии и ее объеме принимается индивидуально (рекомендация). При этом важно предупреждать прогрессирование СОАС, включая меры по устранению постоянного громкого храпа и избыточной массы тела (рекомендация) [23, 37].
Своевременно начатое, по показаниям и правильно проводимое лечение СОАС приводит к уменьшению или устранению дневной сонливости, улучшению качества жизни, а также к достоверному снижению риска сердечно-сосудистой и общей заболеваемости и смертности (стандарт) [11, 12]. Адекватное лечение СОАС должно быть обязательной составляющей терапии таких ассоциированных с апноэ сна патологических состояний, как метаболический синдром, ожирение, артериальная гипертония, нарушения сердечного ритма и проводимости, сахарный диабет второго типа (стандарт) [23].
На сегодняшний день существуют следующие основные подходы к лечению СОАС: снижение массы тела при ожирении, неинвазивная вентиляция постоянным положительным давлением воздушного потока во время сна (СиПАП-терапия) с различными модификациями, внутриротовые устройства и хирургическая коррекция обструкции верхних дыхательных путей, каждый из которых имеет область применения и ограничения (стандарт) [11, 23]. Позиционная терапия (методы, устраняющие сон на спине) может быть использована у пациентов с выраженной позиционной зависимостью (рекомендация) [26, 38]. Метод электростимуляции подъязычного нерва, эффективный при различной степени тяжести СОАС, особенно при ведущей роли снижения тонуса мышц глотки в патогенезе СОАС (рекомендация) [39], остается дорогостоящим и недоступным в Российской Федерации. Другие методы лечения в настоящее время не могут рассматриваться как эффективные при СОАС.
Снижение массы тела
Одним из основных факторов, приводящих к возникновению СОАС, является ожирение, поэтому у всех больных с избыточной массой тела следует добиваться снижения веса. Одного лишь значительного похудения бывает достаточно для устранения или существенного уменьшения нарушений дыхания во время сна (стандарт) [40]. Несмотря на то что не во всех случаях снижение веса приводит к достаточному уменьшению степени тяжести СОАС, постепенная контролируемая нормализация массы тела положительно сказывается на состоянии здоровья в целом.
Консервативные мероприятия, направленные на снижение веса, особенно при морбидном ожирении, часто оказываются недостаточно эффективными. Хирургическая коррекция ожирения (бариатрическая хирургия) обычно дает выраженные результаты по снижению веса. Целесообразность использования бариатрической хирургии в качестве метода лечения СОАС представляется достаточно спорной, учитывая высокий риск различных осложнений при любом хирургическом вмешательстве у этой категории пациентов. Бариатрическая хирургия является методом выбора при лечении резистентного к консервативному лечению морбидного ожирения, а не способом коррекции СОАС. В то же время наличие СОАС необходимо учитывать при принятии решения о проведении бариатрического хирургического вмешательства. У пациентов с выраженной степенью СОАС такая операция требует обязательного использования СиПАП- или БиПАП-терапии в пред- и послеоперационном периоде (стандарт) [37].
Неинвазивная вентиляция постоянным положительным давлением воздушного потока во время сна (СиПАП-терапия и ее модификации)
СиПАП-терапия создает пневматический каркас, предупреждающий смыкание верхних дыхательных путей во время сна. СиПАП-терапия является наиболее эффективным и безопасным методом лечения СОАС средней и тяжелой степени (стандарт). Рутинное использование СиПАП-терапии у пациентов с легким СОАС не рекомендуется (рекомендация) [11, 17, 22, 23].
Аппараты, обеспечивающие вентиляционную поддержку двумя или тремя уровнями положительного давления (БиПАП- и ТриПАП-терапия), могут оказаться полезными при плохой переносимости высокого уровня положительного давления воздушного потока, а также при сочетании СОАС с синдромами альвеолярной гиповентиляции/гипоксемии во сне (при выраженном ожирении, хронической обструктивной болезни легких, нервно-мышечных заболеваниях, патологии грудной клетки и др.) (стандарт) [17].
Адаптивная сервовентиляция может использоваться для лечения сочетания СОАС с синдромами центрального апноэ сна (рекомендация) [41]. Этот метод в настоящее время не рекомендуется применять у пациентов с хронической сердечной недостаточностью и сниженной фракцией выброса левого желудочка (< 45%) (рекомендация) [5].
Абсолютных противопоказаний к лечению СОАС методами вспомогательной вентиляции во время сна не существует (стандарт) [17]. С осторожностью такое лечение следует назначать при буллезной эмфиземе легких, наличии в анамнезе пневмоторакса, пневмомедиастинума, пневмоцефалии, утечек спинномозговой жидкости, рецидивирующем синусите, рецидивирующих глазных инфекциях, тяжелой дыхательной недостаточности, которая может потребовать интубации и дальнейшей искусственной вентиляции легких, выраженной гипотонии, выраженной дегидратации, частых носовых кровотечениях, предшествующих хирургических вмешательствах на головном мозге, среднем или внутреннем ухе.
СиПАП-терапия может применяться как с постоянным, фиксированным в течение всей ночи давлением воздушного потока, так и с автоматической регулировкой давления в зависимости от характеристик дыхания пациента (авто-СиПАП-терапия) [21]. Авто-СиПАП-терапия почти не уступает по эффективности СиПАП-терапии с фиксированным давлением (рекомендация), уменьшает нагрузку давлением воздушного потока, особенно при выраженной позиционной зависимости или зависимости обструкции от стадий сна, и обычно более комфортна. Следует учитывать, что эффективность использования авто-СиПАП-аппаратов разных производителей у одного и того же пациента может отличаться в связи с различными алгоритмами регулировки работы этих аппаратов (рекомендация). Если количество центральных дыхательных событий (при комплексном апноэ сна, хронической сердечной недостаточности, неврологических расстройствах и др.) существенно, то авто-СиПАП-терапия при некоторых алгоритмах работы может оказаться неэффективной, и в этих случаях требуется использование аппаратов с фиксированным давлением дыхательного потока [42].
Традиционно проводится ручная титрация параметров СиПАП-терапии подготовленным персоналом в течение одной ночи в условиях сомнологического центра под контролем полисомнографии (стандарт) [18]. Ручная титрация параметров СиПАП-терапии под контролем кардиореспираторного мониторирования также возможна (рекомендация). Ручная титрация предпочтительна при большей степени тяжести СОАС, вероятности высокого уровня давления воздушного потока для коррекции дыхательных нарушений, при выраженной степени гипоксемии во сне по данным диагностического исследования, при сочетании СОАС с синдромами гиповентиляции/гипоксемии во сне (стандарт). Ручная титрация также может быть более эффективной при необходимости контроля за поведением пациента во время пробной терапии, при его эмоциональной лабильности, наличии хронической инсомнии (мнение).
У пациентов без выраженной коморбидности допустим автоматический подбор параметров СиПАП-терапии, а в некоторых случаях – переход на БиПАП-терапию при помощи авто-СиПАП- и авто-БиПАП-аппаратов, в том числе в амбулаторном режиме (рекомендация) [20]. Программное обеспечение аппарата в этом случае должно давать возможность детально проанализировать дыхательные параметры во время автоматической титрации, а использование дополнительного пульсоксиметрического датчика – проконтролировать сатурацию крови кислородом, если исходно она была существенно снижена. Автоматическую титрацию параметров СиПАП-терапии рекомендуется проводить в соответствии с приведенными рекомендациями.
При лечении СОАС методом СиПАП-терапии предпочтение отдается носовым маскам, а не носоротовым, в связи с большей комфортностью и эффективностью, однако при существенных нарушениях носового дыхания и преимущественно ротовом дыхании применяются носоротовые маски (рекомендация) [43].
Использование подогреваемого увлажнителя (стандарт) и функция снижения давления на выдохе (рекомендация) могут повысить комфортность терапии для некоторых пациентов и улучшить их приверженность лечению. Существенно повышает комфортность терапии титрация комфортного давления для засыпания, которая проводится персоналом в ручном режиме до начала пробной СиПАП-терапии (рекомендация). Пробная СиПАП-терапия в течение трех – семи ночей до назначения постоянной СиПАП-терапии позволяет повысить приверженность лечению (рекомендация) [1].
СиПАП-терапия применяется на постоянной основе в течение длительного времени и может быть отменена только в случае инструментального подтверждения стойкого устранения обструкции верхних дыхательных путей во сне (стандарт). Минимальной продолжительностью СиПАП-терапии для обеспечения ее эффективности считается в среднем четыре часа в сутки за все время использования, не менее пяти ночей в неделю (стандарт) [17]. В то же время при тяжелой степени СОАС эффективность СиПАП-терапии возрастает при увеличении времени использования и в идеале должна охватывать все время сна (рекомендация).
Внутриротовые приспособления
Исходя из понимания процессов, приводящих к обструкции верхних дыхательных путей при СОАС, создан ряд специальных механических устройств, предотвращающих коллапс глотки во время сна. Использование внутриротовых аппликаторов на сегодняшний день является одним из основных методов лечения СОАС и устранения храпа [25, 26, 28].
Существует два принципиально отличающихся по механизму типа внутриротовых приспособлений: выдвигающие вперед нижнюю челюсть и удерживающие корень языка. Эффективность приспособлений, удерживающих во время сна корень языка, до настоящего времени не доказана. Предпочтительно использовать ротовые аппликаторы, обеспечивающие протрузию нижней челюсти (стандарт) [28]. Все приводимые ниже рекомендации касаются внутриротовых устройств, обеспечивающих смещение нижней челюсти вперед во время сна.
Механические внутриротовые приспособления представляют собой возможную альтернативу терапии положительным давлением или хирургическому лечению при легком и среднетяжелом СОАС. Они не рекомендуются для рутинного лечения пациентов с тяжелым апноэ сна, у которых СиПАП-терапия более эффективна (стандарт). Однако при плохой переносимости и приверженности СиПАП-терапии ротовые аппликаторы можно рассматривать в качестве терапевтической опции даже при тяжелом СОАС (стандарт) [44, 45].
Ротовые аппликаторы должны изготавливаться индивидуально, из разрешенных для использования в стоматологии биологически безопасных для пациента материалов, с учетом всех анатомических особенностей больного, строения и состояния его зубов, опытным стоматологом, имеющим должную квалификацию в этой области (стандарт). Ротовой аппликатор должен быть титруемым – иметь механизм, позволяющий изменять величину выдвижения нижней челюсти вперед (стандарт) [28]. Постепенное изменение величины выдвижения нижней челюсти является аналогом титрации величины давления воздушного потока при подборе СиПАП-терапии.
Серийно выпускаемые стандартные внутриротовые приспособления, предполагающие самостоятельную подгонку пациентом, менее эффективны и безопасны и поэтому не рекомендуются для широкого применения (стандарт) [28].
Полученный при использовании ротового аппликатора клинический эффект обязательно должен быть подтвержден с помощью объективных методов исследования – полисомнографии или респираторной полиграфии (стандарт) [28].
При использовании ротовых устройств серьезные побочные эффекты обычно не возникают, тем не менее пациент, использующий ротовой аппликатор, должен проходить регулярные осмотры стоматолога-ортодонта для своевременного выявления возможных стоматологических осложнений и изменения прикуса (стандарт) [28].
Приверженность терапии с использованием внутриротовых устройств весьма индивидуальна, но в целом выше, чем приверженность СиПАП-терапии. Некоторые больные отмечают выраженный дискомфорт при использовании ротовых аппликаторов, и им требуется дополнительное время для привыкания. Эффективность внутриротовых устройств в отношении показателей нарушения дыхания во время сна, качества сна и клинической симптоматики СОАС ниже, чем эффективность СиПАП-терапии (стандарт) [26, 44].
Хирургическая модификация верхних дыхательных путей
Хирургическая коррекция СОАС ставит задачей устранение анатомических причин, лежащих в основе обструкции верхних дыхательных путей во время сна [46]. В настоящее время достигнут значительный прогресс в области хирургической модификации верхних дыхательных путей, и хирургические методы лечения занимают законное место в арсенале имеющихся способов борьбы с СОАС. В то же время оперативное лечение апноэ сна оказывается достаточно эффективным только при исходно правильном отборе кандидатов на хирургическую коррекцию (стандарт) и сопряжено с определенными рисками, характерными для любого инвазивного вмешательства.
Необходимо провести тщательное обследование больного, и только после того, как будет инструментально подтверждено наличие и установлена тяжесть СОАС, выявлены имеющиеся анатомические предпосылки со стороны верхних дыхательных путей и уточнена локализация обструкции, в индивидуальном порядке может быть принято решение о возможности и необходимом объеме хирургического вмешательства (стандарт). Эффективность операции должна в последующем подтверждаться с помощью инструментальных методов исследования – полисомнографии или респираторной полиграфии (стандарт) [26].
Пациент должен быть проинформирован о частоте успешных исходов предлагаемого хирургического вмешательства, потенциальных осложнениях операции, а также альтернативном лечении, в том числе СиПАП-терапии и внутриротовых приспособлениях (стандарт) [26, 46].
Трахеостомия является единственным абсолютно эффективным способом хирургической коррекции СОАС, однако в настоящее время рассматривается как калечащая операция, имеет эффективную альтернативу в виде СиПАП-терапии и применяется лишь в исключительных случаях при тяжелом СОАС, невозможности СиПАП-терапии и по жизненным показаниям (рекомендация) [47].
Ортогнатические операции на лицевом скелете подразумевают выдвижение вперед верхней и нижней челюстей (максилло-мандибулярное выдвижение) или только нижней челюсти, что у отобранных пациентов приводит к значительному увеличению просвета верхних дыхательных путей. Максилло-мандибулярное выдвижение в целом демонстрирует высокую эффективность, в том числе при средней и тяжелой степени СОАС, низкую частоту серьезных осложнений и может быть рекомендовано некоторым пациентам, которые не переносят или не желают использовать СиПАП-терапию (рекомендация). Потенциальной целевой группой для таких хирургических вмешательств являются пациенты с выраженными челюстно-лицевыми аномалиями (стандарт) [48].
Увулопалатопластика предполагает расширение дыхательных путей, расположенных за нёбной занавеской, и включает резекцию и сшивание передних и задних нёбных дужек, иссечение слизистой оболочки мягкого нёба и нёбного язычка. Эта процедура может быть эффективна при СОАС легкой и средней степени тяжести в случае изолированной обструкции верхних дыхательных путей на уровне мягкого нёба (рекомендация) [6, 46, 49]. При увулопалатофарингопластике перед коррекцией мягкого нёба проводятся тонзиллэктомия, выделение и сшивание нёбно-глоточной и нёбно-язычной мышц, что может устранить проявления выраженного СОАС у пациентов с гипертрофией нёбных миндалин второй-третьей степени (стандарт). Если обструкция верхних дыхательных путей связана только с гипертрофией нёбных миндалин, может быть эффективной изолированная тонзиллэктомия, без вмешательства на мягком нёбе (стандарт) [50].
Лазерная увулопалатопластика включает в себя двусторонние вертикальные надрезы или линейные ожоги при помощи лазера непосредственно с обеих сторон от нёбного язычка и его лазерную резекцию. Этот метод в целом недостаточно эффективен в отношении показателей тяжести СОАС, а в ряде случаев может приводить к утяжелению СОАС либо даже к его появлению на фоне ранее неосложненного храпа за счет увеличения ригидности мягкого нёба или формирования рубцового стеноза. При избыточной резекции мягкого нёба возникает нёбно-глоточная недостаточность, существенно снижающая качество жизни пациента. В качестве метода лечения СОАС лазерная увулопалатопластика не показана (стандарт) [19, 51].
Радиочастотная редукция мягкого нёба и корня языка – воздействие волнами радиочастотного диапазона на соответствующие анатомические структуры глотки с целью их последующего уплотнения и уменьшения объема. Если при использовании лазера рубец образуется поверхностно, то при радиочастотной редукции участок повреждения возникает и рубцуется под слизистой оболочкой. В результате такое вмешательство менее болезненно и легче переносится, сопровождается небольшим числом побочных эффектов и может быть эффективно при СОАС легкой и иногда средней степени тяжести (рекомендация) [52].
При выборе метода хирургической модификации верхних дыхательных путей с целью лечения СОАС, устранения храпа и для уточнения хирургической тактики, локализации и объема вмешательства целесообразно проводить эндоскопическое обследование верхних дыхательных путей в условиях медикаментозного сна – слип-эндоскопию (рекомендация) [53].
Хирургическое восстановление носового дыхания может улучшить результат комплексного лечения в сочетании с другими хирургическими методиками (рекомендация), но не является самостоятельным методом лечения СОАС (стандарт). Хирургическое вмешательство, направленное на нормализацию носового дыхания, может повысить эффективность и переносимость СиПАП-терапии (стандарт) [54].
Заключение
СОАС – широко распространенная и негативно влияющая на качество жизни и общее состояние здоровья пациента патология. Это заболевание все еще недостаточно известно отечественным врачам. В результате пациенты годами наблюдаются у специалистов разного профиля, не получая адекватной помощи и приобретая тяжелые осложнения, сокращающие продолжительность жизни. Практический опыт показывает: даже при наличии минимально необходимого набора диагностической и лечебной аппаратуры можно адекватно выявлять и эффективно лечить значительную часть больных с СОАС не только в специализированных сомнологических центрах, но и в лечебных учреждениях терапевтического, хирургического и стоматологического профиля. Авторы рекомендаций выражают надежду, что их труд станет еще одним шагом в повышении уровня знаний врачей широкого профиля и улучшении качества клинической медицины сна в нашей стране.
Утверждено Российским обществом сомнологов на IV Российской научно-практической конференции с международным участием «Клиническая сомнология» 16.02.2018.
R.V. Buzunov, A.D. Palman, A.Yu. Melnikov, V.M. Averbukh, I.M. Madayeva, A.N. Kulikov
Clinical Sanatorium ‘Barvikha’ of the Business Administration of the President of the RF, Moscow
I.M. Sechenov First Moscow State Medical University (Sechenovskiy University)
Scientific and Clinical Center of Otorhinolaryngology FMBA of Russia, Moscow
Scientific Centre for Family Health and Human Reproduction Problems, Irkutsk
Military Medical Academy named after S.M. Kirov, Saint Petersburg
Contact person: Aleksandr Yuzefovich Melnikov, rossleep@yandex.ru
Clinical recommendations on the diagnosis and treatment of obstructive sleep syndrome in adults, based on international experience and systematic literature review, are the first in Russia guideline on this disease for practical physicians, prepared by the professional community of experts in sleep medicine. Key concepts, diagnostic criteria, classification by severity, classification of diagnostic equipment and various management of obstructive sleep apnea syndrome in adults are considered.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.