Эффективность vs неэффективность системных ретиноидов при акне
- Аннотация
- Статья
- Ссылки
- English
Приводятся данные клинической практики в отношении Акнекутана. Под наблюдением находилось 190 пациентов (105 женщин и 85 мужчин) в возрасте от 14 до 27 лет со средней и тяжелой степенью акне, которым проводилась монотерапия данным препаратом. В результате лечения клиническая ремиссия достигнута у 100% пациентов. Через один – три года после лечения у девяти больных отмечен рецидив. Во всех случаях выявлены гормональные нарушения и эндокринная патология.
Приводятся данные клинической практики в отношении Акнекутана. Под наблюдением находилось 190 пациентов (105 женщин и 85 мужчин) в возрасте от 14 до 27 лет со средней и тяжелой степенью акне, которым проводилась монотерапия данным препаратом. В результате лечения клиническая ремиссия достигнута у 100% пациентов. Через один – три года после лечения у девяти больных отмечен рецидив. Во всех случаях выявлены гормональные нарушения и эндокринная патология.
Акне (вульгарные угри) считается одним из наиболее распространенных заболеваний кожи [1]. По разным данным, частота его встречаемости составляет 60–85%. Чаще патологией страдают подростки и лица молодого возраста. Акне занимает первое место среди заболеваний кожи в данной популяции.
Несмотря на обилие лекарственных средств, лечение акне остается сложной задачей.
Недостаточная эффективность лечения, ассоциированные с данной нозологией аффективные расстройства, такие как дисморфофобия и депрессия, существенно снижающие качество жизни больных и способствующие их социальной дезадаптации, обусловливают медико-социальную значимость проблемы.
Патогенез
В большинстве случаев акне рассматривается как конституционально детерминированное заболевание с повышенной чувствительностью себоцитов к андрогенным стимулам. В последние годы установлено, что одним из ключевых компонентов патогенеза является воспаление. Повышенная выработка интерлейкина 1 (ИЛ-1) приводит к усиленной пролиферации кератиноцитов, а избыточная продукция ядерного фактора NF-κβ – к выбросу фактора некроза опухоли альфа (ФНО-альфа), ИЛ-1, -8 и -10.
Воспаление поддерживается липидными медиаторами: лейкотриенами, простагландинами и 15-гидроксиэтоксисатетраеновыми кислотами [2].
Синтез провоспалительных цитокинов осуществляется через NF-κβ или через Toll-подобные рецепторы (Toll-Like Receptors – TLRs). С помощью TLRs происходит высвобождение антимикробных пептидов (бета-дефенсинов) и металлопротеиназ, которые способствуют развитию воспаления и образованию рубцов при акне [3].
Кроме того, в многочисленных исследованиях установлено, что развитие акне происходит на фоне нескольких взаимосвязанных патогенетических процессов. Наиболее значимыми являются нарушение кератинизации, фолликулярный гиперкератоз, избыточная продукция жирового секрета, что сопровождается дисбалансом липидов и размножением микроорганизмов [4].
Усиление секреции кожного сала происходит за счет увеличения синтеза андрогенов или повышения чувствительности рецепторов к ним. Ранее установлено, что андрогены, такие как тестостерон, дегидроэпиандростерон сульфат и дигидротестостерон, регулируют гены, ответственные за рост сальных желез и выработку кожного сала. Фермент альфа-редуктаза катализирует превращение тестостерона в 5-альфа-дегидротестостерон, экспрессирующийся преимущественно в коже. У пациентов с акне выявлена более высокая активность 5-альфа-редуктазы 1-го типа [5].
Гиперандрогения приводит к изменению не только количественного, но и качественного состава себума. Концентрация альфа-линоленовой кислоты – регулятора дифференцировки кератиноцитов фолликула снижается. В результате нарушения последней развивается фолликулярный кератоз, приводящий к закупорке сальной железы.
В пубертатном периоде гипофиз секретирует гормон роста, который стимулирует выработку инсулиноподобных факторов роста. Себоциты содержат рецепторы к инсулиноподобным факторам роста, взаимодействие с которыми приводит к росту сальной железы. Эстрогены напрямую ингибируют секрецию тестостерона и участвуют в регуляции генов роста сальной железы. Нестабильный гормональный фон и низкий уровень эстрогенов также способствуют развитию акне.
Терапия
Лечение акне зависит от степени его тяжести. Так, при легкой степени ограничиваются наружными средствами, при средней – назначают антибиотики.
Изотретиноин
Наиболее эффективными в терапии акне средней и тяжелой степени являются системные ретиноиды – изотретиноин. Изотретиноин показан пациентам с узловато-кистозными угрями и часто рецидивирующими воспалительными высыпаниями, у которых антибиотики оказались неэффективными, а также больным с тенденцией к разрешению акне в виде рубцов.
В последние годы спектр показаний для назначения изотретиноина расширяется, в том числе в отношении лечения единичных, но рецидивирующих высыпаний на лице. Ряду больных они доставляют много страданий. Прежде всего это относится к публичным лицам – артистам, танцорам, журналистам и т.д., которые хотят быстрого и стойкого эффекта.
Являясь комедонолитиком, системный изотретиноин воздействует на патологическую фолликулярную кератинизацию и функцию сальных желез. Несмотря на то что препарат не обладает прямым антибактериальным эффектом, он способен влиять на хемотаксис и фагоцитоз и таким образом уменьшать численность Cutibacterium [6]. Уже через две недели от начала лечения изотретиноином уменьшается продукция кожного сала. Как следствие, рост микроорганизмов и провоспалительных медиаторов резко сокращается.
На сегодняшний день изотретиноин является единственным препаратом, который эффективен в отношении большинства звеньев патогенеза акне. Это обусловлено молекулярными механизмами действия. Взаимодействуя с ядерными рецепторами, изотретиноин уменьшает дифференцировку клеток сальных желез, что способствует выраженному уменьшению размеров и активности себоцитов.
Изотретиноин назначается на шесть месяцев и более в дозе от 0,1 до 1,0 мг/кг в зависимости от тяжести заболевания. Обязательным условием является прием препарата во время еды.
К сожалению, из-за побочных эффектов, в первую очередь тератогенного действия, ряд врачей, прежде всего вследствие недостатка клинического опыта, ограничивают назначение изотретиноина.
Наиболее частыми нежелательными явлениями на фоне терапии изотретиноином считаются хейлит и сухость кожи. Иногда могут отмечаться ухудшение зрения в ночное время, конъюнктивит, повышенная фоточувствительность, транзиторная потеря волос, артралгия и миалгия, головная боль, транзиторное повышение печеночных трансаминаз, триглицеридов и холестерина. Однако частота развития перечисленных явлений крайне низка.
Ввиду тератогенного действия на центральную нервную систему и сердечно-сосудистую систему плода изотретиноин нельзя принимать во время беременности.
Бытует мнение, что после курса системных ретиноидов высока вероятность рождения ребенка с уродствами и планировать беременность следует только через два года по окончании лечения. Однако период полураспада изотретиноина в отличие от других ретиноидов (этретината и ацитретина) составляет 19 часов. Поэтому женщинам, получающим его, необходимо использовать средства контрацепции только в период терапии и еще в течение месяца по ее завершении. Чтобы минимизировать риск развития данного нежелательного явления, все пациентки детородного возраста перед началом лечения должны получить консультацию по поводу методов контрацепции.
Акнекутан
Для лечения среднетяжелых и тяжелых форм акне уже несколько лет с успехом применяется Акнекутан, в производстве которого используется запатентованная технология Lidose® (Бельгия).
Как известно, изотретиноин относится к плохо растворимым соединениям и всасывается в пищеварительном тракте не полностью. Технология Lidose® предполагает добавление двух компонентов в состав каждой капсулы препарата Акнекутан (Гелюцира и Спана). Благодаря этому увеличивается растворенная фракция изотретиноина в капсуле и, как следствие, его абсорбция. Биодоступность увеличивается на 20% по сравнению с обычной формой изотретиноина. Это позволяет уменьшить количество изотретиноина в каждой капсуле, так как количество работающего вещества полностью соответствует таковому в оригинальном препарате (12 мг из 16 мг Акнекутана или 12 мг из 20 мг Роаккутана), а количество неактивного уменьшается на 50% (4 мг в Акнекутане и 8 мг в Роаккутане). В результате риск развития побочных эффектов снижается.
Необходимо отметить, что биодоступность Акнекутана в меньшей степени зависит от приема пищи, чем биодоступность обычной формы изотретиноина. Так, при приеме без пищи Акнекутан абсорбируется на 70%, препараты обычной формы изотретиноина – только на 38%.
Таким образом, применение изотретиноина в составе Акнекутана позволяет на 20% снизить количество принимаемого пациентом изотретиноина без ущерба для терапевтической эффективности, а также быть уверенным в том, что даже при неполном соблюдении пациентом правил по приему препарата с пищей курсовая доза изотретиноина будет набрана.
Рекомендуемая суточная доза Акнекутана составляет 0,4–0,8 мг/кг, курсовая – 100–120 мг/кг.
Опыт применения
Под нашим наблюдением находилось 190 пациентов (105 (55,3%) женщин и 85 (44,7%) мужчин) в возрасте от 14 до 27 лет. Степень тяжести заболевания определяли с помощью дерматологического индекса акне (ДИА) путем подсчета воспалительных элементов – папул, пустул и узлов. У 114 (60%) больных диагностирована средняя степень тяжести, у 76 (40%) – тяжелая. Пациенты ранее применяли разные методы лечения многократными курсами: системные антибиотики, метронидазол, антиандрогены, наружные средства, плазмолифтинг, чистки, пилинги, мезотерапию, физиотерапевтические процедуры и др. Однако эффект был временный.
Акнекутан назначали после обследования, которое включало клинический и биохимический анализ крови, у женщин при наличии болезненных и обильных менархе – исследование гормонального профиля.
Способ применения Акнекутана – из расчета 0,4–0,8 мг/кг/сут во время приема пищи. Суточная доза зависела не только от массы тела, но и от выраженности клинических проявлений акне.
Для нивелирования проявлений ксероза и хейлита пациенты применяли крем для лица Перфэктоин и увлажняющие губные помады.
При достижении выраженного улучшения суточная доза Акнекутана постепенно снижалась.
Длительность лечения определялась сроками достижения кумулятивной дозы препарата – 100–120 мг/кг. В среднем она составила 32,4 ± 4,6 недели.
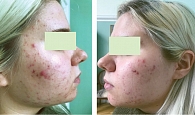
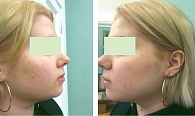
Лечение продолжали до достижения клинической ремиссии. Поэтому редукция показателей ДИА у всех пациентов составила 100% (рис. 1 и 2).
Нежелательные явления носили дозозависимый характер, наблюдались в первые три-четыре месяца и были представлены хейлитом (190 (100%) больных), ретиноевым дерматитом (180 (94,7%)), конъюнктивитом (17 (8,9%)), носовыми кровотечениями (7 (6,7%)), транзиторным повышением трансаминаз (75 (39,4%)), гиперлипидемией (38 (20%)), миалгиями и артралгиями (5 (2,6%)), головной болью (5 (2,6%)).
Побочные явления легко переносились пациентами и не были серьезными.
Нежелательные явления со стороны кожи и органов зрения легко купировались увлажняющими средствами, губными стиками, средствами искусственной слезы.
Изменения показателей клинического и биохимического анализа крови были незначительными и не превышали 20–30% от исходных значений.
При транзиторном повышении трансаминаз назначался гепатопротектор и снижалась суточная доза препарата.
Через один – три года после лечения рецидивы отмечены у девяти пациентов, из них восемь женщин и один мужчина. Эти пациенты были более тщательно обследованы гинекологом и эндокринологом. У шести выявлено повышение уровня тестостерона и дегидроэпиандростерона, у двух – поликистоз яичников по результатам ультразвукового исследования органов малого таза. В двух случаях отмечалось увеличение лютеинизирующего гормона и изменение соотношения «лютеинизирующий гормон/фолликулостимулирующий гормон» > 2. У всех пациенток в анамнезе нарушение менархе.
У двух пациентов (одна женщина и один мужчина) с повышенной массой тела диагностировано нарушение толерантности к глюкозе.
Полученные нами результаты свидетельствуют о высокой эффективности Акнекутана.
Необходимо отметить, что женщинам с рецидивирующими, устойчивыми к проводимой терапии вульгарными угрями и гормональными нарушениями, обусловленными прежде всего гиперандрогенией, рекомендуется лечение половыми гормонами. Прием пероральных гормонов уменьшает секрецию кожного сала, ингибирует эффекты андрогенов в сальных железах.
При угревой болезни используют три группы гормонов: эстрогены, которые подавляют овариальные андрогены, глюкокортикоиды, которые ингибируют надпочечниковые андрогены, и пероральные антиандрогены, которые действуют на периферическом уровне. Эстрогены в небольших дозах (35–50 мкг), применяемые в качестве пероральных противозачаточных средств, способны значительно снизить секрецию сала. Лечение антиандрогенами проводится после консультации с гинекологом-эндокринологом, при этом может потребоваться оценка гормонального профиля крови (уровня лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола, прогестерона, тестостерона, пролактина и дегидроэпиандростерона), ультразвуковое исследование органов малого таза и надпочечников, рентген/томография черепа/мозга.
При средней и тяжелой степени акне лечение гормональными препаратами может проводиться в комплексе с системными ретиноидами или антибиотиками.
Риск развития рецидивов после полноценного курса системных ретиноидов может быть обусловлен синдромом поликистозных (мультифолликулярных) яичников, аденомой гипофиза, опухолью надпочечников или врожденной гиперплазией коры надпочечников, заболеванием щитовидной железы, нарушением толерантности к глюкозе и др. Поэтому необходима консультация гинеколога и эндокринолога.
Другой важной причиной рецидивов является недостаточная суммарная доза изотретиноина или несоблюдение режима приема препарата. Вероятность рецидива при применении низких доз значительно возрастает, что требует более продолжительного курса лечения, чем при использовании стандартных схем [7]. А.L. Zaenglein и соавт. установили, что рецидивы при кумулятивной дозе более 150 мг/кг возникают реже, чем при дозе менее 120 мг/кг [8]. Наименьшая частота рецидивов отмечается при кумулятивной дозе 220 мг/кг [8].
В нашем наблюдении все пациенты получали адекватные дозы в зависимости от степени тяжести кожного процесса и массы тела.
Заключение
Акнекутан является высокоэффективным и безопасным препаратом для лечения акне средней и тяжелой степени. Побочные эффекты незначительны, легко купируются и не требуют отмены препарата.
Как показал наш опыт, рецидивы при применении изотретиноина возникают при наличии сопутствующих эндокринных заболеваний и гормональных нарушений, поэтому лечение акне в таких случаях необходимо проводить совместно с другими специалистами – гинекологами и эндокринологами. Рецидивы могут быть обусловлены назначением неадекватной суточной и кумулятивной дозы препарата, а также нарушением режима его приема.
O.Yu. Olisova, MD, PhD, Prof., Ts. Ma
I.M. Sechenov First Moscow State Medical University
Contact person: Olga Yu. Olisova, olisovaolga@mail.ru
Discussed the epidemiology, pathogenesis and treatment of acne. Special attention is paid to systemic retinoids: their mechanism of action, effectiveness, and safety.
Provided data of clinical practice on Acnecutan use. Under observation there were 190 patients (105 women and 85 men) aged 14 to 27 years with moderate to severe acne treated with monotherapy with this drug. As a result of treatment, clinical remission was achieved in 100% of patients. Nine patients relapsed after one to three years. In all these cases, hormonal disorders and other endocrine abnormalities were detected.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.