Гангренозная пиодермия: опыт применения низкотемпературной аргоновой плазмы
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить эффективность низкотемпературной аргоновой плазмы в комплексной терапии гангренозной пиодермии.
Материал и методы. В исследовании участвовали 50 пациентов женского и мужского пола (26 женщин и 24 мужчины) с впервые или ранее установленным диагнозом «гангренозная пиодермия» в возрасте от 18 до 92 лет. Пациенты были разделены на две рандомизированные группы – 24 и 26 человек соответственно. В первой группе была проведена комплексная терапия с применением НАП – установка «Плазморан» (курс лечения – от 7 до 14 процедур ежедневно и/или через день). Пациенты второй группы получали стандартное лечение, без применения НАП. Всем пациентам проводили исследование особенностей микроциркуляции в краевой зоне язвы. Для изучения влияния заболевания на качество жизни применяли дерматологический индекс качества жизни (ДИКЖ). Для оценки степени болевого синдрома использовали опросник боли PainDetect.
Результаты. Комплексная терапия ГП с применением НАП продемонстрировала ускоренное заживление ран и уменьшение воспаления. У 24 пациентов, получавших терапию НАП, наблюдалось стойкое улучшение состояния. Пациенты отметили заметное уменьшение боли и улучшение качества жизни. На фоне проведенного исследования отмечались повышение величины среднего потока перфузии крови (показатель M) и снижение показателя среднеквадратичного отклонения (показатель σ), при этом положительная динамика в группе комбинированной терапии была существенно сильнее выражена, чем в группе контроля. Фотодокументация (до/после НАП) подтверждает терапевтические преимущества этого дополнительного метода.
Заключение. Низкотемпературная аргоновая плазма значительно повышает эффективность лечения язв у больных с гангренозной пиодермией, что подтверждается результатами визуального осмотра, положительной динамикой лазерной допплеровской флоуметрии микроциркуляции крови, снижением болезненных ощущений и повышением уровня качества жизни пациентов.
Цель – оценить эффективность низкотемпературной аргоновой плазмы в комплексной терапии гангренозной пиодермии.
Материал и методы. В исследовании участвовали 50 пациентов женского и мужского пола (26 женщин и 24 мужчины) с впервые или ранее установленным диагнозом «гангренозная пиодермия» в возрасте от 18 до 92 лет. Пациенты были разделены на две рандомизированные группы – 24 и 26 человек соответственно. В первой группе была проведена комплексная терапия с применением НАП – установка «Плазморан» (курс лечения – от 7 до 14 процедур ежедневно и/или через день). Пациенты второй группы получали стандартное лечение, без применения НАП. Всем пациентам проводили исследование особенностей микроциркуляции в краевой зоне язвы. Для изучения влияния заболевания на качество жизни применяли дерматологический индекс качества жизни (ДИКЖ). Для оценки степени болевого синдрома использовали опросник боли PainDetect.
Результаты. Комплексная терапия ГП с применением НАП продемонстрировала ускоренное заживление ран и уменьшение воспаления. У 24 пациентов, получавших терапию НАП, наблюдалось стойкое улучшение состояния. Пациенты отметили заметное уменьшение боли и улучшение качества жизни. На фоне проведенного исследования отмечались повышение величины среднего потока перфузии крови (показатель M) и снижение показателя среднеквадратичного отклонения (показатель σ), при этом положительная динамика в группе комбинированной терапии была существенно сильнее выражена, чем в группе контроля. Фотодокументация (до/после НАП) подтверждает терапевтические преимущества этого дополнительного метода.
Заключение. Низкотемпературная аргоновая плазма значительно повышает эффективность лечения язв у больных с гангренозной пиодермией, что подтверждается результатами визуального осмотра, положительной динамикой лазерной допплеровской флоуметрии микроциркуляции крови, снижением болезненных ощущений и повышением уровня качества жизни пациентов.
![Критерии диагностики ГП по шкале PARACELSUS (по [13])](/upload/resize_cache/iblock/bc5/wslnjk3ko2syxmhvr0uih2ukrz0dz8bz/195_350_1/Grabovskaya1.jpg)
Гангренозная пиодермия (ГП) – редкое аутовоспалительное заболевание, которое относится к нейтрофильной группе дерматозов [1]. A. Brusting и соавт. в 1930 г. впервые ввели термин гангренозная пиодермия и считали, что это заболевание является формой кожной гангрены, вызванной диссеминированной стрептококковой инфекцией. Несмотря на то что этиология этого заболевания еще до конца не изучена, уже понятно, что ГП не является ни инфекционным заболеванием, ни гангреной, ни пиодермией [2], а представляет собой редкий дерматоз, относящийся к группе аутовоспалительных [2, 3].
Ежегодная заболеваемость ГП составляет 3–6 случаев на 1 млн населения. Встречается в любом возрасте, преимущественно от 40 до 60 лет, чаще у женщин [1, 4]. Актуальность изучения данной темы определяется появлением ГП у трудоспособного населения, отсутствием четких диагностических критериев и недостаточной информированностью врачей о необходимости иммуносупрессивной терпии [2, 5].
ГП, как и другие аутовоспалительные заболевания, генетически детерминирована. Мутации генов, таких как PSTPIP1 и MEFV, были обнаружены у пациентов с синдромальной формой ГП и другими нейтрофильными дерматозами [2, 6].
Воспалительный процесс при ГП запускается преимущественно через механизмы неспецифического врожденного иммунного ответа. На ранней стадии заболевания происходит распознавание патоген-ассоциированных молекулярных структур и повреждение-ассоциированных сигналов, что приводит к активации ряда провоспалительных цитокинов [7]. В последние годы значительное внимание в патогенетических исследованиях ГП уделяется концепции аутовоспаления – термина, впервые предложенного Майклом Ф. Макдермоттом в начале 2000 гг. Под аутовоспалительными состояниями понимают группу наследуемых или спорадических заболеваний, характеризующихся эпизодами локального или системного воспаления, возникающими без идентифицируемых внешних триггеров и в отсутствие классических признаков аутоиммунного ответа. В реализации аутовоспалительного каскада ведущую роль играют клетки фагоцитарного звена врожденного иммунитета, в частности нейтрофилы, макрофаги и дендритные клетки [8].
Несмотря на то что ведущее внимание в исследованиях патофизиологии ГП традиционно уделяется механизмам врожденного иммунного ответа и аутовоспаления, все большее количество источников указывает на значимый вклад адаптивного иммунитета в инициацию и прогрессирование заболевания.
Одним из ключевых свидетельств участия Т-клеточного звена иммунной системы стало гистологическое исследование биоптатов кожи, взятых не из язвенных очагов, а из участков периферической эритемы, окружающей активные поражения. Такой подход позволил изучить ранние стадии воспалительного процесса, предшествующие развитию некроза [9]. Гистологический анализ выявил преобладание лимфоцитарной инфильтрации с выраженной пролиферацией Т-клеток, что было интерпретировано как признак антиген-зависимой клональной экспансии [10]. Хотя природа триггерных антигенов до сих пор не установлена, предполагается, что они могут быть связаны с компонентами дермы или волосяных фолликулов, учитывая характер локализации и морфологии кожных поражений при ГП [11].
В настоящее время считается, что в связи с дисрегуляцией в системе врожденного иммунитета, приводящей к выработке провоспалительных и нейтрофильных хемотаксических факторов, запускается каскад аутовоспалительных реакций с гиперэкспрессией интерлейкинов (ИЛ) 1b, 8, 6, 16, 17, 23 и 36, фактора некроза опухоли альфа (ФНО-α), хемокинов 1, 2, 3 и 16 [1, 2, 11].
ГП имеет тесную связь с аутоиммунными заболеваниями, это чаще всего воспалительные заболевания кишечника (ВЗК), артриты, гемобластозы [8].
Европейской ассоциацией дерматовенерологов в международной классификации 2015 г. предложены клинические формы ГП: язвенная, пустулезная, буллезная, вегетирующая, перистомальная и внекожная. Клинические формы различаются преобладанием соответствующих морфологических элементов и локализацией процесса [9]. В диссертационной работе Д.Т. Кусраевой (2024), в которой впервые наблюдалось 40 больных ГП, предполагается, что буллезная, пустулезная и язвенная формы – это стадии развития заболевания [2].
Язвенная форма ГП – наиболее часто встречающаяся форма заболевания [2, 5]. Gameiro и соавт. описали две различные стадии классической язвенной формы: активную язвенную стадию и стадию заживления язв. Язвенная форма характеризуется быстрорастущей язвой с валикообразно приподнятыми краями багрово-синюшной окраски. Дно язвы обычно покрыто гнойно-геморрагическим отделяемым. На стадии заживления раны проявляется симптом Гулливера: нитевидные выступы эпителия, которые «перекидывают мост» через границу язвы и окружающую нормальную кожу. Данный симптом указывает на то, что воспаление находится под контролем. В итоге происходит образование атрофического рубца, напоминающего «папиросную бумагу» [10].
Патергия – это процесс, при котором после дебридмента появляются новые язвы и усиливается рост прежних, наблюдается у 30% больных ГП [1, 3]. Эта особенность способствует развитию перистомальных и постоперационных поражений ГП [4, 7]. Возраст больных ГП обычно не влияет на клиническую картину, за исключением случаев, связанных с сопутствующими заболеваниями. У пациентов старше 65 лет по сравнению с более молодыми чаще встречалась патергия (36,3 в сравнении с 24,3%) [11].
Поскольку при ГП имеются язвы, которые надо дифференцировать с некротически-язвенными васкулитами, предложена в 2018 г. диагностическая шкала PARACELSUS, которая представляет собой балльную систему, разработанную на основе мета-аналитического обобщения клинических данных (таблица) [12, 13].
Однако последние рекомендации по диагностике язвенной ГП основаны на критериях, установленных в ходе дельфийского консенсуса (The Delphi Consensus of International Experts, 2018), в число дополнительных критериев включают наличие ассоциированного заболевания. Для постановки диагноза ГП необходимо наличие одного основного и хотя бы четырех из восьми приведенных дополнительных критериев (Diagnostic Criteria of Ulcerative Pyoderma Gangrenosum A Delphi Consensus of International Experts, 2018) [14].
Наиболее частыми ассоциированными заболеваниями считают ревматоидный артрит, ВЗК, гематологические злокачественные новообразования и солидные опухоли. ГП ассоциируется с язвенным колитом в 5–12% случаев и с болезнью Крона – в 1–2% случаев, иногда происходит излечение ГП при лечении сопутствующего заболевания кишечника [2, 15].
За последние годы достигнут огромный прогресс в диагностике и терапии ГП, однако лечение этого заболевания все еще представляет большие сложности [16]. Для большинства больных ГП терапия первой линии – это системные глюкокортикостероиды, которые обладают противовоспалительным и иммуносупрессивным эффектами. Преднизолон в дозе от 0,5 до 1,0 мг/кг/сут с успехом сочетают с азатиоприном, циклоспорином А, метотрексатом, микофенолата мофетилом, системным такролимусом, дапсоном, сульфасалазином, внутривенным иммуноглобулином; применяется генно-инженерная биологическая терапия (ингибиторы ФНО-α, ИЛ-1β, ИЛ-1α, ИЛ-17 и др.) [17]. Схемы лечения, как правило, зависят от тяжести клинических проявлений ГП.
Комплексный подход (системная и адекватная местная терапия) позволяет добиться превосходных клинических результатов. Наружно применяются примочки с растворами антисептиков, гелевые и мазевые повязки, по периферии очагов – кортикостероидные мази и пасты.
Для оптимизации лечения ГП после стабилизации процесса и для ускорения рубцевания перспективным методом считается использование низкотемпературной аргоновой плазмы (НАП). Применение НАП при лечении раневых процессов в хирургии позволяет предположить эффективность этого метода и при лечении ГП. Широта физиотерапевтического воздействия обосновывает актуальность внедрения методики НАП при ГП. При назначении НАП следует учитывать фазы и стадии раневого процесса, характер повреждения, бактериальную обсемененность, вирулентность микрофлоры, состояние реактивности организма [18]. Результаты исследования влияния на выживаемость микроорганизмов in vitro низкотемпературной аргоновой плазмы подтвердили ее антимикробное действие. НАП приводит к уничтожению грамположительных и грамотрицательных бактерий, а также дрожжевых грибков при определенных параметрах работы установки [19].
Исследования воздействия НАП на заживление хронических и послеоперационных ран продемонстрировали, что ее применение ускоряет процесс заживления и уменьшает выраженность болевого синдрома.
Преимуществами данного метода являются антимикробное воздействие на раневую поверхность и подлежащие ткани, а также противовоспалительный, обезболивающий, противоотечный эффекты и ускорение всех фаз заживления раны. При этом ткани организма не повреждаются [20]. Эти особенности стали основанием для проведения проспективного рандомизированного исследования применения низкотемпературной аргоновой плазмы в комплексном лечении ГП.
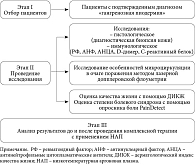
В исследовании приняли участие 50 пациентов женского и мужского пола (26 женщин и 24 мужчины) с впервые или ранее установленным диагнозом гангренозная пиодермия в возрасте от 18 до 92 лет. 24 пациентам с ГП была проведена комплексная терапия с применением иммуносупрессивных препаратов, местной терапии с дополнением курса НАП, проведенным на установке «Плазморан»; курс лечения включал от 8 до 14 процедур ежедневно и/или через день. Группу контроля составили 26 пациентов, которые получали комплексную терапию без применения НАП (рис. 1).
Материал и методы
Все пациенты, включенные в исследование, после подписания информированного согласия прошли обследование, которое включало:
- сбор медицинского анамнеза (длительность основного заболевания, перенесенные и сопутствующие заболевания, предшествующая терапия, динамика кожного процесса);
- выявление основного ассоциированного заболевания (ревматоидный артрит, неспецифический язвенный колит, болезнь Крона, лимфопролиферативные заболевания, моноклональные гаммапатии, злокачественные новообразования внутренних органов);
- оценку клинической картины;
- стандартную программу лабораторного обследования в стационаре: клинический и биохимический анализы крови, коагулограмма, общий анализ мочи;
- определение основных показателей жизнедеятельности (измерение частоты сердечных сокращений, частоты дыхательных движений, артериального давления, температуры тела);
- диагностику системных поражений внутренних органов;
- бактериологический анализ отделяемого язв с определением чувствительности к антибиотикам.
Дополнительно оценивали качество жизни пациентов с помощью дерматологического индекса качества жизни (ДИКЖ), а по опроснику PainDetect учитывали все возможные параметры боли, что позволило отследить картину болевого синдрома в динамике.
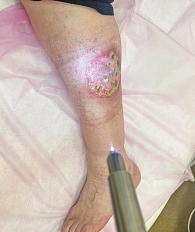
При поступлении в стационар кожный процесс у всех пациентов носил островоспалительный характер; был локализован в подавляющем большинстве случаев в области нижних конечностей; был представлен язвами различных размеров с четкими контурами, имеющими округлые и полициклические очертания, с валикообразно приподнятыми краями багрово-синюшной окраски; дно язв покрыто геморрагически-гнойным экссудатом, вокруг язв – зона фиолетово-розовой эритемы, на месте прежних зарубцевавшихся язв – атрофические рубцы и неравномерная пигментация. Субъективно: выраженная болезненность язвенных дефектов.
По результатам лабораторных исследований пациентов в клиническом анализе крови выявлены: нейтрофильный лейкоцитоз, анемия, повышение скорости оседания эритроцитов; по результатам гистологического исследования, выявлена обильная нейтрофильная инфильтрация с явлениями лейкоцитокластического васкулита.
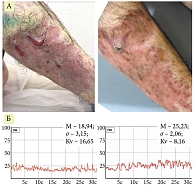
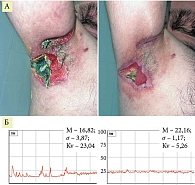
Всем пациентам проведено лечение: системные кортикостероиды (преднизолон, начальная доза 0,5–1 мг/кг) в сочетании с корригирующей терапией, при упорном развитии болезни – азатиоприн по 100 мг в сутки; по показаниям – нестероидные противовоспалительные средства, антибиотики, сосудистые, антигистаминные препараты. Наружно: антисептическая обработка раневой поверхности, эпителизирующие мази, коллагеновые губки, сетки, гидрогелевые повязки. 24 пациентам дополнительно проводили процедуры с НАП. У этих пациентов (группа комплексной терапии + НАП) после проведения 8–14 процедур на установке «Плазморан» наблюдалась положительная динамика в виде уменьшения гиперемии вокруг очагов, очищения язв от гнойно-некротических наслоений и частичного рубцевания язвенных дефектов; субъективные симптомы были купированы; появление новых высыпаний не отмечено (рис. 2–6).
При оценке болевого синдрома у пациентов с гангренозной пиодермией до лечения среднее значение по опроснику PainDetect составляло 25,1 балла, что по оценочной шкале соответствует высокой вероятности невропатического компонента боли. После проведенного лечения у 26 пациентов из группы контроля среднее значение составило 22,35 балла. В то время как у пациентов, которым проводили комплексное лечение с применением НАП, отмечалась редукция значений данного индекса в 1,4 раза: среднее значение данного показателя у пациентов этой группы составило 15,8 балла, что свидетельствовало об уменьшении болевого синдрома.
До лечения среднее значение дерматологического индекса качества жизни (ДИКЖ) у всех участников исследования составляло 18,28 балла, что отражало сильное негативное влияние заболевания на качество жизни больных. После лечения данный индекс у пациентов из группы контроля составил 15,47, а у пациентов, получавших комплексную терапию с применением НАП, снизился в 1,4 раза и составил 10,92 балла. Назначенные процедуры пациенты переносили хорошо, дискомфорта и нежелательных явлений не отмечали.
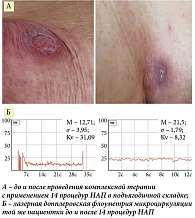
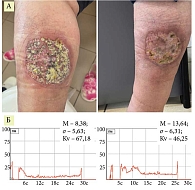
Результаты проведения лазерной флоуметрии позволяют подтвердить положительное влияние НАП. Пациенты первой группы, получавшие НАП, демонстрируют значительно более выраженное увеличение перфузии, что может свидетельствовать о более эффективном лечении, лучшей реактивности сосудов и подтверждается выраженным снижением показателя σ (среднеквадратичное отклонение), чем в группе контроля. Kv – интегральный коэффициент вариации перфузии, отражающий вазомоторную активность микроциркуляторного русла, рассчитывается Kv = σ/М × 100%. Лечение привело к статистически значимому снижению показателя Kv как в группе комплексной терапии с применением НАП, так и в группе контроля, что свидетельствует об эффективности. При этом пациенты группы комплексной терапии с применением НАП продемонстрировали более выраженное снижение показателя по сравнению с группой контроля, что может указывать на больший ответ на терапию в этой группе.
Наличие выбросов до лечения (особенно в группе комплексной терапии с применением НАП ) свидетельствует о высокой вариабельности исходных значений, однако после лечения разброс значений снизился, что указывает на стабилизацию показателя под влиянием терапии.
Таким образом, применение НАП (установка «Плазморан») в комплексной терапии способствует более выраженной стабилизации гемомикроциркуляции, что подтверждается объективными параметрами лазерной допплерографии.
Выводы
- Включение в комплексную терапию процедур воздействия низкотемпературной аргоновой плазмой значительно повышает эффективность лечения язв у больных с ГП.
- После проведения семи процедур у пациентов наблюдался положительный клинический ответ в виде уменьшения размера язв и купирования воспалительных явлений.
- Эффективность комбинированной терапии с применением НАП подтверждается результатами лазерной допплеровской флоуметрии.
- Местная терапия ГП с дополнением курса НАП на установке «Плазморан» позволяет улучшить качество жизни, что подтверждается индексом ДИКЖ.
- Процедуры НАП абсолютно безболезненны, более того, в процессе обработки язв уменьшаются болезненные ощущения, что подтверждено с помощью использования опросника PainDetect.
- Высокая мобильность оборудования позволяет проводить процедуры непосредственно в палате, особенно для тяжелых пациентов.
- С учетом рецидивирующего течения ГП, зачастую торпидного к проводимой терапии, целесообразно назначение повторных курсов НАП на установке «Плазморан» и динамическое наблюдение за пациентами.
Авторы заявляют об отсутствии конфликта интересов.
O.Yu. Olisova, PhD, Prof., Corresponding member of the RAS, O.V. Grabovskaya, PhD, Prof., L.N. Kayumova, PhD, A.E. Bobkova
I.M. Sechenov First Moscow State Medical University (Sechenov University)
Contact person: Anna E. Bobkova, anya_bobkova98@mail.ru
Pyoderma gangrenosum (PG) is a rare neutrophilic dermatosis characterized by a complex pathophysiology involving dysregulation of the innate immune system, neutrophil dysfunction, and excessive expression of pro-inflammatory cytokines (IL-1β, IL-17, TNF-α). PG is an extremely rare condition, most commonly diagnosed in individuals aged 40–60 years, and typically begins with the formation of pustules that rapidly evolve into painful ulcers. Patients with PG require a comprehensive, multidisciplinary approach and long-term monitoring. Although current therapeutic strategies developed by dermatologists – including systemic corticosteroids and immunosuppressants – are effective, they still require adjunctive interventions to accelerate ulcer dehydratation and scar formation. There is a clear need to develop novel therapeutic approaches, applied after disease stabilization, to optimize wound healing and scar formation in PG. As an adjunctive therapy, the efficacy of low-temperature argon plasma (LAP) has been investigated.
Objective. To evaluate the efficacy of low-temperature argon plasma (LAP) in the comprehensive treatment of pyoderma gangrenosum (PG).
Material and methods. The study included 50 patients (26 women and 24 men) aged 18 to 92 years, with either newly diagnosed or previously confirmed pyoderma gangrenosum. Patients were randomly divided into two groups: 24 and 26 individuals, respectively. The first group received comprehensive therapy incorporating low-temperature argon plasma using the “Plazmoran” device (a treatment course consisting of 7 to 14 sessions, administered daily or every other day). Patients in the second group received standard treatment without the use of NAP. All patients underwent assessment of microcirculatory features in the ulcer margin zone. The Dermatology Life Quality Index (DLQI) was used to evaluate the impact of the disease on quality of life, and the PainDetect questionnaire was employed to assess the severity of pain.
Results. Comprehensive PG therapy combined with LAP demonstrated accelerated wound healing and reduced inflammation. Among the 24 patients treated with LAP, sustained clinical improvement was observed. Patients reported significant reduction in pain and marked improvement in quality of life. During the study, an increase in the mean perfusion flow (M parameter) and a decrease in the standard deviation (σ parameter) were noted; these positive trends were significantly more pronounced in the combined therapy group compared to the control group. Photodocumentation (before/after LAP) confirmed the therapeutic advantages of this adjunctive modality.
Conclusion. Low-temperature argon plasma significantly enhances the effectiveness of ulcer treatment in patients with pyoderma gangrenosum, as evidenced by clinical examination findings, positive changes in laser Doppler flowmetry parameters of microcirculation, reduced pain levels, and improved patient quality of life.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.