Лечение ограниченной склеродермии метотрексатом
- Аннотация
- Статья
- Ссылки
- English
В последнее время ограниченная склеродермия все чаще встречается в клинической практике. Возрастание заболеваемости, особенно среди социально активных групп населения, влечет за собой необходимость поиска эффективных методов лечения.
До недавнего времени препаратами первой линии считались препараты пенициллинового ряда. Однако применение данных лекарственных средств не всегда приводило к желаемым результатам. У некоторых больных на фоне такой терапии продолжали появляться высыпания, сохранялся «венчик роста» по периферии старых пятен. В связи с этим алгоритм лечения был пересмотрен. В настоящее время, согласно стандартам оказания медицинской помощи больным с ограниченной склеродермией, утвержденным приказом Министерства здравоохранения и социального развития Российской Федерации от 28.12.2012 № 1591н, в качестве первой линии рекомендованы глюкокортикостероиды. Однако в зарубежной литературе большое внимание уделяется применению при ограниченной склеродермии метотрексата или комбинации метотрексата с глюкокортикостероидами.
В последнее время ограниченная склеродермия все чаще встречается в клинической практике. Возрастание заболеваемости, особенно среди социально активных групп населения, влечет за собой необходимость поиска эффективных методов лечения.
До недавнего времени препаратами первой линии считались препараты пенициллинового ряда. Однако применение данных лекарственных средств не всегда приводило к желаемым результатам. У некоторых больных на фоне такой терапии продолжали появляться высыпания, сохранялся «венчик роста» по периферии старых пятен. В связи с этим алгоритм лечения был пересмотрен. В настоящее время, согласно стандартам оказания медицинской помощи больным с ограниченной склеродермией, утвержденным приказом Министерства здравоохранения и социального развития Российской Федерации от 28.12.2012 № 1591н, в качестве первой линии рекомендованы глюкокортикостероиды. Однако в зарубежной литературе большое внимание уделяется применению при ограниченной склеродермии метотрексата или комбинации метотрексата с глюкокортикостероидами.
Введение
Ограниченная склеродермия – хроническое заболевание соединительной ткани, которое характеризуется нарушением микроциркуляции и синтеза коллагена, воспалением, аутоиммунной и тканевой реконструкцией. Патологией чаще страдают женщины в возрасте от 20 до 50 лет.
Этиология ограниченной склеродермии остается не до конца понятной. На ее развитие могут влиять генетические факторы, сопутствующие заболевания. В настоящее время большое значение отводится нарушению клеточного и гуморального иммунитета, а также выработке аутоантител против компонентов клетки. Именно поэтому для лечения данного дерматоза применяются иммуносупрессанты.
Согласно стандартам оказания медицинской помощи больным с ограниченной склеродермией, утвержденным приказом Министерства здравоохранения и социального развития Российской Федерации от 28.12.2012 № 1591н, в качестве препаратов первой линии показаны глюкокортикостероиды. Несмотря на то что данный метод лечения позволяет достичь хорошего результата, назвать его идеальным невозможно. Поэтому поиск новых терапевтических опций продолжается. Метотрексат может стать достойным претендентом на эту роль. Необходимо также отметить, что в педиатрической практике при ограниченной склеродермии метотрексат успешно применяется достаточно широко и давно.
Метотрексат
Метотрексат является цитостатиком, который блокирует синтез ДНК, угнетает продукцию провоспалительных и усиливает продукцию противовоспалительных цитокинов, что и обусловливает его противовоспалительный и иммуномодулирующий эффект. Если иммунная теория патогенеза ограниченной склеродермии является главной, то назначение препарата оправданно.
Применение при разных видах ограниченной склеродермии
M. Řiháček и соавт. [1] описали фармакокинетические и фармакодинамические характеристики метаболитов метотрексата, который является антионкологическим препаратом и применяется для лечения тяжелых процессов, в том числе детского острого лимфобластного лейкоза и хориокарциномы.
Низкие дозы метотрексата используют при ревматоидном артрите, псориазе, системном склерозе и других аутоиммунных заболеваниях.
Побочные эффекты данного препарата хорошо изучены и описаны. Однако их появление может быть непредсказуемым из-за отсутствия специфических биомаркеров токсичности.
Уровень метотрексата в плазме должен регулярно контролироваться при помощи проведения лабораторных анализов.
S. Kafaja и соавт. [2] предположили, что уплотнение кожи является одним из ранних проявлений системного склероза и оказывает большое влияние на качество жизни больных. В связи с этим они рекомендовали применять метотрексат на начальном этапе диффузного кожного заболевания.
J.S. Mertens и соавт. [3] исследовали эффективность и безопасность метотрексата у 107 взрослых, страдавших ограниченной склеродермией. Через один и два года 26 и 63% больных соответственно прекратили терапию в связи с ремиссией процесса. Из-за неэффективности в течение первого года препарат был отменен только в 24% случаев. Пациенты с поверхностной ограниченной склеродермией в отличие от лиц с другими формами ограниченной склеродермии труднее соглашались на такое лечение. Чтобы свести к минимуму неэффективность метотрексата при ограниченной склеродермии, наиболее важными мерами признаны назначение фолиевой кислоты и уменьшение времени отсрочки с лечением.
S. Kassira и соавт. [4] описали опыт применения метотрексата при келоидной склеродермии. У 41-летней женщины были отмечены темно-коричневые плотные экзофитные узлы на груди наряду с гиперпигментированными бляшками, рассеянными по животу, и склеродактилия. Результаты клинических, лабораторных и гистологических исследований соответствовали диагнозу «келоидная склеродермия». Больной назначили метотрексат. На фоне терапии снизилась твердость очагов и отсутствовали новые высыпания. Был сделан вывод, что метотрексат можно рассматривать в качестве начального варианта лечения у пациентов с прогрессирующей келоидной склеродермией.
Метотрексат применяли при ограниченной склеродермии по типу «удар саблей» (en coup de sabre). D. Van der Veken и соавт. [5] описали случай с 19-летней пациенткой, которая обратилась по поводу бледного, атрофичного, линейного участка с правой стороны лица, который простирался от носа до верхней губы. Клиническая картина позволила поставить диагноз «ограниченная склеродермия по типу удара саблей». Для оценки патологии использовали компьютерную томографию, количественную полимеразную цепную реакцию и результаты гистологии. Было проведено лечение метотрексатом. Через 12 месяцев рецессии не наблюдалось.
S.B. Couto и соавт. [6] использовали метотрексат при лечении пациентки с почечным синдромом в качестве первого проявления ювенильной системной склеродермии с фокально-сегментарным гломерулосклерозом. В 12 лет у больной развился стероидочувствительный почечный синдром. В 14 лет появились отеки орбитальных областей и нижних конечностей, склеродактилия. Пациентка получала 25-гидроксивитамин D (800 МЕ/сут), метотрексат (0,5 мг/кг/нед) и амлодипин (0,15 мг/кг). Преднизолон в дозе 60 мг/м2/сут вводили в течение четырех недель, затем через день по 40 мг/м2 в течение двух месяцев со снижением дозы в течение четырех месяцев. По окончании терапии пациентка продолжила получать метотрексат 15 мг/нед. Отеков и протеинурии не зафиксировано.
M. Spalek и соавт. [7] сделали обзор литературы с 1989 г. в отношении 66 случаев склеродермии, вызванной радиацией. Необходимо отметить, что склеродермия, вызванная радиацией, – редкое осложнение после радиотерапии. Она часто неправильно диагностируется – как другие дерматологические заболевания или злокачественные новообразования, поскольку имеет сходные клинические характеристики. Методы лечения данной патологии неизвестны. Обычно применяются топические и системные глюкокортикостероиды, ингибиторы кальциневрина, системные супрессанты, такие как метотрексат, такролимус, гепарин, гиалуронидаза, системные антибиотики, Имиквимод, микофенолата мофетил, фототерапия (UVA, UVA1, UVB, PUVA), фотофорез.
A.H. Hanson и соавт. [8] использовали метотрексат при линейной ограниченной склеродермии. Они описали случай с 17-летней пациенткой, которая обратилась для оценки лечения линейного очага на левом боку. Данные биопсии соответствовали диагнозу «склеродермия». Терапия началась с внутриочагового введения стероидов и нанесения мази кальципотриола, затем применялся метотрексат и эксимерный лазер. За семь месяцев зона поражения значительно уменьшилась в размерах. Кроме того, снизился симптоматический дискомфорт. Исследователи отметили, что метотрексат может быть полезен при глубоких и острых формах склеродермии. Он приводит к снижению уровня интерлейкинов 2 и 6, а также мастоцитов.
F. Porta и соавт. [9] обследовали десять больных (семь мальчиков и три девочки) с юношеской ограниченной склеродермией. Возраст участников – 101,7 ± 66,2 месяца. Состояние кожи оценивалось в начале и через шесть месяцев после лечения. Утолщение кожи измерялось при помощи высокочувствительного ультразвукового исследования (18 МГц). Помимо этого состояние кожи определялось по модифицированной шкале Роднана (Modified Rodnan Skin Score – mRSS). Исходно шесть больных из десяти получили три курса глюкокортикостероидов (Солу-Медрол 30 мг/кг/сут в течение трех дней, затем 1 мг/кг), метотрексат подкожно (15 мг/нед). Через шесть месяцев одному пациенту из шести был добавлен микофенолата мофетил (25 мг/кг/сут) в связи с неэффективностью метотрексата, четверо больных из десяти не получали дополнительной терапии. Результаты ультразвукового исследования свидетельствовали об утолщении дермы и истончении гиподермы в очагах поражения у больных по сравнению со здоровыми лицами (p < 0,05). После лечения у семи пациентов зафиксировано клиническое улучшение – снижение значений mRSS. У них же отмечалось снижение утолщения дермы, свидетельствующее о корреляции с клиническими данными. У троих больных, не получавших препараты, изменения кожи отсутствовали как по результатам ультразвукового исследования, так и по результатам оценки клинической картины.
S. Cappelli и соавт. [10] предположили, что метотрексат можно использовать как препарат первой линии при поражении кожи при системном склерозе в отсутствие интерстициальной болезни легких.
M. Piram и соавт. [11] оценивали эффективность метотрексата у 52 детей с линейной склеродермией, пролеченных с 1990 по 2010 г. Для оценки долгосрочных результатов в 2011 г. был проведен телефонный опрос этих больных. 31% пациентов отметили активацию заболевания через десять лет. Все, кроме одного пациента, указали на эстетические последствия. У 38% наблюдались функциональные ограничения. Низкая активность метотрексата и системных глюкокортикостероидов была очевидной в краткосрочной перспективе. M. Piram и соавт. пришли к выводу, что комбинация метотрексата и глюкокортикостероидов эффективна на раннем этапе болезни, но не предупреждает активации процесса или рецидива в долгосрочной перспективе.
T.M. Frech и соавт. [12], проанализировав данные, относящиеся к наиболее часто используемым методам лечения раннего диффузного системного склероза, включая метотрексат, микофенолата мофетил, циклофосфамид, азатиоприн и внутривенный иммуноглобулин, пришли к выводу о необходимости эффективного лечения на начальной стадии заболевания, а также его более детального изучения.
F. Zulian и соавт. [13] подтвердили важную роль метотрексата в лечении ювенильной ограниченной склеродермии. Они провели двойное слепое мультицентровое рандомизированное исследование и долгосрочные наблюдения. Ученые указали на важность отражения результатов терапии ювенильной ограниченной склеродермии и введении оценки тяжести данной патологии, а также на роль метотрексата при лечении пациентов с ювенильной ограниченной склеродермией.
S.B. Koch и соавт. [14] изучили долгосрочную эффективность метотрексата у больных линейной склеродермией. Они обследовали детей и лиц молодого возраста, страдавших данной патологией, и оценили результаты лечения препаратом. 17 пациентов, соответствовавших критериям включения, наблюдались в среднем 6,6 года. Семи (41%) потребовался второй курс метотрексата после ремиссии, средний срок наблюдения – 21 месяц. Одному (6%) пациенту был назначен третий курс после 6,9 года ремиссии. Таким образом, исследователи установили, что метотрексат является эффективным препаратом для достижения ремиссии у детей и лиц молодого возраста с линейной склеродермией. Однако многим пациентам требуется более одного курса препарата.
Еще один случай лечения линейной склеродермии метотрексатом представили M.Z. Handler и соавт. [15]. 15-летний пациент в течение десяти лет страдал линейной склеродермией. Патологию лечили метотрексатом, топическими и пероральными глюкокортикостероидами, топическим препаратом витамина D, однако очаги сохранялись и распространялись вниз по всей медиальной части левой ноги. У больного отмечались атрофия и задержка роста левой ноги, что привело к укорочению кости нижней конечности на 3 см и боли в суставах.
Y. Inamo и соавт. [16] описали случай прогрессирующей юношеской ограниченной склеродермии, которую лечили комбинацией иматиниба, метотрексата и глюкокортикостероидов. На фоне терапии удалось остановить утолщение кожи на пальцах рук и деформацию суставов на ранних стадиях заболевания.
F. Zulian и соавт. [17] также изучали терапевтический эффект метотрексата у детей с ювенильной ограниченной склеродермией при длительном применении. Было проведено двойное слепое рандомизированное плацебоконтролируемое исследование. Его участники принимали метотрексат перорально в дозе 15 мг/нед и преднизолон в дозе 1 мг/кг/сут (максимум 50 мг) в течение первых трех месяцев. Повреждения оценивались клинически, при помощи инфракрасной термографии и компьютеризированной шкалы. Ответ на лечение определяли следующим образом: 1 – отсутствие новых очагов, 2 – размер очагов уменьшился, 3 – снижение в очагах температуры не менее чем на 10% по сравнению с исходным уровнем. Клиническая ремиссия устанавливалась, если ответ на лечение сохранялся не менее шести месяцев, полная ремиссия, если ответ сохранялся в отсутствие лечения не менее шести месяцев. Из 65 получавших метотрексат 48 (73,8%) ответили на лечение, у десяти (15,4%) отмечен рецидив через 24 месяца от начала приема препарата. Семь (10,8%) больных были потеряны для наблюдения. У 35 (72,9%) пациентов ремиссия сохранялась в среднем 25 месяцев. У 13 (27,1%) зафиксирована клиническая ремиссия на фоне приема метотрексата. Побочные эффекты отмечались у 28 (48,3%) больных, как правило, они носили легкий характер и не требовали прекращения лечения. Был сделан вывод о том, что долгосрочный прием метотрексата полезен и хорошо переносится больными ювенильной ограниченной склеродермией.
A. Kreuter [18] в практическом обзоре представил данные об эпидемиологии, патогенезе, клинических подтипах и классификации, дифференциальном диагнозе, клинических показателях, а также о текущей стратегии лечения ограниченной склеродермии. Ученый отметил положительный эффект ультрафиолетовой фототерапии в диапазоне А-1 (УФ-А-1) и метотрексата как в виде монотерапии, так и в сочетании с системными глюкокортикостероидами при более серьезной форме заболевания, когда поражены внекожные структуры.
L. Weibel и соавт. [19] подчеркнули, что комбинация системных глюкокортикостероидов и метотрексата является общепринятой в качестве первой линии при прогрессирующей стадии, особенно линейной склеродермии, в то время как фототерапия (УФ-А-1 и узкополосная УФ-B) подходит для подростков с поверхностными подтипами ограниченной склеродермии.
K.S. Torok и соавт. [20] оценили эффективность единого протокола лечения, состоящего из высоких доз метотрексата и системных глюкокортикостероидов, в педиатрии. Обследовано 36 детей с ограниченной склеродермией, из них 25 женского пола. Средний возраст начала заболевания – 7,86 года. Средняя продолжительность болезни от дебюта до начала лечения – 19,2 месяца. Пациенты с активной формой заболевания (эритематозные очаги и/или наличие новых очагов или расширение уже имеющихся поражений) получали преднизолон 2 мг/кг/сут (максимально 60 мг/сут) и подкожно метотрексат 1 мг/кг/нед (не более 25 мг/нед). Дозу преднизолона снижали и сохраняли на уровне 0,25 мг/кг/сут в течение 12 месяцев. Метотрексат подкожно применяли 24 месяца, затем перорально в течение 36 месяцев. Медиана длительности наблюдения – 36,4 месяца.
Во время терапии существенные побочные реакции или обострение патологии не наблюдались. K.S. Torok и соавт. сделали вывод, что данный протокол лечения эффективен и хорошо переносится. На клинический результат влияют доза и способ применения иммуносупрессивной терапии. Данный режим лечения следует рассматривать как один из возможных при ограниченной склеродермии.
Пациенты, страдающие ограниченной склеродермией, практически не жалуются на неприятные субъективные ощущения. Среди наиболее частых следует выделить стянутость кожи и незначительный зуд, крайне редко пациенты жалуются на боль. H. Jeon и соавт. [21] описали случай с пациенткой с ограниченной склеродермией, у которой отмечалась изнуряющая боль в области бляшек. Больная не реагировала на местную терапию, поэтому потребовалось системное применение препарата. Для облегчения боли проводилась титрация дозы метотрексата. Несмотря на нехарактерность боли при ограниченной склеродермии, она может быть изнурительной, поэтому в зависимости от ее выраженности должно быть назначено соответствующее лечение.
A. Khaled и соавт. [22] описали развитие глубокой формы склеродермии после вакцинации ребенка. У двухлетней здоровой девочки наблюдалось уплотнение на передней поверхности левого бедра в течение девяти месяцев. Очаг развился через три месяца после введения третьей дозы прививки от дифтерии, кори и столбняка. Обследование показало уплотнение размером 7 × 7 см2 с симптомом «апельсиновая корка» при пощипывании кожи. Гистологическое исследование подтвердило диагноз «ограниченная склеродермия». Применение системных стероидов в дозе 1 мг/кг/сут привело к стабилизации процесса. Через четыре месяца лечения добавлен метотрексат перорально в дозе 10 мг/нед в течение двух месяцев. Использование метотрексата в виде монотерапии было продолжено в течение десяти месяцев, что привело к значительному регрессу уплотнения без рецидивов.
За последнее время в клинике им. В.Г. Короленко комплексное лечение с метотрексатом получил 41 пациент. У 15 женщин и пяти мужчин диагностирована распространенная форма ограниченной склеродермии. У 12 пациенток в анамнезе – оперативное вмешательство по поводу онкопроцесса разной локализации. Девять мужчин страдали аденомой предстательной железы. У таких пациентов существует ограничение для применения глюкокортикостероидов и физиотерапии, в связи с чем был назначен метотрексат. Метотрексат вводили внутримышечно в дозе 10–15 мг в зависимости от веса пациента. Курс терапии предполагал не менее десяти инъекций. Его можно было повторить через четыре-пять месяцев. Уже после первого курса наблюдалось уменьшение активности кожного процесса, площади очагов склеротических изменений и отсутствие новых высыпаний.
Клинический случай
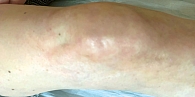
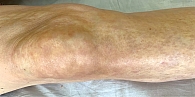
Под нашим наблюдением находилась пациентка Г., 67 лет. Больна предположительно в течение трех лет. Именно тогда появились высыпания на коже передней поверхности правой голени и ограничение движения в голеностопном и коленном суставах. За это время получила пять курсов комбинированной терапии (пенициллин, сосудистые препараты, топические глюкокортикостероиды).
С марта по апрель 2018 г. принимала преднизолон в дозе 40 мг/сут с постепенным снижением дозы и ультрафонофорез с гидрокортизоном на очаги поражения. Однако кожный процесс не регрессировал, появились новые высыпания.
Пациентке были назначены внутримышечные инъекции метотрексата 20 мг один раз в неделю под контролем лабораторных показателей. В дальнейшем доза метотрексата снижалась до 7,5 мг.
Общая длительность терапии – 18 недель.
На фоне лечения отмечался регресс высыпаний и практически полное восстановление подвижности правого коленного сустава (рис. 1 и 2).
Заключение
Метотрексат показан в комплексной терапии распространенных форм ограниченной склеродермии. В тех случаях, когда применение глюкокортикостероидов или физиотерапии невозможно, он остается единственным эффективным методом лечения.
Z.A. Nevozinskaya, PhD, Ye.Ye. Radionova, PhD, Yu.A. Koshelev, Ye.V. Denisova, PhD, I.M. Korsunskaya, MD, PhD, Prof.
Moscow Scientific-Practical Center of Dermatovenerology and Cosmetology
Center for Physical and Chemical Pharmacology Theoretical Problems
Contact person: Irina M. Korsunskaya, marykor@bk.ru
Limited scleroderma is a chronic connective tissue disease with lesions of the skin and underlying tissues, characterizing by the appearance of foci of sclerosis on the background of inflammatory phenomena (erythema, edema) and subsequent atrophy, as well as hypo- and hyperpigmentation of the skin.
Recently, limited scleroderma is increasingly common in clinical practice. The increase in the incidence of disease, especially among socially active groups of the population, entails the need to find effective methods of treatment.
Until recently, first-line drugs were considered to be penicillin-type drugs. However, the use of these drugs did not always lead to the desired results. In some patients, on the background of such therapy, rashes continued to appear, and a ‘corolla of growth’ remained along the periphery of old spots. In this regard, the treatment algorithm has been revised. Currently, according to the standards of medical care for patients with limited scleroderma, approved by the order of the Ministry of Health and Social Development of the Russian Federation dated 28.12.2012 No. 1591н, glucocorticosteroids are recommended as the first line. However, in the foreign literature, much attention is paid to the use of methotrexate or the combination of methotrexate with glucocorticosteroids for limited scleroderma.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.