Место ингибиторов ДПП-4 в современной диабетологической практике
- Аннотация
- Статья
- Ссылки
ГПП-1 и ингибиторов ДПП-4 по сравнению с традиционно используемыми сахароснижающими препаратами (метформином, препаратами сульфонилмочевины, тиазолидиндионами). На примере вилдаглиптина показано, что ингибиторы ДПП-4
могут назначаться больным СД 2 типа в виде монотерапии при дебюте заболевания, а также в комбинации с основными сахароснижающими препаратами других групп и с препаратами инсулина с целью интенсификации лечения.
ГПП-1 и ингибиторов ДПП-4 по сравнению с традиционно используемыми сахароснижающими препаратами (метформином, препаратами сульфонилмочевины, тиазолидиндионами). На примере вилдаглиптина показано, что ингибиторы ДПП-4
могут назначаться больным СД 2 типа в виде монотерапии при дебюте заболевания, а также в комбинации с основными сахароснижающими препаратами других групп и с препаратами инсулина с целью интенсификации лечения.




Поиск новых, эффективных и безопасных препаратов для лечения сахарного диабета (СД) 2 типа остается наиболее актуальной задачей современной диабетологии. Согласно данным национальных систем здравоохранения, в большинстве стран мира доля пациентов, достигающих устойчивой компенсации сахарного диабета, не превышает 50%. Этот факт во многом объясняется такими субъективными причинами, как нерациональный выбор препаратов и схем их назначения врачом, а также недостаточная комплаентность пациентов. Вместе с тем важнейшими объективными факторами, снижающими эффективность терапии СД 2 типа, являются недостатки и ограничения традиционных сахароснижающих препаратов, во многом обусловленные тем, что ни один из них не воздействует на все патогенетические дефекты, характерные для пациентов c СД 2 типа: инсулинорезистентность, острую и хроническую дисфункцию бета-клеток, нарушение функции альфа-клеток поджелудочной железы (рис. 1).
До недавнего времени наиболее близким к критериям «идеального» сахароснижающего средства был метформин, обладающий такими преимуществами, как хорошая доказательная база, низкий риск гипогликемий на фоне выраженного сахароснижающего эффекта, нейтральность по отношению к массе тела, наличие плейотропных эффектов, доступность. В связи с этим в международные алгоритмы ADA/EASD 2006 и 2009 гг. метформин был включен в качестве единственного препарата первой линии, назначение которого рекомендовалось одновременно с изменением образа жизни в качестве стартовой терапии СД 2 типа [5]. Однако очевидно, что данный подход имел определенные ограничения. Во-первых, как показали результаты масштабных проспективных исследований UKPDS и ADOPT [1, 2], лечение метформином не позволяло у значительной части пациентов добиться целевых показателей углеводного обмена и долгосрочно их поддерживать, а также предотвратить прогрессирующее снижение функции бета-клеток у большинства пациентов.
Кроме того, общеизвестны и другие недостатки и ограничения терапии метформином, к которым относятся достаточно высокая частота нежелательных явлений со стороны желудочно-кишечного тракта, ограниченность использования этого препарата при гипоксических состояниях, анемии, нарушениях функции печени и почек, плохая совместимость с алкоголем [5].
Новые перспективы в клинической диабетологии появились с открытием роли инкретиновых гормонов в регуляции углеводного обмена. Основным «игроком» здесь выступает глюкагоноподобный полипептид 1 типа (ГПП-1). Оказалось, что инкретины обеспечивают более 60% прироста секреции инсулина после приема пищи [3]. Уникальным свойством ГПП-1 оказалась его способность влиять на углеводный обмен через глюкозозависимую стимуляцию секреции инсулина, а также глюкозозависимое подавление продукции глюкагона панкреатическими альфа-клетками, что приводило к снижению центральной и периферической инсулинорезистентности. Работами ряда авторов было показано, что секреция ГПП-1 снижена у больных СД 2 типа, а инфузия ГПП-1 способна улучшить показатели углеводного обмена, восстанавливая физиологическую секрецию инсулина даже при выраженной декомпенсации сахарного диабета. Кроме того, in vitro и in vivo на животных было показано, что ГПП-1 обладает способностью усиливать пролиферацию и снижать апоптоз бета-клеток, то есть потенциально обладает способностью влиять на естественное течение СД 2 типа [3].
Основным ограничением применения нативного ГПП-1 в клинической практике оказался его короткий период полужизни, составляющий всего 2–3 минуты, что определяло необходимость постоянной инфузии ГПП-1. Исследования по созданию приемлемых для клинического применения фармакологических препаратов на основе инкретинов проводились в двух направлениях: создание аналогов молекулы ГПП-1 человека или поиск молекул, сходных с ГПП-1 по биологическим эффектам, но с большей продолжительностью действия, а также разработка препаратов, пролонгирующих действие эндогенных инкретинов с помощью подавления активности фермента, разрушающего в крови ГПП-1, – дипептидилпептидазы 4 типа.
С 2005 г. по настоящее время в Российской Федерации, как и во многих странах мира, зарегистрированы 5 препаратов, обладающих инкретиновой активностью, которые относятся к двум группам сахароснижающих средств: агонистам рецепторов ГПП-1 (инкретинмиметики/аналоги ГПП-1) и ингибиторам дипептидилпептидазы 4 типа (табл. 1).
Уникальные свойства и большой терапевтический потенциал инкретиновых препаратов позволили им за беспрецедентно короткий срок завоевать прочное место в современных алгоритмах лечения СД 2 типа. Действительно, всего через 4 года после начала широкого клинического применения первого инкретинмиметика – эксенатида – и через 3 года после одобрения FDA первого ингибитора ДПП-4 – ситаглиптина – препараты указанных групп стали рекомендоваться экспертами в области диабетологии для стартовой терапии СД 2 типа или с целью интенсификации лечения этого заболевания.
Так, если в консенсусном алгоритме лечения СД 2 типа ADA/EASD (2009) агонисты ГПП-1 рекомендованы как препараты 2-го ряда при неэффективности стартовой фармакотерапии метформином у больных, для которых особенно нежелательны гипогликемические состояния [5], то в конце того же 2009 г. экспертами Ассоциации американских клинических эндокринологов (AACE) и Американского колледжа эндокринологии представлен новый консенсус по терапии СД 2 типа [6], в котором ингибиторы ДПП-4 наряду с метформином, тиазолидиндионами и ингибиторами альфа-глюкозидаз фактически были отнесены к препаратам первого ряда и рекомендованы в качестве монотерапии при инициации лечения пациентов с умеренными нарушениями углеводного обмена (уровень HbA1c 6,5–7,5%). Кроме того, ингибиторы ДПП-4 рекомендовались в качестве препаратов для интенсификации сахароснижающей терапии в комбинации с метформином, тиазолидиндионами и препаратами сульфонилмочевины (ПСМ). Агонисты рецепторов ГПП-1 в указанном консенсусе предлагается использовать как при старте лечения у пациентов с уровнем HbA1c более 7,5%, так и в качестве компонента комбинированной терапии с другими сахароснижающими препаратами, включая инсулин [6].
В первом номере журнала «Сахарный диабет» 2011 г. был опубликован проект Консенсуса совета экспертов Российской ассоциации эндокринологов (РАЭ) по инициации и интенсификации сахароснижающей терапии СД 2 типа, в котором основными приоритетами в выборе терапии признаны безопасность и эффективность лечения, а также выделены 3 этапа лечения (старт – интенсификация – дальнейшая интенсификация) [4]. Консенсус совета экспертов РАЭ рекомендует индивидуализированный выбор целевого уровня HbA1c и стратификацию терапевтической тактики в зависимости от исходного уровня HbA1c у больного, а также определяет место ингибиторов ДПП-4 в алгоритмах сахароснижающей терапии.
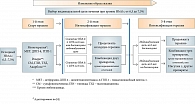
При уровне HbA1c от 6,5 до 7,5% для старта сахароснижающей терапии Консенсус совета экспертов РАЭ рекомендует использовать следующие препараты: метформин, ингибиторы ДПП-4, агонисты рецепторов ГПП-1 (рис. 2). Кроме того, в качестве препаратов резерва при инициации лечения могут использоваться препараты сульфонилмочевины (кроме глибенкламида), глиниды, пиоглитазон, акарбоза.
Учитывая возможность нескольких вариантов для старта сахароснижающей терапии, практическую важность имеет вопрос выбора для этой цели наиболее эффективного и безопасного препарата. Если сравнивать группы препаратов с инкретиновой активностью между собой, то положительными свойствами агонистов рецепторов ГПП-1 (эксенатид, лираглютид) и ингибиторов ДПП-4 являются отсутствие гипогликемий при их применении и потенциальная способность положительно влиять на функцию бета-клеток [4]. Аналоги ГПП-1 по сравнению с ингибиторами ДПП-4 обладают большей сахароснижающей активностью, а также способствуют снижению массы тела [3]. Вместе с тем очевидными недостатками этой группы препаратов является необходимость инъекций, частые побочные эффекты со стороны желудочно-кишечного тракта и высокая стоимость лечения, что существенно ограничивает их клиническое применение.
Ингибиторы ДПП-4 при инициации терапии СД 2 типа могут рассматриваться в качестве альтернативного метформину препарата, так как, обладая сопоставимой сахароснижающей активностью и низким риском гипогликемий, характеризуются лучшей переносимостью, не вызывают желудочно-кишечных расстройств и не ограничены при использовании у лиц с гипоксическими состояниями различной этиологии, а также с умеренными нарушениями функции почек и печени.
Преимуществами ПСМ по сравнению с ингибиторами ДПП-4 являются более высокая сахароснижающая активность, хорошая доказательная база и наименьшая, по сравнению с другими сахароснижающими препаратами, стоимость лечения. Тем не менее лечение ПСМ сопряжено с более высоким риском гипогликемий и различных лекарственных взаимодействий, увеличением массы тела, ограничениями при использовании у больных с почечной и печеночной недостаточностью, а также с риском развития ряда побочных эффектов.
При сопоставимой с ингибиторами ДПП-4 сахароснижающей активностью и низким риском гипогликемий тиазолидиндионы способны положительно влиять на течение неалкогольной жировой болезни печени. Однако существенным недостатком препаратов этой группы является их способность увеличивать риск переломов (особенно у женщин), вызывать периферические отеки, гепатотоксический эффект и усиливать проявления сердечной недостаточности.
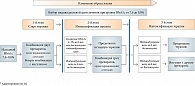
Согласно Консенсусу совета экспертов РАЭ, при инициации терапии СД 2 типа у больных с уровнем HbA1c от 7,6 до 9% (рис. 3), а также с целью интенсификации лечения у пациентов, не достигших цели гликемического контроля при монотерапии, необходимо использовать такие рациональные комбинации сахароснижающих препаратов, как «метформин + ингибиторы ДПП- 4 / агонисты рецепторов ГПП-1 / ПСМ / глиниды». Допустимыми комбинациями являются и другие сочетания препаратов, за исключением таких, как «ПСМ + глинид», «ингибитор ДПП-4 + агонист ГПП-1», «ПСМ + ПСМ» и «ДПП-4 или агонист ГПП-1 + глинид», которые признаны нерациональными или не разрешенными к применению [4].
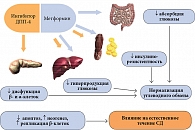
Наиболее физиологически обоснованной из перечисленных выше является комбинация метформина и ингибитора ДПП-4, которая воздействует на все основные патогенетические механизмы развития СД 2 типа (рис. 4). К клиническим преимуществам сочетанного использования ингибиторов ДПП-4 и метформина относятся: потенцирование и усиление сахароснижающего эффекта, низкий риск гипогликемий, отсутствие прибавки массы тела пациента, сохранение плейотропных эффектов метформина, а также предполагаемая способность сохранять и восстанавливать функцию бета-клеток.
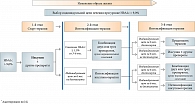
У больных с выраженной декомпенсацией углеводного обмена, когда уровень HbA1c превышает 9%, Консенсус совета экспертов РАЭ рекомендует стартовать с различных режимов инсулинотерапии: базальный инсулин (предпочтительно беспиковый аналог инсулина длительного действия) в комбинации с метформином или ингибитором ДПП-4 или ПСМ; готовые смеси инсулина продленного и короткого действия или базально-болюсная инсулинотерапия (рис. 5). Инсулинотерапия также рекомендована в тех случаях, когда не достигается индивидуальная цель при использовании комбинации из 2–3 пероральных сахароснижающих препаратов.
При достижении необходимого эффекта (снижение уровня HbA1c более чем на 1,5% за 6 мес. терапии) возможна отмена инсулинотерапии и переход на комбинацию пероральных препаратов, одним из которых должен быть метформин (при отсутствии противопоказаний к его применению) [4].
Таким образом, согласно современным отечественным и зарубежным рекомендациям, ингибиторы ДПП-4 могут назначаться больным СД 2 типа в виде монотерапии при дебюте заболевания, а также в комбинации с основными сахароснижающими препаратами других групп с целью интенсификации лечения.
Благодаря своим положительным свойствам и клиническим преимуществам ингибиторы ДПП-4с каждым годом все активнее используются в отечественной клинической практике. Так, результаты анкетирования 92 врачей-эндокринологов Санкт-Петербурга, проведенные в 2010 г., свидетельствуют о том, что около 60% из них регулярно применяют ингибиторы ДПП-4 у больных СД 2 типа. При этом 72% опрошенных врачей чаще назначают больным СД 2 типа ингибиторы ДПП-4, чем аналоги ГПП-1. В качестве преимуществ данного класса препаратов 28% врачей отметили возможность сохранения бета-клеток поджелудочной железы, 27% – низкий риск гипогликемий, 18% – отсутствие серьезных побочных эффектов, а остальные участники опроса оценили удобство применения (13%) и эффективность (13%) препаратов. Данную группу препаратов были готовы использовать при впервые выявленном СД 2 типа 27% врачей, а 57% опрошенных считали необходимым их применение при плохой переносимости и неэффективности монотерапии метформином [7].
Одним из современных и хорошо изученных препаратов, относящихся к группе ингибиторов ДПП-4, является вилдаглиптин (Галвус®, «Новартис»), поскольку в программе (более 70 рандомизированных многоцентровых исследований) по изучению его клинической эффективности участвовало более 22 000 пациентов, из которых более 14 000 принимали данный препарат. В 2010 г. в России препараты Галвус и комбинированный препарат ГалвусМет получали более 10 000 пациентов с СД 2 типа.
Изучение фармакокинетики вилдаглиптина показало его быстрое всасывание при приеме внутрь (tmax 0,5–1,5 часа), дозозависимое, высокоселективное, быстрое и обратимое подавление активности ДПП-4 [8]. Биодоступность препарата, превышающая 80%, не зависит от приема пищи. Вилдаглиптин в незначительной степени связывается с белками крови (9%), а метаболизм осуществляется путем гидролиза, при этом действующее вещество не является ингибитором или индуктором P450 (CYP), основные метаболиты не обладают фармакологической активностью и на 85% выводятся с мочой, а на 15% – с калом [8, 9].
Анализ клинических исследований, в общей сложности включающих результаты наблюдения более 20 тыс. больных СД 2 типа, показал, что вилдаглиптин эффективен при гипергликемии различной степени тяжести, у пациентов с разным ИМТ, а также у больных различных возрастных групп [3]. При назначении вилдаглиптина в дозе 100 мг/сут в течение 24 недель было отмечено снижение уровня HbA1c от 0,6% при исходном уровне HbA1c ≤ 8% до 1,9% при уровне HbA1c > 10% [10]. Также уровень HbA1c снизился в среднем на 1,0% как у больных СД 2 типа с нормальной массой тела без ожирения, так и у обследованных с ИМТ ≥ 35 кг/м2. Кроме того, степень снижения уровня HbA1c в группах пациентов с СД 2 типа моложе 65 лет и более старшего возраста на фоне лечения вилдаглиптином составила в среднем 1,1% [10].
В других рандомизированных клинических исследованиях было показано, что монотерапия вилдаглиптином в течение 6 месяцев и более по эффективности сопоставима с монотерапией метформином, тиазолидиндионами и акарбозой [11, 12, 13]. Так, пациенты с СД 2 типа, получавшие вилдаглиптин в дозе 100 мг/сут или метформин в дозе до 2000 мг/сут, с исходным уровнем HbA1с, составлявшим 7,5–11,0%, через 54 недели наблюдения отметили значительное снижение уровня HbA1c на фоне приема как вилдаглиптина (1,0 ± 0,1%), так и метформина (1,4 ± 0,1%), при этом различия в уровне HbA1c между группами обследованных после лечения оказались недостоверными [11].
Учитывая сравнительно небольшой срок практического применения ингибиторов ДПП-4, особое место в программе клинических исследований вилдаглиптина занимают вопросы безопасности терапии этим препаратом. Многочисленные клинические плацебоконтролируемые исследования продемонстрировали отличную переносимость вилдаглиптина (частота нежелательных явлений была сопоставима с таковой при использовании плацебо) и низкий риск развития гипогликемий [3, 14]. Кроме того, в метаанализах результатов проведенных исследований было убедительно показано, что терапия вилдаглиптином не повышает риск развития панкреатитов, не оказывает негативного влияния на гепатобилиарную и иммунную системы, а также не увеличивает риски сердечно-сосудистых и цереброваскулярных событий [15, 16, 17].
По результатам исследований на здоровых добровольцах, у которых вилдаглиптин применялся в дозе 100 мг один раз в день в комбинации с рамиприлом, дигоксином, варфарином, симвастатином, валсартаном, амлодипином, не отмечено клинически значимых случаев взаимодействия между вилдаглиптином и исследуемыми препаратами, что подтверждает низкий риск лекарственных взаимодействий при его использовании [19, 20, 21].
Необходимо подчеркнуть, что проведенные клинические исследования подтвердили высокую эффективность комбинации вилдаглиптина с метформином и другими пероральными сахароснижающими препаратами. Так, пациентам с СД 2 типа и неудовлетворительной компенсацией углеводного обмена (HbA1c – 7,5–11%) на фоне приема метформина в максимальной дозе был добавлен вилдаглиптин в дозе 50–100 мг в сутки. В группе сравнения пациенты продолжали принимать метформин в прежней дозировке. Результаты исследования через 24 недели лечения показали существенное снижение уровня HbA1c в среднем на 0,7% и 1,1% в группах больных на комбинации метформина и вилдаглиптина в дозе 50 мг и 100 мг соответственно по сравнению с группой больных, получавших монотерапию метформином [22].
Добавление вилдаглиптина к терапии метформином также продемонстрировало высокую эффективность у различных категорий больных СД 2 типа: у лиц пожилого возраста, пациентов с ожирением и у лиц с неудовлетворительным гликемическим контролем.
Представляют интерес данные Элизабет Мигойи (Elizabeth M. Migoya) и соавт. [28], свидетельствующие о том, что вилдаглиптин, назначенный больным СД 2 типа, ранее получавшим метформин, приводит к более выраженному повышению уровня активного ГПП-1 в крови, чем терапия вилдаглиптином пациентов без предшествующего лечения метформином. Предполагается, что потенцирование эффекта вилдаглиптина обусловлено независимым от ингибиции ДПП-4 стимулированием под влиянием метформина секреции ГПП-1.
При прямой сравнительной оценке результатов лечения больных СД 2 типа в течение 24 недель комбинациями «вилдаглиптин + метформин» и «ситаглиптин + метформин» с суточным мониторированием гликемии и оценкой уровней активного ГПП-1 и глюкагона в крови до и после лечения показано, что сахароснижающий эффект обеих комбинаций существенно не различался, однако на фоне терапии вилдаглиптином средняя амплитуда суточных колебаний гликемии (самостоятельный фактор риска развития сосудистых осложнений диабета) составила 1,8 ± 0,3 ммоль/л, что было существенно ниже данного показателя у лиц, получавших вилдаглиптин, который составил 3,3 ± 1,9 ммоль/л (рис. 6). Полученные данные, вероятно, объясняются более выраженным посталиментарным подавлением секреции глюкагона на фоне более высоких уровней ГПП-1 в промежутках между приемами пищи, что было установлено в группе пациентов, получавших вилдаглиптин [23].
Добавление вилдаглиптина в дозе 100 мг/сут больным СД 2 типа с неудовлетворительным гликемическим контролем на фоне лечения современным препаратом сульфонилмочевины глимепиридом приводило к достоверному снижению уровня HbA1c на 0,7 ± 0,1% по сравнению с группой пациентов, получавших глимепирид + плацебо. В этом исследовании также отмечено снижение HbA1c у больных старше 65 лет (0,8 ± 0,2%) и у пациентов с исходным уровнем HbA1c > 9% (0,9 ± 0,2%) [24].
Назначение вилдаглиптина в дозе 100 мг/сут больным с декомпенсацией СД 2 типа на терапии пиоглитазоном в дозе 45 мг/сут показало достоверное снижение уровня HbA1c за 24 недели на 1,0 ± 0,1% в группах, получавших вилдаглиптин по сравнению с комбинацией «плацебо + пиоглитазон» [25].
В настоящее время вилдаглиптин является единственным препаратом группы ингибиторов ДПП-4, комбинация которого с препаратами инсулина разрешена в РФ. Вивиан Фонсека (Vivian A. Fonseca) и соавт. (2008) показали, что сочетание вилдаглиптина и инсулина позволяет достичь снижения уровня HbA1c у больных СД 2 типа на 0,3% больше по сравнению с группой пациентов, получавшей инсулин в сочетании с плацебо (рис. 7). Отмечено, что добавление вилдаглиптина к инсулину обеспечивало более выраженное снижение уровня HbA1c у обследованных пациентов старше 65 лет. Так, в подгруппе пожилых больных СД 2 типа снижение уровня HbA1c составило на 0,6% больше, чем в группе плацебо [26]. Кроме того, добавление вилдаглиптина пациентам, получавшим инсулинотерапию, сопровождалось достоверным снижением общего числа случаев гипогликемий, а также гипогликемий тяжелой степени. Предполагается, что выявленные благоприятные эффекты объясняются тем, что вилдаглиптин может восстанавливать функцию альфа-клеток поджелудочной железы, улучшая их чувствительность к глюкозе в плазме крови [27].
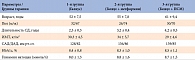
С целью оценки эффективности вилдаглиптина в реальной клинической практике в Санкт-Петербурге в 2010 г. стартовала открытая наблюдательная программа по изучению эффективности и безопасности применения препарата Галвус в моно- и комбинированной терапии у пациентов с СД 2 типа и неудовлетворительным контролем на предшествующей терапии. Всего в программу было включено 670 пациентов с СД 2 типа, из которых к настоящему времени 599 человек прошли второй визит и 100 пациентов – третий визит. Все больные были рандомизированы на 3 группы (табл. 2):
- 1-я группа (n = 134) – больные, получающие монотерапию Галвусом;
- 2-я группа (n = 349) – больные, получающие комбинацию «Галвус + метформин»;
- 3-я группа (n = 187) – больные, получающие комбинацию «Галвус + ПСМ».
Обследованные пациенты были сопоставимы по полу, возрасту, длительности диабета, уровню артериального давления, степени компенсации углеводного обмена (табл. 2).
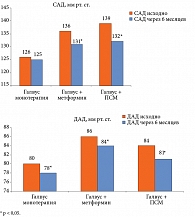
Результаты оценки исследования 599 пациентов, прошедших 2-й визит через 5–6 месяцев терапии, показали снижение уровня HbA1c на 1,4% в 1-й группе, на 1,3% – во 2-й и на 1,7% – в 3-й группе обследованных. Кроме того, по сравнению с исходными значениями достоверно (р < 0,001) снизился уровень гликемии натощак во всех группах пациентов (на 1,2 ммоль/л; 1,9 ммоль/л и 1,8 ммоль/л соответственно). Также отмечено статистически значимое снижение значений ИМТ во 2-й (с 34 кг/м2 до 32 кг/м2, р < 0,03) и 3-й группах (с 29 кг/м2 до 27 кг/м2, р < 0,03) при отсутствии прибавки массы тела в 1-й группе (ИМТ исходно составлял 30,3 кг/м2, через 6 месяцев терапии – 29 кг/м2, р > 0,05). Кроме того, в ходе исследования зарегистрировано снижение уровней систолического (САД) и диастолического (ДАД) артериального давления по сравнению с исходными уровнями во всех группах больных СД 2 типа (рис. 8).
Результаты опроса участников программы с помощью анкеты показали, что практически все больные (98%) были удовлетворены терапией препаратом Галвус (61% ответов – «очень удовлетворен» и 37% ответов – «удовлетворен»). Неудовлетворенными терапией остались 1% пациентов и еще 1% опрошенных затруднились с ответом. 97% больных, принимавших Галвус, хотели бы продолжить лечение данным препаратом.
Промежуточные результаты проведенного исследования показали, что в реальной диабетологической практике применение Галвуса в виде монотерапии или в комбинации с основными группами сахароснижающих препаратов способствует достижению строгого гликемического контроля у больных СД 2 типа, препарат хорошо переносится, благоприятно влияет на массу тела и уровень артериального давления, что определяет высокую приверженность пациентов рекомендованному лечению.
Таким образом, применение в качестве сахароснижающей терапии ингибиторов ДПП-4 у больных СД 2 типа является эффективной и безопасной терапией, преимущества которой обусловлены как многосторонним воздействием на основные патогенетические механизмы развития этого заболевания (особенно при использовании в комбинации с метформином), так и физиологичностью сахароснижающего действия. Современный препарат группы ингибиторов ДПП-4 вилдаглиптин и его фиксированная комбинация с метформином в наибольшей степени соответствуют критериям «идеального» сахароснижающего препарата, главными из которых являются высокая сахароснижающая активность в сочетании с низким риском гипогликемий и различных побочных эффектов, достаточная доказательная база. Это позволяет рекомендовать применение вилдаглиптина и его фиксированной комбинации с метформином в качестве препаратов выбора при инициации терапии, а также на всех этапах интенсификации лечения больных СД 2 типа.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.