Метформин в лечении сахарного диабета 2 типа: новые данные об известном препарате
- Аннотация
- Статья
- Ссылки
Последние 2 десятилетия можно охарактеризовать как настоящий «ренессанс» метформина в диабетологии. Его основой стал стремительный рост интереса к синдрому инсулинорезистентности, а также публикация результатов британского проспективного исследования UKPDS (United Kingdom Prospective Diabetes Study). В этом масштабном и самом продолжительном в истории диабетологии исследовании была показана высокая эффективность метформина по влиянию на углеводный обмен и смертность при СД. Летальность, обусловленная диабетом, при интенсивном лечении метформином в UKPDS была на 42% ниже, чем на диетотерапии. Общая смертность при интенсивном контроле гликемии с помощью метформина уменьшилась на 36%. Этот показатель был значительно лучше, чем в группах больных, получавших другие режимы лечения (2).
Последующие исследования подтвердили вывод UKPDS о благоприятном влиянии метформина на развитие сердечно-сосудистых осложнений СД. Метаанализ 29 исследований (3), включавших в общей сложности 5259 пациентов, показал, что лечение метформином тучных больных с СД 2 типа снижает смертность от всех причин, связанных с диабетом (р = 0,03), общую смертность (р = 0,01) и частоту инфаркта миокарда (р = 0,02). Вероятно, это связано не только с сахароснижающими свойствами метформина, но и с его способностью влиять на инсулинорезистентность и другие факторы сердечно-сосудистого риска. Установлено, что метформин оказывает благоприятное действие на гликемию, массу тела, параметры липидного обмена, диастолическое артериальное давление, а также на фибринолиз и эндотелиальную дисфункцию (3, 4).
Новый стимул к повышению интереса к метформину дали исследования, показавшие протективное действие метформина в отношении некоторых видов рака (5). По обобщенным данным (6), у больных CД 2 типа повышен риск ряда злокачественных опухолей, в том числе карциномы кишечника (~ 30%), поджелудочной железы (~ 50%), молочной железы (у женщин в постменопаузе ~ 20%). Риск новообразований зависит от вида сахароснижающей терапии. Установлено, что у больных, получающих метформин, частота рака кишечника и поджелудочной железы ниже, чем у пациентов, получающих инсулин или препараты сульфонилмочевины (7).
Фармакоэкономический анализ подтверждает обоснованность применения метформина в лечении СД 2 типа. Детальный анализ «затраты – эффективность», проведенный группой UKPDS, показал, что дополнительные расходы при лечении метформином в сравнении с диетотерапией (стоимость препарата, необходимость более частых визитов к врачу) с избытком компенсируются за счет профилактики осложнений. В среднем назначение метформина позволило сэкономить 258 фунтов стерлингов (GBP) на пациента и повысить ожидаемую продолжительность жизни на 1 год (8).
Механизм действия метформина на углеводный обмен связан с улучшением чувствительности к инсулину. При этом, во-первых, уменьшается печеночная продукция глюкозы (за счет ингибирования глюконеогенеза и гликогенолиза в печени). Во-вторых, повышается захват глюкозы мышцами и жировой тканью (за счет увеличения количества глюкозных транспортеров и уменьшения инсулинорезистентности). Кроме того, метформин является слабым аноректиком. Анорексигенный эффект обусловлен прямым контактом препарата со слизистой желудочно-кишечного тракта. Уменьшение аппетита ведет к снижению потребления пищи и способствует уменьшению концентрации глюкозы в крови (9, 10).
В соответствии с механизмом своего действия метформин снижает уровень глюкозы крови натощак. По данным систематического анализа исследований, проведенного A. Natali и E. Ferrannini, в среднем снижение гликемии натощак при применении метформина составляет 20-29%. Абсолютный сахароснижающий эффект тем больше, чем выше исходный уровень глюкозы (11).
В последние годы открыты новые эффекты метформина, не связанные напрямую с его эффектами в инсулинзависимых тканях. Так, противоопухолевое действие метформина связывают с влиянием на сигнальный путь АФМ-активируемой протеинкиназы. Данный фермент играет большую роль в энергетическом балансе и регуляции пролиферативной активности клеток, в том числе опухолевых. Другой возможный механизм противоопухолевого эффекта метформина связан с влиянием на Т-клетки памяти (6).
Режим дозирования. Оригинальным препаратом метформина, имеющимся на фармацевтическом рынке, является препарат Глюкофаж® (производитель «Мерк Сантэ с.а.с», Франция, в России представлен компанией «Никомед»). Глюкофаж выпускается в таблетках 500, 850 и 1000 мг. Принимается во время или сразу после еды. Лечение можно начинать с приема 1 таблетки (500 или 850 мг) во время завтрака или ужина. Постепенно, с интервалом в 1-2 недели, доза увеличивается на 500-850 мг. Полная терапевтическая доза метформина (2000 мг/сут.) принимается в 2-3 приема. Максимальная терапевтическая доза составляет 3000 мг/сут.
При подборе дозы метформина больному СД следует помнить, что препарат оказывает дозозависимый эффект на уровень глюкозы в крови (10).
Побочные эффекты и противопоказания. Наиболее частыми побочными эффектами метформина являются желудочно-кишечные расстройства, такие как тошнота, рвота, диарея, металлический или горький привкус во рту, анорексия (последнее явление можно рассматривать и как положительное у больных с ожирением). Побочные эффекты развиваются у 5-20% пациентов в начале лечения метформином. Уменьшению их выраженности способствует прием препарата во время или сразу после еды, а также начало терапии с малой дозы с постепенным ее повышением до терапевтической. Редким осложнением терапии метформином является недостаточность витамина В12 и фолиевой кислоты. При назначении в качестве монотерапии метформин практически не вызывает гипогликемий (9, 10).
Традиционно специфичным осложнением терапии бигуанидами, связанным с их способностью стимулировать анаэробный гликолиз, считался лактацидоз. Многочисленные клинические исследования показали, что сам по себе метформин вызывает незначительное увеличение концентрации молочной кислоты в крови, однако это увеличение может потенцироваться другими факторами и состояниями. К числу последних относятся состояния, при которых:
- повышено образование лактата (выраженная декомпенсация СД, кетоацидоз, «ацидоз голодания»);
- снижен клиренс лактата (поражения паренхимы печени, алкоголизм);
- снижен клиренс лактата и метформина (нарушение функции почек, внутривенное введение рентгеноконтрастных веществ);
- имеет место выраженная тканевая гипоксия (болезни легких и сердца с функциональной недостаточностью этих органов, тяжелые анемии, гемобластозы, выраженные облитерирующие поражения периферических артерий).
Сочетанное действие нескольких факторов, способствующих лактацидозу, наблюдается при инфекциях, операциях, травмах. Все перечисленные состояния считаются противопоказаниями к назначению метформина. Об этом следует помнить не только эндокринологам, но и врачам других специальностей. Метформин не должен применяться в переоперационном периоде (отменяется не позднее чем за 48 часов до оперативного лечения с общей анестезией), при проведении рентгеновских исследований с йодсодержащим контрастом (48 часов до исследования и 48 часов после него), у больных с тяжелыми инфекциями с лихорадкой. В этих ситуациях показан временный переход на инсулинотерапию (9, 10).
Следует заметить, что в реальной клинической практике противопоказания к назначению метформина часто недоучитываются. Анализ ряда популяционных и когортных исследований выявил случаи назначения метформина больным с сердечной недостаточностью, нарушением функции почек и печени (12). Несмотря на то, что в этих исследованиях суммарно участвовало около 2500 человек, сообщается лишь об одном случае лактацидоза, развившегося у больного на фоне острого инфаркта миокарда и почечной недостаточности. Интересные данные получены в израильском исследовании, в котором участвовали 393 пациента с СД 2 типа и сопутствующими заболеваниями: умеренной почечной недостаточностью (креатинин сыворотки 130-220 ммоль/л), ишемической болезнью сердца, сердечной недостаточностью III и IV функционального класса по NYHA, поражениями печени, хронической обструктивной болезнью легких. После рандомизации одна часть больных продолжала лечение метформином, другая не получала лечения. Спустя 4 года пациенты, получавшие метформин, имели более низкий индекс массы тела и лучшие показатели углеводного и липидного обмена. Ни одного случая лактацидоза не было зафиксировано. Различий в темпах прогрессирования почечной недостаточности, а также в смертности между группами не отмечено (13).
Безопасность метформина доказана в исследовании COSMIC (Comparative Outcomes Study of Metformin Intervention vs Conventional approach). В рамках данного проекта сравнивали частоту случаев лактацидоза, смерти и госпитализации у 7200 пациентов c CД 2 типа, получавших лечение метформином, и у 1505 больных на других режимах лечения. Исследователи не выявили каких-либо различий по изучавшимся конечным точкам между группами (14). При метаанализе 194 проспективных сравнительных и когортных исследований, включавших пациентов с СД 2 типа, не найдено значительных различий в частоте лактацидоза у больных, получавших терапию метформином, и у пациентов, не получавших ее (15).
Новые данные по эффективности и безопасности метформина позволили критически пересмотреть некоторые ограничения к применению этого препарата. Прежде всего это касается возрастного лимита к его назначению, который в недалеком прошлом определялся как 65 лет. Поскольку не существует доказательств, что возраст сам по себе является фактором риска лактацидоза, при назначении метформина следует учитывать не возраст как таковой, а наличие заболеваний, являющихся противопоказаниями (9, 12). Вряд ли можно считать оправданным «вето» на использование метформина у больных со стабильной сердечной недостаточностью I или II функционального класса по NYHA, эффективно контролируемой диуретиками и ингибиторами АПФ. Вместе с тем в случае развития острого инфаркта миокарда или другого кардиального осложнения, ведущего к нарушению гемодинамики и гипоперфузии тканей, метформин должен быть отменен (12). Результаты метаанализа (15) и проспективных исследований (13, 14) позволяют считать, что назначение метформина может быть безопасным у больных с начальными стадиями почечной недостаточности, при уровне креатинина крови менее 133 мкмоль/л.
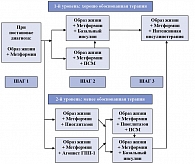
Метформин в комбинированной сахароснижающей терапии. Вопрос о назначении комбинированной сахароснижающей терапии рассматривается при недостаточной неэффективности монотерапии метформином. Последняя определяется как уровень гликированного гемоглобина (HbA1c) через 3 месяца лечения > 7%. Согласно алгоритму экспертов ADA и EASD, к «хорошо обоснованной» терапии относится комбинация метформина с препаратом сульфонилмочевины или базальным инсулином (1).
Сочетание «метформин + сульфонилмочевина» является наиболее распространенным вариантом комбинированной терапии у больных с сохранной секрецией инсулина. Такая терапия оправдана патогенетически, так как она влияет на два основных механизма развития и прогрессирования СД 2 типа: инсулинорезистентность и дисфункцию b-клеток. Назначение комбинации метформина и препарата сульфонилмочевины позволяет снизить уровень гликемии и HbA1c в ситуациях, когда целевой уровень этих показателей не достигается на фоне терапии одним из препаратов (10).
Поскольку при назначении сочетанной терапии большее значение приобретает приверженность пациентов лечению, определенные преимущества могут иметь фиксированные комбинации препаратов. В контролируемых исследованиях и клинической практике хорошо зарекомендовал себя Глюкованс®, в состав которого входит метформин и глибенкламид. Глюкованс® выпускается в 2 лекарственных формах, содержащих: 500 мг метформина и 2,5 мг глибенкламида; 500 мг метформина и 5 мг глибенкламида. Глюкованс® – единственный комбинированный препарат, имеющий в своем составе микронизированную форму глибенкламида, что позволяет снизить риск гипогликемий. Обычно начальная доза Глюкованса составляет: 1 таблетка 500 мг/2,5 мг 1 раз во время еды. При замещении предшествующей терапии метформином и глибенкламидом назначают 1-2 таблетки по 500 мг/2,5 мг в зависимости от предыдущего уровня доз. Каждые 1-2 недели после начала лечения дозу препарата корректируют в зависимости от уровня гликемии. Максимальная доза составляет 4 таблетки в сутки Глюкованса 500 мг/2,5 мг или 4 таблетки в сутки Глюкованса 500 мг/5 мг.
Эффективность Глюкованса показана в ряде хорошо спланированных клинических исследований. В одном из наиболее крупных рандомизированных исследований (16), включавшем 411 больных СД 2 типа, установлено, что применение Глюкованса в течение 16 недель обеспечивает более эффективный контроль гликемии по сравнению с монотерапией метформином и глибенкламидом. Целевой уровень HbA1c < 7% был достигнут у 75% и 64% пациентов, получавших Глюкованс 500 мг/2,5 мг и 500 мг/5 мг соответственно, только у 42% больных на глибенкламиде и у 38% больных на метформине (р = 0,001). Интересно, что адекватный контроль гликемии при лечении Глюковансом достигается на фоне меньших доз метформина и глибенкламида, чем при раздельном назначении этих препаратов (16, 17). Очевидно, это связано с лучшей приверженностью лечению, судя по количеству реально принимаемых пациентами таблеток (18).
Другим вариантом «хорошо обоснованной терапии» с точки зрения экспертов ADA и EASD является сочетание метформина с базальным инсулином или интенсивной инсулинотерапией (1). Присоединение метформина позволяет избежать нежелательной прибавки веса на фоне инсулинотерапии, а также снизить потребность в инсулине в среднем на 20-30% (19). Показано, что метформин в комплексе лечения СД 2 типа нивелирует повышение риска рака опухолей кишечника и поджелудочной железы, которое наблюдается на фоне терапии инсулином (7). По данным И. Ю. Демидовой и соавт., лечение СД 2 типа с использованием метформина в дозе 2000 мг/сут. совместно с базальным инсулином экономически более целесообразно, чем любая сахароснижающая терапия без метформина (20).
В последние годы изучается эффективность и безопасность комбинаций метформина с инсулиновыми сенситизаторами класса тиазолидиндионов, агонистами глюкагоноподобного пептида-1 (ГПП-1), ингибиторами дипептидилпептидазы IV типа (ДПП-IV) и другими сахароснижающими препаратами.
Анализ 5 контролируемых исследований (10) показал, что тиазолидиндионы (розиглитазон и пиоглитазон) способны оказывать дополнительный гипогликемизирующий эффект при добавлении к метформину. Помимо уменьшения уровня гликемии натощак и HbA1c, присоединение пиоглитазона к метформину повышает уровень холестерина ЛПВП, общего холестерина, адипонектина и снижает содержание инсулина, свободных жирных кислот натощак, а также индекс инсулинорезистентности HOMA (21). Дополнительные благоприятные эффекты сочетанной терапии двумя классами «сенситизаторов инсулина» объясняются тем, что эти препараты действуют через разные молекулярные механизмы и в неодинаковой степени влияют на продукцию глюкозы печенью, глюконеогенез и липолиз (11, 22).
В настоящее время установлена эффективность сочетания метформина с инкретиномиметиками: аналогами ГПП-1 и ингибиторами ДПП-IV. Сахароснижающее действие ГПП-1 осуществляется в основном за счет стимуляции секреции инсулина и подавления секреции глюкагона поджелудочной железой. Показано, что назначение аналога ГПП-1 экзенатида больным с недостаточным гликемическим контролем на монотерапии метформином значимо снижает гликемию и массу тела (23). Ингибиторы ДПП-IV – фермента, расщепляющего ГПП-1: ситаглиптин, вилдаглиптин и саксаглиптин также показали свою эффективность в комбинации с метформином (24). Способность ингибировать ДПП-IV обнаружена и у самого метформина (25). Хотя этот эффект не достаточен для изменения уровня циркулирующего ГПП-1 и инсулина, по-видимому, он может способствовать повышению сахароснижающего эффекта комбинаций метформина и инкретиномиметиков.
Итак, в настоящее время метформин (Глюкофаж®) является препаратом первой линии в лечении СД 2 типа. Улучшая чувствительность тканей к инсулину, метформин не только способствует достижению оптимального контроля гликемии, но и воздействует на целый ряд факторов сердечно-сосудистого риска. При необходимости назначения комбинированной сахароснижающей терапии метформин остается обязательным компонентом терапии. Определенные преимущества при этом имеют фиксированные комбинации препаратов, например, комбинация метформина с микронизированной формой глибенкламида (Глюкованс®). Применение метформина в составе комбинированой терапии повышает эффективность контроля гликемии и уменьшает неблагоприятные эффекты других сахароснижающих средств. Это способствует снижению частоты фатальных осложнений и улучшает прогноз пациентов с СД.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.