Мини-мозг как инновация в персонализированной медицине
- Аннотация
- Статья
- Ссылки
- English

Введение
Актуальной проблемой в нейронауках является поиск репрезентативной модельной системы, которая всецело отражала бы особенности человеческого мозга. Модели на животных и культуры первичных клеток хотя и существенно расширили наши знания, но не лишены фундаментальных недостатков – от отсутствия человеческого генетического контекста и трехмерной цитоархитектоники до этических и практических сложностей в получении материала. Появление мозговых органоидов на основе индуцированных плюрипотентных стволовых клеток (ИПСК) ознаменовало революцию в этой области, поскольку они обладают рядом преимуществ перед животными моделями и 2D-клеточными культурами. Кокультивирование различных типов клеток и формирование органоподобных структур [1–4] позволяют изучать нейровоспалительные и нейроваскулярные процессы, а также взаимодействие с другими областями мозга, которые также затрагиваются на фоне заболевания. Микрофлюидные системы обеспечивают доставку нутриентов и кислорода, улучшая физиологическую релевантность этих моделей и решая ограничения, связанные с диффузией нутриентов и клеточным ростом. Скаффолды и 3D-биопринтинг оказывают структурную поддержку, способствующую более сложной тканевой организации и обеспечивающую цитоархитектонику мозговых органоидов.
Эти достижения делают возможным долгосрочное культивирование, создание условий, напоминающих среду in vivo [5], а также анализ генетических особенностей и влияния эпигенетических факторов. Такие достижения позволяют релевантно оценивать эффективность и безопасность лекарственных препаратов в персонализированной медицине [6, 7].
Несмотря на значительный потенциал мини-мозга (мозговых органоидов) в моделировании заболеваний человека, его широкое применение сопряжено с определенными проблемами, в частности валидностью и экстраполяцией. Так, вариабельность в генерации органоидов между лабораториями и партиями может привести к несоответствию в отношении размера, формы и клеточного состава [8], а отсутствие системных взаимодействий, таких как вовлечение иммунной и сосудистой систем [9], полностью развитых синаптических связей и зрелых глиальных клеток, ограничивает способность мини-мозга реплицировать сложные взаимодействия сформированного мозга [8].
В статье рассматриваются современные исследования, демонстрирующие, как инновационные подходы к генерации и использованию мини-органоидов помогают преодолеть указанные ограничения. Особое внимание уделяется стандартизированным протоколам дифференцировки и перспективным стратегиям, повышающим релевантность и воспроизводимость моделей для доклинических исследований.
Тенденции применения мозговых органоидов
Изучение патогенеза нейродегенеративных заболеваний
Мозговые органоиды показали высокую эффективность в моделировании нарушений нейроразвития с реальным патогенезом, поскольку они рекапитулируют развитие мозга плода, имитируя различные аспекты развития тканевой структуры и клеточного состава [10]. В частности, мозговые органоиды эффективно воспроизводят ключевые элементы патогенеза болезни Паркинсона (БП) и болезни Альцгеймера (БА) [11, 12] и опиоид-индуцированного нейровоспаления.
Изучение патогенеза БА. В данном случае можно выделить два основных направления с помощью мозговых органоидов – моделирование патогенеза семейной и спорадической формы болезни [13].
Установлено, что органоиды от лиц с гомозиготным ApoE4 показывают усиленный апоптоз, снижение синаптической целостности и увеличение содержания тау-белка. РНК-секвенирование выявило обогащение генов, вовлеченных в формирование стрессовых гранул и нарушенный метаболизм РНК [14]. Кроме того, нейроны ApoE4 продемонстрировали увеличение синаптического ApoE4 с нарушением поглощения бета-амилоида (Aβ) и накоплением холестерина в астроцитах. В то же время в клетках, подобных микроглии, наблюдалось снижение фагоцитоза Aβ [13]. Кроме того, в анализе церебральных органоидов, содержащих мутантный PSEN2 (ген высокого риска развития семейной формы БА), выявлялся дефицит в сигналинге Notch и нейрогенезе [15].
Спорадическая форма БА встречается чаще семейной – свыше 90% случаев в популяции [16]. Спорадическая БА, вероятно, вызвана комбинацией генетических вариантов, взаимодействующих с факторами окружающей среды. Применение мозговых органоидов, полученных от пациентов со спорадической формой БА, особенно актуально, поскольку появляется возможность оценивать влияние генетических вариантов на патогенез заболевания. S. Pavoni и соавт. наблюдали зависящее от времени увеличение уровней Aβ-40 и Aβ-42 после обработки афтином-5 (индуктором Aβ-42). Показано, что мини-мозг, полученный из клеточной линии, не связанной с БА, реагирует на индукцию химическими соединениями, вызывая изменение физиологических концентраций Aβ [17].
Таким образом, моделирование на церебральных органоидах позволяет детально изучать патогенез обеих форм БА. В случае спорадической БА органоиды демонстрируют ценность как инструмент для изучения комплексного взаимодействия генетической предрасположенности и внешних факторов. Это открывает путь к исследованию патофизиологии наиболее распространенной формы заболевания и скринингу потенциальных терапевтических вмешательств.
Изучение патогенеза БП. Мозговые органоиды, полученные из ИПСК, все чаще используются для моделирования БП. Но в данном случае обычно применяются органоиды среднего мозга, поскольку БП обусловлена избирательной потерей дофаминергических нейронов в компактной части черной субстанции, берущей начало в вентральной покрышечной области среднего мозга [18, 19]. Используя органоиды среднего мозга, N. Wulansari и соавт. обнаружили, что мутации в гене, ассоциированном с ранним началом БП (DNAJC6), приводят к патологической агрегации альфа-синуклеина, а также к митохондриальным и лизосомным аномалиям [20].
Кроме того, S.W. Kim и соавт. отмечали возможность трансплантации нейральных стволовых клеток-предшественников, выделенных из органоидов среднего мозга (Og-NSC), крысам с гемипаркинсонизмом, после чего Og-NSC развились в дофаминовые нейроны среднемозгового типа (mDA-нейроны) и интегрировались в цепь среднего мозга [21]. Нейрональную активность Og-NSC in vivo оценивали с помощью трансдукции в стриатум GCaMP6s (белок – индикатор кальция, который излучает зеленую флуоресценцию при связывании Ca++). Многочисленные зеленые флуоресцентные сигналы в состоянии анестезии детектировались с помощью двухфотонной эндомикроскопии в трансплантатах, сформированных через месяц, что указывает на спонтанную активность нейронов (причем частота потенциалов действия аналогична базальной частоте разрядов дофаминергических нейронов в компактной части черной субстанции). Кроме того, у крыс отмечалось значительное улучшение поведения и двигательных функций передних конечностей. Моделирование БП с помощью органоидов среднего мозга не только позволяет успешно воспроизводить ключевые клеточные патологии, характерные для БП, но и открывает перспективы для регенеративной медицины. Трансплантация клеток, полученных из мозговых органоидов, подтверждает их способность дифференцироваться в функциональные дофаминергические нейроны, интегрироваться в нейронные цепи и вызывать значительное поведенческое улучшение in vivo. Это подчеркивает высокий потенциал технологии мозговых органоидов.
Изучение патогенеза опиоид-индуцированного нейровоспаления. На модели мини-мозга было воспроизведено опиоид-индуцированное нейровоспаление. Показано, что микроглия in vivo запускает нейровоспаление под воздействием опиоидов через пути, опосредованные инфламмасомой NLRP3 [22, 23]. Под влиянием опиоидов на рецепторы TLR4 микроглии может запускаться колокализация NLRP3/ASC с активацией каспазы 1 для продукции интерлейкина (ИЛ) 1-бета, ИЛ-18 и фактора некроза опухоли (ФНО) альфа, что в свою очередь вызывает секрецию провоспалительных цитокинов нейронами и астроцитами, приводя к нейровоспалению.
Тестирование противомигренозных препаратов
Мигрень – сложное расстройство, обусловленное множеством патогенных изменений. В силу этого, а также видовых различий многие аспекты мигрени не могут быть смоделированы на животных [24]. В настоящее время активно рассматривается возможность применения технологии «мини-мозг» в тестировании препаратов от мигрени. Важным преимуществом мозговых органоидов является то, что они могут выживать в культуре приблизительно в течение года [25]. Исследования факторов, влияющих на созревание нейронов и развитие мозга при мигрени, позволяют тестировать различные аспекты патогенеза этого заболевания.
Мигрень – расстройство мозга, которое предположительно связано как с генетическими, так и с эпигенетическими факторами. Следовательно, органоиды мозга потенциально могут быть использованы для моделирования патогенеза мигрени. Кроме того, для этой цели можно изучать как направленные, так и ненаправленные органоиды [26]. Поскольку патогенез мигрени затрагивает различные области мозга, целесообразно исследовать ассемблоиды [26]. Оптимальная модель позволила бы проводить тестирование лекарственных средств и идентификацию механизм-ориентированных терапевтических эффектов. Последнее особенно важно, поскольку большинство доступных противомигренозных препаратов направлены на симптоматическую терапию, а не на модификацию или излечение мигрени [27].
Мозговые органоиды представляют собой высокоперспективную модель для изучения патогенеза мигрени и разработки новых терапевтических стратегий. Ключевое преимущество мозговых органоидов заключается в способности преодолевать ограничения животных моделей, воспроизводить сложное взаимодействие генетических и эпигенетических факторов, лежащих в основе мигрени.
Изучение механизмов формирования нервной трубки и возможных патологий развития
E. Karzbrun и соавт. разработали воспроизводимую модель для изучения морфогенеза человеческой нервной трубки, совместимую с прижизненной визуализацией, генетическими манипуляциями и пригодную для фармацевтического скрининга [28]. Передняя идентичность нервной ткани указывала на релевантность для краниального закрытия нервной трубки. Показано, что после нервной индукции нервная эктодерма складывается в нервную трубку длиной в несколько миллиметров, покрытую неневральной эктодермой. Процесс складывания происходит с эффективностью 90% и анатомически напоминает развивающуюся человеческую нервную трубку. Установлено, что нервная и неневральная эктодерма необходима и достаточна для морфогенеза складывания. Идентифицировано также два механизма, управляющих этим процессом: апикальное сокращение нервной эктодермы и базальная адгезия, опосредованная синтезом внеклеточного матрикса невральной эктодермой. Воздействие на эти два механизма с помощью лекарственных препаратов приводит к дефектам, сходным с пороками развития нервной трубки.
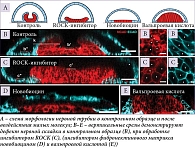
Чтобы проверить пригодность стволовоклеточной системы для моделирования дефектов нервной трубки, было применено три низкомолекулярных ингибитора (рис. 1). Во-первых, ингибитор ROCK (Shroom3-Rho-киназы). Shroom3 контролирует апикальную нейральную контрактильность и ассоциирован с дефектами нервной трубки [29, 30]. Во-вторых, ингибитор HSP-90 новобиоцин, который увеличивает содержание фибронектина (фибронектин играет роль в ранней нейруляции [31]). Наконец, в-третьих, ассоциированный с дефектами нервной трубки препарат вальпроевой кислоты.
Образцы с ингибированием ROCK показали утолщение нервной ткани. Кроме того, нарушенная локализация F-актина и Shroom3 на апикальной поверхности свидетельствовала о разрушении апикальной актомиозиновой сборки и прекращении апикального сокращения нервной ткани. Это согласуется с ингибированием ROCK во время закрытия нервной трубки у мышей, при котором ингибирование ROCK снижает апикальное нейрональное натяжение и локализацию F-актина [32]. Применение новобиоцина ассоциировалось с плоской и тонкой нервной пластинкой, что напоминало фенотип, остановившийся на стадии нейральной индукции. Иммуноокрашивание подтвердило, что новобиоцин значительно снижает уровни фибронектина. Это означает, что матрикс фибронектина, синтезируемый неневральной эктодермой, необходим для формирования бислоя и нервной складки. Наконец, применение вальпроевой кислоты ассоциировалось с обратно изогнутой нервной пластинкой с отрицательной кривизной.
Разработанная модель органоида нервной трубки представляет собой эффективный инструмент как для изучения механизмов нейруляции и патогенеза пороков развития у человека, так и для тестирования фармакологических агентов.
Изучение механизмов развития расстройств аутистического спектра
Сложный клеточный состав и 3D-пространственная конфигурация органоидов позволяют изучать сложные взаимодействия между нейронами и глиальными клетками, которые схожи с их естественной конфигурацией в нервной системе. Это делает возможным моделирование нейрональных сетей пациентов с расстройствами аутистического спектра (РАС) [33]. Показано снижение спонтанной нейронной активности в корковых органоидах с мутацией KMT5B (ген высокого риска РАС) [34].
Исследования с использованием органоидов мозга, полученных от четырех индивидуумов с РАС, выявили снижение активности клеточного цикла в нейрональных клетках-предшественниках (при неизменной пролиферации клеток) и сверхпродукции ГАМКергических нейронов [35].
В другом исследовании мутация в гене высокого риска РАС (PTEN) способствовала экспансии популяции клеток-предшественников и задержке нейрональной дифференцировки [36].
Следует также отметить, что макроцефалия – одна из часто наблюдаемых особенностей РАС. Большинство пациентов, от которых получены церебральные органоиды, демонстрировали фенотип макроцефалии [36, 37].
Мозговые органоиды служат релевантной моделью для изучения клеточно-молекулярных механизмов РАС. Исследования выявляют общие паттерны нарушений, в частности аномалии развития нейрональных сетей, дисбаланс процессов пролиферации и дифференцировки нейрональных предшественников, а также изменения в соотношении возбуждающих и тормозных нейронов.
Изучение механизмов канцерогенеза
Мини-мозг представляет собой перспективную доклиническую модель:
- для оценки эффективности противоопухолевых препаратов;
- получения более глубокого механистического понимания биологии канцерогенеза;
- генерации биобанков опухолевых органоидов, полученных от пациентов;
- исследований, связанных с разработкой лекарственных средств;
- терапии опухолей мозга в персонализированной и регенеративной медицине.
Мозговые органоиды позволяют тестировать несколько методов лечения и прогнозировать ответ на применение препарата за короткое время, а также идентифицировать средство, максимально эффективное в борьбе с опухолью мозга у конкретного индивидуума [38]. Так, органоиды, полученные из биоптатов пациентов, предоставляют микроокружение опухоли, которое имеет критическое значение для изучения механизмов инфильтрации клеток глиобластомы в здоровую ткань мозга [38, 39].
На мозговых органоидах показано, что макрофаги индуцируют прогрессию и инвазивность клеток глиобластомы в мозговых органоидах. Кармустин, AS1517499 (ингибитор Stat6) и BLZ945 (ингибитор рецептора колониестимулирующего фактора 1, Csf-1r) могут ингибировать взаимодействие между макрофагами, ассоциированными с глиобластомой, и опухолевыми клетками, что приводит к уменьшению роста опухоли и большей чувствительности к химиотерапии [40]. Кроме того, ингибитор ADAM10 предотвращает интеграцию глиальных стволовых клеток в органоиды мозга, как было показано в ортотопических ксенотрансплантационных тестах на мышах [41].
В исследовании M.S. Choe и соавт. была разработана простая трехмерная модель in vitro для лучшего воспроизведения метастазов в головном мозге с использованием раковых клеток человека и церебральных органоидов, полученных из эмбриональных стволовых клеток человека. Исследователи отмечали накопление астроцитов и их взаимодействие с раковыми клетками через коннексин 43 [42].
Последние достижения в технологии мозговых органоидов и CRISPR-геномной инженерии позволили создать генетически определенную модель глиобластомы путем введения онкогенных мутаций в церебральные органоиды с помощью CRISPR/Cas9-опосредованного мутагенеза [43].
Ключевое преимущество технологии «мини-мозг» в моделировании опухолей головного мозга заключается в способности воспроизводить сложное микроокружение опухоли, включая взаимодействия между раковыми клетками, здоровой тканью мозга и иммунными клетками. Это позволяет изучать механизмы инвазии и тестировать таргетные препараты.
Экзосомы, полученные с помощью мини-мозга, как метод коррекции заболеваний
Экзосомы – наноразмерные внеклеточные везикулы диаметром 50–150 нм, которые инкапсулируют груз из нуклеиновых кислот, белков и липидов. Многие авторы определяют экзосомы как потенциальные терапевтические мишени при различных заболеваниях. Например, показано, что экзосомная miR-124-3p микроглиального происхождения оказывает нейропротективное действие за счет влияния на сигнальный путь Rela/ApoE, тем самым смягчая повреждение нейронов и нейровоспаление [44]. Экзосомы, полученные из мезенхимальных стволовых клеток (МСК), способны снижать экспрессию глиального фибриллярного кислого белка (GFAP), подавляя секрецию ИЛ-1-бета и ФНО-альфа и уменьшая приток внутриклеточного Ca [45]. Как следствие – улучшение пространственного обучения и памяти, связанное с восстановлением функции астроцитов и митохондриального гомеостаза. Механизмы, участвующие в регуляции окислительно-восстановительного гомеостаза и воспалительных реакций, включают в себя активацию транскрипционного фактора Nrf2 и ингибирование активности ядерного фактора NF-kB. Показано, что сигнальный путь «Nrf2 – NF-kB» участвует в регуляции активации астроцитов у мышей [45]. Экзосомы, полученные из МСК, подавляют образование нейротоксичных астроцитов типа А1, индуцированных провоспалительными цитокинами (ИЛ-1-альфа, ФНО-альфа и C1q) [46].
На основании этих данных были проведены исследования по доставке нутриентов и противовоспалительных агентов к органам-мишеням. Интраназальное введение экзосом, полученных из МСК, позволило эффективно таргетировать гиппокамп, уменьшить повреждение мозга, сохранить нейрогенез и поддержать когнитивные показатели [47]. Такие положительные эффекты в основном обеспечиваются благодаря усилению выживания и дифференцировки поврежденных нейронов, ослаблению глиальной активации (впоследствии снижению нейровоспаления и окислительного стресса), активации нейроваскулярной регенерации и восстановлению системного метаболического гомеостаза [48].
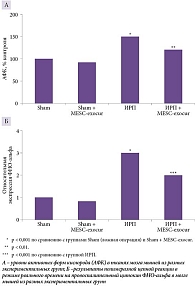
A. Kalani и соавт. проверили, можно ли с помощью MESC-exocur (куркумин, загруженный в экзосомы, полученные из эмбриональных стволовых клеток мыши) восстановить нейроваскулярные потери после ишемического реперфузионного повреждения (ИРП) у мышей. Показано, что на фоне введения MESC-exocur отмечаются снижение нейровоспаления (рис. 2), нормализация экспрессии астроцитов и нейронов (уменьшается уровень глиального фибриллярного кислого белка GFAP, увеличивается уровень NeuN-позитивных нейронов), снижение экспрессии сосудистых молекул межклеточной адгезии ICAM, сокращение потери белков плотных контактов (таких как клаудин 5 и окклюдин) [49].
Таким образом, экзосомы, полученные с помощью технологии «мини-мозг», демонстрируют значительный потенциал в коррекции неврологических заболеваний. Успешное применение экзосом, нагруженных куркумином, для восстановления функций нервных клеток после ишемического повреждения подтверждает перспективность разработки экзосомальных препаратов.
Технология получения мини-мозга
Получение клеточной культуры
Первым этапом является получение клеточной культуры. Ее основные источники – плюрипотентные эмбриональные стволовые клетки [50], нейральные стволовые клетки пуповинной крови человека [51], мультипотентные соматические стволовые клетки костного мозга, ИПСК [52]. На практике обычно применяются ИПСК, впервые полученные путем репрограммирования фибробластов кожи человека с использованием специальных факторов (OCT3/4, SOX2, KLF4 и c-MYC) в «коктейле Яманаки» [53]. Выделяют три основных метода репрограммирования [54]: трансфекцию эписомальными векторами, трансдукцию вирусом Сендай и использование матричной РНК. Полученную в результате репрограммирования клеточную культуру необходимо проверять на стерильность, плюрипотентность (репрограммированные клетки экспрессируют маркеры OCT4, NANOG, SOX2 и LIN28 до уровня, сравнимого с человеческими эмбриональными стволовыми клетками) [55], элиминацию трансгена, идентичность и генетическую стабильность.
Получение эмбриональных телец
Процесс дифференцировки эмбриональных телец (ЭТ) включает несколько этапов:
- агрегацию: дифференцировка начинается с самосборки клеточного агрегата, размер которого определяется количеством клеток, самоорганизуемых посредством рецепторов межклеточной адгезии;
- образование примитивной эндодермы;
- дифференцировку клеток примитивной энтодермы в висцеральную и париетальную эндодерму, их участие в образовании базальной мембраны;
- появление трех зародышевых листков;
- ДНК-микрочиповый анализ, указывающий, что ЭТ временно экспрессируют гены таким образом, что это воспроизводит последовательность нормального развития от формирования примитивной эктодермы до гаструляции и последующей ранней клеточной спецификации перед органогенезом.
При формировании ЭТ можно использовать метод висячей капли [56], статистическую суспензионную культуру [57], иммобилизацию в гидрогелях (метилцеллюлоза [58], фибрин [59], гиалуроновая кислота [60]). Размеры эмбриональных телец, растворимые факторы, взаимодействие с внеклеточным матриксом и клеточная адгезия – эти механизмы участвуют в контроле дифференцировки ЭТ [61].
Культивирование нервных клеток с добавлением нейротрофических факторов
Существует два основных метода дифференцировки мозговых органоидов. Первый (направленный метод) заключается в создании неуправляемых органоидов, которые используют способность ИПСК к спонтанному морфогенезу и внутренней клеточной сигнализации. Данные клетки потенциально могут развиваться в линии клеток дорсального переднего мозга, вентрального переднего мозга, среднего мозга, сосудистого сплетения, гиппокампа, сетчатки и заднего мозга [62].
Мозговые органоиды называют органоидами целого мозга, так как они спонтанно моделируют разнообразную нейральную популяцию развивающегося мозга [63]. Главный недостаток – спонтанная дифференцировка, способная привести к непредсказуемому расположению клеток внутри органоида.
Второй (ненаправленный) метод генерации органоидов мозга – управляемый подход, при котором паттернирующие факторы используются для индукции специфических клеточных линий в специфических локациях внутри органоида [64]. Эти паттерны могут воссоздавать регионы, сходные по структуре и клеточному составу с корой головного мозга, средним мозгом, глазным бокалом, сосудистым сплетением, гипоталамусом, мозжечком, ганглионарными возвышениями, таламусом и гиппокампом [65]. Основные методологии получения органоидов различных отделов головного мозга приведены в таблице [66].
Заключение
Проведенный анализ демонстрирует, что технология мозговых органоидов представляет собой перспективный инструмент в современной нейробиологии и биомедицинских исследованиях. Трехмерные модели, созданные из ИПСК, преодолевают ограничения традиционных двухмерных культур и животных моделей, обеспечивая релевантную платформу для изучения развития человеческого мозга, патогенеза заболеваний и скрининга терапевтических средств. Ключевые преимущества технологии заключаются в способности рекапитулировать сложные процессы нейроразвития, включая пролиферацию, дифференцировку, миграцию и синаптогенез. Это позволило успешно моделировать широкий спектр патологий: от нейродегенеративных заболеваний (БА и БП) и расстройств аутистического спектра до пороков развития нервной трубки и онкологических процессов.
Персонализированные органоиды, полученные от пациентов, открывают путь для изучения взаимодействия комплекса «ген – среда» и развития таргетной терапии. Особый потенциал органоидов связывают с доклиническим скринингом лекарственных препаратов, в том числе противомигренозных и противоопухолевых, что позволит прогнозировать индивидуальный ответ на терапию.
Кроме того, использование экзосом, секретируемых клетками органоидов, открывает новые горизонты для разработки методов регенеративной медицины и нейропротекции.
Несмотря на значительный прогресс, технология «мини-мозг» имеет ряд ограничений, связанных с валидностью и экстраполяцией на организм человека, отсутствием сосудистой и иммунной систем. Однако благодаря последним достижениям, связанным с использованием микрофлюидных систем, 3D-биопринтинга и кокультивирования с различными типами клеток, удалось решить часть проблемы. Речь идет о повышении физиологической релевантности и стабильности органоидов.
Таким образом, технология «мини-мозг» не только расширяет знания о развитии и патологии человеческого мозга, но и обеспечивает персонализированный подход, предлагая в каждом конкретном случае более этичные, точные и эффективные решения для выбора терапии и борьбы с заболеванием.
A.I. Prilepin
I.M. Sechenov First Moscow State Medical University
Contact person: Aleksandr I. Prilepin, prilepinsasa1@gmail.com
Mini-brain is a technology representing a three-dimensional model derived from induced pluripotent stem cells (iPSCs) for studying human brain development, disease pathogenesis, and drug screening. This technology enables the modeling of neurodegenerative disease pathogenesis: Alzheimer's disease and Parkinson's disease, viral infections, migraine, carcinogenesis, autism spectrum disorders, and also allows for the reproduction of neural tube defects under the influence of pharmaceutical drugs. Furthermore, this model reflects key processes occurring in brain cells: differentiation, migration, axonal growth, dendritic branching and synaptogenesis, intercellular interactions, myelination, as well as the influence of epigenetics on these processes. Personalized models based on iPSCs from patients with various genetic characteristics provide a unique opportunity for tailoring therapies, assessing individual drug response, and titrating drug dosage.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.