Нарушения ходьбы высшего уровня и когнитивные расстройства при болезни Паркинсона
- Аннотация
- Статья
- Ссылки
- English
![Таблица 1. Уровни организации движения [3]](/upload/resize_cache/iblock/a7f/sltggph7hayxx53sxkwg754rjvdi29p5/195_350_1/Dynin1.jpg)
![Таблица 2. Патофизиологические и клинические особенности подтипов НХВУ [3, 19, 20]](/upload/resize_cache/iblock/267/ak62ykcc89121dnm6f1h1r73vgcqm8ls/195_350_1/Dynin2.jpg)
Клиническая феноменология расстройств движения при болезни Паркинсона (БП), связанных с поражением базальных ганглиев и прогрессирующим истощением дофамина, широко известна. Типичные клинические двигательные симптомы включают тремор покоя, ригидность, брадикинезию, постуральные нарушения [1]. Изменения ходьбы при БП ассоциированы с замедленностью, осторожностью, модификацией собственно паттерна походки, обусловленного указанными проявлениями [2, 3]. Актуальна проблема оценки подобных нарушений относительно пространственных или временных аспектов контроля функции ходьбы. Сложность выявления ведущего фактора нарушений ходьбы объясняется тем, что длина шага, вероятно, относится к характеристикам, положительно реагирующим на дофаминергическую терапию. Между тем временные флюктуации походки (включая паттерн ходьбы) не всегда оправданы эффектом замещающей дофаминергической терапии [4]. Наиболее явно это прослеживается при выполнении когнитивных или иных моторных задач при ходьбе [5].
Термин «нарушение ходьбы высшего уровня» (НХВУ) объединяет в себе изменения ходьбы и постурального баланса, которые не объясняются модификацией силы, тонуса, чувствительности или координации [3]. НХВУ характеризуется различными комбинациями постуральных нарушений и локомоции. Важно, что такие изменения и при БП, и при иных нейродегенеративных и сосудистых патологиях не связаны с периферическими двигательными, сенсорными, пирамидными, мозжечковыми нарушениями или дефицитом дофамина [6]. Для обозначения указанных паттернов походки используется ряд терминов, в частности «апраксия ходьбы», «лобная атаксия», «семенящая походка», «паркинсонизм нижней половины тела» [3, 6].
Целесообразность использования термина НХВУ связана с относительной условностью применения перечисленных выше терминов, которые, по сути, описывают специфические паттерны походки, например нарушение инициации ходьбы. Иными словами, НХВУ можно рассматривать не как специфический паттерн нарушений, а как отдельную категорию нарушений походки, не объясняемых двигательным, чувствительным и в полной мере дофаминергическим дефицитом.
Классически паттерн движения формируется на трех уровнях (в порядке усложнения организации). Речь идет о периферическом моторном нейроне и двигательном нерве (простой/низший уровень организации движения), кортикоспинальном пути и базальных ганглиях (средний уровень) и префронтальной коре (высший уровень) (табл. 1) [3, 6].
Очевидно, механизм ходьбы интегрирует чувствительную и двигательную функции, что в свою очередь проявляется изменением походки при патологиях сенсорной и моторной систем на разных уровнях. Так, на простом уровне организации кроме двигательного пути в формировании механизма движения непосредственную роль играет чувствительность, обеспечивающая ориентацию в пространстве: зрительная, вестибулярная и проприоцептивная. Двигательная система низшего уровня необходима для создания силы, обеспечивающей равновесие и локомоцию. Простая чувствительность предоставляет информацию, касающуюся ориентации в пространстве и наличия опорной поверхности. На среднем уровне организации движения (базальные ядра) происходят модуляция и коррекция усилий и тонуса для изменения положения тела, поддержания равновесия и локомоции. Следует отметить, что в структуре и физиологии базальных ганглиев четко определены двигательные возбуждающие и тормозящие структуры и нейромедиаторы как по механизму действия, так и по локализации. Это позволяет влиять на двигательную активность при патологии на фоне применения не только лекарственных средств и немедикаментозной терапии, но и высокотехнологичного нейрохирургического лечения (стереотаксические операции, глубокая стимуляция мозга) [7]. При этом зоны чувствительных взаимосвязей среднего уровня (по сравнению с низшим) четко не определены. У пациентов с БП с постурально-фобическими нарушениями ходьбы на фоне повышенного риска падения, обусловленного сенсорной недостаточностью, например при зрительно-пространственных и чувствительных нарушениях (полиневропатия, нарушение зрения), может повышаться патологический тонус [8, 9]. Такая особенность, вероятно, носит защитный характер, для которого на сегодняшний день не установлено четкой прямой интегративной взаимосвязи. В свою очередь префронтальная кора (высший уровень) интерпретирует и интегрирует сенсорную информацию, что делает возможным выбор двигательного паттерна, соответствующего потенциально желаемому производимому действию [3].
Существует множество комбинаций нарушения высших корковых функций, корковых и корково-подкорковых (базальные ядра, ствол) взаимосвязей, в результате чего меняется походка и утрачивается равновесие. Многообразие вариантов нарушений взаимодействия обозначенных структур приводит к различным паттернам локомоторных и постуральных изменений. У многих пациентов с БП наблюдаются нарушения равновесия и локомоции. В частности, речь идет о замедлении ходьбы, использовании большей площади опоры, укорочении длины шага, патологических паттернах выполнения поворота (голова, туловище и таз вращаются как единое целое), нарушении равновесия, феноменах застывания и падения, которые не могут объясняться нарушениями более низкого уровня [6, 10]. Таким образом, признаки НХВУ иногда рассматриваются как единое целое. При этом наличие, степень выраженности и время появления (ухудшения/улучшения/исчезновения) общих признаков НХВУ варьируются у разных пациентов и, вероятно, отражают различия в паттерне разрушения корковых областей и их связей с нижерасположенными сенсомоторными интегративными центрами. Кроме того, для НХВУ не определены четкие топографические зоны поражения или нарушения функции.
Клиническая диагностика НХВУ затруднена, поскольку наличие патологических нарушений ходьбы и постурального баланса не связано со слабостью, спастичностью, ригидностью, изменением мышечно-суставного чувства, атаксией, брадикинезией. Нельзя забывать и о потенциальном наличии у пациента двух и более патологических феноменов одновременно (невольная «маскировка» НХВУ под поражение периферических и центральных моторных и сенсорных структур иного генеза и уровня). Что же касается БП, специалисту, возможно, проще у пациента с жалобами на нарушение ходьбы увидеть дофаминергический дефицит и придерживаться тактики коррекции дофаминергической терапии. При этом подобная тактика может оказаться ошибочной и даже нанести потенциальный вред. Наряду с традиционными побочными эффектами дофаминергических препаратов усиление дофаминергической стимуляции способно привести к ухудшению именно выраженности симптомов НХВУ – «леводопа-парадоксу» [4, 11]. Важно, что НХВУ не является самостоятельным заболеванием и может быть следствием нейродегенеративной, сосудистой, опухолевой и иной патологии [3, 12, 13].
Тяжесть и динамика развития проявлений у пациентов с НХВУ неодинаковы, вероятно, в силу индивидуальных особенностей поражения корково-подкорковых связей. Например, пациент может жаловаться на сложность инициации ходьбы, невозможность оторвать стопу от поверхности, эпизоды застываний/замираний, нарушение ходьбы при двойных моторных (ходьба + иная двигательная функция, в частности во время движения нести чашку в руках, или скандинавская ходьба) и моторно-когнитивных задачах (разговор по телефону при ходьбе, необходимость сосредоточивания на иной задаче при ходьбе) [13, 14].
В таких ситуациях кроме классического неврологического обследования для полноценной оценки нарушений ходьбы и равновесия целесообразна оценка:
- положения тела при сидении и стоянии;
- способности пациента встать из сидячего положения, особенностей походки, поворотов во время ходьбы;
- ходьбы по линии;
- реакции на пробы определения постурального баланса;
- ходьбы по меткам (цифры/буквы/цвета и т.п.);
- изменения параметров ходьбы при смене паттерна походки (поднимать высоко бедра/перешагивать объекты, совершать движения под ритм метронома или музыку) [15].
Подобные тесты при постановке диагноза используются намного реже, чем классическое неврологическое обследование. Кроме того, в специализированных медицинских учреждениях возможно обследование с использованием современных методик, информативных в аспекте контроля осевых мышц, ориентации в пространстве и гравитационном поле, а также сенсомоторной интеграции (стабилометрические платформы и интерактивные эргометрические комплексы, например C-mill VR – реабилитационный комплекс с виртуальной реальностью для восстановления навыков ходьбы и координации движений) [16].
Как уже отмечалось, диагноз НХВУ не означает отсутствия признаков нарушения более низкоуровневых функций, но указывает на то, что такие нарушения недостаточны для объяснения генеза расстройства походки. Кроме того, ряд таких расстройств может дебютировать в формате нарушений среднего уровня и со временем переходить в НХВУ. Например, при БП изначально может наблюдаться простое замедление ходьбы, которое хорошо поддается лечению препаратами леводопы, агонистами дофаминовых рецепторов и классифицируется как расстройство походки среднего уровня. Однако со временем развиваются нарушения равновесия и застывания/замирания, которые плохо поддаются дофаминергической терапии и могут расцениваться как НХВУ. Интересно, что в случае комбинированных вариантов хороший эффект оказывают препараты, влияющие как на подкорковые, так и на корковые функции. Так, амантадина сульфат воздействует на глутаматергическую систему как на среднем (в большей степени), так и на высшем уровне [17].
Несмотря на полиморфизм проявлений, специалисты на протяжении последних десятилетий предпринимают попытки классифицировать НХВУ. Согласно классификации J.G. Nutt и соавт., НХВУ подразделяют на пять подкатегорий [18]. В основу данной классификации легло описание взаимосвязи походки и предполагаемого топического происхождения. Однако при использовании этой классификации возникала сложность дифференциальной диагностики, обусловленная двумя факторами. Во-первых, анатомо-физиологические основы НХВУ изучены недостаточно. Во-вторых, по мере прогрессирования основного заболевания подтипы часто копируют друг друга. Патофизиологическая классификация, разработанная J.G. Nutt в 2001 г. и модифицированная R.J. Elble в 2007 г., подразделяет НХВУ на два подтипа – передний (лобный) и задний (височно-теменно-затылочный). Особенности каждой формы представлены в табл. 2 [3, 19, 20]. Указанные нарушения, безусловно, предполагают адаптационные механизмы, возникающие у пациентов с НХВУ [3, 20].
Упреждающая осторожность при ходьбе. Нагляднее всего представляется сравнение походки и движений в этом случае со здоровым человеком, попавшим на лед или ступившим на только что вымытый пол (скользкое покрытие). Может наблюдаться замедление походки или укорочение длины шага.
Стереотип поворота «блоком». Обычно поворот во время ходьбы обеспечивается последовательным вращением сегментов тела: сначала поворачивается голова, затем плечи, туловище и, наконец, бедра, что обеспечивает плавное и эффективное изменение направления. Стереотип поворота «блоком» характеризуется почти одновременным вращением головы, туловища и таза как единого целого. Пациенты часто делают несколько небольших, шаркающих шагов для завершения поворота, вместо того чтобы плавно поворачиваться на ногах. Наряду с этим из-за отсутствия независимого вращения позвоночника, которое в норме частично сепарирует движения верхней и нижней частей тела, происходит менее эффективный и более длительный процесс поворота.
Увеличение площади опоры. Если здоровый человек окажется на палубе корабля во время шторма, у него возникнет неопределенность времени контакта стоп с опорной поверхностью во время ходьбы. Подобный паттерн может периодически или постоянно наблюдаться у пациентов с НХВУ при обычной ходьбе как на сознательном (осознанная компенсация нарушения равновесия при ходьбе), так и на подсознательном уровне.
Чрезмерно осторожная походка. По аналогии с персистирующим постурально-перцептивным головокружением, часто возникающим на фоне перенесенной острой вестибулопатии, у пациентов с НХВУ может формироваться страх ходьбы/неустойчивости/падений. Такие нарушения в большей степени заметны у лиц, перенесших один или несколько эпизодов падений (особенно если такая ситуация привела к травме). Безусловно, личностные особенности также вносят вклад в формирование данного паттерна. Из-за страха упасть возникает необходимость держаться за других людей, опираться на стены, мебель. При этом степень выраженности нарушений ходьбы непропорциональна проявлениям осторожности. Отсюда термин – «чрезмерно осторожная походка». Важно, что оценить состояние походки и равновесия пациента сложно из-за его нежелания ходить в силу страха. Так, в ряде случаев пациенты могут предъявлять дополнительные жалобы на слабость, головокружение, неустойчивость.
Неосторожная (безрассудная/опрометчивая) походка. Дезадаптивным вариантом поведения считается неосторожная или безрассудная походка, которая связана с импульсивностью и отсутствием самокритики, особенно у пациентов с нарушениями лобной психики. Такие нарушения часто приводят к падениям из-за отсутствия страха неустойчивости.
J. Larsson и соавт. в 2025 г. опубликовали исследование распространенности НХВУ среди населения старшего возраста (65–84 лет) [21]. Согласно первичным опросникам, из 3769 человек субъективно оценили нарушения ходьбы 1510. 798 из них согласились принять участие в повторном, более основательном тестировании вместе с 249 пациентами контрольной группы, не определившими у себя нарушений ходьбы. При этом исследователи не использовали методы нейровизуализации. Выбор был сделан в пользу клинических способов оценки: неврологический осмотр, шкала оценки равновесия и ходьбы Тинетти, тест «Встань и иди» и видеозапись с оценкой паттернов ходьбы [22]. Итоговый результат был крайне интересным: в первой группе (n = 798) объективно нарушения ходьбы были выявлены у 511, во второй (n = 249) – у 50. НХВУ обнаружены у 87 человек. Такие результаты подчеркивают необходимость объективизации нарушений ходьбы специалистами, поскольку в ряде случаев (по данным исследования, до 20%) сами пациенты не способны определить у себя нарушения ходьбы. Кроме того, НХВУ корреспондировали с более значимым ухудшением показателей по гериатрической шкале депрессии – 15 [21, 23]. Согласно итоговому статическому расчету, НХВУ как причина нарушений ходьбы выявлены у 15,5% лиц с нарушениями ходьбы. Это значимые 5,8% общего количества лиц, участвовавших в исследовании изначально (всего в исследованной возрастной группе нарушения ходьбы определялись у 38% лиц).
Согласно данным современных исследований, к причинам НХВУ относят дегенеративные заболевания нервной системы, инсульт в бассейне крупной артерии, поражение малых сосудов и белого вещества, мультифокальные лакунарные инфаркты, опухоли и нормотензивную гидроцефалию [24]. Многофакторная этиология предполагает различную скорость развития клинической картины, что в парадигме оценки НХВУ может отражать темп основного патологического процесса. Так, стремительное развитие НХВУ часто связано с инсультом в стратегически важной зоне. Однако чаще клинические признаки развиваются постепенно, например при БП и сосудистом паркинсонизме. При этом описание сосудистого паркинсонизма нередко включает понятие «паркинсонизм нижней половины тела». Подобные клинические проявления в сочетании с сосудистым поражением соответствующих зон, по данным нейровизуализации, предполагают постановку данного диагноза [25]. Для сосудистого паркинсонизма характерен более короткий промежуток времени между дебютом симптоматики и постановкой диагноза, проблемы с походкой и равновесием на момент постановки диагноза, а также более поздний возраст начала заболевания, неуклонное прогрессирование, быстрое течение (раньше появляется потребность в дополнительных средствах опоры) на фоне указанного сосудистого поражения [3, 26].
Исключая вариант острого нарушения мозгового кровообращения, при котором очевидны причина и быстрая скорость развития НХВУ, иногда распознать наиболее ранние признаки НХВУ при постепенном прогрессировании достаточно сложно как пациенту, так и специалисту. Целесообразно обращать внимание:
- на осторожность пациента при ходьбе, не всегда имеющую специфическую природу;
- осознанное или неосознанное ухудшение способности поддерживать равновесие, темп и другие параметры ходьбы;
- неоднократные падения или ухудшения ходьбы/равновесия в анамнезе со слов как пациента, так и родственников (критика в отношении нарушений ходьбы может отсутствовать, что важно учитывать).
Подобные паттерны часто рассматриваются как возрастные изменения. Однако современные исследования (в том числе трехлетнее наблюдение) показывают прямую взаимосвязь степени выраженности патологических изменений белого вещества (тенденция к увеличению во времени и пространстве) головного мозга и нарушений ходьбы и равновесия у лиц старшего возраста [3, 27].
Задний (височно-теменно-затылочный) вариант НХВУ может развиться в результате острой сосудистой катастрофы (быстрое развитие) или прогрессирования хронического поражения субкортикальных малых сосудов и нейродегенеративного процесса с вовлечением данных зон (чаще стертое, незаметное начало и постепенное ухудшение). В первом случае чаще может иметь место гравицептивный неглект-синдром, или синдром отталкивания. Такой патологический паттерн наблюдается в положении сидя и стоя и характеризуется неосознанным отклонением туловища пациента от вертикали, соответствующей направлению действия силы тяжести, в сторону поражения на угол до 20° [28, 29].
В 1988 г. J.C. Masdeu и P.B. Gorelick представили данные 15 пациентов с астазией, ассоциированной с односторонним поражением таламуса, подтвержденным компьютерной томографией [30]. Поражения, включая инфаркт (n = 6), кровоизлияние (n = 7) и опухоль (n = 2), касались преимущественно верхних заднебоковых отделов таламуса, но не затрагивали дентаторуброталамический тракт. У всех пациентов отсутствовали количественные и качественные нарушения сознания и параличи, наблюдалась различная степень утраты чувствительности. Все 15 человек были неспособны находиться в положении стоя, а семь из них не сидели без посторонней помощи. Отмечались падения назад или в сторону, контралатеральную поражению, нарушения автоматизированных двигательных навыков. У пациентов с цереброваскулярной патологией регистрировалось улучшение в течение нескольких дней или недель, но сохранялась склонность к падениям в периоде реабилитации. Таким образом, был предложен термин «таламическая астазия», который также можно отнести к заднему (височно-теменно-затылочному) варианту НХВУ [31, 32].
НХВУ и повседневная активность. По данным исследований, в случайных выборках пожилых людей состояние регуляторных функций и скорости обработки информации обратно пропорционально скорости и вариабельности ходьбы [3, 33]. Решение зрительно-пространственных задач требует большей вариабельности фазы двойной опоры независимо от регуляторных функций и скорости обработки информации. Эти же исследователи показали, что влияние нарушения регуляторных функций, замедленной скорости обработки информации, нарушений памяти и зрительно-пространственного восприятия на параметры походки и равновесия значимо повышают риск частых падений [34].
Распространенным симптомом у пациентов с НХВУ является страх падения [35]. Интересно, что этот феномен может быть реакцией на ухудшение равновесия и походки, а также способствовать усилению данных нарушений. Поддержка пациента за руку, сопровождение его при ходьбе (страхование) или движение с ходунками уменьшает страх падения, но существенно не изменяет скорость ходьбы или вариативность шага. Приведенные данные подтверждают, что НХВУ не объясняются просто страхом падения [35].
Исследования показывают, что апраксию конечностей, сопряженную с поражением теменной доли и подкорковых структур (таламуса и базальных ганглиев), не следует рассматривать как НХВУ с застываниями. При этой патологии может наблюдаться двустороннее поражение медиальных отделов лобной доли [36]. Таким образом, нарушения равновесия и походки при НХВУ соответствуют широкому определению апраксии, но явно отличаются от общего понятия апраксии в контексте термина «апраксия конечности» [36].
В метаанализе A.S. Monaghan и соавт. (2023) сравнивали когнитивные функции у пациентов с БП и наличием/отсутствием застываний при ходьбе, а также оценивали влияние тяжести заболевания и приема лекарственных средств на эту взаимосвязь. В анализ было включено 145 статей (9010 пациентов) [37]. Систематический анализ показал, что у пациентов с БП с застываниями при ходьбе когнитивный дефицит выражен сильнее, чем у лиц без них. Исследователи оценили глобальные когнитивные показатели, исполнительные/регуляторные функции (управление изменением поведения), речь, память и зрительно-пространственную сферу. Прием леводопы и состояние «включения» у пациентов на более тяжелых стадиях заболевания изменяли взаимосвязь между застываниями при ходьбе и когнитивными функциями в глобальных когнитивных показателях, но не в отдельных когнитивных областях. Метаанализ подтвердил, что когнитивные функции у пациентов с БП и эпизодами застывания хуже, чем у пациентов без них, а также влияние на эту связь тяжести заболевания и приема препаратов. Однако важным аспектом в парадигме оценки применяемой лекарственной терапии является описанный в литературе «леводопа-парадокс» – потенциальное усиление выраженности НХВУ у пациентов при увеличении дозы препаратов леводопы или в периоде «включения» [4, 11]. С учетом этого необходимо оценивать роль как дофаминергической терапии, так и ацетилхолинэстеразы и антагонистов NMDA у пациентов с НХВУ.
Резюмируя изложенное, можно утверждать, что основным дискуссионным аспектом является оценка связи нарушения исполнительных/регуляторных функций (управление изменением поведения) с нарушениями параметров ходьбы и застыванием при ходьбе. Связано ли это с тем, что обе функции просто локализуются в лобной доле, или исполнительные/регуляторные функции (управление изменением поведения) и ходьба/равновесие имеют общие нейронные цепи?
В стволе головного мозга локализованы локомоторные области, стимуляция которых вызывает стереотипные постуральные и двигательные (ходьба) реакции [38]. Две из этих локомоторных областей – мезенцефальная и мозжечковая – могут быть визуализированы у человека с помощью позитронно-эмиссионной или функциональной магнитно-резонансной томографии (МРТ). Для этого испытуемому предлагается представить, что он выполняет различные двигательные паттерны (ходьба по прямой и кривой траектории, удержание равновесия, подъем по лестнице и т.п.) в момент проведения исследования [39, 40]. Для изучения патогенеза НХВУ важна оценка состояния функционально активируемых и подавляемых во время ходьбы зон головного мозга. Эти участки отвечают за преобразование ходьбы из стереотипного поведения, генерируемого локомоторными областями ствола мозга, в целенаправленную деятельность. К наиболее функционально значимым участкам относятся премоторная область, теменная кора, участвующая в зрительно-моторной интеграции, и парагиппокампальная зона (распознавание объектов и пространств) [40]. Функционально активируемые и подавляемые участки данных областей различаются при воображении пациентом стояния, ходьбы, бега или ходьбы по кривой траектории. Таким образом, различные целенаправленные движения при ходьбе и поддержании равновесия представляют сложный многокомпонентный физиологический процесс с нелинейным вовлечением ряда функционально значимых областей головного мозга. Неслучайно фенотипы нарушения равновесия и походки в структуре НХВУ зависят от зоны поражения.
Термин «лобная атаксия», или «апраксия ходьбы», часто применяемый у пациентов с НХВУ, изначально ассоциировался с обширными поражениями лобной доли, включая опухоли, абсцессы, гидроцефалию и инфаркты в бассейне передней мозговой артерии [3, 6]. С внедрением МРТ стало возможным выявление у пациентов с нарушением ходьбы и равновесия подкорковых гиперинтенсивных T2-очагов в белом веществе, особенно в перивентрикулярных и лобных областях [41]. Применение МР-трактографии (диффузно-тензорной визуализации) еще больше расширило диагностические возможности. Показано, что у пациентов с НХВУ могут иметь место патологические изменения проводящих путей подкоркового белого вещества даже в отсутствие гиперинтенсивных T2-очагов на нативных МРТ [42]. Трактографические признаки дегенерации путей в лобной доле, проходящих через переднюю часть внутренней капсулы, а также трактов в колене мозолистого тела выявлены у пациентов с сосудистым паркинсонизмом [42]. Кроме того, трактографические изменения при HХВУ могут выявляться в педункулопонтинном ядре, кортикоспинальных путях и ножках мозга [43]. У пациентов с БП с диагностированными застываниями при ходьбе, по данным МР-трактографии, обнаруживаются нарушения взаимосвязи медиальной лобной и префронтальной областей и педункулопонтинного ядра [3]. Таким образом, можно предположить, что вариабельность фенотипов переднего (лобного) варианта НХВУ обусловлена разными комбинациями и вариантами поражения вышеуказанных структур (лобная и префронтальная области, базальные, педункулопонтинное и клиновидное ядра, мозолистое тело) [3].
Количественное (недостаточная афферентация) и качественное искажение визуальной и пространственной информации затрудняет ходьбу и поддержание равновесия. За зрительно-пространственное восприятие ответственны преимущественно задние отделы головного мозга – теменная, височная и затылочная доли, функционально связанные с лобными областями.
Наиболее яркие примеры заднего (височно-теменно-затылочного) варианта НХВУ – гравицептивный неглект-синдром (синдром отталкивания) и таламическая астазия, нередко возникающие на фоне острой цереброваскулярной катастрофы [32].
Наряду с более ранними исследованиями, подтвердившими взаимосвязь поражения белого вещества лобной доли и перивентрикулярных областей и нарушений равновесия и походки, в литературе описана корреляция между поражением белого вещества в теменной доле, валике мозолистого тела и падениями [44].
Важность состояния задних мультисенсорных областей для локомоторных функций увеличивается с возрастом. В исследовании с использованием функциональной МРТ с «воображаемыми движениями» показано, что задние кортикальные области связаны с сенсорными и сенсорно-интегративными функциями, касающимися баланса и локомоции. Это может быть обусловлено локализацией функций в теменных, височных и затылочных областях коры, а также влиянием этих областей на процессы, связанные с балансом и локомоцией [3].
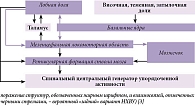
Предполагаемая схема взаимодействия функционально значимых областей головного мозга, нарушение связи которых приводит к формированию переднего (лобного) и заднего (височно-теменно-затылочного) вариантов НХВУ, представлена на рисунке [3].
■■■
НХВУ является достаточно распространенным симптомокомплексом и играет значимую роль в инвалидизации преимущественно лиц пожилого возраста. Клинический полиморфизм проявлений и различная этиологическая принадлежность осложняют диагностику НХВУ. В ряде случаев недостаточно традиционного неврологического обследования, оценки походки и равновесия, их связи с когнитивными функциями и бытовыми аспектами. Целесообразно применение нетривиальных методов оценки, таких как тест «Встань и иди», тест Тинетти двойных моторных (нести чашку с водой при ходьбе) и моторно-когнитивных (простые арифметические задачи, тесты литеральных и/или категориальных вербальных ассоциаций при ходьбе) задач. Углубленное обследование предполагает также использование современных методов диагностики и лечения: МР-трактографию, стабилометрическую платформу, интерактивный эргометрический комплекс, транскраниальную магнитную стимуляцию, системы видеозахвата, а также адекватный подбор терапии, направленной на различные звенья патогенеза (с учетом риска «леводопа-парадокса» – рациональная дофаминергическая терапия, блокаторы NMDA-рецепторов, антихолинэстеразные препараты) [16, 45–48].
P.S. Dynin, PhD, I.V. Litvinenko, PhD, Prof., V.Yu. Lobzin, PhD, Prof., N.V. Tsygan, PhD, Prof., N.V. Makeev
Military Medical Academy named after S.M. Kirov, Saint-Petersburg
Saint-Petersburg State University
Contact person: Pavel S. Dynin, pavdynin@yandex.ru
Higher-level walking disorders are a symptom complex of gait modification and postural balance unrelated to changes in strength, tone, sensitivity, or coordination. The nature of the development of the symptom complex is not entirely clear. In some cases, the diagnosis and treatment of such disorders are difficult. According to the literature, early impairments of cognitive processes such as attention, regulatory functions, and working memory are associated with changes in walking speed, potential loss of mobility, falls, and the progression of dementia. The article examines the etiopathogenesis, clinical manifestations, diagnosis of higher-level walking disorders, and the relationship of progressive walking changes with cognitive impairment in patients with Parkinson's disease and other pathologies of the nervous system. The data presented in the article from clinical practice, epidemiological studies and clinical trials show that walking impairment has a direct and inverse relationship with cognitive functions. The features and clinical patterns of higher-level walking disorders are revealed. Attention is drawn to the need for differential diagnosis with other causes of walking disorders. Modern data are presented that the quality of walking and postural reflexes reflects the state of cognitive functions, and the relationship with the risk of falls is shown. To this end, the advantages of gait assessment when performing two tasks (for example, walking while performing a cognitive-motor or dual-motor task) as a marker of fall risk are reflected. Therapeutic approaches to reducing the risk of falls by improving cognitive functions through both non-medicinal and pharmacological methods are analyzed. A comprehensive description of this problem aims to form an idea of the key features of higher-level walking disorders in Parkinson's disease and other neurodegenerative and vascular diseases.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.