Новые подходы к ведению больных ХОБЛ
- Аннотация
- Статья
- Ссылки
- English
Наиболее авторитетным источником информации по вопросам ведения пациентов с хронической обструктивной болезнью легких (ХОБЛ) является Глобальная стратегия по диагностике, лечению и профилактике заболевания (Global initiative for chronic Obstructive Lung Disease – GOLD), подготовленная ведущими международными экспертами на основе доказательных данных. Новая версия документа была опубликована в феврале 2013 г. [1]. В основе рекомендаций лежит персонализированный подход к лечению ХОБЛ, предусматривающий комбинированную оценку тяжести заболевания – степень бронхиальной обструкции, влияние заболевания на качество жизни и прогноз. Экспертами GOLD даны рекомендации по применению как традиционно используемых при ХОБЛ лекарственных препаратов, так и новых, недавно вошедших в клиническую практику. Среди новых классов лекарственных препаратов для лечения ХОБЛ особый интерес вызывают ингибиторы фосфодиэстеразы 4 типа (ФДЭ4).
Рофлумиласт: основные характеристики
Представителем ингибиторов фосфодиэстеразы 4 типа является рофлумиласт, появившийся на отечественном фармацевтическом рынке в сентябре 2011 г. Механизм его действия связан с подавлением активности ФДЭ4 – фермента, регулирующего метаболизм циклического аденозинмонофосфата (цАМФ). Накопление в клетке цАМФ сопровождается активацией клеточной протеинкиназы, осуществляющей фосфорилирование эффекторных белков. Результатом модификации белковых молекул помимо прочего является снижение продукции провоспалительных медиаторов, замедление клеточной пролиферации и апоптоза и, как следствие, уменьшение выраженности воспаления. Действие циклического нуклеотида ограничено активностью фосфодиэстеразы (ФДЭ).
В настоящее время известно 11 изоформ данного фермента, локализованных в различных органах и тканях. Преобладающей изоформой фермента, экспрессируемой провоспалительными и иммунными клетками, ответственными за развитие хронического воспаления при ХОБЛ, считается ФДЭ4. Данный тип фермента имеет несколько подтипов – A, B и D. Действие всех подтипов фермента направлено на уменьшение концентрации цАМФ, что сопровождается повышением провоспалительного потенциала клеток, в том числе нейтрофилов, Т-лимфоцитов (CD8+) и макрофагов. Высвобождая различные медиаторы, эти клетки запускают каскад воспалительных реакций, приводящих к ограничению бронхиальной проходимости и развитию системного воспаления [2]. Подавление активности ФДЭ4, напротив, способствует накоплению в клетках циклического нуклеотида и повышению противовоспалительной клеточной активности. Существует ряд препаратов, способных блокировать действие ФДЭ. Неселективным ингибитором различных типов фермента является теофиллин. В то же время активность препарата в отношении ФДЭ4, а значит, и его противовоспалительный эффект выражены слабо. Кроме того, применение теофиллина сопряжено с развитием множества различных эффектов, среди которых влияние на сократительную активность гладкой мускулатуры, мукоцилиарный клиренс, тонус кровеносных сосудов, частоту и силу сердечных сокращений, кислотность желудочного содержимого и т.д. Применение препарата ассоциируется с высоким риском развития нежелательных реакций и клинически значимых лекарственных взаимодействий. Эффективность теофиллина снижается у курильщиков.
Рофлумиласт, будучи селективным ингибитором ФДЭ4, обладает выраженной активностью в отношении всех подтипов данного фермента. Результатом действия препарата является уменьшение активности клеток, участвующих в развитии воспаления при ХОБЛ. Как показали результаты исследований, взаимодействие рофлумиласта с ФДЭ4 гладкомышечных клеток бронхов не сопровождается выраженной бронходилатацией, в связи с чем препарат не может использоваться для купирования бронхоспазма.
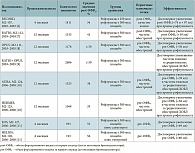
Ингибитор ФДЭ4 обладает благоприятными фармакокинетическими характеристиками. Он быстро и достаточно полно (биодоступность 80%) всасывается в желудочно-кишечном тракте. Максимальная сывороточная концентрация достигается через 0,5–2 часа после приема препарата. Подвергаясь метаболизму ферментами системы цитохрома Р450 (CYP 3A4 и 1A2), ингибитор ФДЭ4 образует активный метаболит – N-оксид рофлумиласта, превосходящий по фармакокинетическим параметрам исходную молекулу (табл. 1) [3]. Длительный период полувыведения рофлумиласта и его активного метаболита позволяет принимать препарат один раз в сутки. Элиминация препарата осуществляется преимущественно почками (70%) в виде неактивных метаболитов [4].
Участие в метаболизме рофлумиласта ферментов системы цитохрома Р450 определяет вероятность возникновения клинически значимых лекарственных взаимодействий с такими выраженными индукторами печеночных ферментов, как рифампицин, фенобарбитал и карбамазепин, а также ингибиторами CYP 3A4 и 1A2 эноксацином и циметидином. В то же время не получено данных о взаимодействии препарата с варфарином, дигоксином, теофиллином, мидазоламом, антацидами.
Наличие выраженной печеночной недостаточности (класс B и C по классификации Чайлда – Пью) сопровождается значимым увеличением максимальной концентрации в сыворотке крови (Cmax) и площади под фармакокинетической кривой «концентрация – время» (AUC0-∞) ингибитора ФДЭ4 и служит противопоказанием для его назначения. Одновременный прием пищи снижает максимальную сывороточную концентрацию рофлумиласта, не влияя на фармакокинетические характеристики его активного метаболита. Курение также не отражается на фармакокинетическом профиле ингибитора ФДЭ4 и не снижает его эффективность [5].
Данные о переносимости рофлумиласта, полученные в ходе плацебоконтролируемых исследований, представлены в табл. 2. Наиболее часто прием ингибитора ФДЭ4 ассоциируется с возникновением диареи и тошноты (10,1 и 5,2% соответственно). Кроме того, применение препарата может быть связано с развитием таких нежелательных реакций, как головокружение, головная боль, бессонница, повышение риска психических расстройств. Не получено данных о влиянии рофлумиласта на частоту возникновения инфекций дыхательных путей. Нежелательные явления (НЯ), связанные с использованием ингибитора ФДЭ4, обычно возникают в первые недели лечения и впоследствии разрешаются, не требуя отмены препарата [5].
При анализе данных клинических исследований был выявлен достаточно неожиданный эффект ингибитора ФДЭ4. У пациентов снижалась масса тела, как правило, в течение первых 6 месяцев лечения. Наиболее выраженным данный эффект оказался у пациентов, страдавших ожирением (индекс массы тела > 30 кг/м²). Прекращение приема препарата, согласно имеющимся данным, сопровождается восстановлением исходной массы тела [5].
Рофлумиласт назначается взрослым внутрь по 500 мкг один раз в сутки независимо от приема пищи. У пожилых пациентов, а также при наличии почечной недостаточности коррекция дозы препарата не требуется.
Эффективность при ХОБЛ
Доказательства эффективности рофлумиласта в лечении больных ХОБЛ получены в ходе многочисленных плацебоконтролируемых клинических исследований [6–11] (табл. 3). Анализ представленных данных свидетельствует о том, что применение препарата сопровождается достоверным увеличением объема форсированного выдоха за первую секунду (ОФВ₁) по сравнению с плацебо. Пациенты, принимавшие ингибитор ФДЭ4 в рамках проведенных исследований, имели выраженные нарушения бронхиальной проходимости (ОФВ₁ < 60% от должных значений). Достоверное улучшение вентиляционной функции легких отмечалось через четыре недели применения рофлумиласта и сохранялось на протяжении всего периода лечения. Согласно имеющимся данным, степень бронхиальной обструкции коррелирует с выраженностью воспаления в дыхательных путях, что позволяет объяснить увеличение ОФВ₁ на фоне приема препарата, не являющегося бронхолитиком.
Особого внимания заслуживает влияние ингибитора ФДЭ4 на частоту обострений заболевания. Как показали результаты недавно проведенных исследований, именно частота обострений – один из наиболее важных факторов, определяющих качество жизни больных ХОБЛ, темпы прогрессирования заболевания и связанные с ним экономические потери [12, 13]. По мнению международных экспертов, снижение частоты и тяжести обострений является одной из основных целей лечения заболевания [1].
Показано, что рофлумиласт достоверно снижает частоту тяжелых и среднетяжелых обострений ХОБЛ по сравнению с плацебо. Наиболее выраженным данный эффект оказался у пациентов, клиническая картина заболевания которых характеризовалась наличием симптомов хронического бронхита. Применение ингибитора ФДЭ4 у данной категории пациентов позволило снизить частоту обострений заболевания на 26,2%. В то же время у пациентов с эмфиземой и без хронического бронхита этот показатель составил 1,1% [9]. Более выраженный эффект рофлумиласта отмечался у пациентов, принимавших ингаляционные глюкокортикостероиды (ИГКС). Снижение частоты обострений среди пациентов, принимавших ИГКС (в дозе эквивалентной ≤ 2000 мкг беклометазона), и пациентов, не принимавших их, составило 18,8 и 7,7% соответственно [9]. Кроме того, была выявлена корреляция между снижением частоты обострений на фоне приема ингибитора ФДЭ4 и количеством обострений в анамнезе пациентов. Наличие частых обострений ХОБЛ (два и более в течение предшествовавших 12 месяцев) ассоциировалось с большей эффективностью препарата [14].
Использование ингибитора ФДЭ4 в комбинации с бронхолитиками повышает эффективность лечения заболевания. Так, добавление рофлумиласта (500 мкг один раз в сутки) к тиотропию позволило достоверно повысить пребронходилатационный ОФВ₁ по сравнению с плацебо [11]. Назначение препарата пациентам, принимавшим бета-2-агонисты длительного действия, также сопровождалось достоверным улучшением бронхиальной проходимости и снижением частоты тяжелых и среднетяжелых обострений ХОБЛ (рис. 1) [5].
Показания к применению
Одним из ключевых принципов современных рекомендаций по ведению пациентов с ХОБЛ стал персонализированный подход к лечению заболевания. Так, по мнению экспертов GOLD, основой для определения объема необходимой терапии должна стать комбинированная оценка ХОБЛ, учитывающая, помимо степени бронхиальной обструкции, влияние заболевания на качество жизни пациента и прогноз. В зависимости от выраженности симптомов, нарушений вентиляционной функции легких и частоты возникновения обострений выделяют четыре группы пациентов.
Пациентов групп A и B характеризует легкая или средняя степень бронхиальной обструкции (ОФВ₁ > 50% от должного значения) и редкие обострения ХОБЛ (0–1 в течение предшествующих 12 месяцев). Пациенты группы В отмечают также значительное влияние заболевания на качество жизни. Так, при оценке выраженности симптомов ХОБЛ с помощью теста оценки ХОБЛ (COPD Assessment Test – CAT) количество баллов составляет ≥ 10, а тяжесть одышки, определяемая по модифицированному вопроснику Британского медицинского исследовательского совета (modified Medical Research Council – mMRC), оценивается в 2 балла и выше. Для пациентов групп С и D характерны тяжелые или крайне тяжелые нарушения бронхиальной проходимости и/или частые обострения ХОБЛ (≥ 2/12 мес.), что свидетельствует о высоком риске последующих обострений заболевания. Симптомы ХОБЛ в группе C выражены слабо, в то время как в группе D они значительно влияют на качество жизни пациентов (рис. 2) [2].
Результаты исследований, посвященных оценке эффективности рофлумиласта у пациентов с ХОБЛ, свидетельствуют о том, что назначение препарата наиболее оправданно у пациентов с симптомами хронического бронхита и высоким риском обострений заболевания. Полученные данные позволили международным экспертам рекомендовать применение препарата в качестве средства дополнительной терапии ХОБЛ у пациентов групп C и D [1].
Приведем клинические примеры использования ингибитора
ФДЭ4.
Клинический случай 1
Пациент К., 1946 года рождения. Основные жалобы: одышка при умеренной физической нагрузке, кашель с отхождением слизистой мокроты. Количество баллов при оценке выраженности симптомов заболевания с помощью теста оценки ХОБЛ (CAT) – 9.
Более 30 лет назад установлен диагноз «хронический бронхит». В 2003 г. диагностирована ХОБЛ. С этого времени пациент регулярно использовал тиотропия бромид 18 мкг один раз в сутки. В течение предыдущих 12 месяцев наблюдалось три среднетяжелых обострения заболевания, характеризовавшихся усилением одышки, кашля и увеличением количества отделяемой мокроты. С целью лечения обострения ХОБЛ не госпитализировался. Пациент прекратил курить в течение года. До этого курил в течение 44 лет (по 20 сигарет в день). При выполнении пробы с 6-минутной ходьбой прошел 460 м. По данным пульсоксиметрии, степень насыщения гемоглобина кислородом до нагрузки составила 97%, после – 95%. Данные, полученные при исследовании функции внешнего дыхания до и после ингаляции бронхолитика (сальбутамол 400 мкг), представлены
на рис. 3.
Согласно полученным данным, у пациента наблюдались среднетяжелые нарушения бронхиальной проходимости (50% ≤ post-ОФВ₁ < 80% от должного значения). Проба с бронхолитиком отрицательная. Заболевание не оказывало выраженного влияния на качество жизни (CAT = 9). Вместе с тем наличие частых обострений ХОБЛ (3/12 мес.) определило принадлежность пациента к группе С (рис. 4).
В качестве средства дополнительной терапии пациенту был назначен рофлумиласт 500 мкг 1 раз в сутки. В течение последующего года на фоне комбинированного применения м-холинолитика длительного действия и ингибитора ФДЭ4 отмечалось уменьшение частоты среднетяжелых обострений заболевания (1/12 мес.).
Клинический случай 2
Пациент A., 1938 года рождения. Предъявлял жалобы на одышку при умеренной физической нагрузке, кашель с отхождением большого количества слизистой мокроты. Количество баллов при оценке выраженности симптомов заболевания с помощью теста оценки ХОБЛ – 19.
Вышеуказанные жалобы беспокоили в течение многих лет. Диагноз ХОБЛ установлен в 2002 г. Пациент регулярно принимал салметерол/флутиказона пропионат 50/250 мкг два раза в сутки. В течение предыдущих 12 месяцев отмечалось три среднетяжелых обострения заболевания, характеризовавшихся усилением одышки, увеличением количества и изменением характера отделяемой мокроты, а также одно тяжелое обострение ХОБЛ, потребовавшее госпитализации.
На момент обследования пациент являлся курильщиком (курил в течение 57 лет по 20 сигарет в день).
При выполнении пробы с 6-минутной ходьбой пациент прошел 320 м. По данным пульсоксиметрии, степень насыщения гемоглобина кислородом до нагрузки составила 95%, после – 92%. Данные, полученные при исследовании функции внешнего дыхания до и после приема бронхолитика (сальбутамол 400 мкг), представлены на рис. 5.
Полученные результаты свидетельствовали о тяжелой степени ограничения воздушного потока (post-ОФВ₁ < 50% от должного значения). Проба с бронхолитиком – отрицательная. Наличие выраженных симптомов ХОБЛ (CAT = 19), частых обострений заболевания (4/12 мес.) и тяжелой бронхиальной обструкции определили принадлежность пациента к группе D (рис. 6).
В качестве средства дополнительной терапии был назначен рофлумиласт 500 мкг один раз в сутки. В течение последующего года после назначения препарата у пациента регистрировалось только два среднетяжелых обострения ХОБЛ, госпитализаций не было.
Заключение
Персонализированный подход к лечению ХОБЛ, предложенный международными экспертами, представляется эффективным средством оптимизации ведения больных ХОБЛ. Появление рофлумиласта в арсенале средств, используемых для лечения заболевания, позволяет расширить возможности фармакотерапии у пациентов с высоким риском обострений.
Novel approaches to COPD management
A.I. Sinopalnikov, A.G. Romanovskikh
Russian Medical Academy of Postgraduate Education
Contact person: Anna Gennadyevna Romanovskikh, anngerom@gmail.com
Tailoring of treatment is one of key principles in the management of chronic obstructive pulmonary disease (COPD) set out in Global Initiative for Chronic Obstructive Lung Disease (GOLD). Tailored therapy implies that treatment should be preceded by comprehensive disease severity assessment taking into consideration airway obstruction severity and effect of the disease on quality of life and prognosis. Difficult-to-treat COPD is characterized by frequent exacerbations and/or severe airway obstruction. In such patients, novel drugs phosphodiesterase 4 inhibitors affecting specific inflammation in COPD are recommended as add-on therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.