количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Новый взгляд на хроническую тазовую боль в гинекологической практике
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Неврология и Психиатрия" №3 (32)
- Аннотация
- Статья
- Ссылки
- English
Эндометриоз – наиболее частая причина хронической тазовой боли. Представлены данные собственного исследования у 62 пациенток с эндометриозом I–IV степени распространения, продемонстрировавшие клиническую эффективность назначения в послеоперационном периоде диеногеста 2 мг/сут перорально в непрерывном режиме.
В течение 9 месяцев гормональной терапии после лапароскопии отмечался регресс тазовых болей, отсутствие рецидива исходного уровня болей. Препарат хорошо переносился. Рекомендовано долговременное лечение диеногестом пациенток с эндометриозом для профилактики рецидивов заболевания и купирования болевого синдрома после хирургического вмешательства.
В течение 9 месяцев гормональной терапии после лапароскопии отмечался регресс тазовых болей, отсутствие рецидива исходного уровня болей. Препарат хорошо переносился. Рекомендовано долговременное лечение диеногестом пациенток с эндометриозом для профилактики рецидивов заболевания и купирования болевого синдрома после хирургического вмешательства.
Эндометриоз – наиболее частая причина хронической тазовой боли. Представлены данные собственного исследования у 62 пациенток с эндометриозом I–IV степени распространения, продемонстрировавшие клиническую эффективность назначения в послеоперационном периоде диеногеста 2 мг/сут перорально в непрерывном режиме.
В течение 9 месяцев гормональной терапии после лапароскопии отмечался регресс тазовых болей, отсутствие рецидива исходного уровня болей. Препарат хорошо переносился. Рекомендовано долговременное лечение диеногестом пациенток с эндометриозом для профилактики рецидивов заболевания и купирования болевого синдрома после хирургического вмешательства.
В течение 9 месяцев гормональной терапии после лапароскопии отмечался регресс тазовых болей, отсутствие рецидива исходного уровня болей. Препарат хорошо переносился. Рекомендовано долговременное лечение диеногестом пациенток с эндометриозом для профилактики рецидивов заболевания и купирования болевого синдрома после хирургического вмешательства.
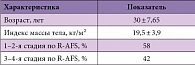
Таблица. Основные клинические характеристики обследованных женщин
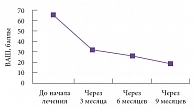
Рис. 1. Динамика профиля болевого синдрома на фоне приема диеногеста
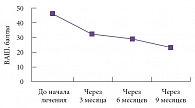
Рис. 2. Степень выраженности диспареунии на фоне приема диеногеста
Эндометриоз как причина хронической тазовой боли
Хроническая тазовая боль (ХТБ) в настоящее время является одной из важных медицинских проблем в связи с неясной этиологией, разнообразными клиническими проявлениями и высокой частотой рецидивов. Высказываются мнения о необходимости междисциплинарного подхода к ведению больных с ХТБ, который бы учитывал анатомию, физиологию и патологию тазовых органов [1].
Согласно определению Международной ассоциации по изучению боли (International Association for the Study of Pain, IASP), ХТБ представляет собой самостоятельное заболевание, проявляющееся постоянными болями в нижних отделах живота и поясницы, длящееся, по крайней мере, в течение 6 месяцев и приводящее к функциональной недееспособности или требующее медикаментозного и/или хирургического лечения [2]. Симптомы ХТБ могут значительно варьировать как у разных пациентов, так и в течение времени у одного и того же больного.
Эпидемиологическое исследование ВОЗ показало, что ХТБ встречается приблизительно у 15% женщин репродуктивного возраста [3]. Согласно результатам 40 исследований с репрезентативными группами участниц, распространенность дисменореи колебалась в различных странах от 16,8 до 81%, диспареунии – от 8 до 21,8% и нециклической тазовой боли – от 2,1 до 24%. Согласно данным Международного общества по тазовой боли (International Pelvic Pain Society), 20% всех лапароскопий, а также 10–15% гистерэктомий проводится по поводу тазовых болей. ХТБ также является причиной 10% всех обращений к гинекологу. Кроме того, многие женщины с умеренной тазовой болью не прибегают к медицинской помощи или остаются без установленного диагноза [4]. ХТБ значительно ухудшает качество жизни женщины: считается, что ХТБ коррелирует с мигренью и головной болью [5]. Кроме того, диагностика и лечение ХТБ требуют серьезных финансовых затрат: только в США на это выделяется более 2 млрд долл. ежегодно [6].
Среди причин развития ХТБ можно выделить следующие [7]:
Эндометриоз, являющийся наиболее частой причиной ХТБ, поражает 10% женщин репродуктивного возраста в целом (WERF) и 50–60% девочек-подростков и женщин с тазовой болью, охватывая период времени от менархе до пременопаузы. Всего около 176 млн женщин от 17 до 49 лет во всем мире страдают эндометриозом. По данным эпидемиологических исследований, примерно у четверти женщин с ХТБ диагностируется лапароскопически подтвержденный эндометриоз [11].
Принципы диагностики и лечения эндометриоза
Классически эндометриоз проявляется следующей триадой симптомов: киста яичника (эндометриома), бесплодие и тазовая боль. Боль, ассоциированная с эндометриозом, почти всегда начинается как менструальная боль и затем прогрессирует, не прекращаясь в лютеиновой фазе цикла. Многие женщины испытывают постоянную боль, которая обостряется в предменструальный период и во время менструации. Кроме того, у 90% женщин эндометриоз-ассоциированной боли сопутствует тяжелая дисменорея, у 40% – диспареуния.
Точность клинической диагностики эндометриоза, основанной на анамнезе и физикальном осмотре, у женщин с хронической тазовой болью составляет около 80%. Однако для верификации диагноза международными экспертами рекомендовано проведение лапароскопии с гистологическим исследованием очагов эндометриоза [10]. Проспективное когортное исследование выявило, что гистологический диагноз «эндометриоз» подтвердил наличие заболевания у 81% пациенток, прошедших хирургическое лечение по поводу эндометриоза в специализированной клинике. Исключительно визуальный диагноз во время лапароскопии имеет значительный ложноположительный уровень [12].
Согласно утверждению экспертов Американского общества по репродуктивной медицине (ASRM), «эндометриоз следует рассматривать как хроническое заболевание, которое требует разработки плана долговременного ведения пациентки с целью максимального использования медикаментозного лечения и исключения повторных хирургических вмешательств» [4]. Согласно общему мнению экспертов в области исследования эндометриоза, из-за того что патогенетические механизмы развития заболевания все еще не ясны, универсального метода лечения не существует. В этой связи вопросы лечения эндометриоза являются особенно актуальными [13, 14]. Следует отметить необходимость междисциплинарного подхода как к диагностике, так и к лечению данного заболевания. Пациенток с ХТБ должен консультировать не только гинеколог, но и невролог, уролог, психолог.
Первым этапом лечения эндометриоза является оперативное вмешательство, так как хирургический метод лечения был и остается единственной возможностью удалить морфологический субстрат эндометриоза. «Золотым стандартом» хирургического лечения остается операция, выполненная лапароскопическим доступом. С целью дифференциальной диагностики и исключения интерстициального цистита интраоперационно необходимо проведение цистоскопии. Одним из ключевых вопросов эндометриоза является проблема рецидивов. По данным различных исследователей, частота рецидивов с возобновлением симптомов после хирургического лечения через 1–2 года составляет 15–21%, через 5 лет – 36–47%, через 5–7 лет – 50–55% [15, 16].
Гормонотерапия является вторым основным компонентом комплексного лечения. Считается, что эндометриоз чаще всего развивается на фоне относительной и абсолютной гиперэстрогении при дефиците прогестерона. Именно поэтому патогенетической основой гормональной терапии является временное угнетение функции яичников, то есть уменьшение секреции эстрадиола – создание состояния «псевдоменопаузы» за счет блокады гипофизарно-яичниковой системы с инициацией гипоэстрогении, приводящее к регрессу очагов эндометриоза [17]. Отметим, что молодым пациенткам с дисменореей при отсутствии анатомических образований в малом тазу может быть рекомендован прием комбинированных оральных контрацептивов без хирургического вмешательства.
Рекомендуемые гормональные препараты (комбинированные оральные контрацептивы, даназол, гестринон, медроксипрогестерона ацетат и агонисты гонадотропин-рилизинг-гормонов) имеют сходную эффективность, однако различаются по возможности долговременного использования из-за побочных эффектов или развития непереносимости. Недавно проведенный метаанализ эффективности использования современных комбинированных оральных контрацептивов и агонистов гонадотропин-рилизинг-гормонов не выявил значимых различий в результатах лечения: оба метода терапии были одинаково эффективны для купирования болевых ощущений, связанных с эндометриозом. Эффективность лечения с использованием комбинированных оральных контрацептивов при легких формах эндометриоза и аденомиоза I степени составляет более 60%. Прогестагены также являются высокоэффективной терапией тазовой боли, связанной с эндометриозом, при ежедневном приеме в достаточной дозе [15].
Агонисты гонадотропин-рилизинг-гормонов, которые используются с начала 1980-х гг. для лечения эндометриоза, до недавнего времени считались «золотым стандартом» медикаментозной терапии (по заключению Международного консенсуса по лечению эндометриоза в Зальцбурге, 2005) [18]. Данная фармакологическая группа представлена широким спектром препаратов, различных по способу введения (Бусерелин, Супрефакт депо, Золадекс, Декапептил депо, Диферелин). Однако при их применении более 6 месяцев (без возвратной терапии эстрогенами) возникают нежелательные гипоэстрогенные эффекты: приливы, сухость влагалища, головная боль, снижение либидо, потеря минеральной плотности костной ткани [19].
В связи с тем что эндометриоз требует длительного лечения, важную роль играют безопасность и переносимость препаратов. Ведущие специалисты международных обществ к терапии первой линии относят комбинированные оральные контрацептивы и прогестагены (уровень доказательности Ia).
Впервые за последние 20 лет в нашей стране зарегистрирован препарат, который был непосредственно разработан для лечения эндометриоза. Диеногест – это прогестин, производное 19-норстерона. Диеногест имеет высокую биодоступность при пероральном применении и высокое сродство к рецепторам прогестерона. Диеногест обладает ановуляторным и антипролиферативным действием на изолированные клетки эндометрия человека, ингибирует секрецию цитокинов в клетках стромы эндометрия [20]. Эти свойства обеспечивают эффективность диеногеста в лечении эндометриоза. По рекомендациям SOGC Clinical Practice Guideline (2008) пероральная монотерапия прогестинами является терапией первой линии. Отличием диеногеста от прочих препаратов, использующихся для лечения эндометриоза, является отсутствие андрогенной активности, негативных метаболических, сосудистых и печеночных эффектов, антиандрогенное действие без минерало- и глюкокортикоидной активности, долгосрочное облегчение хронических тазовых болей, хорошая переносимость. Диеногест не обладает сопутствующим гипоэстрогенным побочным действием, таким как снижение минеральной плотности костной ткани, и не вызывает симптомов менопаузы (например, приливов), которые чаще всего развиваются во время приема препаратов агонистов гонадотропин-рилизинг-гормонов. Диеногест подходит для длительного применения благодаря своему благоприятному профилю безопасности и переносимости. Диеногест оказывает антипролиферативное и противовоспалительное действие на клетки эндометрия и эндометриоидные стромальные клетки, что позволяет использовать этот препарат целенаправленно и эффективно для лечения эндометриоза. По сравнению с другими лекарственными препаратами для лечения эндометриоза диеногест при непрерывном лечении вызывает децидуализацию эктопической ткани эндометрия и атрофию поврежденной ткани, создавая гипоэстрогенную и гиперпрогестагенную эндокринную среду. Диеногест был включен в «Консенсус по современному ведению эндометриоза» (Всемирный конгресс по эндометриозу в Монпелье) [21], который позиционирует данный препарат в качестве лекарственного препарата первой линии для лечения эндометриоза.
Еще одной группой препаратов, используемых в медикаментозном лечении боли, ассоциированной с эндометриозом, являются противовоспалительные препараты. Нестероидные противовоспалительные средства (аспирин, ибупрофен, мефенамовая кислота, напроксен, нимесулид, фенопрофен) прерывают каскад синтеза простагландинов и вызванные ими спастические боли при эндометриозе (уровень доказательности IIIа).
По данным отечественных и зарубежных авторов, целесообразным является включение антиоксидантов (витамины Е, С, пентоксифиллин и др.) в комплексное лечение наружного генитального эндометриоза, ассоциированного с ХТБ [22, 23].
Следует отметить, что помимо медикаментозного лечения пациент с хронической тазовой болью должен получать и психологическую помощь. У пациентов с ХТБ развиваются психологические изменения, которые поддерживают или увеличивают страдание от боли независимо от степени физической травмы или заболевания. Психотерапия (обычно познавательно-поведенческая терапия), наряду с традиционным хирургическим или консервативным лечением, позволяет достичь лучших результатов по сравнению с только хирургической или консервативной терапией [10].
Диеногест в послеоперационном лечении женщин с эндометриозом
Нами было проведено исследование возможности применения диеногеста в послеоперационном периоде у женщин с эндометриозом. Исследование проводилось в гинекологическом отделении (база кафедры репродуктивной медицины и хирургии МГМСУ) ГКБ № 50 Департамента здравоохранения Москвы при участии специалистов междисциплинарного Центра боли при ГКБ № 50 Москвы и Медицинского общества специалистов по дисфункциональным неврологическим расстройствам и нейростоматологии. Так, в период с ноября 2011 г. по май 2013 г. в исследование были включены 62 женщины в возрасте от 18 до 45 лет (средний возраст больных составил 30 ± 7,65 лет) с лапароскопически и гистологически верифицированным диагнозом наружного генитального эндометриоза I–IV степени распространения согласно классификации Американского общества фертильности R-AFS. Основные характеристики обследованных женщин представлены в таблице. Критериями исключения являлись беременность и лактация, злокачественные новообразования или подозрения на таковые, экстрагенитальная патология в стадии декомпенсации и системные заболевания.
Всем женщинам были выполнены операции лапароскопическим доступом. Пациентки в послеоперационном периоде получали диеногест (2 мг в сутки перорально в непрерывном режиме). Общая продолжительность лечения составила 9 месяцев. Часть пациенток продолжают его прием в настоящее время. Все пациентки при лечении должны были использовать барьерный метод контрацепции. В ходе исследования оценивалась динамика болевого синдрома, а также регистрировались побочные эффекты лечения, проводился гинекологический осмотр и ультразвуковое исследование органов малого таза трансвагинальным датчиком.
Больше всего ухудшает качество жизни при эндометриозе тазовая боль. Выраженность болевых ощущений носит субъективный характер ввиду индивидуальных различий порога болевой чувствительности, в этой связи ее трудно объективизировать. С целью проведения количественной оценки болевых симптомов, определения тяжести и интенсивности боли была использована визуальная аналоговая шкала (ВАШ), которая позволяет оценить выраженность болевого синдрома от 0 (нет боли) до 100 мм (нестерпимая боль). Оценка проводилась до лечения и каждые 3 месяца в ходе лечения. Всем пациенткам предлагалось оценить по ВАШ тяжесть дисменореи, диспареунии и интенсивность хронической тазовой боли.
До начала лечения средняя интенсивность тазовых болей по ВАШ составила 65,3 ± 11,5 балла. Этот показатель к концу лечения снизился на 18,45 ± 3,6 балла (р < 0,05). Динамика регресса болевого синдрома после комплексного лечения представлена на рисунке 1. Среднее значение ВАШ снизилось через 3 месяца от исходного уровня на 26 мм, или 39,8%, что статистически значимо (р < 0,05); через 6 месяцев – на 5 мм (7,6%); через 9 месяцев – на 13 мм (19%).
Оценка выраженности диспареунии оценивалась также через 3, 6 и 9 месяцев (рис. 2). Этот параметр, снижающий качество половой жизни, достоверно улучшался при проведении лечения диеногестом. Однако 7% пациенток отмечали ухудшение либидо в течение первых трех месяцев приема препарата.
Побочные эффекты при лечении диеногестом отметили в процессе лечения 33% женщин. Из них чаще всего (26%) регистрировались метроррагии (включая скудные выделения), наблюдавшиеся преимущественно в первые месяцы приема диеногеста. Головные боли впервые отметили 4% женщин, повышенную эмоциональную лабильность – 13%, снижение либидо – 7%.
Заключение
Наше исследование продемонстрировало клиническую эффективность диеногеста, которая проявилась в регрессе тазовых болей в течение 9 месяцев лечения. В этот период у пациенток не отмечено рецидива исходного уровня болей, у 5 женщин наступила самопроизвольная беременность.
Таким образом, комплексное лечение, включающее хирургический метод с последующей гормонотерапией современными препаратами, может быть рекомендовано для длительного лечения болевого синдрома и профилактики рецидивов эндометриоза.
Хроническая тазовая боль (ХТБ) в настоящее время является одной из важных медицинских проблем в связи с неясной этиологией, разнообразными клиническими проявлениями и высокой частотой рецидивов. Высказываются мнения о необходимости междисциплинарного подхода к ведению больных с ХТБ, который бы учитывал анатомию, физиологию и патологию тазовых органов [1].
Согласно определению Международной ассоциации по изучению боли (International Association for the Study of Pain, IASP), ХТБ представляет собой самостоятельное заболевание, проявляющееся постоянными болями в нижних отделах живота и поясницы, длящееся, по крайней мере, в течение 6 месяцев и приводящее к функциональной недееспособности или требующее медикаментозного и/или хирургического лечения [2]. Симптомы ХТБ могут значительно варьировать как у разных пациентов, так и в течение времени у одного и того же больного.
Эпидемиологическое исследование ВОЗ показало, что ХТБ встречается приблизительно у 15% женщин репродуктивного возраста [3]. Согласно результатам 40 исследований с репрезентативными группами участниц, распространенность дисменореи колебалась в различных странах от 16,8 до 81%, диспареунии – от 8 до 21,8% и нециклической тазовой боли – от 2,1 до 24%. Согласно данным Международного общества по тазовой боли (International Pelvic Pain Society), 20% всех лапароскопий, а также 10–15% гистерэктомий проводится по поводу тазовых болей. ХТБ также является причиной 10% всех обращений к гинекологу. Кроме того, многие женщины с умеренной тазовой болью не прибегают к медицинской помощи или остаются без установленного диагноза [4]. ХТБ значительно ухудшает качество жизни женщины: считается, что ХТБ коррелирует с мигренью и головной болью [5]. Кроме того, диагностика и лечение ХТБ требуют серьезных финансовых затрат: только в США на это выделяется более 2 млрд долл. ежегодно [6].
Среди причин развития ХТБ можно выделить следующие [7]:
- Гинекологические и акушерские: послеоперационная боль из-за наличия спаек, которые могут вовлекать тазовые органы и стенки; хроническая цервикальная инфекция, провоцирующая цервикальный стеноз; послеоперационное осложнение после крио/лазеро/диатермохирургического лечения; воспалительные заболевания органов малого таза (ВЗОМТ); эндометриоз и аденомиоз.
- Урологические: рецидивирующий и/или интерстициальный цистит; осложнение после хирургического лечения; нефролитиаз; мочекаменная болезнь.
- Желудочно-кишечные: синдром раздраженной толстой кишки; хроническое воспалительное заболевание кишечника, дивертикулез, полипоз.
- Сосудистые заболевания: варикозное расширение вен малого таза [8].
- Скелетно-мышечные заболевания (синдром миофасциальных болей).
- Неврологические: измененный спинной мозг и мозговая обработка стимулов у женщин с хронической тазовой болью [8].
- Психологические: депрессия и/или тревожное расстройство могут спровоцировать боль в тазовой области [9].
Эндометриоз, являющийся наиболее частой причиной ХТБ, поражает 10% женщин репродуктивного возраста в целом (WERF) и 50–60% девочек-подростков и женщин с тазовой болью, охватывая период времени от менархе до пременопаузы. Всего около 176 млн женщин от 17 до 49 лет во всем мире страдают эндометриозом. По данным эпидемиологических исследований, примерно у четверти женщин с ХТБ диагностируется лапароскопически подтвержденный эндометриоз [11].
Принципы диагностики и лечения эндометриоза
Классически эндометриоз проявляется следующей триадой симптомов: киста яичника (эндометриома), бесплодие и тазовая боль. Боль, ассоциированная с эндометриозом, почти всегда начинается как менструальная боль и затем прогрессирует, не прекращаясь в лютеиновой фазе цикла. Многие женщины испытывают постоянную боль, которая обостряется в предменструальный период и во время менструации. Кроме того, у 90% женщин эндометриоз-ассоциированной боли сопутствует тяжелая дисменорея, у 40% – диспареуния.
Точность клинической диагностики эндометриоза, основанной на анамнезе и физикальном осмотре, у женщин с хронической тазовой болью составляет около 80%. Однако для верификации диагноза международными экспертами рекомендовано проведение лапароскопии с гистологическим исследованием очагов эндометриоза [10]. Проспективное когортное исследование выявило, что гистологический диагноз «эндометриоз» подтвердил наличие заболевания у 81% пациенток, прошедших хирургическое лечение по поводу эндометриоза в специализированной клинике. Исключительно визуальный диагноз во время лапароскопии имеет значительный ложноположительный уровень [12].
Согласно утверждению экспертов Американского общества по репродуктивной медицине (ASRM), «эндометриоз следует рассматривать как хроническое заболевание, которое требует разработки плана долговременного ведения пациентки с целью максимального использования медикаментозного лечения и исключения повторных хирургических вмешательств» [4]. Согласно общему мнению экспертов в области исследования эндометриоза, из-за того что патогенетические механизмы развития заболевания все еще не ясны, универсального метода лечения не существует. В этой связи вопросы лечения эндометриоза являются особенно актуальными [13, 14]. Следует отметить необходимость междисциплинарного подхода как к диагностике, так и к лечению данного заболевания. Пациенток с ХТБ должен консультировать не только гинеколог, но и невролог, уролог, психолог.
Первым этапом лечения эндометриоза является оперативное вмешательство, так как хирургический метод лечения был и остается единственной возможностью удалить морфологический субстрат эндометриоза. «Золотым стандартом» хирургического лечения остается операция, выполненная лапароскопическим доступом. С целью дифференциальной диагностики и исключения интерстициального цистита интраоперационно необходимо проведение цистоскопии. Одним из ключевых вопросов эндометриоза является проблема рецидивов. По данным различных исследователей, частота рецидивов с возобновлением симптомов после хирургического лечения через 1–2 года составляет 15–21%, через 5 лет – 36–47%, через 5–7 лет – 50–55% [15, 16].
Гормонотерапия является вторым основным компонентом комплексного лечения. Считается, что эндометриоз чаще всего развивается на фоне относительной и абсолютной гиперэстрогении при дефиците прогестерона. Именно поэтому патогенетической основой гормональной терапии является временное угнетение функции яичников, то есть уменьшение секреции эстрадиола – создание состояния «псевдоменопаузы» за счет блокады гипофизарно-яичниковой системы с инициацией гипоэстрогении, приводящее к регрессу очагов эндометриоза [17]. Отметим, что молодым пациенткам с дисменореей при отсутствии анатомических образований в малом тазу может быть рекомендован прием комбинированных оральных контрацептивов без хирургического вмешательства.
Рекомендуемые гормональные препараты (комбинированные оральные контрацептивы, даназол, гестринон, медроксипрогестерона ацетат и агонисты гонадотропин-рилизинг-гормонов) имеют сходную эффективность, однако различаются по возможности долговременного использования из-за побочных эффектов или развития непереносимости. Недавно проведенный метаанализ эффективности использования современных комбинированных оральных контрацептивов и агонистов гонадотропин-рилизинг-гормонов не выявил значимых различий в результатах лечения: оба метода терапии были одинаково эффективны для купирования болевых ощущений, связанных с эндометриозом. Эффективность лечения с использованием комбинированных оральных контрацептивов при легких формах эндометриоза и аденомиоза I степени составляет более 60%. Прогестагены также являются высокоэффективной терапией тазовой боли, связанной с эндометриозом, при ежедневном приеме в достаточной дозе [15].
Агонисты гонадотропин-рилизинг-гормонов, которые используются с начала 1980-х гг. для лечения эндометриоза, до недавнего времени считались «золотым стандартом» медикаментозной терапии (по заключению Международного консенсуса по лечению эндометриоза в Зальцбурге, 2005) [18]. Данная фармакологическая группа представлена широким спектром препаратов, различных по способу введения (Бусерелин, Супрефакт депо, Золадекс, Декапептил депо, Диферелин). Однако при их применении более 6 месяцев (без возвратной терапии эстрогенами) возникают нежелательные гипоэстрогенные эффекты: приливы, сухость влагалища, головная боль, снижение либидо, потеря минеральной плотности костной ткани [19].
В связи с тем что эндометриоз требует длительного лечения, важную роль играют безопасность и переносимость препаратов. Ведущие специалисты международных обществ к терапии первой линии относят комбинированные оральные контрацептивы и прогестагены (уровень доказательности Ia).
Впервые за последние 20 лет в нашей стране зарегистрирован препарат, который был непосредственно разработан для лечения эндометриоза. Диеногест – это прогестин, производное 19-норстерона. Диеногест имеет высокую биодоступность при пероральном применении и высокое сродство к рецепторам прогестерона. Диеногест обладает ановуляторным и антипролиферативным действием на изолированные клетки эндометрия человека, ингибирует секрецию цитокинов в клетках стромы эндометрия [20]. Эти свойства обеспечивают эффективность диеногеста в лечении эндометриоза. По рекомендациям SOGC Clinical Practice Guideline (2008) пероральная монотерапия прогестинами является терапией первой линии. Отличием диеногеста от прочих препаратов, использующихся для лечения эндометриоза, является отсутствие андрогенной активности, негативных метаболических, сосудистых и печеночных эффектов, антиандрогенное действие без минерало- и глюкокортикоидной активности, долгосрочное облегчение хронических тазовых болей, хорошая переносимость. Диеногест не обладает сопутствующим гипоэстрогенным побочным действием, таким как снижение минеральной плотности костной ткани, и не вызывает симптомов менопаузы (например, приливов), которые чаще всего развиваются во время приема препаратов агонистов гонадотропин-рилизинг-гормонов. Диеногест подходит для длительного применения благодаря своему благоприятному профилю безопасности и переносимости. Диеногест оказывает антипролиферативное и противовоспалительное действие на клетки эндометрия и эндометриоидные стромальные клетки, что позволяет использовать этот препарат целенаправленно и эффективно для лечения эндометриоза. По сравнению с другими лекарственными препаратами для лечения эндометриоза диеногест при непрерывном лечении вызывает децидуализацию эктопической ткани эндометрия и атрофию поврежденной ткани, создавая гипоэстрогенную и гиперпрогестагенную эндокринную среду. Диеногест был включен в «Консенсус по современному ведению эндометриоза» (Всемирный конгресс по эндометриозу в Монпелье) [21], который позиционирует данный препарат в качестве лекарственного препарата первой линии для лечения эндометриоза.
Еще одной группой препаратов, используемых в медикаментозном лечении боли, ассоциированной с эндометриозом, являются противовоспалительные препараты. Нестероидные противовоспалительные средства (аспирин, ибупрофен, мефенамовая кислота, напроксен, нимесулид, фенопрофен) прерывают каскад синтеза простагландинов и вызванные ими спастические боли при эндометриозе (уровень доказательности IIIа).
По данным отечественных и зарубежных авторов, целесообразным является включение антиоксидантов (витамины Е, С, пентоксифиллин и др.) в комплексное лечение наружного генитального эндометриоза, ассоциированного с ХТБ [22, 23].
Следует отметить, что помимо медикаментозного лечения пациент с хронической тазовой болью должен получать и психологическую помощь. У пациентов с ХТБ развиваются психологические изменения, которые поддерживают или увеличивают страдание от боли независимо от степени физической травмы или заболевания. Психотерапия (обычно познавательно-поведенческая терапия), наряду с традиционным хирургическим или консервативным лечением, позволяет достичь лучших результатов по сравнению с только хирургической или консервативной терапией [10].
Диеногест в послеоперационном лечении женщин с эндометриозом
Нами было проведено исследование возможности применения диеногеста в послеоперационном периоде у женщин с эндометриозом. Исследование проводилось в гинекологическом отделении (база кафедры репродуктивной медицины и хирургии МГМСУ) ГКБ № 50 Департамента здравоохранения Москвы при участии специалистов междисциплинарного Центра боли при ГКБ № 50 Москвы и Медицинского общества специалистов по дисфункциональным неврологическим расстройствам и нейростоматологии. Так, в период с ноября 2011 г. по май 2013 г. в исследование были включены 62 женщины в возрасте от 18 до 45 лет (средний возраст больных составил 30 ± 7,65 лет) с лапароскопически и гистологически верифицированным диагнозом наружного генитального эндометриоза I–IV степени распространения согласно классификации Американского общества фертильности R-AFS. Основные характеристики обследованных женщин представлены в таблице. Критериями исключения являлись беременность и лактация, злокачественные новообразования или подозрения на таковые, экстрагенитальная патология в стадии декомпенсации и системные заболевания.
Всем женщинам были выполнены операции лапароскопическим доступом. Пациентки в послеоперационном периоде получали диеногест (2 мг в сутки перорально в непрерывном режиме). Общая продолжительность лечения составила 9 месяцев. Часть пациенток продолжают его прием в настоящее время. Все пациентки при лечении должны были использовать барьерный метод контрацепции. В ходе исследования оценивалась динамика болевого синдрома, а также регистрировались побочные эффекты лечения, проводился гинекологический осмотр и ультразвуковое исследование органов малого таза трансвагинальным датчиком.
Больше всего ухудшает качество жизни при эндометриозе тазовая боль. Выраженность болевых ощущений носит субъективный характер ввиду индивидуальных различий порога болевой чувствительности, в этой связи ее трудно объективизировать. С целью проведения количественной оценки болевых симптомов, определения тяжести и интенсивности боли была использована визуальная аналоговая шкала (ВАШ), которая позволяет оценить выраженность болевого синдрома от 0 (нет боли) до 100 мм (нестерпимая боль). Оценка проводилась до лечения и каждые 3 месяца в ходе лечения. Всем пациенткам предлагалось оценить по ВАШ тяжесть дисменореи, диспареунии и интенсивность хронической тазовой боли.
До начала лечения средняя интенсивность тазовых болей по ВАШ составила 65,3 ± 11,5 балла. Этот показатель к концу лечения снизился на 18,45 ± 3,6 балла (р < 0,05). Динамика регресса болевого синдрома после комплексного лечения представлена на рисунке 1. Среднее значение ВАШ снизилось через 3 месяца от исходного уровня на 26 мм, или 39,8%, что статистически значимо (р < 0,05); через 6 месяцев – на 5 мм (7,6%); через 9 месяцев – на 13 мм (19%).
Оценка выраженности диспареунии оценивалась также через 3, 6 и 9 месяцев (рис. 2). Этот параметр, снижающий качество половой жизни, достоверно улучшался при проведении лечения диеногестом. Однако 7% пациенток отмечали ухудшение либидо в течение первых трех месяцев приема препарата.
Побочные эффекты при лечении диеногестом отметили в процессе лечения 33% женщин. Из них чаще всего (26%) регистрировались метроррагии (включая скудные выделения), наблюдавшиеся преимущественно в первые месяцы приема диеногеста. Головные боли впервые отметили 4% женщин, повышенную эмоциональную лабильность – 13%, снижение либидо – 7%.
Заключение
Наше исследование продемонстрировало клиническую эффективность диеногеста, которая проявилась в регрессе тазовых болей в течение 9 месяцев лечения. В этот период у пациенток не отмечено рецидива исходного уровня болей, у 5 женщин наступила самопроизвольная беременность.
Таким образом, комплексное лечение, включающее хирургический метод с последующей гормонотерапией современными препаратами, может быть рекомендовано для длительного лечения болевого синдрома и профилактики рецидивов эндометриоза.
1. Neis K.J., Neis F. Chronic pelvic pain: cause, diagnosis and therapy from a gynaecologist’s and an endoscopist’s point of view // Gynecol. Endocrinol. 2009. Vol. 25. № 11. P. 757–761.
2. Flor H., Turk D.C. Chronic pain: an integrated biobehavioral approach. London: Informa Healthcare Publishing Group, 2011. 547 p.
3. Latthe P., Latthe M., Say L. et al. WHO systematic review of prevalence of chronic pelvic pain: a neglected reproductive health morbidity // BMC Public Health. 2006. Vol. 6. P. 177–184.
4. Treatment of pelvic pain associated with endometriosis / Practice Committee of the American Society for Reproductive Medicine // Fertil. Steril. 2008. Vol. 90. № 5. Suppl. P. 260–269.
5. Karp B.I., Sinaii N., Nieman L.K. et al. Migraine in women with chronic pelvic pain with and without endometriosis // Fertil. Steril. 2011. Vol. 95. № 3. P. 895–899.
6. Mathias S.D., Kuppermann M., Liberman R.F. et al. Chronic pelvic pain: prevalence, healthrelated quality of life, and economic correlates // Obstet. Gynecol. 1996. Vol. 87. № 3. P. 321–327.
7. Moore J., Kennedy S. Causes of chronic pelvic pain // Baillieres Best Pract. Res. Clin. Obstet. Gynaecol. 2000. Vol. 14. № 3. P. 389–402.
8. Stones R.W., Mountfield J. Interventions for treating chronic pelvic pain in women // Cochrane Database Syst. Rev. 2000. Vol. 4. CD000387.
9. Weijenborg P.T., Ter Kuile M.M., Stones W. A cognitive behavioural based assessment of women with chronic pelvic pain // J. Psychosom. Obstet. Gynaecol. 2009. Vol. 30. № 4. P. 262–268.
10. Howard F.M., Berkley K. Chronic abdominopelvic pain in women // Pain 2012: refresher courses, 14th world congress on pain. Seattle: IASP Press, 2012. P. 209–225.
11. Giudice L.С. Clinical practice. Endometriosis // N. Engl. J. Med. 2010. Vol. 362. № 25. P. 2389–2398.
12. Walter A.J., Hentz J.G., Magtibay P.M. et al. Endometriosis: correlation between histologic and visual findings at laparoscopy // Am. J. Obstet. Gynecol. 2001. Vol. 184. № 7. P. 1407–1411.
13. Ярмолинская М.И., Тарасова М.А., Сельков С.А. и др. Наружный генитальный эндометриоз: пособие для врачей. СПб.: Н-Л, 2010. 24 c.
14. Адамян Л.В., Андреева Е.Н., Аполихина И.А. и др. Эндометриоз: диагностика, лечение и реабилитация. Клинические рекомендации по ведению больных. М., 2013. 12 с.
15. Leyland N., Casper R., Laberge Ph. et al. Endometriosis: diagnosis and management // J. Obstet. Gynaecol. Can. 2010. Vol. 32. № 7. Suppl. 2. P. 1–32.
16. Cosson M., Querleu D., Donnez J. et al. Dienogest is as effective as triptorelin in the treatment of endometriosis after laparoscopic surgery: Results of a prospective, multicenter, randomized study // Fertil. Steril. 2002. Vol. 77. № 4. P. 684–692.
17. Адамян Л.В., Кулаков В.И. Эндометриозы: руководство для врачей. М., 1998. С. 8–32; 216–310.
18. Schweppe K.W.S. Guidelines for the use of GnRH-analogues in the management of endometriosis-results on an international consensus. Salzburg, 2005.
19. Sagsveen M., Farmer J.E., Prentice A. et al. Gonadotrophin-releasing hormone analogues for endometriosis: bone mineral density // Cochrane Database Syst. Rev. 2003. Vol. 4. CD001297.
20. Horie S., Harada T., Mitsunari M. et al. Progesterone and progestational compounds attenuate tumor necrosis factor alpha – induced interleukin – 8 production via nuclear factor kappa B inactivation in endometriotic stromal cells // Fertil. Steril. 2005. Vol. 83. № 5. P. 1530–1535.
21. Johnson N.P., Hummelshoj L. Consensus on current management of endometriosis // Hum. Reprod. 2013. Vol. 28. № 6. P. 1552–1568.
22. Адамян Л.В., Бургова Е.Н., Сонова М.М. и др. Применение антиоксидантных и противовоспалительных средств в комплексной терапии наружного генитального эндометриоза // Проблемы репродукции. Материалы третьего международного конгресса по репродуктивной медицине «Репродуктивное здоровье семьи». М., 2009. C. 162.
23. Gupta S., Agarwal A., Krajcir N. et al. Role of oxidative stress in endometriosis // Reprod. Biomed. Online. 2006. Vol. 13. № 1. P. 126–134.
A new look at chronic pelvic pain in gynecological practice
L.V. Adamyan, Kulakov Research Center for Obstetrics, Gynecology and Perinatology of the Ministry of Health of Russia
L.V. Adamyan, Kulakov Research Center for Obstetrics, Gynecology and Perinatology of the Ministry of Health of Russia
M.N. Sharov, Moscow State University of Medicine and Dentistry named after A.I. Evdokimov, City Hospital No 50, Moscow
M.M. Sonova, Moscow State University of Medicine and Dentistry named after A.I. Evdokimov
A.V. Laskevich, Moscow State University of Medicine and Dentistry named after A.I. Evdokimov, City Hospital No 50, Moscow
A.P. Ponomaryov, City Hospital No 50, Moscow
Contact person: Anastasiya Vladimirovna Laskevich, laskevichn@gmail.com
Endometriosis is the most common cause of chronic pelvic pain. The data from our research, in 62 patients with endometriosis grades I-IV, demonstrate the clinical efficacy of postoperative use of dienogest 2 mg / day orally used continuously. At 9 months post-laparoscopy, with 9 months of continuous dienogest use, patients showed regression of pelvic pain and baseline pain relapse. The drug was well tolerated. We therefore recommend long-term treatment of patients with endometriosis post laparoscopy with dienogest to prevent a recurrence of the disease and to relieve pain after surgery.
Keywords: chronic pelvic pain, endometriosis, dienogest
Contact person: Anastasiya Vladimirovna Laskevich, laskevichn@gmail.com
Endometriosis is the most common cause of chronic pelvic pain. The data from our research, in 62 patients with endometriosis grades I-IV, demonstrate the clinical efficacy of postoperative use of dienogest 2 mg / day orally used continuously. At 9 months post-laparoscopy, with 9 months of continuous dienogest use, patients showed regression of pelvic pain and baseline pain relapse. The drug was well tolerated. We therefore recommend long-term treatment of patients with endometriosis post laparoscopy with dienogest to prevent a recurrence of the disease and to relieve pain after surgery.
Keywords: chronic pelvic pain, endometriosis, dienogest
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Эндометриоз – наиболее частая причина хронической тазовой боли. Представлены данные собственного исследования у 62 пациенток с эндометриозом I–IV степени распространения, продемонстрировавшие клиническую эффективность назначения в послеоперационном периоде диеногеста 2 мг/сут перорально в непрерывном режиме.
В течение 9 месяцев гормональной терапии после лапароскопии отмечался регресс тазовых болей, отсутствие рецидива исходного уровня болей. Препарат хорошо переносился. Рекомендовано долговременное лечение диеногестом пациенток с эндометриозом для профилактики рецидивов заболевания и купирования болевого синдрома после хирургического вмешательства.
В течение 9 месяцев гормональной терапии после лапароскопии отмечался регресс тазовых болей, отсутствие рецидива исходного уровня болей. Препарат хорошо переносился. Рекомендовано долговременное лечение диеногестом пациенток с эндометриозом для профилактики рецидивов заболевания и купирования болевого синдрома после хирургического вмешательства.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
