Опыт применения лекарственного препарата Суперлимф® в комплексной терапии пациенток с гиперактивным мочевым пузырем в перименопаузе
- Аннотация
- Статья
- Ссылки
- English
В последние годы изучаются возможности комбинированной терапии, направленной на потенцирование эффекта базового препарата и улучшение состояния урогенитального тракта на основе белково-пептидного комплекса (Суперлимф®) в урологической и гинекологической практике.
Цель – оценить эффективность и безопасность комбинированной терапии ГМП у женщин в перименопаузе.
Материал и методы. В исследовании участвовало 70 пациенток с симптомами ГМП, разделенных на две равные группы. Средний возраст участниц исследования составил 49,5 ± 3,7 года. Длительность заболевания – от трех до семи лет (в среднем 4,4 ± 1,7 года). Пациентки первой группы получали Суперлимф® интравагинально по одной свече на ночь 30 дней и агонист β3-АР мирабегрон 50 мг (Бетмига 50 мг/сут) в течение трех месяцев. Пациентки второй группы принимали только агонист β3-АР мирабегрон (Бетмига 50 мг/сут) в течение трех месяцев.
Результаты. Основными жалобами пациенток были учащенное дневное мочеиспускание и ургентность. Ноктурия отмечалась у 55 (78,6%) пациенток, ургентное недержание мочи – у 9 (12,9%). Через три месяца терапии в обеих группах наблюдалось значительное клиническое улучшение. По сравнению с исходными показателями учащенное мочеиспускание снизилось на 94,3% (n = 33) в первой группе и на 88,6% (n = 31) – во второй; эпизоды ноктурии сократились на 71,4 (n = 25) и 65,7% (n = 23), а ургентные позывы – на 97,2 (n = 34) и 91,4% (n = 32) соответственно. Эпизодов ургентного недержания мочи в первой группе не зафиксировано. Во второй группе такие эпизоды зарегистрированы у 1 (2,8%) пациентки.
- Белково-пептидный комплекс Суперлимф® эффективнее монотерапии агонистами β3-АР в восстановлении функции мочевого пузыря у пациенток с ГМП в перименопаузе.
- На основании дневников мочеиспускания выявлено более выраженное снижение поллакиурии в первой группе по сравнению со второй – на 94,3 (n = 33) и 88,6% (n = 31), ургентности – на 97,2 (n = 34) и 91,4% (n = 32) соответственно. Кроме того, по данным цистометрии зафиксировано увеличение объема мочевого пузыря в обеих группах с 166,4 ± 24,2 до 305,6 ± 19,8 мл.
- Применение комплексной терапии характеризуется более выраженной эффективностью терапии ургентного недержания мочи через месяц терапии и пролонгацией клинического эффекта на срок до трех месяцев.
В последние годы изучаются возможности комбинированной терапии, направленной на потенцирование эффекта базового препарата и улучшение состояния урогенитального тракта на основе белково-пептидного комплекса (Суперлимф®) в урологической и гинекологической практике.
Цель – оценить эффективность и безопасность комбинированной терапии ГМП у женщин в перименопаузе.
Материал и методы. В исследовании участвовало 70 пациенток с симптомами ГМП, разделенных на две равные группы. Средний возраст участниц исследования составил 49,5 ± 3,7 года. Длительность заболевания – от трех до семи лет (в среднем 4,4 ± 1,7 года). Пациентки первой группы получали Суперлимф® интравагинально по одной свече на ночь 30 дней и агонист β3-АР мирабегрон 50 мг (Бетмига 50 мг/сут) в течение трех месяцев. Пациентки второй группы принимали только агонист β3-АР мирабегрон (Бетмига 50 мг/сут) в течение трех месяцев.
Результаты. Основными жалобами пациенток были учащенное дневное мочеиспускание и ургентность. Ноктурия отмечалась у 55 (78,6%) пациенток, ургентное недержание мочи – у 9 (12,9%). Через три месяца терапии в обеих группах наблюдалось значительное клиническое улучшение. По сравнению с исходными показателями учащенное мочеиспускание снизилось на 94,3% (n = 33) в первой группе и на 88,6% (n = 31) – во второй; эпизоды ноктурии сократились на 71,4 (n = 25) и 65,7% (n = 23), а ургентные позывы – на 97,2 (n = 34) и 91,4% (n = 32) соответственно. Эпизодов ургентного недержания мочи в первой группе не зафиксировано. Во второй группе такие эпизоды зарегистрированы у 1 (2,8%) пациентки.
- Белково-пептидный комплекс Суперлимф® эффективнее монотерапии агонистами β3-АР в восстановлении функции мочевого пузыря у пациенток с ГМП в перименопаузе.
- На основании дневников мочеиспускания выявлено более выраженное снижение поллакиурии в первой группе по сравнению со второй – на 94,3 (n = 33) и 88,6% (n = 31), ургентности – на 97,2 (n = 34) и 91,4% (n = 32) соответственно. Кроме того, по данным цистометрии зафиксировано увеличение объема мочевого пузыря в обеих группах с 166,4 ± 24,2 до 305,6 ± 19,8 мл.
- Применение комплексной терапии характеризуется более выраженной эффективностью терапии ургентного недержания мочи через месяц терапии и пролонгацией клинического эффекта на срок до трех месяцев.






Гиперактивный мочевой пузырь (ГМП) – хронический синдром, существенно снижающий качество жизни. Характерными симптомами ГМП являются императивные (ургентные) позывы с ургентным недержанием мочи или без него, учащенное дневное (поллакиурия) и ночное (ноктурия) мочеиспускание в отсутствие органической патологии мочеполовой системы или метаболических факторов, которые могли бы объяснить эти симптомы [1–3]. Ключевым симптомом, характеризующим ГМП, является ургентность (императивность) – внезапное и непреодолимое желание опорожнить мочевой пузырь. ГМП встречается у одной шестой части населения Европы в возрасте 40 лет и старше [4, 5]. Сходные показатели распространенности зарегистрированы и в США: симптомы ГМП отмечаются примерно у каждого шестого взрослого американца в возрасте от 45 лет [6]. Результаты крупных популяционных исследований также свидетельствуют о том, что императивное недержание мочи наблюдается у трети населения мира, причем распространенность ГМП увеличивается с возрастом [7].
Традиционно при ГМП применяют М-холинолитики и агонист β3-адренорецепторов (β3-АР). Вместе с тем с 2022 г. при ГМП используется новый вид лекарственных средств – полипептиды мочевого пузыря [8], характеризующиеся высокой эффективностью и безопасностью [9]. Несмотря на долгие годы изучения, проблема лечения ГМП до сих пор не имеет идеального решения, что обусловливает необходимость поиска новых терапевтических возможностей.
На сегодняшний день в лечении заболеваний урогенитального тракта хорошо зарекомендовал себя иммунотропный препарат Суперлимф®, представляющий комплекс противомикробных пептидов и цитокинов [10, 11].
Согласно Государственному реестру лекарственных средств, препарат Суперлимф® относится к фармакотерапевтической группе иммуномодуляторов. Он обладает противовирусным, противомикробным, противогрибковым, антиоксидантным и иммуномодулирующим действием, а также способностью подавлять воспалительную реакцию. Одним из ключевых преимуществ препарата являются его репаративные свойства [12].
Репарация – сложный, динамичный процесс, каскад сигнальных взаимодействий, поддерживаемый множеством клеточных механизмов, скоординированность которых необходима для эффективного восстановления тканей. Репаративная (восстановительная) регенерация подразумевает восстановление структурных элементов клеток и тканей после их патологической гибели, вызванной, например, хирургическим вмешательством, травмой или лучевым повреждением [13, 14].
В настоящее время изучение процессов регенерации представляет самостоятельное направление медицины – регенеративную медицину [15].
К сожалению, достижения регенеративной медицины редко доходят до практического здравоохранения, поскольку данное направление во многом остается экспериментальным. Соответствующие методы и препараты часто не включаются в клинические рекомендации, отличаются высокой стоимостью, а информация о механизмах их действия доступна преимущественно в рамках профильных образовательных мероприятий. Между тем методы регенеративной медицины направлены на полноценное восстановление структуры и функции поврежденных органов и тканей, что в свою очередь способствует повышению качества жизни пациентов, продлению их трудоспособного возраста и снижению затрат на долгосрочную терапию хронических заболеваний [16].
Способность препарата Суперлимф® влиять на процессы репарации вызывает особый интерес в контексте регенеративной медицины [17]. С учетом того, что в патогенезе ГМП у женщин в перименопаузе существенную роль играют хроническое вялотекущее воспаление и атрофические изменения уротелия, применение препаратов с репаративным действием представляется патогенетически обоснованным. Топический характер и физиологичность механизмов действия препарата Суперлимф® позволяют рассматривать его в качестве перспективного компонента комбинированной терапии, способного не только купировать симптомы, но и влиять на ключевые звенья патогенеза [18]. Действие Суперлимфа реализуется на рецепторном уровне и направлено на регуляцию системы врожденного иммунитета, что неоднократно подтверждалось в исследованиях у пациентов с хроническим рецидивирующим циститом – заболеванием, в развитии которого важную роль играет дисбаланс факторов врожденного иммунитета. Ключевой особенностью терапевтического эффекта препарата является топическая физиологическая регуляция патологического процесса [19]. Физиологичность действия лекарственного препарата выражается в локальной (топической) стимуляции функциональной активности клеток фагоцитарного ряда (моноцитов и нейтрофилов).
Хронические воспалительные и атрофические изменения являются одними из ключевых факторов развития ГМП. Это послужило основанием для проведения наблюдательного исследования по применению препарата Суперлимф® в комбинированной терапии данной патологии [20].
Цель настоящего исследования – оценить клиническую эффективность и безопасность препарата Суперлимф® в составе комплексной терапии ГМП у женщин в перименопаузе.
Материал и методы
В наблюдательное исследование было включено 70 пациенток с симптомами ГМП. Возраст участниц исследования составил 45–55 лет (средний возраст – 49,5 ± 3,7 года), длительность заболевания – от трех до семи лет (в среднем 4,4 ± 1,7 года).
Все пациентки случайным образом (метод простой фиксированной рандомизации, запечатанных конвертов) были разделены на две равные группы. Пациентки первой группы получали агонист β3-АР мирабегрон (Бетмига 50 мг утром) в течение трех месяцев и белково-пептидный препарат Суперлимф® интравагинально по одной свече на ночь 30 дней, пациентки второй – только агонист β3-АР мирабегрон (Бетмига 50 мг/сут) в течение трех месяцев.
Критерии включения в исследование:
- возраст от 45 до 55 лет включительно;
- индекс массы тела (ИМТ) ≤ 29 и ≥ 19 кг/м2;
- наличие по меньшей мере одного из симптомов ГМП:
- учащенное дневное мочеиспускание (более восьми раз);
- учащенное ночное мочеиспускание (ноктурия) (более одного раза);
- ургентные позывы;
- недержание мочи;
- отрицательный результат цитологического исследования на наличие интраэпителиального поражения/неоплазии шейки матки, полученный на скрининге или в течение шести месяцев до него;
- отрицательный результат маммографического исследования на наличие злокачественных новообразований в молочной железе, полученный на скрининге или в течение 12 месяцев до него;
- отрицательные результаты анализов на ВИЧ, гепатиты В и С, сифилис, выполненных во время скрининга или в течение трех предшествовавших месяцев;
- отсутствие вредной привычки курения на момент включения в исследование;
- согласие пациентки на использование в период исследования барьерных методов контрацепции во время полового акта;
- подписанное информированное согласие на участие в исследовании.
В исследование не включались пациентки, удовлетворявшие хотя бы одному из следующих критериев:
- установленная гиперчувствительность к любому из компонентов исследуемых препаратов;
- использование системных или вагинальных форм антибиотиков, противогрибковых или антитрихомонадных лекарственных препаратов менее чем за месяц до скрининга;
- сопутствующая патология со стороны органов малого таза (утеровагинальный пролапс 2-й степени и более);
- неконтролируемый сахарный диабет;
- клинические признаки и симптомы инфекции мочеполовой системы;
- системные заболевания соединительной ткани, красный плоский лишай, склерозирующий лихен;
- любые сопутствующие соматические заболевания или состояния, которые, по мнению врача-исследователя, затрудняют интерпретацию результатов лечения или представляют опасность для пациентки при ее участии в исследовании;
- алкогольная или наркотическая зависимость, психические заболевания;
- нежелание или неспособность пациентки (по мнению врача-исследователя) соблюдать процедуры протокола;
- участие в другом клиническом исследовании в течение трех месяцев до включения в настоящее исследование;
- прочие условия, которые, по мнению врача-исследователя, препятствуют включению пациентки в исследование.
В ходе исследования заполнялся дневник мочеиспускания в течение трех дней (табл. 1), проводились осмотр, функциональные пробы (проба Вальсальвы, кашлевая проба), комплексное уродинамическое (урофлоуметрия, цистометрия, профилометрия (для исключения стрессового недержания мочи)) и общеклиническое исследование.
Все полученные данные обработаны методом вариационной статистики.
Частота обследования пациенток с ГМП представлена в табл. 2.
Результаты
По данным заполненных анкет, у пациенток выявлены следующие симптомы нарушений мочеиспускания: учащенное мочеиспускание – 70 (100%) случаев, ноктурия – 55 (78,6%), ургентность – 70 (100%), ургентное недержание мочи – 9 (12,9%).
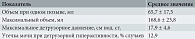
Все пациентки имели нормальную массу тела, средний вес – 72,3 кг, средние значения ИМТ – 25,6 кг/м2, средний рост – 168,7 см.
Все участницы исследования заполняли дневники мочеиспускания, где отмечали частоту и объем мочеиспусканий, наличие ургентного позыва и потери мочи в течение трех суток.
При объективном обследовании оценивали соматический анамнез, ИМТ. Экстрагенитальная патология включала хронические болезни легких (вне обострения), артериальную гипертензию (медикаментозно корригированную), хронические заболевания желудочно-кишечного тракта (вне обострения), варикозную болезнь вен нижних конечностей (без осложнений), узловой зоб щитовидной железы (медикаментозный эутиреоз). Более чем у половины женщин отмечалась ко- и полиморбидность – сочетание нескольких экстрагенитальных заболеваний.
Всем пациенткам проводилось цитологическое исследование шейки матки (по классификации Папаниколау и системе Бетесда). У подавляющего большинства женщин диагностированы атрофические или метапластические реактивные изменения слизистой оболочки шейки матки в отсутствие атипических клеток эндо- и экзоцервикса.
В ходе стандартного исследования в показателях общих анализов крови и мочи, биохимического анализа крови, гемостазиограммы клинически значимых отклонений не обнаружено. Во всех случаях каких-либо противопоказаний для включения в исследование не выявлено.
Оценка параметров комплексного уродинамического исследования
Исходно всем пациенткам проводилось комплексное уродинамическое исследование. При урофлоуметрии проводился расчет количественных показателей урофлоуграммы (табл. 3).
После выполнения урофлоуметрии определяли объем остаточной мочи. Его величина не превысила 30,0 мл.
В ходе цистометрии наполнения вычисляли детрузорное давление, цистометрическую емкость мочевого пузыря, его чувствительность, оценивали провокационные пробы (кашлевая проба, проба с водой) (табл. 4).
Фазовая детрузорная гиперактивность отмечалась у всех пациенток и характеризовалась волнообразным типом сокращений. Терминальная детрузорная гиперактивность, проявлявшаяся непроизвольным сокращением детрузора при достижении цистометрической емкости, выявлялась у всех женщин и завершалась непроизвольным мочеиспусканием у 9 (12,9%).
Оценка эффективности комбинированного лечения (агонист β3-АР и Суперлимф®) и монотерапии (агонист β3-АР)
Объективная и субъективная оценка эффективности комбинированной терапии (агонист β3-АР мирабегрон 50 мг по одной таблетке утром + Суперлимф® интравагинально по одной свече на ночь в течение 30 дней) и монотерапии (агонист β3-АР мирабегрон 50 мг по одной таблетке утром) проводилась через один и три месяца лечения, а также после его завершения. Полученные результаты представлены в табл. 5–7.
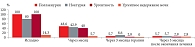
Установлено, что через месяц лечения в первой группе частота мочеиспусканий (поллакиурия) снизилась на 51,4% (n = 18) по сравнению с исходными показателями, эпизоды ноктурии сократились на 37,1% (n = 13) (р < 0,05). Положительная динамика отмечалась у пациенток с ургентностью (снижение частоты на 60%) (n = 21) и ургентным недержанием мочи (снижение на 8,6%) (n = 3) (р < 0,05). Во второй группе через месяц лечения также отмечалось снижение частоты мочеиспусканий на 42,9% (n = 15) по сравнению с исходными показателями и эпизодов ноктурии на 28,5% (n = 10) (р < 0,05). Частота ургентности снизилась на 51,4% (n = 18), ургентного недержания мочи на 2,8% (n = 1) (р < 0,05). Несмотря на значительное улучшение, симптомы ГМП сохранялись при всех схемах лечения через месяц терапии (р > 0,05) (рис. 1 и 2).
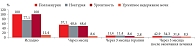
Через три месяца лечения у пациенток обеих групп отмечалось значительное клиническое улучшение: частота мочеиспусканий снизилась на 94,3% (n = 33) в первой группе и на 88,6% (n = 31) – во второй по сравнению с исходными показателями, эпизодов ноктурии – на 71,4 (n = 25) и 65,7% (n = 23), ургентности – на 97,2 (n = 34) и 91,4% (n = 32) соответственно. Эпизодов ургентного недержания мочи в первой группе не зафиксировано. У 1 (2,8%) пациентки второй группы такие эпизоды имели место.
В исследовании продемонстрирована более высокая эффективность комбинированной терапии (агонист β3-АР мирабегрон 50 мг + Суперлимф®) у пациенток с симптомами ГМП через три месяца по сравнению с монотерапией мирабегроном (р < 0,05).
Положительная динамика в отношении основных симптомов ГМП – поллакиурии и ургентности – отмечалась уже через месяц терапии в обеих группах (статистически значимо по сравнению с исходными данными), но значительно более выраженной была у пациенток первой группы, получавших комбинированное лечение (рис. 1).
Через три месяца терапии оба вида лечения продемонстрировали сопоставимую эффективность, однако более быстрое нивелирование всех симптомов ГМП отмечалось в группе комбинированной терапии. Так, частота возникновения основных симптомов ГМП – поллакиурии и ургентности – снизилась в первой группе на 94,3 (n = 33) и 97,2% (n = 34), во второй – на 88,6 (n = 31) и 91,4% (n = 32) соответственно.
По окончании лечения анализировалось возникновение потенциальных побочных эффектов препаратов. Нежелательных явлений ни в одной из групп не выявлено.
Контрольные показатели стандартного лабораторного обследования, включая биохимический анализ крови, гемостазиограмму, общий анализ мочи, через три месяца лечения у всех пациенток находились в пределах нормативных значений и не имели существенных различий.
Через три месяца после окончания терапии (четвертый визит) было проведено обследование всех пациенток для оценки продолжительности терапевтического эффекта двух режимов лечения – комбинированного (мирабегрон + Суперлимф®) и монотерапии (мирабегрон). К этому сроку оба вида терапии продемонстрировали сопоставимую эффективность, однако более длительное отсутствие симптомов ГМП зафиксировано в группе комбинированной терапии. Так, возобновление поллакиурии зарегистрировано у 2 (5,7%) пациенток первой группы и 15 (42,9%) – второй; ургентности – у 1 (2,8%) и 11 (31,4%) соответственно. Всем пациенткам с рецидивом симптомов был предложен пролонгированный курс лечения мирабегроном (агонистом β3-АР) в сочетании с препаратом Суперлимф® (по одной свече интравагинально на ночь в течение 30 дней).
Безопасность препарата Суперлимф® оценивали у всех пациенток первой группы. Нежелательных явлений не зарегистрировано, отмечалась высокая приверженность терапии.
Выводы
В ходе настоящего исследования установлено:
- У пациенток с проявлениями ГМП преобладали учащенное мочеиспускание (100%) и ургентность (100%). Ноктурия отмечалась у 55 (78,6%) женщин, ургентное недержание мочи – у 9 (12,9%).
- Эффективность комбинированной терапии (мирабегрон и Суперлимф®) в отношении основных симптомов ГПМ у женщин в период перименопаузы статистически значимо превосходит таковую монотерапии мирабегроном.
- Комбинированная схема терапии демонстрирует три ключевых преимущества: более выраженное купирование симптомов ГМП у пациенток через один и три месяца лечения в первой группе, высокую скорость наступления эффекта при поллакиурии (через месяц) (18 (51,4%) пациенток в первой группе и 15 (42,8%) – во второй) и пролонгированное сохранение результата по истечении трех месяцев после окончания терапии и возобновление поллакиурии (2 (5,7%) случая в первой группе и 15 (42,9%) – во второй).
- Комбинированная терапия характеризуется удовлетворительным профилем безопасности и может быть рекомендована в целях повышения эффективности стандартной терапии ГМП, особенно у пациенток с сопутствующими урогенитальными нарушениями, характерными для перименопаузального периода.
Заключение
Расстройства мочеиспускания представляют собой важнейшую междисциплинарную проблему современной медицины, особенно для таких направлений, как гинекология, урология и геронтология. Существует много теорий патогенеза ГМП, однако ни одна из них не признана ведущей. В контексте предиктивной и профилактической медицины выявление факторов риска нарушений мочеиспускания у женщин становится ключевой задачей для снижения их частоты и оптимизации затрат на лечение.
До настоящего времени основными классами препаратов, применяемых при ГМП, считались антихолинергические (антимускариновые) средства и β3-адреномиметики. Однако применение антимускариновых препаратов ассоциировано с феноменом «антихолинергической нагрузки», способствующим развитию когнитивных нарушений [21]. В свою очередь колебания артериального давления у ряда пациенток, использующих агонисты β3-АР, могут негативно отразиться на приемлемости лечения. Между тем ГМП – хроническое заболевание, требующее длительной и приемлемой терапии.
Приемлемость – это многогранная конструкция, позволяющая пациентам и медицинским работникам оценивать степень целесообразности вмешательства исходя из ожидаемых или испытанных когнитивных и эмоциональных реакций на него. Возможно, комбинированная терапия (агонист β3-АР мирабегрон 50 мг и Суперлимф®) будет отличаться более высокой приемлемостью по сравнению с монотерапией агонистом β3-АР (мирабегрон 50 мг) вследствие более высокой эффективности и пролонгирования положительного результата.
Полученные нами данные согласуются с мнением исследователей, связывающих пролонгированный эффект комбинированной терапии со специфической реакцией уротелия и инициацией каскада регуляторных процессов, необходимых для восстановления локального врожденного иммунитета, структуры и функции клеток, регуляции передачи нервно-мышечного сигнала и паракринной регуляции органа, то есть стойкого улучшения функционального взаимодействия клеток уротелия, субуротелиального пространства, миоцитов детрузора и нейронов, осуществляющих контроль над сократительной активностью детрузора [22]. Очевидно, исследования эффективности комбинированной терапии будут продолжены, что позволит получить более точное представление о механизме действия препарата Суперлимф®.
E.V. Tikhomirova, PhD, V.E. Balan, PhD, Prof., E.A. Chulkova, PhD, M.A. Orlyuk, PhD, O.V. Abanina, PhD, E.K. Moiseeva, V.YA. Yatsyuk, PhD, Prof., V.A. Komarov
Moscow University ‘Synergy’
Moscow Regional Research and Clinical Institute
Kursk State Medical University
Russian University of Medicine
Contact person: Elena V. Tikhomirova, heltik03@gmail.com
Relevance. Overactive bladder (OAB) is a common chronic condition that significantly reduces the quality of life of patients. The diagnosis is based on the presence of imperative urges, frequent daytime urination, nocturia and urgent urinary incontinence in the absence of obvious local pathology or metabolic disorders. Progressive estrogen deficiency in perimenopause leads to atrophic changes in the tissues of the lower urinary tract, rich in estrogen receptors. Traditionally, a beta-3-adrenergic receptor (β3-AR) agonist is used for OAB. However, there is evidence of the effectiveness of polypeptide preparations. Experimental studies have shown that Superlymph® (a fraction of antimicrobial peptides and a natural cytokine complex) is characterized by a wide range of effects on cells involved in innate immunity reactions and improvement of tissue microcirculation. In recent years, the possibilities of combination therapy aimed at potentiating the effect of the base drug and improving the condition of the urogenital tract based on the protein-peptide complex (Superlymph®) in urological and gynecological practice have been studied.
The aim is to evaluate the efficacy and safety of combination therapy of OAB in perimenopausal women.
Material and methods. The study involved 70 patients with symptoms of OAB, divided into two equal groups. The average age of the study participants was 49.5 ± 3.7 years. The duration of the disease is from three to seven years (on average 4.4 ± 1.7 years). Patients of the first group received Superlymph®, one vaginal suppository at night for 30 days, and the β3-AR agonist mirabegron 50 mg (Betmiga 50 mg/day) for three months. The patients of the second group took only the β3-AR agonist mirabegron (Betmiga 50 mg/day) for three months.
Results. The main complaints of the patients were frequent daytime urination and urgency. Nocturia was observed in 55 (78,6%) patients, urgent urinary incontinence – in 9 (12.9%). After three months of therapy, significant clinical improvement was observed in both groups. Compared to baseline, the frequency of urination decreased by 94.3% (n = 33) in the first group and by 88.6% (n = 31) in the second; nocturia episodes decreased by 71.4 (n = 25) and 65.7% (n = 23), and urge to urinate decreased by 97.2 (n = 34) and 91.4% (n = 32), respectively. There were no episodes of urgent urinary incontinence in the first group. In the second group, such episodes were registered in 1 (2.8%) patient.
Conclusions. Based on the results, the following conclusions were drawn:
- In contrast to monotherapy with β3-AR agonists, the use of the protein-peptide complex Superlymph® showed a higher effectiveness in restoring bladder function in patients with OAB in the perimenopausal period.
- Based on the urination diaries, a more pronounced decrease in pollakiuria was observed in the first group (by 94,3%; n = 33) compared to the second group (88,6%; n = 31), a decrease in urgency of 97.2 (n = 34) and 91.4% (n = 32), respectively, and an increase in bladder volume in both groups from 166.4 ± 24.2 to 305.6 ± 19.8 ml, according to cystometry data.
- The use of complex therapy is characterized by a significant decrease in the severity of urgency incontinence after 1 month of therapy and an extension of the clinical effect for up to 3 months.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.