Оценка эффективности и безопасности комбинированного применения биологически активной добавки Витисурин и препарата Суперлимф у женщин с неосложненным циститом: открытое проспективное наблюдательное исследование
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В открытое проспективное несравнительное наблюдательное исследование включены 30 женщин в возрасте 27–50 лет (средний возраст 38,9 ± 5,1 года) с клиническими и лабораторными признаками неосложненного цистита. Пациентки получали Витисурин по 2,8 г внутрь один раз в сутки и Суперлимф по 25 ЕД ректально один раз в сутки в течение 20 дней. Оценка проводилась на трех визитах (V1 – исходно, V2 – 11-й день, V3 – 21-й день). Анализировались показатели шкалы оценки симптомов острого цистита (Acute Cystitis Symptom Score, ACSS), шкалы симптомов тазовой боли (ШСТБ), индекс качества жизни (Quality of Life, QoL), дневник симптомов, данные общего анализа мочи и бактериологического исследования. Статистическая обработка выполнена с применением критерия Вилкоксона; уровень значимости p < 0,05.
Результаты. Исследование завершили 29 пациенток. К 21-му дню отмечено статистически значимое снижение среднего балла ACSS (9,31 ± 1,64 против 0,69 ± 0,71; p < 0,001), показателя по ШСТБ (6,55 ± 2,63 против 0,76 ± 0,94; p < 0,001) и показателя дневника симптомов (6,38 ± 1,78 против 0,55 ± 0,57; p < 0,001). Индекс QoL увеличился с 5,21 ± 1,92 до 8,59 ± 1,32 (p < 0,001). Частота положительных посевов снизилась с 93,3 до 34,5%. Зарегистрировано одно нежелательное явление легкой степени; серьезных нежелательных явлений не выявлено.
Заключение. В условиях открытого несравнительного исследования применение комбинации сопровождалось положительной динамикой симптомов и лабораторных показателей при хорошей переносимости. Результаты носят описательный характер и требуют подтверждения в рандомизированных контролируемых исследованиях.
Материал и методы. В открытое проспективное несравнительное наблюдательное исследование включены 30 женщин в возрасте 27–50 лет (средний возраст 38,9 ± 5,1 года) с клиническими и лабораторными признаками неосложненного цистита. Пациентки получали Витисурин по 2,8 г внутрь один раз в сутки и Суперлимф по 25 ЕД ректально один раз в сутки в течение 20 дней. Оценка проводилась на трех визитах (V1 – исходно, V2 – 11-й день, V3 – 21-й день). Анализировались показатели шкалы оценки симптомов острого цистита (Acute Cystitis Symptom Score, ACSS), шкалы симптомов тазовой боли (ШСТБ), индекс качества жизни (Quality of Life, QoL), дневник симптомов, данные общего анализа мочи и бактериологического исследования. Статистическая обработка выполнена с применением критерия Вилкоксона; уровень значимости p < 0,05.
Результаты. Исследование завершили 29 пациенток. К 21-му дню отмечено статистически значимое снижение среднего балла ACSS (9,31 ± 1,64 против 0,69 ± 0,71; p < 0,001), показателя по ШСТБ (6,55 ± 2,63 против 0,76 ± 0,94; p < 0,001) и показателя дневника симптомов (6,38 ± 1,78 против 0,55 ± 0,57; p < 0,001). Индекс QoL увеличился с 5,21 ± 1,92 до 8,59 ± 1,32 (p < 0,001). Частота положительных посевов снизилась с 93,3 до 34,5%. Зарегистрировано одно нежелательное явление легкой степени; серьезных нежелательных явлений не выявлено.
Заключение. В условиях открытого несравнительного исследования применение комбинации сопровождалось положительной динамикой симптомов и лабораторных показателей при хорошей переносимости. Результаты носят описательный характер и требуют подтверждения в рандомизированных контролируемых исследованиях.

Введение
Неосложненный острый цистит относится к наиболее распространенным формам инфекций мочевыводящих путей (ИМП) у женщин. По эпидемиологическим данным, до 50–60% женщин переносят хотя бы один эпизод ИМП в течение жизни, а у 20–30% развивается рецидив в течение последующих 6–12 месяцев [1–3]. Основным этиологическим агентом остается Escherichia coli (70–90% случаев), реже выделяются представители родов Klebsiella, Proteus, Enterococcus [4]. Несмотря на высокую эффективность краткосрочной антибактериальной терапии, глобальный рост антибиотикорезистентности уропатогенов, в том числе штаммов, продуцирующих β-лактамазы расширенного спектра, представляет серьезную клиническую проблему [1]. В рекомендациях Европейской ассоциации урологии (European Association of Urology, EAU) подчеркивается необходимость рационального применения антимикробных препаратов и поиск альтернативных или адъювантных подходов к ведению пациенток с неосложненными ИМП [1].
С патофизиологической точки зрения острый цистит является результатом каскада последовательных процессов: периуретральной колонизации, восходящего инфицирования, адгезии бактерий к уротелию посредством фимбрий типа 1, внутриклеточной инвазии и формирования бактериальных сообществ и биопленок [4, 5]. Последующая активация Toll-подобных рецепторов 4 типа и сигнальных путей NF-κB приводит к высвобождению провоспалительных цитокинов (интерлейкинов) ИЛ-6, ИЛ-8, что обусловливает развитие воспалительного ответа и клинической симптоматики – дизурии, учащенного мочеиспускания и тазовой боли [4, 5]. В современных представлениях о патогенезе ИМП также подчеркивается роль мукозального иммунитета и дисбаланса локальной иммунной регуляции в поддержании воспаления и формировании рецидивирующего течения [5]. В этой связи интерес представляют препараты и биологически активные добавки, потенциально способные модифицировать воспалительную реакцию, поддерживать барьерную функцию уротелия и способствовать снижению выраженности симптомов.
В последние годы все больше внимания уделяется поиску альтернативных методов лечения ИМП, позволяющих избегать применения антибиотиков или сокращать время их использования.
Одним из альтернативных препаратов для лечения ИМП является Суперлимф – лекарственный препарат, применяемый в клинической практике при хроническом рецидивирующем неосложненном цистите для увеличения длительности ремиссий. Его можно применять как в монотерапии, так и в комбинации с антибиотиками, что приводит к усилению их действия и, следовательно, к уменьшению длительности антибактериальной терапии. Суперлимф® является иммуномодулятором, представляет собой естественный комплекс природных противомикробных пептидов и цитокинов – универсальных стимуляторов иммунной системы с активностью фактора, угнетающего миграцию макрофагов, интерлейкина 1 (ИЛ-1), ИЛ-6, фактора некроза опухоли (ФНО), трансформирующего фактора роста, секретируемых лейкоцитами периферической крови свиньи. Обладает противовирусным, противомикробным и противогрибковым действием. Препарат стимулирует функциональную активность клеток фагоцитарного ряда (моноцитов и нейтрофилов): активирует фагоцитоз, выработку цитокинов (ИЛ-1, ФНО), индуцирует противоопухолевую цитотоксичность макрофагов, регулирует миграцию клеток в очаг воспаления, увеличивает активность естественных киллеров. Препарат обладает антиоксидантной активностью, снижает развитие воспалительных реакций, стимулирует регенерацию и эпителизацию раневых дефектов.
Другое альтернативное направление в лечении и профилактике ИМП – это применение биологически активных добавок (БАД), содержащих D-маннозу, проантоцианидины и витамины. Например, Витисурин содержит D-маннозу, витамин С, экстракты виноградных косточек, клюквы и листьев толокнянки.
D-манноза, блокируя взаимодействие фимбрий бактериальной клетки с уротелием, препятствует адгезии бактерий к слизистой оболочке и их колонизации. Образованный комплекс D-манноза – Escherichia coli «смывается» током мочи, тем самым предотвращая абсорбцию различных бактерий (уропатогенных штаммов Escherichia coli, Pseudomonas aeruginosa, Shigella, Leischmania, Mycobacterium и других) на поверхности тканей, что позволяет предупреждать развитие рецидива инфекций мочеполовых путей [6, 7].
Активные компоненты клюквы обладают доказанно выраженным противовоспалительным действием, снижая уровень С-реактивного белка (высокочувствительного показателя повреждения тканей при воспалении) и интерлейкинов. Проантоцианидины препятствуют адгезии кишечной палочки (E. coli) к клеткам уротелия за счет блокирования P-фимбрий бактериальной клетки. Листья толокнянки содержат гликозид арбутин, органические кислоты, дубильные вещества. Арбутин оказывает антисептическое, противовоспалительное и диуретическое действие в отношении мочевыводящих путей.
Комбинацию иммуномодулятора (Суперлимф) и БАД, содержащих D-маннозу, экстракты клюквы и виноградной косточки, в клинической практике можно рассматривать как альтернативу антибиотикотерапии, особенно у пациенток с аллергией и антибиотикорезистентными штаммами, а также для снижения частоты использования антибиотикотерапии при периодических рецидивах циститов.
Таким образом, комбинированные терапевтические подходы, сочетающие противовоспалительный и иммуномодулирующий потенциал, требуют клинической оценки в условиях реальной практики. Проведение наблюдательных исследований позволяет получить предварительные данные о клинической динамике и переносимости подобных схем.
Материал и методы
Дизайн исследования – открытое проспективное несравнительное наблюдательное. Критерии включения: женщины старше 18 лет; клинические признаки неосложненного цистита и аллергия или непереносимость антибиотиков в анамнезе; лабораторное подтверждение лейкоцитурии и/или бактериурии. Информированное согласие получено от всех участниц исследования.
Схема терапии: Витисурин 2,8 г перорально один раз в сутки; Суперлимф 25 ЕД ректально один раз в сутки; продолжительностью 20 дней. Первичные конечные точки: изменение показателей по шкале оценки симптомов острого цистита (Acute Cystitis Symptom Score, ACSS); динамика лабораторных показателей. Вторичные конечные точки: динамика показателей по шкале симптомов тазовой боли (ШСТБ), индекса качества жизни (Quality of Life, QoL), частота нежелательных явлений.
Статистический анализ проводился с применением критерия Вилкоксона. Данные представлены в виде M ± SD. Статистическая значимость – p < 0,05.
Исследование завершили 29 пациенток (96,7%). Одна пациентка выбыла из наблюдения по личным причинам, не связанным с безопасностью или переносимостью терапии. Таким образом, анализ эффективности и безопасности проводился в группе из 29 участниц.
Средний возраст пациенток составил 38,9 ± 5,1 года. У большинства участниц отмечалась типичная клиническая картина неосложненного цистита, включавшая дизурию, учащенное мочеиспускание, императивные позывы и болевые ощущения в надлобковой области. При лабораторном обследовании у всех пациенток исходно выявлена лейкоцитурия (в среднем 26,1 лейкоцита в п/зр), а у подавляющего большинства участниц подтверждена бактериурия (концентрация Escherichia coli – 105 КОЕ/мл).
Результаты
Динамика клинических показателей
При анализе показателей шкал симптомов отмечена выраженная положительная динамика в течение периода наблюдения. Уже к промежуточному визиту на 11-й день терапии (V2) отмечалась достоверная положительная динамика по всем оцениваемым шкалам: балл ACSS снизился в среднем на 54,5% (с 9,31 ± 1,64 до 4,24 ± 1,85; p < 0,001), ШСТБ – на 51,0% (с 6,55 ± 2,63 до 3,21 ± 1,98; p < 0,001), балл дневника симптомов – на 51,9% (с 6,38 ± 1,78 до 3,07 ± 1,62; p < 0,001). Одновременно достоверно улучшилось качество жизни (с 5,21 ± 1,92 до 7,38 ± 1,65; p < 0,001), отмечалась тенденция к уменьшению выраженности симптомов, включая снижение частоты дизурии и интенсивности тазовой боли. К завершению курса терапии (V3, 21-й день) наблюдалось статистически значимое улучшение по всем анализируемым клиническим шкалам. Средний суммарный балл ACSS снизился с 9,31 ± 1,64 на исходном визите до 0,69 ± 0,71 к V3 (p < 0,001). Абсолютное снижение показателя составило более 8 баллов, что соответствует выраженному клиническому улучшению и практически полному регрессу симптомов у большинства пациенток. Аналогичная динамика отмечена по ШСТБ. Средний показатель уменьшился с 6,55 ± 2,63 до 0,76 ± 0,94 (p < 0,001), что свидетельствует о значительном снижении болевого синдрома и уменьшении выраженности воспалительного процесса. По данным дневников симптомов, заполнявшихся пациентками в ходе исследования, также отмечалось последовательное уменьшение частоты и интенсивности дизурических проявлений. Средний показатель снизился с 6,38 ± 1,78 до 0,55 ± 0,57 (p < 0,001). Отдельного внимания заслуживает динамика QoL. На исходном визите большинство пациенток отмечали выраженное влияние симптомов заболевания на повседневную активность, включая ограничение физической активности, нарушение сна и снижение работоспособности. К 21-му дню индекс QoL увеличился с 5,21 ± 1,92 до 8,59 ± 1,32 (p < 0,001), что отражает значительное субъективное улучшение состояния и уменьшение влияния заболевания на повседневную жизнь. В совокупности полученные данные свидетельствуют о выраженной клинической эффективности наблюдаемой терапевтической схемы (рис. 1).
Динамика лабораторных показателей
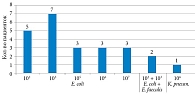
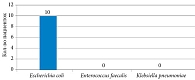
Положительная динамика была отмечена и по результатам лабораторных исследований мочи. По данным общего анализа, исходно у всех пациенток регистрировалась значимая лейкоцитурия (среднее значение – 26,1 лейкоцита в п/зр), что соответствовало активному воспалительному процессу в нижних мочевых путях. В ходе наблюдения отмечалась выраженная тенденция к нормализации лабораторных показателей. К завершению терапии лейкоцитурия сохранилась лишь у трех пациенток, то есть частота лейкоцитурии снизилась со 100% до 10,3%. Микробиологическое исследование мочи показало снижение частоты положительных бактериологических посевов с 80,0% (24/30) на исходном визите до 34,5% (10/29) к 21-му дню терапии. Основным возбудителем был Escherichia coli, выявленный у 23 женщин (95,8% среди положительных посевов), в том числе у двух пациенток – в ассоциации с Enterococcus faecalis. У одной пациентки была обнаружена монокультура Klebsiella pneumoniae (рис. 2). К 21-му дню терапии бактериурия сохранялась у 10 (34,5%) из 29 пациенток, во всех случаях обусловленная E. coli; другие патогены, включая K. pneumoniae и E. faecalis, на фоне терапии не обнаруживались (рис. 3).
У 14 (58,3%) из 24 пациенток с исходно положительным бактериологическим посевом к 21-му дню терапии наблюдалась полная элиминация патогена. У остальных 10 (41,7%) женщин сохранялась моноинфекция Escherichia coli, однако во всех случаях отмечалось снижение титра (от 105–107 до 102–105 КОЕ/мл). Ассоциативные формы (с Enterococcus faecalis) и Klebsiella pneumoniae к завершению курса терапии не выявлялись. Данные изменения лабораторных показателей согласуются с динамикой клинических симптомов и могут указывать на снижение активности инфекционно-воспалительного процесса в мочевом пузыре.
Безопасность и переносимость терапии
Оценка безопасности проводилась на протяжении всего периода наблюдения. Нежелательное явление было зарегистрировано у одной (3,3%) пациентки и характеризовалось легкой степенью выраженности. Данное событие не потребовало отмены терапии или проведения дополнительных медицинских вмешательств.
Серьезных нежелательных явлений, а также случаев прекращения терапии по причине плохой переносимости зарегистрировано не было. В целом комбинация исследуемых средств продемонстрировала благоприятный профиль безопасности и хорошую переносимость у большинства участниц исследования.
Обсуждение
Полученные результаты демонстрируют статистически значимое снижение выраженности клинических проявлений неосложненного цистита в течение 20-дневного курса комбинированной терапии. Выраженная положительная динамика показателей ACSS и ШСТБ свидетельствует о регрессе как дизурических, так и болевых симптомов заболевания. Снижение суммарного балла ACSS более чем на 8 пунктов может рассматриваться как клинически значимое улучшение состояния пациенток. В исследованиях, посвященных клинической валидности шкалы ACSS, показано, что изменение данного показателя отражает динамику симптомов и может использоваться для оценки эффективности терапии при остром цистите [8]. В нашем исследовании практически полное исчезновение симптомов к 21-му дню наблюдения сопровождалось выраженным снижением показателей дневников симптомов и шкалы тазовой боли.
Важным аспектом полученных результатов является значительное улучшение показателей качества жизни. Известно, что острый цистит оказывает выраженное влияние на повседневную активность женщин, включая нарушения сна, снижение работоспособности и ограничение социальной активности. Улучшение индекса QoL в ходе исследования отражает уменьшение субъективных симптомов и подтверждает клиническую значимость наблюдаемой динамики. С точки зрения патофизиологии инфекции мочевых путей уменьшение выраженности симптомов может быть связано со снижением активности локального воспалительного ответа уротелия. В экспериментальных и клинических исследованиях показано, что взаимодействие уропатогенных бактерий с клетками уротелия активирует Toll-подобные рецепторы и внутриклеточные сигнальные пути, приводящие к высвобождению провоспалительных цитокинов, включая ИЛ-6 и ИЛ-8 [4, 5]. Эти медиаторы играют ключевую роль в формировании клинических проявлений заболевания. Потенциальное влияние терапии на воспалительные механизмы может способствовать более быстрому купированию симптоматики. Отдельного внимания заслуживает выявленная динамика микробиологических показателей. Снижение частоты положительных бактериологических посевов с 93,3 до 34,5% может указывать на уменьшение бактериальной персистенции в мочевых путях.
По данным исследования Х.С. Ибишева и соавт. [9], у пациенток с установленным диагнозом «хронический цистит» в моменте обострения, получавших фосфомицина трометамол 3 г однократно с последующим наблюдением в течение трех недель, частота отрицательного посева мочи достигала 72,2%. В проведенном исследовании после комплексного применения препарата Суперлимф и БАД Витисурин к 21-му дню терапии частота отрицательного посева мочи приблизилась к 65,5%, что является сравнимым результатом с однократным воздействием фосфомицина трометамола на бактериальную персистенцию в мочевых путях.
В ряде клинических исследований показано, что у части пациенток острый цистит может иметь тенденцию к самостоятельному разрешению без антибактериальной терапии [10, 11]. Иногда лечение без назначения антибиотиков следует рассматривать как приемлемый вариант лечения цистита, который необходимо обсудить с пациентом. В последние годы в научной литературе активно обсуждаются возможности использования неантибактериальных подходов в лечении и профилактике инфекций мочевых путей. Это связано с глобальным ростом антибиотикорезистентности уропатогенов и необходимостью поиска альтернативных или адъювантных терапевтических стратегий. Согласно современным рекомендациям и обзорам, перспективными направлениями являются применение фитопрепаратов, иммуномодуляторов и средств, направленных на восстановление барьерной функции уротелия [10, 11].
Т.С. Перепанова и соавт. [12] в недавнем обзоре оценили высокую эффективность и безопасность препарата Суперлимф, его успешность в комплексном лечении больных хроническим циститом подтверждена в целом ряде работ [13–16].
К.П. Тевлин и соавт. [13] продемонстрировали действенность монотерапии препаратом Суперлимф хронического рецидивирующего цистита у женщин по сравнению со стандартным лечением, а также доказали снижение уровня метаплазии уротелия к концу 20-дневного курса цитокинотерапии, что свидетельствует о репаративных свойствах препарата, способствующих увеличению межрецидивного периода.
В нашем исследовании, касающемся применения препарата Суперлимф в комплексной терапии с БАД Витисурин (без применения антибиотиков), мы получили следующие данные: к концу терапии Витисурином в комплексе с Суперлимфом лейкоцитурия сохранялась лишь у 10,3% пациенток, что свидетельствует о выраженном противовоспалительном эффекте применяемого курса. В своем исследовании Е.В. Кульчавеня и соавт. [17] установили, что при монотерапии препаратом Суперлимф хронического цистита рецидив хронического цистита был купирован у 86,7% пациенток и только в 13,3% наблюдений потребовалось дополнительное назначение антибактериальных препаратов.
В последние годы для лечения и профилактики ИМП широко используются D-манноза, витамины, экстракты клюквы и другие фитоэкстракты. М.Н. Слесаревская и соавт. [18] показали, что назначение комбинированного БАД, содержащего D-маннозу, витамин D и экстракт клюквы, пациентам с инфекциями нижних мочевых путей при обострении цистита представляется патогенетически обоснованной альтернативой использованию антибиотиков в качестве первого этапа лечения до получения результатов микробиологического исследования мочи.
В настоящем исследовании подтверждена высокая эффективность и безопасность применения комбинации препарата Суперлимф и БАД Витисурин у женщин с неосложненным циститом в качестве альтернативы антибиотикотерапии.
В контексте этих данных наблюдаемое уменьшение симптомов и улучшение лабораторных показателей может свидетельствовать о потенциальной роли комбинированных терапевтических подходов, направленных не только на подавление бактериального роста, но и на модуляцию воспалительного ответа слизистой оболочки мочевого пузыря. С практической точки зрения полученные результаты подтверждают целесообразность дальнейшего изучения комбинированных схем терапии, включающих препараты с противовоспалительным и иммуномодулирующим потенциалом. Подобные стратегии могут рассматриваться как альтернатива к стандартным методам лечения или как компонент комплексного подхода к ведению пациенток с неосложненными ИМП.
Следует учитывать ряд ограничений настоящего исследования. Прежде всего, работа имеет открытый несравнительный дизайн и относительно небольшой объем выборки. Кроме того, не проводились стратификация возбудителей и анализ их антибиотикочувствительности, что могло бы дополнительно уточнить микробиологические аспекты заболевания. Однако именно в ситуации, когда чувствительность микроорганизмов к антибиотикам неизвестна, является целесообразным включение в схему терапии иммуномодулятора Суперлимф, который, благодаря присутствию антимикробных пептидов в своем составе, позволяет преодолеть антибиотикорезистентность возбудителей.
Полученные данные демонстрируют благоприятный профиль переносимости исследуемой комбинации и выраженную положительную динамику клинических показателей. В дальнейшем представляется целесообразным проведение рандомизированных контролируемых исследований с более длительным периодом наблюдения, включающих оценку частоты рецидивов инфекции, динамики уровня воспалительных маркеров и количественной бактериурии.
Заключение
Комбинированное применение комбинации БАД Витисурин и препарата Суперлимф в качестве альтернативы антибиотикотерапии в рамках наблюдательного исследования ассоциировалось с регрессом клинической симптоматики и улучшением лабораторных показателей при хорошей переносимости.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
S.P. Darenkov, PhD, Prof., E.A. Pronkin, PhD, A.M. Domnikova, PhD
Central State Medical Academy of Department of Presidential Affairs, Moscow
Lopukhin Federal Research and Clinical Center of Physical-Chemical Medicine of Federal Medical Biological Agency, Moscow
Contact person: Evgeny A. Pronkin, dr.pronkin@gmail.com
Aim. To evaluate the clinical outcomes and tolerability of a 20-day combined administration of the dietary supplement Vitisurin and the immunomodulatory drug Superlymph in women with uncomplicated cystitis.
Material and methods. An open-label prospective non-comparative observational study included 30 women aged 27–50 years (mean age 38.9 ± 5.1 years) with clinical and laboratory signs of uncomplicated cystitis. Patients received Vitisurin 2.8 g orally once daily and Superlymph 25 IU rectally once daily for 20 days. Assessments were performed at three visits (V1 – baseline, V2 – day 11, V3 – day 21). Outcomes included the Acute Cystitis Symptom Score (ACSS), pelvic pain symptom scale, quality-of-life (QoL) index, symptom diary data, urinalysis, and urine culture results. Statistical analysis was performed using the Wilcoxon test, with significance set at p < 0.05.
Results. Twenty-nine patients completed the study. By day 21, a statistically significant reduction in symptom severity was observed. The mean ACSS score decreased from 9.31 ± 1.64 at baseline to 0.69 ± 0.71 (p < 0.001). Pelvic pain scores decreased from 6.55 ± 2.63 to 0.76 ± 0.94 (p < 0.001), and symptom diary scores from 6.38 ± 1.78 to 0.55 ± 0.57 (p < 0.001). The QoL index improved from 5.21 ± 1.92 to 8.59 ± 1.32 (p < 0.001). The proportion of positive urine cultures decreased from 93.3% to 34.5%. One mild adverse event was reported; no serious adverse events occurred.
Conclusion. In this open observational study, the combined use of Vitisurin and Superlymph was associated with improvement of clinical symptoms and laboratory parameters in women with uncomplicated cystitis and demonstrated good tolerability. The findings are preliminary and require confirmation in randomized controlled trials.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.