Опыт применения препарата Нурдати® в реальной клинической практике
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В публикации представлен клинический опыт применения препарата Нурдати® у шести пациентов. На момент начала комбинированной иммунотерапии группа характеризовалась гетерогенностью по возрасту, клинической стадии заболевания, объему предшествующей терапии и наличию сопутствующей патологии. Представлены результаты проводимого лечения, включая оценку эффективности, продолжительность терапии, а также профиль нежелательных явлений (НЯ) и методы их коррекции.
Результаты. Терапия препаратом Нурдати® характеризовалась эффективностью и удовлетворительным профилем безопасности, что подтверждает потенциал режима в реальной клинической практике онколога.
Обсуждение. Комбинированная иммунотерапия нурулимабом и пролголимабом продемонстрировала клиническую эффективность с достижением частичного регресса у одного пациента и стабилизации опухолевого процесса у трех больных. Прогрессирование заболевания после двух и одного цикла лечения установлено у двух пациентов. У большинства пациентов иммуноопосредованные НЯ не наблюдались. Только в двух случаях отмечены НЯ 2–3-й степени, которые были успешно купированы стандартной терапией.
Материал и методы. В публикации представлен клинический опыт применения препарата Нурдати® у шести пациентов. На момент начала комбинированной иммунотерапии группа характеризовалась гетерогенностью по возрасту, клинической стадии заболевания, объему предшествующей терапии и наличию сопутствующей патологии. Представлены результаты проводимого лечения, включая оценку эффективности, продолжительность терапии, а также профиль нежелательных явлений (НЯ) и методы их коррекции.
Результаты. Терапия препаратом Нурдати® характеризовалась эффективностью и удовлетворительным профилем безопасности, что подтверждает потенциал режима в реальной клинической практике онколога.
Обсуждение. Комбинированная иммунотерапия нурулимабом и пролголимабом продемонстрировала клиническую эффективность с достижением частичного регресса у одного пациента и стабилизации опухолевого процесса у трех больных. Прогрессирование заболевания после двух и одного цикла лечения установлено у двух пациентов. У большинства пациентов иммуноопосредованные НЯ не наблюдались. Только в двух случаях отмечены НЯ 2–3-й степени, которые были успешно купированы стандартной терапией.
Введение
Меланома относится к агрессивным злокачественным опухолям кожи и занимает одно из ведущих мест среди онкологических заболеваний в возрастной группе 15–29 лет. Частота ее выявления существенно увеличивается с возрастом [1, 2]. По статистическим данным 2023 г., в России было зарегистрировано 13 270 новых случаев меланомы, при этом у 7,9% пациентов заболевание было диагностировано уже на IV стадии [1]. Несмотря на значительный прогресс в развитии лекарственной терапии онкологических заболеваний, возможности эффективного лечения больных неоперабельными и метастатическими формами меланомы по-прежнему остаются ограниченными [2, 3]. В настоящее время в качестве приоритетной опции первой линии лечения пациентов с неоперабельной и метастатической меланомой рассматривается применение ингибиторов контрольных точек иммунного ответа вне зависимости от молекулярно-генетических характеристик опухоли, в том числе статуса мутаций BRAF V600 [4]. Наибольшую клиническую эффективность демонстрирует комбинированная иммунотерапия с использованием моноклональных антител, ингибирующих PD-1 и CTLA-4 [3].
Доказательная база данного подхода сформирована на основании результатов крупных рандомизированных клинических исследований, таких как CheckMate 067 и CheckMate 069, в которых продемонстрировано преимущество комбинированной иммунотерапии перед монотерапией ингибиторами CTLA-4 по ключевым показателям, включая выживаемость без прогрессирования (ВБП) и общую выживаемость (ОВ) [5–7].
В реальной клинической практике наиболее широко применяется режим с использованием ипилимумаба 3 мг/кг в комбинации с ниволумабом 1 мг/кг, однако частота развития иммуноопосредованных нежелательных явлений (НЯ) 3–4-й степени при применении данного режима достигает 48%. Согласно результатам рандомизированного исследования III фазы CheckMate 511, применение альтернативного режима с ипилимумабом 1 мг/кг и ниволумабом 3 мг/кг ассоциировано со снижением частоты НЯ 3–4-й степени с 48% до 34%. Однако снижается и частота объективных ответов (с 50,6% до 45,6%), что также заслуживает внимания при определении тактики лечения [8].
Именно выраженная токсичность комбинированной иммунотерапии представляет собой значимую клиническую проблему как для пациентов, так и для практикующих специалистов, что ограничивает ее широкое применение в рутинной клинической практике, несмотря на высокую эффективность. В связи с этим современные исследования направлены на оптимизацию терапевтических режимов с целью снижения частоты и тяжести НЯ без потери эффективности лечения.
В России до 2023 г. единственной опцией комбинированной иммунотерапии являлась схема с применением ингибиторов CTLA-4 (ипилимумаба) и PD-1 (ниволумаба). 12 декабря 2023 г. в Российской Федерации был зарегистрирован оригинальный отечественный комбинированный препарат Нурдати® (международное непатентованное наименование нурулимаб + пролголимаб), разработанный АО «БИОКАД», показанный для лечения пациентов с неоперабельной или метастатической меланомой. Согласно результатам клинического исследования II фазы (OBERTON/BCD-217), фиксированная комбинация нурулимаба (ингибитора CTLA-4) и пролголимаба (ингибитора PD-1) в соотношении 1:3 продемонстрировала более высокую эффективность по сравнению с монотерапией ингибиторами PD-1 в первой линии терапии у пациентов с неоперабельной или метастатической меланомой.
Один из действующих компонентов комбинации BCD-217 пролголимаб был зарегистрирован в Российской Федерации в 2020 г. для терапии пациентов с неоперабельной или метастатической меланомой [9]. Пролголимаб относится к ингибиторам PD-1 и представляет собой полностью человеческое моноклональное антитело. В отличие от других представителей данной группы он относится к подклассу IgG1, что обусловливает его повышенную стабильность. Дополнительной особенностью препарата является наличие мутации LALA в Fc-фрагменте, которая приводит к снижению эффекторных свойств антитела и, как следствие, к уменьшению риска разрушения PD-1-позитивных лимфоцитов [10]. Второй компонент комбинации – препарат нурулимаб, который является оригинальным отечественным ингибитором CTLA-4, представляет собой моноклональное антитело изотипа IgG1 с модифицированным Fc-фрагментом.
Препарат был изучен в режиме монотерапии в рамках клинического исследования I фазы (NCT03472027), целью которого являлась оценка его фармакокинетических и фармакодинамических характеристик, а также определение максимально переносимой дозы лекарственного средства [11]. Преимуществом комбинации нурулимаба и пролголимаба является то, что это единственная в мире комбинация ингибиторов CTLA-4 и PD-1 в одном флаконе, что обеспечивает удобство применения, экономит время медицинского персонала на введение, а также исключает риски отсутствия одного из компонентов при проведении терапии.
Согласно результатам рандомизированного многоцентрового двойного слепого плацебо-контролируемого исследования III фазы № BCD-217-2/OCTAVA, применение комбинации нурулимаба и пролголимаба (0,2 мл/кг 1 раз в 3 недели, четыре инфузии) с последующей поддерживающей терапией пролголимабом (1 мг/кг каждые 2 недели) обеспечило значимое увеличение ВБП по сравнению с монотерапией пролголимабом.
Медиана ВБП составила 15,4 мес. при комбинированной терапии препаратом Нурдати® (95%-ный доверительный интервал (ДИ) 8,4; НД) против 8,3 мес. в группе получающих монотерапию пролголимабом (95% ДИ 4,2; 14,8, iRECIST). Двухлетняя ВБП достигла 43,9% в группе комбинированной терапии и 35,3% при монотерапии пролголимабом.
Медиана ОВ в обеих группах на момент анализа не была достигнута, при этом 24-месячная ОВ составила 76,1% и 71,7% соответственно.
Общая частота ответов составила 54,2 (95% ДИ 45,3; 62,9) в группе, получавшей комбинированную иммунотерапию, и 43,24% (95% ДИ 34,6; 52,1) в группе, получавшей пролголимаб по критериям iRECIST. Полный ответ был зарегистрирован у 17,6% пациентов, получавших Нурдати®, и у 9,8% пациентов, получавших монотерапию. Частичный ответ был зарегистрирован у 36,6% пациентов в группе, получавшей Нурдати®, и у 33,3% пациентов в группе, получавшей пролголимаб в режиме монотерапии. Комбинированная терапия также продемонстрировала преимущество по частоте контроля над заболеванием: 78,6% (95% ДИ 70,6; 85,3) против 61,4% (95% ДИ 52,5; 69,7). Медиана длительности ответа не была достигнута в обеих группах. Медиана времени достижения ответа на терапию по критериям iRECIST в группе комбинированной иммунотерапии составила 2,1 мес. (95% ДИ 1,5; 2,8) против 2,8 мес. (95% ДИ 1,7; 2,9) при монотерапии.
Профиль безопасности оставался приемлемым при применении комбинированной иммунотерапии: НЯ ≥ 3 степени наблюдались у 31,1% пациентов, серьезные НЯ – у 19,3%, а прекращение терапии вследствие токсичности потребовалось лишь в 11,1% случаев [12]. При сопоставлении полученных данных с результатами исследований CheckMate 067 и CheckMate 511 в группе ниволумаба и ипилимумаба обращает на себя внимание более высокая частота развития НЯ: серьезные НЯ регистрировались в 74% и 47,8% случаев, а отмена терапии вследствие токсичности – в 38% и 24% случаев соответственно.
Препарат Нурдати® является новой опцией комбинированной иммунотерапии метастатической меланомы.
Материал и методы
В данной публикации представлен уникальный клинический опыт лечения шести пациентов препаратом Нурдати® (нурулимаб + пролголимаб).
Пациент Л., 65 лет
Анамнез заболевания: считает себя больным с 2021 г., когда самостоятельно выявил новообразование кожи верхней части спины слева. К врачам более двух лет не обращался. В 2023 г. в связи с быстрым ростом новообразования в течение 6 мес. и изменением его цвета обратился к терапевту по месту жительства и был направлен к онкологу. В апреле 2023 г. выполнена эксцизионная биопсия новообразования кожи спины. Послеоперационное гистологическое заключение: неизъязвленная узловая смешанная меланома кожи спины со слабой внутриопухолевой лимфоидной инфильтрацией, высокой митотической активностью (3 митоза на 1 мм2 опухоли). Уровень инвазии по Кларку V, толщина по Бреслоу 11 мм. Лимфоваскулярная и периневральная инвазия не выявлены. Края резекции вне опухоли (рТ4а). По данным проведенного дообследования отдаленных метастазов не выявлено. В Федеральном онкологическом центре выполнена реэксцизия послеоперационного рубца кожи спины с биопсией сигнальных лимфатических узлов левой подмышечной области в июле 2023 г. Согласно результатам гистологического исследования, обнаружен метастаз меланомы кожи спины в одном сигнальном лимфоузле левой подмышечной области, 4 мм в наибольшем измерении, с выходом за пределы капсулы лимфоузла. Выполнено молекулярно-генетическое исследование, по результатам которого обнаружена мутация в гене NRAS и не выявлена мутация в гене BRAF. Назначена адъювантная иммунотерапия в течение года препаратом пембролизумаб с августа 2023 г. по август 2024 г. Далее пациент динамически наблюдался. По данным контрольного обследования в октябре 2024 г. выявлены признаки прогрессирования заболевания – появились метастазы в мягких тканях спины. Операция в декабре 2024 г. в объеме широкого иссечения опухоли мягких тканей левой лопаточной области. Гистологическое послеоперационное исследование подтвердило метастаз меланомы.
В январе 2025 г. контрольные обследования (компьютерная томография (КТ) органов грудной клетки и брюшной полости, ультразвуковое исследование мягких тканей) выявили прогрессирование заболевания в виде новых метастатических очагов в подкожной клетчатке спины, в легких.
Учитывая степень распространенности опухоли, ее гистологический тип, прогрессирование заболевания, пациенту показано проведение лекарственной терапии первой линии – комбинированной анти-PD-1- + анти-CTLA-4-терапии по схеме: нурулимаб 1 мг/кг в/в капельно + пролголимаб 3 мг/кг в/в 1 раз в 3 недели с оценкой эффекта после четырех циклов лечения. С апреля 2025 г. по июнь 2025 г. проведено четыре цикла комбинированной иммунотерапии с эффектом частичного регресса по оценке iRECIST. С июня 2025 г. по настоящее время (март 2026 г.) пациент продолжает анти-PD-1-терапию с эффектом стабилизации заболевания. За время лечения не было зарегистрировано никаких НЯ. Состояние пациента соответствует ECOG 0.
Пациент Ш., 51 год
Пациент считает себя больным с июля 2023 г., когда впервые отметил периодическое появление примеси крови в стуле. К врачам не обращался. В августе 2023 г. симптомы участились, появились не только примеси крови, но и слизь в кале. За медицинской помощью не обращался. Только в ноябре 2023 г. пациент обратился к врачу по месту жительства и был направлен на колоноскопию. По заключению эндоскопического исследования выявлено новообразование проксимальной трети нисходящей кишки, выполнена биопсия.
Гистологическое исследование биопсийного материала – опухоль гнездного строения, сформированная из клеток эпителиоидного типа с очаговым содержанием пигмента, морфологически определен метастаз меланомы. По данным молекулярно-генетического исследования обнаружена мутация BRAF V600Е.
Пациент дообследован в объеме КТ органов грудной клетки и брюшной полости, установлен диагноз: опухоль без выявленного первичного очага с метастатическим (метастаз пигментной меланомы) поражением лимфатических узлов, ободочной кишки, надпочечников, верхней доли левого легкого. сТхNхM1, IV стадия.
С ноября 2023 г. по ноябрь 2024 г. проводилась первая линия лекарственной терапии ингибиторами BRAF/MEK – дабрафенибом + траметинибом. На фоне лечения достигнут частичный ответ в феврале 2024 г. В октябре 2024 г. планировалось начало очередного цикла комбинированной таргетной терапии, однако на фоне выраженной астении выявлена анемия III степени. Пациент направлен на обследование с целью исключения желудочно-кишечного кровотечения и прогрессирования болезни. По результатам колоноскопии визуализировано новообразование и выполнена биопсия новообразования печеночного изгиба ободочной кишки. Гистологическое исследование биоптата – метастаз пигментной меланомы. Лучевые методы диагностики установили появление метастаза в тонкой кишке, увеличение размеров ранее определяемых очагов (внутрибрюшных лимфатических узлов). Заключение абдоминального хирурга: принимая во внимание выявленное вторичное новообразование тонкой кишки с признаками интимного прилежания к верхним брыжеечным, почечным сосудам, крайне высокий риск периоперационных осложнений, хирургическое лечение нецелесообразно. С учетом клинических признаков прогрессирования опухолевого процесса, роста контрольных очагов (по данным КТ) пациенту показано проведение комбинированной анти-PD-1- + анти-CTLA-4-терапии по схеме нурулимаб + пролголимаб в/в 1 раз в 3 недели (суммарно четыре введения). На момент начала второй линии лекарственного лечения пациента вновь стала беспокоить примесь крови в кале, отмечены выраженная слабость, тахикардия, головокружение. ECOG 2, анемия III степени. Была выполнена гемотрансфузия двух доз эритроцитарной массы. Анемия купирована до II степени.
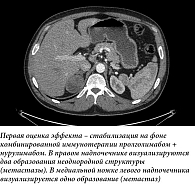
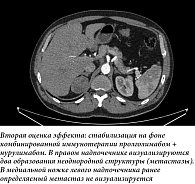
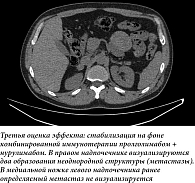
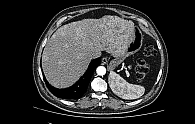
В декабре 2024 г. проведен один цикл терапии нурулимабом + пролголимабом. К началу второго цикла клинические признаки заболевания полностью отсутствовали, анемия купирована до I степени. По данным КТ органов грудной клетки и органов брюшной полости, после четвертого цикла Нурдати® отмечено уменьшение таргетных очагов в рамках стабилизации опухолевого процесса. Анемия купирована. НЯ не отмечены. Учитывая стабилизацию заболевания, с апреля 2025 г. по настоящее время (март 2026 г.) продолжена анти-PD-1-терапия. По результатам контрольных обследований от ноября 2025 г., сохраняется стабилизация заболевания (рис. 1–3). Анемия купирована (Hb 138 г/л), состояние пациента – ECOG 0. За все время лечения не было зарегистрировано никаких иммуноопосредованных НЯ.
Пациентка С., 62 года
В 2023 г. пациентка впервые отметила снижение зрения на правый глаз. Обратилась к офтальмологу по месту жительства. Установлен диагноз: отслойка сетчатки. Рекомендована консервативная терапия, от которой пациентка воздержалась. В 2024 г. выполнена магнитно-резонансная томография (МРТ) орбит, выявлены новообразование, заполняющее на 50% стекловидное тело, прилежащее к оболочкам глазного яблока, размерами 21 × 14 × 17 мм, а также отслойка сетчатки правого глаза. В ноябре 2024 г. проведено хирургическое лечение в объеме энуклеации правого глаза с формированием опорно-двигательной культи. По результатам послеоперационного гистологического исследования верифицирована пигментная меланома хориоидеи, смешанно-клеточный вариант, базальный диаметр – 18 мм, высота – 13 мм, с вовлечением цилиарного тела, 7 митозов/мм2, с инвазией в мембрану Бруха, с очаговой инвазией в склеру без экстраокулярного распространения, без достоверных признаков сосудистой инвазии (рТ4b). Пациентке рекомендовано динамическое наблюдение. В январе 2025 г. по результатам контрольных обследований (КТ органов грудной клетки и брюшной полости) установлено прогрессирование заболевания в виде появления внутригрудных лимфатических узлов и метастаза в печени. С учетом стадии заболевания пациентке показано проведение комбинированной анти-PD-1- + анти-CTLA-4-терапии по схеме нурулимаб + пролголимаб в/в 1 раз в 3 недели (суммарно четыре введения). С февраля 2025 г. по апрель 2025 г. проведено четыре цикла терапии с эффектом стабилизации заболевания. С мая 2025 г. по настоящее время (март 2026 г.) продолжена анти-PD-1-терапия пролголимабом в/в 1 раз в 3 недели с сохраняющимся эффектом стабилизации. За все время проведения лечения не было зарегистрировано никаких НЯ. Состояние пациентки – ECOG 0.
Пациент К., 60 лет
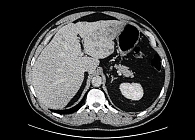
Пациент считает себя больным с 2021 г., когда стал отмечать снижение зрения. Обратился к офтальмологу по месту жительства. Установлен диагноз катаракты и начато консервативное лечение, длившееся на протяжении одного года без эффекта. В 2022 г. самостоятельно обратился к офтальмологу в Санкт-Петербурге. Обследован, диагностировано новообразование сосудистой оболочки глаза. В марте 2022 г. выполнена энуклеация правого глаза. По данным послеоперационного гистологического исследования и инструментальных методов обследования в марте 2022 г. установлен диагноз: меланома сосудистой оболочки правого глаза (T4N0M0). Рекомендовано динамическое наблюдение. По данным плановых контрольных обследований в феврале 2025 г. выявлены множественные метастазы в печени (рис. 4). Выполнена трепан-биопсия одного очага печени с гистологическим исследованием и подтверждением метастаза эпителиоидноклеточной пигментной меланомы. Установлено прогрессирование опухолевого процесса. С учетом степени распространенности опухоли, ее гистологического типа и прогрессирования заболевания пациенту показано проведение первой линии лекарственного лечения – комбинированной анти-PD-1- + анти-CTLA-4-терапии нурулимабом + пролголимабом в/в 1 раз в 3 недели (суммарно четыре введения).
С марта по апрель 2025 г. проведено два цикла иммунотерапии нурулимабом + пролголимабом. После двух циклов лечения пациент предъявлял жалобы на дискомфорт в левом боку, постоянные подъемы температуры тела до 39 °C. Гипертермия 2-й стадии расценена как иммуноопосредованное НЯ. С целью лечения осложнения в апреле 2025 г. назначена системная терапия преднизолоном в дозе 2 мг/кг/сут с полным купированием иммуноопосредованных НЯ к маю 2025 г. Далее проводилось ступенчатое снижение дозы глюкокортикоидов до полной отмены преднизолона в июле 2025 г. В мае 2025 г. выполнено плановое контрольное обследование, по результатам которого выявлено увеличение ранее определяемых и появление множественных новых метастазов в печени (рис. 5). У пациента установлено прогрессирование заболевания. При выполнении КТ органов грудной клетки отмечено появление воспалительных изменений в обоих легких. Пациент консультирован пульмонологом, назначена антибактериальная терапия.
Трепан-биопсия метастаза правой доли печени произведена в июне 2025 г., по гистологическому исследованию биоптата подтвержден метастаз эпителиоидноклеточной пигментной меланомы сосудистой оболочки правого глаза в S6 печени. Последующее лечение пациенту проводилось по месту жительства. На данный момент связи с пациентом нет, и дальнейшая судьба его неизвестна.
Пациент А., 56 лет
Пациент считает себя больным с июня 2020 г., когда самостоятельно отметил увеличение в размерах ранее существующего невуса в области передней поверхности грудной стенки слева. Обратился к хирургу по месту жительства, где в августе 2020 г. выполнено иссечение новообразования. Послеоперационное гистологическое исследование установило беспигментную меланому, 4-й уровень инвазии по Кларку, толщина по Бреслоу 3 мм. Отмечены высокая митотическая активность и отсутствие изъязвления. В августе 2020 г. в условиях специализированного онкологического учреждения произведены реэксцизия новообразования и полное обследование.
Установлен диагноз – меланома кожи передней грудной стенки слева Т3aN0M0 IIА ст. после хирургического лечения. Рекомендовано динамическое наблюдение. Ремиссия заболевания длилась три года. В июле 2023 г. пациент самостоятельно отметил увеличение подмышечных лимфатических узлов слева, в связи с чем в онкологическом учреждении в июле 2023 г. выполнена подмышечная лимфаденэктомия слева. По результатам гистологического и молекулярно-генетического исследований подтвержден метастаз низкодифференцированной эпителиоидноклеточной опухоли без мутации в гене BRAF. Инструментальные методы не выявили признаков отдаленного метастазирования, назначена и проведена адъювантная иммунотерапия анти-PD1-препаратом ниволумаб в течение года (с августа 2023 г. по август 2024 г.) без НЯ и признаков прогрессирования болезни. Период динамического наблюдения ремиссии заболевания длился 6 мес. В феврале 2025 г. по результатам очередного контрольного обследования без предъявления жалоб выявлены новые мелкие очаги в обоих легких вторичного генеза и установлено прогрессирование заболевания.
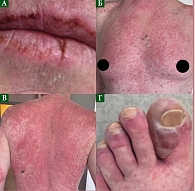
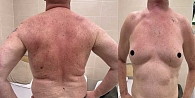
С учетом степени распространенности опухоли, ее гистологического типа, прогрессирования заболевания пациенту показано проведение первой линии лекарственного лечения – комбинированной анти-PD-1- + анти-CTLA-4-терапии нурулимабом + пролголимабом в/в 1 раз в 3 недели до четырех введений. С февраля 2025 г. по 8 апреля 2025 г. проведено три цикла комбинированной иммунотерапии нурулимабом + пролголимабом. В апреле 2025 г. (после третьего цикла лечения) пациент предъявлял жалобы на боли в правом подреберье, кожную сыпь, гиперемию и воспаление красной каймы губ. По результатам дообследования зарегистрировано развитие иммуноопосредованных НЯ в виде гепатита 3-й степени, дерматита 3-й степени (папул, пустул, булл, геморрагической сыпи, поражения более 30% туловища), хейлита 3-й степени (рис. 6). Назначена стандартная терапия глюкокортикоидами – преднизолон в дозе 1 мг/кг. Через 72 часа положительной динамики не отмечено, доза преднизолона увеличена до 2 мг/кг. В течение месяца наблюдался постепенный регресс симптомов, и только через два месяца терапии к июлю 2025 г. иммуноопосредованные НЯ были купированы до 1-й степени, отмечен регресс папул и булл, но сохранялись единичные пустулы и эритема (рис. 7). Ступенчатое снижение дозы преднизолона проведено до полной отмены к июлю 2025 г. и полного купирования НЯ. По данным контрольного обследования в июле 2025 г., признаков прогрессирования опухолевого процесса не установлено, произошла стабилизация заболевания. Учитывая иммуноопосредованные НЯ 3-й степени на фоне комбинированной иммунотерапии анти-CTLA-4- и анти-PD1-препаратами, решено продолжить монотерапию анти-PD-1-препаратом пролголимаб. С июля 2025 г. по настоящее время (март 2026 г.) пациент получает анти-PD-1-терапию с эффектом стабилизации опухолевого процесса, общим состоянием ECOG 0 и без НЯ.
Пациент С., 30 лет
Пациент считает себя больным с мая 2023 г., когда самостоятельно выявил пигментное новообразование кожи спины. Сразу обратился к дерматологу, и в кожно-венерологическом диспансере по месту жительства было выполнено иссечение новообразования. Со слов пациента, гистологическое исследование не выполнялось. В апреле 2024 г., через 11 месяцев после первичного иссечения новообразования кожи, пациент отметил увеличение подмышечных лимфатических узлов справа, обратился к онкологу по месту жительства. В мае 2024 г. выполнена лимфаденэктомия правой аксиллярной области с гистологическим, иммуногистохимическим подтверждением метастаза эпителиоидноклеточной меланомы. PD-L TPS менее 1, CPS 20%. Молекулярно-генетический анализ подтвердил мутацию в гене BRAF.
По данным лучевых методов обследования (КТ органов грудной клетки, брюшной полости и забрюшинного пространства, МРТ головного мозга), признаков отдаленного метастазирования не выявлено. С целью адъювантного лечения с мая по август 2024 г. пациент получал анти-PD-1-терапию препаратом ниволумаб. По данным очередного контрольного обследования в сентябре 2024 г. установлено прогрессирование заболевания в виде появления множественных метастазов печени и внутрикожных метастазов, увеличения аксиллярных и субпекторальных лимфатических узлов справа, образования новых метастазов в костях. По решению онкологической комиссии с учетом гистологического типа опухоли, наличия BRAF-мутации, распространенности опухолевого процесса, прогрессирования заболевания пациенту показано лечение ингибиторами BRAF/MEK: дабрафениб + траметиниб до прогрессирования болезни или непереносимой токсичности. Лечение начато в сентябре 2024 г. с эффектом частичного регресса (-60% по RECIST 1.1), согласно данным контрольного обследования в декабре 2024 г. В январе 2025 г., через месяц после контрольного обследования, пациент отметил увеличение числа кожных уплотнений и увеличение объема живота. По клиническим данным и результатам повторного обследования установлено прогрессирование опухолевого процесса в виде увеличения количества внутрикожных метастазов, появление асцита, признаков карциноматоза брюшины. С учетом прогрессирования заболевания пациенту показано проведение комбинированной анти-PD-1- + анти-CTLA-4-терапии по схеме нурулимаб + пролголимаб в/в 1 раз в 3 недели до четырех введений. На момент начала второй линии лечения общее состояние пациента оценено как ECOG 3, болевой синдром в области позвоночника – 7 баллов по визуально-аналоговой шкале (ВАШ). В феврале 2025 г. начата комбинированная иммунотерапия (нурулимаб + пролголимаб). Пациенту проводилась симптоматическая терапия, направленная на купирование болевого синдрома, коррекцию электролитного баланса и белкового обмена. Произведен лапароцентез и эвакуация 17 литров асцитической жидкости, однако состояние прогрессивно ухудшалось, появились головные боли до 9 баллов по ВАШ и усилился болевой синдром. По экстренным показаниям выполнена МРТ головного мозга с контрастированием, выявлены множественные метастазы в головном мозге. 18 февраля 2025 г. пациент скончался. Вероятно, в данном случае не успел развиться эффект от препарата Нурдати® во второй линии. Из этого следует, что оптимальное место комбинированной иммунотерапии – первая линия вне зависимости от BRAF-статуса.
Результаты
В представленной серии клинических наблюдений комбинированная иммунотерапия нурулимабом и пролголимабом продемонстрировала клиническую эффективность, обеспечивая контроль над заболеванием при удовлетворительном профиле переносимости, несмотря на предшествующую терапию и наличие сопутствующей патологии у части пациентов.
Обсуждение
Наилучший достигнутый эффект соответствовал частичному регрессу и был зарегистрирован у одного пациента. У трех пациентов отмечена стабилизация заболевания, сохраняющаяся на момент написания статьи (март 2026 г.). У двух пациентов установлено прогрессирование заболевания: в одном случае – после двух циклов терапии, в другом – после первого цикла. Профиль безопасности терапии в целом благоприятный. У одного пациента после второго цикла комбинированной иммунотерапии развилось иммуноопосредованное НЯ 2-й степени (гипертермия), купированное стандартной симптоматической терапией. Еще у одного пациента отмечены иммуноопосредованные НЯ 3-й степени (гепатит и дерматит), потребовавшие назначения глюкокортикостероидов в стандартных дозах. В дальнейшем лечение было продолжено в режиме монотерапии анти-PD-1-препаратом с достижением стабилизации заболевания. У остальных четырех пациентов НЯ на фоне терапии не зарегистрированы.
Заключение
Полученные клинические наблюдения еще раз подтверждают перспективность использования комбинированной иммунотерапии препаратом Нурдати® и потенциал для его применения в реальной клинической практике.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Исследование проведено без спонсорской поддержки.
A.N. Turomsha, A.E. Protasova, M.Yu. Sheremet, I.E. Panina
AVA-PETER LLC, Saint Petersburg
Saint Petersburg State University
V.A. Almazov National Medical Research Center, Saint Petersburg
Sergei Berezin Treatment and Diagnostic Center of the International Institute of Biological Systems LLC, Saint Petersburg
N.N. Petrov National Medical Research Center of Oncology, Saint Petersburg
Contact person: Alesia N. Turomsha, turomsha-an@avaclinic.ru
Melanoma is one of the most aggressive malignant skin tumors. The drug treatment options for patients with inoperable and metastatic forms of the disease remain extremely limited. Therefore, the development of the domestically produced combination drug Nurdati® (nurulimab + prolgolimab) opens up new possibilities thanks to its proven efficacy and favorable toxicity profile. Since this drug is relatively new to the market, each treatment case and the exchange of clinical data represent a valuable contribution to treatment evaluation.
Material and methods. This publication presents clinical experience with Nurdati® in six patients. At the time of initiation of combination immunotherapy, the group was heterogeneous in terms of age, clinical stage of the disease, amount of prior therapy, and the presence of comorbidities. Treatment outcomes are presented, including an assessment of efficacy, duration of therapy, adverse event profile, and treatment options.
Results. Nurdati® therapy was effective and had a satisfactory safety profile, confirming the potential of this regimen for real-world clinical practice.
Discussion. Combination immunotherapy with nurulimab and prolgolimab demonstrated clinical efficacy, achieving partial tumor regression in one patient and tumor stabilization in three patients. Disease progression was observed in two patients after two and one cycle of treatment. Most patients did not experience immune-mediated adverse events. Grade 2–3 adverse events were observed in only two cases, which were successfully managed with standard therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.