Патологические паттерны артериальной гипертензии и мочекаменной болезни
- Аннотация
- Статья
- Ссылки
- English



Введение
В Российской Федерации на долю мочекаменной болезни (МКБ) в структуре урологической патологии приходится от 28,3 до 38,2%, причем этот показатель продолжает расти [1]. В 2010 г. заболеваемость МКБ составила 535,7 случая на 100 тыс. населения. В период с 2005 по 2012 г. число пациентов с МКБ увеличилось на 15,7% [2].
Мочекаменная болезнь (МКБ) относится к многофакторным заболеваниям. На сегодняшний день известно более 200 факторов риска развития различных заболеваний, в том числе уролитиаза, и это число растет [3]. Все факторы риска подразделяют на три группы: поведенческие, биологические, экологические (табл. 1). Они, несомненно, взаимообусловлены, но подробный анализ позволяет оценить значимость каждого из них для конкретного заболевания. Так, для развития МКБ экологические факторы играют не такую важную роль, как, например, социально-экономические [4, 5]. Тесно связанные между собой поведенческие и биологические факторы могут привести к развитию многофакторных нозологических форм, представляющих значительную угрозу для населения. По этой причине особый интерес представляет корреляция заболеваний сердечно-сосудистой системы и других полиэтиологических патологий. Известно, что за последние 15 лет общая заболеваемость населения России выросла более чем на 30%, а частота болезней системы кровообращения – на 96%. В структуре заболеваемости они занимают второе место, уступая лидерство только болезням органов дыхания. При этом артериальная гипертензия (АГ) рассматривается не только как заболевание, но и как отдельный триггер болезней системы кровообращения [6].
Цель исследования
Провести патогенетическую параллель между развитием МКБ и АГ, чтобы определить стратегически важные позиции лечения и профилактики этих заболеваний.
Материал и методы
Исследование проведено в условиях консультативно-диагностической поликлиники Северо-Западного государственного медицинского университета им. И.И. Мечникова.
На Всемирном конгрессе урологов в Сан-Франциско (1980) докладывалось о двух подходах к выявлению МКБ: первый – скрининг-метод, второй – обследование больных, обратившихся к врачу со специфичными жалобами. Первый подход требует определенных экономических затрат, но дает возможность диагностировать менее запущенные случаи болезни. Дополнительная диспансеризация населения и углубленные медицинские осмотры лиц, занятых на работах с вредными и опасными условиями труда, позволяют не только обнаруживать заболевания на ранних сроках, но и собирать сведения о состоянии здоровья большого количества людей (отягощенный анамнез, клинические и биохимические анализы крови и мочи, результаты рентгенологических и ультразвуковых исследований и т.п.).
В период с 2006 по 2010 г. обследовано, в том числе в рамках приоритетного национального проекта «Здоровье», 21 597 человек, занятых на работах с вредными и опасными условиями труда. В соответствии с нормативными документами, помимо осмотра терапевтом, снятия и расшифровки электрокардиограммы, измерения артериального давления (АД), пациентов консультировали узкие специалисты: хирург, офтальмолог, невролог и отоларинголог, уролог и эндокринолог. В результате 543 пациента прошли дополнительное комплексное обследование. Оно включало в себя ультразвуковое исследование верхних мочевых путей и в ряде случаев оценку суточной экскреции кальция (Са++), оксалатов, цитратов и магния. Исследование биохимического состава суточной мочи выполнялось методом капиллярного электрофореза на приборе «Капель-105М» (Россия). Кроме того, рассчитывался индекс массы тела (ИМТ), оценивалось наличие сопутствующей эндокринной патологии и заболеваний желудочно-кишечного тракта, собирался пищевой анамнез (прием биологических добавок, содержащих кальций, пристрастия в еде, соблюдение диеты). При проведении исследования пользовались классификацией МКБ, предложенной L. Roger и М. Preminger (2005), и классификацией АГ в соответствии с критериями Объединенного национального комитета США по предупреждению, распознаванию, оценке и лечению повышенного АД (1993).
Результаты
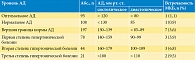
МКБ и характерные для нее метаболические нарушения достоверно чаще обнаруживались у лиц с повышенным уровнем АД. Несмотря на то что частота МКБ в указанной группе пациентов не превышала таковую в популяции (чуть более 3%), предварительные результаты показали определенную взаимосвязь уровня АД и встречаемости МКБ (выявление конкрементов, солей, песка в верхних мочевых путях) с характерными для уролитиаза метаболическими нарушениями катионно-анионного равновесия мочи (табл. 2).
Формирование камней в мочевой системе обусловлено множеством факторов. Нами выдвинута гипотеза о возможной причинно-следственной связи МКБ и АГ. За указанный период обследовано 340 больных с высоким уровнем АД. При этом пациенты с повышенным давлением отличались от пациентов контрольной группы в основном антропометрическими данными (ИМТ). Удалось установить зависимость частоты встречаемости факторов риска камнеобразования от уровня АД и ИМТ (табл. 3). Примечателен тот факт, что больные АГ, получавшие гипотензивную терапию, также оказались в группе риска.
Обсуждение результатов
Несмотря на достаточно большое количество исследований, патогенетическая связь между МКБ и АГ до конца не ясна. Первые публикации на эту тему появились в 1960-х гг. и носили в основном описательный характер. Большинство исследований, освещавших данную проблему, пришлось на период с 1979 по 1986 г. Связь между МКБ и АГ была частично обоснована после ряда экспериментальных и клинических исследований [7, 8]. Как показали эксперименты, крысы со спонтанной гипертензией оказались более предрасположены к формированию конкрементов в мочевой системе, чем особи с нормальным АД [9]. Получены факты, указывающие на нарушение кальциевого обмена как у подопытных животных, так и у людей с АГ.
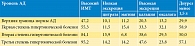
Проведенные эпидемиологические исследования выявили значимую корреляцию между высоким уровнем АД и экскрецией кальция. Эти наблюдения дали основания считать, что АГ и МКБ патогенетически связаны с повышенной экскрецией кальция. На роль алиментарных факторов в развитии МКБ указывали и в дальнейшем [10, 11]. Продемонстрировано, что количества Са++, выделяющегося за сутки с мочой, вполне достаточно, для того чтобы прореагировать с повышенным количеством оксалата и образовать нерастворимую соль СаС2О4 в почечных канальцах. Расчеты показывают, что, согласно стехиометрии данной реакции, для связывания 90 мг оксалат-иона необходимо 1,02 ммоль Са++ [12]. Следовательно, уровень суточной экскреции Са++ и оксалатов обследованных больных заведомо превышал критические значения. Между тем известно, что формирование камней в мочевой системе обусловлено множеством факторов, которые не изучались у людей с повышенным давлением. Нами проанализированы результаты лабораторных исследований (экскреции литогенных факторов и ингибиторов камнеобразования) у гипертоников и пациентов контрольной группы (нормотоников) (табл. 4).
С учетом значимости реакции мочи как проявления метаболического синдрома в формировании мочевых камней изучалась связь между ИМТ, уровнем АД и суточной реакцией мочи (24-рН) [13, 14]. Предварительные данные подтвердили связь между указанными факторами, но требуются исследования, направленные на установление корреляции между характером питания, физико-химическими свойствами мочи и суточным мониторированием АД при исключении заболеваний со стороны органов эндокринной системы. Зависимость 24-рН мочи от ИМТ убедительно показали N.M. Maalouf и соавт., проанализировавшие изменение суточной реакции мочи и уровня АД у пациентов с метаболическим синдромом (табл. 5) [15]. Оказалось, что у больных АГ имеется значительное количество факторов риска МКБ, что может объясняться пищевыми пристрастиями и метаболическими нарушениями, характерными для гипертоников. Несомненно, целесообразно проведение дальнейших исследований, направленных на определение корреляции между обнаруженными факторами риска развития уролитиаза и повышенным АД.
Собранный при помощи специально разработанной и адаптированной анкеты пищевой анамнез позволил выявить ряд социальных факторов риска развития МКБ у гипертоников.
Во-первых, высокое потребление животного белка, характерное для состоятельных людей (наибольшая встречаемость в экономически развитых регионах мира). Так, А.К. Полиенко приводит следующие данные: в индустриально развитых странах с потреблением белка животного происхождения 30 г/сут и более отмечен значительный уровень заболеваемости МКБ, а в развивающихся странах с потреблением животного белка менее 15 г/сут уровень заболеваемости значительно ниже. Кроме того, потребление белка повышает экскрецию кальция и мочевой кислоты.
Во-вторых, прием диуретиков при лечении АГ. Диуретики повышают экскрецию натрия и воды, подавляя механизм активной реабсорбции в различных отделах почечных канальцев, изменяют экскрецию калия, кальция, магния, хлора, фосфатов и бикарбонатов, что проявляется нежелательными эффектами при длительной терапии этими препаратами.
В-третьих, потребление поваренной соли. Соленая пища обоснованно считается одной из существенных причин возникновения мочекаменной болезни, поскольку ведет к снижению растворимости мононатриевой соли мочевой кислоты, которая, выпадая в осадок, участвует в формировании конкрементов в мочевыводящих путях. Известно, что эскимосы Аляски практически всегда недосаливают еду. Вполне возможно, что по этой причине никто из них не страдает АГ и МКБ [16]. Известно, что одни и те же отделы дистальных канальцев конкурируют за реабсорбцию натрия и кальция и, следовательно, повышенное потребление поваренной соли сопровождается увеличением экскреции кальция. Повторное образование камней в почках через пять лет зафиксировано у 20% мужчин, придерживавшихся диеты с малым количеством животного белка и соли. У тех, кто ограничивал себя только в потреблении кальция, рецидив камнеобразования произошел в 38% случаев [17].
К факторам, способствующим формированию почечных конкрементов в пожилом и старческом возрасте, относятся:
- привычка потреблять небольшое количество жидкости, как следствие моча оказывается концентрированной и выделяется в малом количестве;
- перенасыщение мочи солями в связи с необходимостью их избыточного выделения («порочные» пищевые пристрастия и малый объем выделяемой мочи), если реакция мочи препятствует их растворению;
- режим питания;
- нарушения мочеиспускания при обструкции нижних мочевых путей;
- возрастные сосудистые изменения в почках.
Заключение
Результаты исследования указывают на новый подход в лечении и профилактике мочекаменной болезни [18]. Снижение потребления кальция не сокращает риск повторного образования камней, но может привести к дефициту кальция, и, как следствие, к остеопорозу. Наиболее эффективный и простой метод профилактики МКБ – ограничение потребления животного белка и соли.
A.B. Batko, MD, PhD
‘Family Doctor’ Multidisciplinary Clinic, Saint Petersburg
Contact person: Andrey B. Batko, abb69@mail.ru
The article presents an analysis of common biological and behavioral risk factors for urolithiasis – excess body weight, salt consumption and arterial hypertension. The correlation between these factors is determined. Behavioral and biological risk factors have a significant contribution to the development of urolithiasis and may be obscured by simple recommendations. It is proved that a simple method to prevent stone formation is to limit the consumption of animal protein and salt, as well as control of body weight, limiting salt.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.